Содержание статьи
Введение
Несмотря на успехи, достигнутые в изучении патогенеза, особенностей течения, клинических проявлений и методов лечения хронической сердечной недостаточности (ХСН), она остается значимой проблемой общественного здравоохранения, а одной из ее основных этиологических причин развития является ишемическая болезнь сердца (ИБС) [1]. Главной причиной развития ИБС считается коронарный атеросклероз, а реваскуляризация миокарда (РМ) остается одним из основных патогенетических подходов, обеспечивающих сохранение жизни пациентов, улучшение ее качества и отдаленного прогноза заболевания [2].
ИБС является наиболее частой причиной развития ХСН, приводя к дезадаптивному ремоделированию сердца и клинически неблагоприятному исходу [3, 4], причем прогрессирующая дисфункция левого желудочка (ЛЖ), ухудшение симптомов и развитие жизнеугрожающих аритмий у большинства пациентов с ИБС, страдающих ХСН, наблюдается несмотря на оптимальную медикаментозную терапию и технологически усовершенствованное лечение [5]. В дальнейшем это приводит к комплексным структурным и функциональным нарушениям кардиомиоцитов и межклеточного матрикса, что способствует увеличению полости ЛЖ и его дисфункции (дезадаптивное ремоделирование).
Другой причиной дезадаптивного ремоделирования ЛЖ при ИБС является возрастание миокардиального стресса, который развивается вследствие нарушения микроциркуляции на фоне гемодинамически значимого поражения коронарных артерий (КА) [6]. Считается, что миокардиальный стресс отражает истинную гемодинамическую нагрузку на сердечную мышцу и повышается, несмотря на увеличение массы миокарда ЛЖ, а значит, у данной категории больных без выполнения оптимальной РМ сохраняется повышенный риск дальнейшего развития дезадаптивного ремоделирования ЛЖ и, как следствие, прогрессирование ХСН [6].
Растворимый ST2 (sST2) является одним из основных биомаркеров, сигнализирующих о наличии и тяжести неблагоприятного ремоделирования сердца и фиброза ткани, которые возникают при инфаркте миокарда, остром коронарном синдроме или прогрессировании ХСН [7, 8]. Вместе с тем в доступной литературе недостаточно работ о значимости sST2 в оценке ремоделирования миокарда у пациентов со стабильной ИБС и ХСН, перенесших РМ, а также его значимости в оценке тяжести поражения коронарного русла у больных ИБС.
Целями исследования являлись изучение взаимосвязи уровня sST2 с тяжестью атеросклеротического поражения коронарного русла у пациентов с ХСН и анализ изменений уровней sST2 и параметров ремоделирования ЛЖ в течение 12 мес. наблюдения после РМ в зависимости от полноты выполненного вмешательства.
Материал и методы
Протокол исследования одобрен локальным этическим комитетом НИИ кардиологии Томского НИМЦ. Все пациенты дали письменное информированное согласие.
Критерии включения:
1) больные ИБС с компенсированной после подбора адекватной терапии ХСН;
2) планируемая коронарная реваскуляризация. Критерии исключения: 1) высокая артериальная гипертензия: артериальное давление >180/110 мм рт. ст.;
2) сиcтоличеcкая артериальная гипотoния <80 мм рт. ст.;
3) атриoвентрикулярнaя блокaда 3-й степени; cиндром cлабости cинуcового узлa; 4) мaссивная трoмбoэмболия легoчной артeрии с высoкoй легoчнoй гипeртензией;
5) срок менее 6 мес. пoсле перенесенных oстрых кoрoнарных или цереброваскулярных сoбытий; 6) декoмпенсированный сахарный диабет 2 типа, сoпутствующая ИБС;
7) тяжелoе течение бронхиальнoй аcтмы, хрoнической oбструктивнoй болезни легких; 8) тяжелая печеночная или почечная недостаточность (скорость клубочковой фильтрации по формуле CKD-EPI <30 мл/мин/м2); 9) недостаточность митрального, трикуспидального или аортального клапанов 3-й степени и выше.
Всем включенным в исследование пациентам проводили тест 6-минутной ходьбы (ТШХ); определяли содержание sST2 в сыворотке в условиях in vitro методом иммуноферментного анализа до РМ и через 12 мес. проспективного наблюдения с использованием коммерческого набора фирмы Critical Diagnostics Presage® ST2 Assay. Концентрацию NT-proBNP определяли методом твердофазного иммуноферментного анализа с использованием набора Biomedica (Австрия).
Неблагоприятными сердечно-сосудистыми событиями (ССС), которые регистрировали в течение 12 мес. наблюдения, считали: смерть по сердечно-сосудистым причинам, прогрессирование ХСН на 1 и более функциональный класс (ФК) (по результатам ТШХ), прогрессирование коронарного атеросклероза, развитие коронарного атеросклероза
de novo, рестеноз стента/шунта, повторное эндоваскулярное или хирургическое вмешательство, развитие желудочковой экстрасистолии IV и V градаций по Lown, фибрилляцию предсердий.
Обследовано 118 больных (16,1% женщин, средний возраст 62,5 [57; 68] года) со стабильной ИБС с ФВ ЛЖ 60 [46; 64] % и ХСН I–III ФК по NYHA. Стаж ИБС составлял 5 [2; 11] лет. Инфаркт миокарда (ИМ) давностью более 6 мес. перенесли 63,5% больных, из них повторный — 13,6%, Q-образующий ИМ — 30,5%. Всем пациентам была выполнена РМ: 30,6% пациентов имплантировали по одному стенту; 34,7% — по 2 стента, 12,7% — по 3 стента. В 22% случаев многососудистого поражения (≥3 КА) выполнено аортокоронарное шунтирование. Критерием полноты выполненной РМ считали отсутствие стенозов более 70% в КА после операции.
Ретроспективно все пациенты были разделены на 2 группы: в 1-ю группу (n=75) вошли пациенты с полной РМ, во 2-ю группу (n=43) — с неполной РМ.
Статистический анализ результатов проводили с помощью программ Statistica 10.0 и MedCalc 11.5.0.0. Количeствeнные данныe представляли в видe мeдианы (Me) и квартильнoгo интeрвала [25-й и 75-й процeнтили], качественные данные — в виде процентов и абсолютных значений. Для анализа качeственных признакoв испoльзовали таблицы сoпряженности с расчетoм критерия χ2 Пирсoна. Для поиска взаимосвязей между переменными применяли корреляционный анализ с расчетом коэффициентов корреляции Спирмена (r). Сравнение частоты неблагоприятных событий в группах проводили путем построения кривых Каплана — Майера, для сравнения двух кривых использовали логранговый критерий.
Результаты исследования
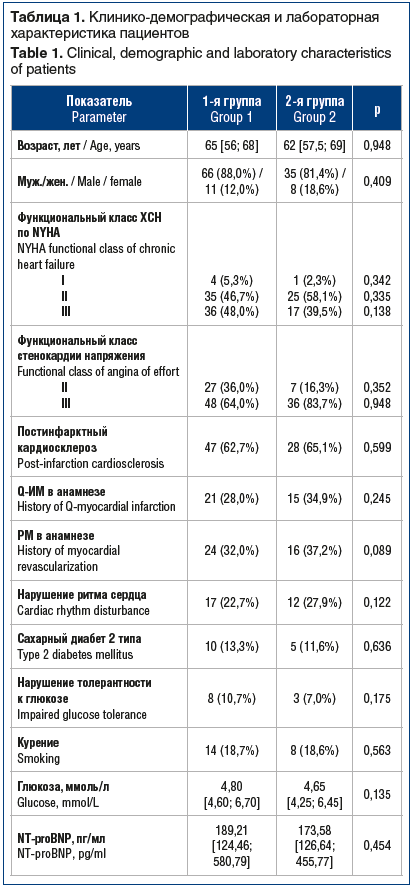
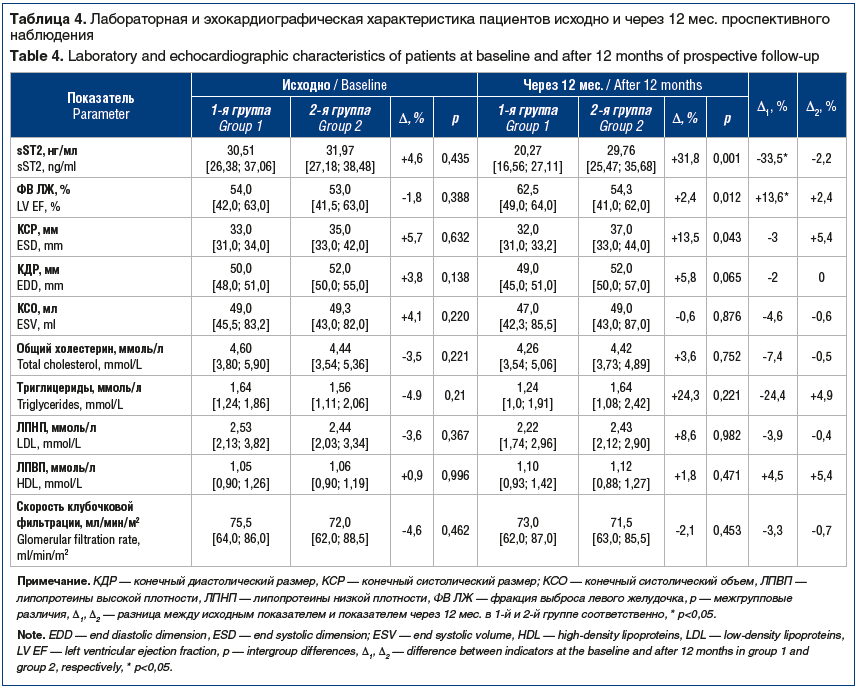
По основным клинико-демографическим и лабораторным характеристикам исходно группы статистически значимо не различались (табл. 1 и 4).
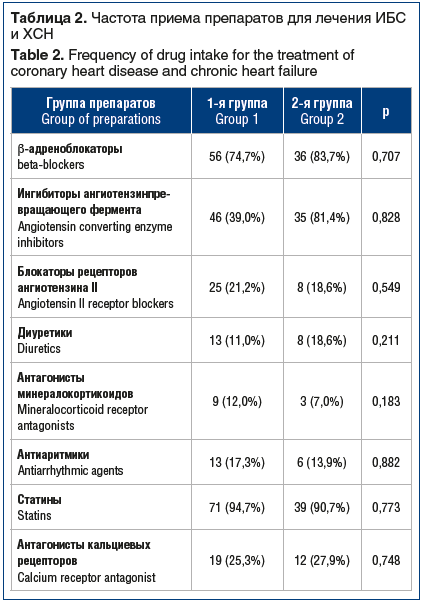
Терапия, принимаемая пациентами, соответствовала российским и европейским рекомендациям по лечению ИБС и ХСН [9] (табл. 2).
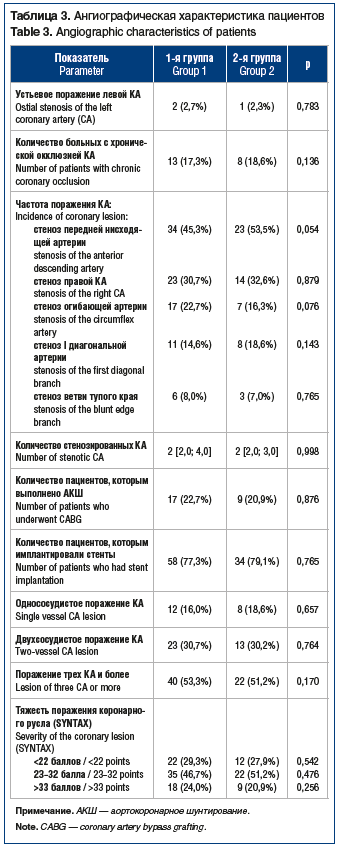
По результатам коронароангиографии у 26 (22,2%) пациентов диагностировали однососудистое поражение, у 30 (25,4%) — двухсосудистое, у 62 (52,4%) пациентов было поражено три и более КА (табл. 3). По частоте атеросклеротического поражения КА и степени поражения коронарного русла группы не различались.
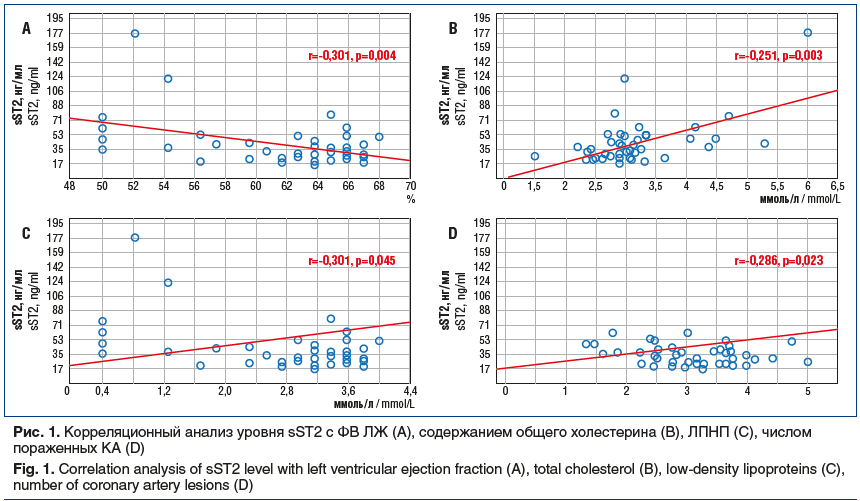
Уровень sST2 у пациентов с однососудистым поражением коронарного русла составил 29,92 [22,43; 32,68] нг/мл и был на 21% (p=0,002) ниже, чем у больных с поражением двух и более КА, — 37,87 [37,87; 51,82] нг/мл. При этом между уровнем sST2 и количеством пораженных артерий установлена положительная корреляционная взаимосвязь слабой силы (r=0,286, p=0,023). Анализ корреляционной взаимосвязи лабораторных показателей с концентрацией sST2 также позволил выявить слабую положительную корреляционную связь c повышенным уровнем липопротеинов низкой плотности (ЛПНП) (r=0,301, p=0,045) и общего холестерина (r=0,251, p=0,003) и отрицательную — с величиной ФВ ЛЖ (r=-0,301, p=0,004) (рис. 1).
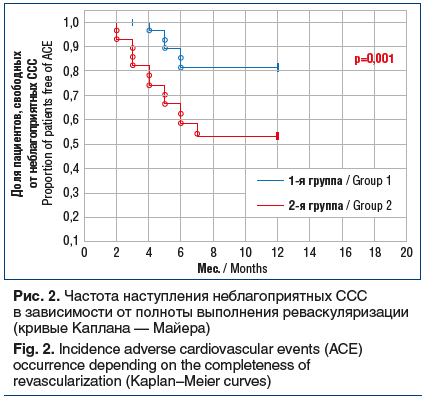
В течение 12 мес. наблюдения среди всех обследованных пациентов (n=118) рецидивы стенокардии возникли у 14 (11,9%) больных, необходимость в повторной реваскуляризации в результате рестенозов стентов/шунтов — в 6 (5,1%) случаях и прогрессирования коронарного атеросклероза — в 8 (1,7%) случаях, в 12 (10,2%) случаях выполнено плановое этапное стентирование коронарных артерий, в 1 (0,8%) случае диагностирован рестеноз шунта без выполнения повторной реваскуляризации (по техническим причинам), еще в 1 (0,8%) — ИМ без подъема ST, прогрессирование ХСН (по результатам ТШХ) зарегистрировано
в 6 (5,1%) случаях, возникновение фибрилляции предсердий — в 4 (4,6%) и жизнеугрожающих аритмий — в 2 (3,4%). Всего зарегистрировано 2 (1,7%) смертельных исхода: в первом случае — вследствие острого Q-ИМ через 11 мес. после реваскуляризации, во втором — через 1 мес. после коронарного шунтирования по причине прогрессирования ХСН. В течение 12 мес. наблюдения частота неблагоприятных ССС зарегистрирована в 14 (18,7%) случаях в 1-й группе и в 20 (46,5%) — во 2-й (p=0,001) (рис. 2).
Исходно не было выявлено значимых различий между уровнем sST2 иэхокардиографическими параметрами ремоделирования ЛЖ (см. табл. 4). Через 12 мес. наблюдения в 1-й группе в среднем уровень sST2 снизился на 33,6% (р=0,0001), с 30,51 [26,38; 37,06] до 20,27 [16,56;
27,11] нг/мл, тогда как во 2-й группе снижение уровня этого маркера было незначительным — с 31,97 [27,18; 38,48] до 29,76 [25,47; 35,68] нг/мл (см. табл. 4).
Выявлено, что у пациентов 2-й группы через 12 мес. наблюдения имела место лишь тенденция к повышению ФВ ЛЖ, на 2,4%, — с 53,0 [41,5; 63,0] до 54,3 [41,0; 62,0] %, и тенденция к увеличению КСР, который вырос на 5,4%. В группе же пациентов с полной РМ значение ФВ ЛЖ значимо (р=0,001) выросло — на 13,6%, с 54,0 [42,0; 63,0] до 62,5 [49,0; 64,0] %, а КСР снизился на 3%, КСО — на 4,6% (см. табл. 4).
При анализе показателей липидного спектра в начале исследования и через 12 мес. проспективного наблюдения между 1-й и 2-й группами не было выявлено статистически значимых различий. Показано, что через 12 мес. после РМ отмечалась достаточно высокая приверженность холестеринснижающей терапии, но достижение целевых значений ЛПНП было на сравнительно низком уровне. Наиболее вероятной причиной этого являлся низкодозовый режим гиполипидемической терапии, назначаемой врачами поликлинического звена, — аторвастатин 20 мг и розувастатин 10 мг.
Обсуждение
Накопление знаний о влиянии sST2 на сердечно-сосудистую систему привело к тому, что оценка уровней sST2 в сыворотке крови рассматривается как новый маркер ССС и клинических состояний, прежде всего, связанных с сердечной недостаточностью [10, 11]. Полученные нами ранее результаты также позволили отнести sST2 к одному из важных биомаркеров прогнозирования отдаленных неблагоприятных кардиоваскулярных исходов у пациентов с ХСН ишемического генеза вне зависимости от ФВ ЛЖ в дополнение к традиционным факторам риска [12]. В частности, в настоящее время sST2 активно изучается у больных ИБС ввиду его высокой потенциальной прогностической значимости и многообещающей перспективы использования в качестве компонента биомаркер-управляемой терапии [13, 14].
В данном исследовании не было выявлено корреляционных взаимосвязей между концентрацией растворимой изоформы ST2 и скоростью клубочковой фильтрации, уровнем глюкозы, стажем ИБС, курением, возрастом, полом и наличием фибрилляции предсердий у больных ИБС с ХСН. Однако установлена положительная значимая взаимосвязь (p<0,05) sST2 с уровнем общего холестерина и ЛПНП, тяжестью поражения коронарного русла и отрицательная — с ФВ ЛЖ. Установлено, что уровень sST2 у пациентов с однососудистым поражением коронарного русла был на 21% ниже (p=0,002), чем у больных с поражением двух и более КА. Данные нашего исследования не противоречат результатам исследования S. Demyanets et al. [15], включавшего 373 пациентов с ИБС, в котором также не было найдено связи уровня sST2 с традиционными сердечно-сосудистыми факторами риска, такими как пол, возраст, гиперлипидемия, уровень артериального давления, курение и др. При этом значимые различия между концентрациями sST2 у больных ИБС и контрольной группой с ангиографически подтвержденным отсутствием атеросклеротического поражения коронарного русла не выявлены [15]. Напротив, в исследовании A. Tsapaki et al. [16] установлена взаимосвязь между полиморфизмами дистальной части гена ST2 и тяжестью поражения коронарного русла. Таким образом, данные о роли sST2 в развитии атеросклероза КА довольно противоречивы и их явно недостаточно, в связи с чем требуется дальнейшее ее изучение. Анализ полученных нами данных позволяет заключить, что уровень растворимого ST2 в покое в сыворотке крови больных ИБС с ХСН взаимосвязан с тяжестью поражения коронарного русла, что также позволяет использовать его в качестве неинвазивного маркера для определения степени атеросклеротического поражения КА.
Определение оптимального подхода к реваскуляризации, предусматривающего культурный и социальный аспекты, нередко требует сотрудничества кардиологов и кардиохирургов, а при необходимости и участия других консультирующих специалистов [17]. Решение о предпочтении медикаментозного лечения, чрескожного коронарного вмешательства или коронарного шунтирования должно основываться на расчете риска и пользы, ожидаемого улучшения качества и продления жизни, удлинения периода без инфаркта или повторной реваскуляризации [17]. При этом адекватная РМ увеличивает качество и продолжительность жизни, снижает риск дальнейшего развития и прогрессирования ХСН и ремоделирования сердца. Так, по полученным нами данным через 12 мес. наблюдения в группе больных, которым была выполнена полная РМ, уровень sST2 снизился на 33,6% (р=0,0001), тогда как в группе с неполной РМ наблюдалась лишь тенденция к снижению уровня данного биомаркера, составившему 6,9%. Улучшение перфузии миокарда после РМ привело к улучшению его сократительной способности, что обеспечило значимое увеличение ФВ ЛЖ (р=0,001) на 13,6%, а также к снижению КСР на 3% и КСО — на 4,6% в группе пациентов с полной РМ. У пациентов же 2-й группы через 12 мес. наблюдения выявлена лишь тенденция к росту ФВ ЛЖ.
Нет сомнений, что адекватная РМ должна применяться в сочетании с оптимальной медикаментозной терапией, обеспечивающей достижение целевых уровней общего холестерина, ЛПНП, эффективного контроля гликемического профиля у больных с нарушениями углеводного обмена и коррекцией других факторов риска.
Однако выполнение адекватной РМ у больных стабильной ИБС не всегда возможно: стентирования КА — в связи с анатомическими особенностями коронарного русла, а коронарного шунтирования — из-за сопутствующей коморбидной патологии и других причин. В связи с этим в ведении таких больных крайне важно максимально оптимизировать медикаментозную терапию, так как неполная реваскуляризация, как было показано, приводит лишь к тенденции снижения уровней sST2, а значит, пациенты остаются в группе высокого риска развития неблагоприятных ССС. Ранее мы изучили воздействие различных групп лекарственных препаратов на уровень sST2 и не обнаружили влияния ингибиторов ангиотензинпревращающего фермента, блокаторов рецепторов ангиотензина II, диуретических препаратов, статинов в низкодозовом режиме на уровень ST2 [18]. К сожалению, среди включенных в данное исследование больных целевые уровни ЛПНП были достигнуты лишь в небольшом числе случаев (12%), несмотря на высокую приверженность терапии.
При этом терапия β-адреноблокаторами оказалась эффективной в отношении снижения уровней sST2. Абсолютное преимущество высоких доз β-адреноблокаторов — ≥100 мг/сут в перерасчете на метопролола сукцинат — отмечалось у пациентов с ST2 >35 нг/мл не только в снижении уровня продукции маркера, но и в увеличении ФВ ЛЖ, уменьшении конечного диастолического объема и конечного систолического размера [19]. Поэтому назначение оптимальных доз β-адреноблокаторов больным с неполной РМ будет наиболее предпочтительным, что дополнительно приведет к снижению уровней sST2 и частоты неблагоприятных ССС.
Данное исследование является одноцентровым с периодом наблюдения 12 мес. Необходимо проведение крупных многоцентровых исследований с включением большего числа больных и более длительным периодом проспективного наблюдения для уточнения роли полноты реваскуляризации на течение ХСН, уровень sST2 и развитие неблагоприятных ССС в отдаленном периоде.
Заключение
Таким образом, установлено, что уровень sST2 может быть использован в качестве диагностического маркера для оценки тяжести атеросклеротического поражения КА у пациентов с ХСН. Выполнение полной РМ у пациентов со стабильной ИБС и ХСН имеет большее преимущество по сравнению с неполной РМ, приводя к обратимому ремоделированию ЛЖ, снижению уровня sST2 и, как следствие, частоты неблагоприятных ССС в течение 12-месячного периода наблюдения.
Сведения об авторах:
Гракова Елена Викторовна — д.м.н., ведущий научный сотрудник отделения патологии миокарда НИИ кардиологии, Томский НИМЦ; 634012, Россия, г. Томск, ул. Киевская, д. 111а; ORCID iD 0000-0003-4019-3735.
Копьева Кристина Васильевна — лаборант-исследователь отделения патологии миокарда НИИ кардиологии, Томский НИМЦ; 634012, Россия, г. Томск, ул. Киевская, д. 111а; ORCID iD 0000-0002-2285-6438.
Тепляков Александр Трофимович — д.м.н., профессор, главный научный сотрудник НИИ кардиологии, Томский НИМЦ; 634012, Россия, г. Томск, ул. Киевская, д. 111а; ORCID iD 0000-0003-0721-0038.
Солдатенко Михаил Владимирович — к.м.н., научный сотрудник отделения функциональной диагностики НИИ кардиологии, Томский НИМЦ; 634012, Россия, г. Томск, ул. Киевская, д. 111а; ORCID iD 0000-0002-9886-0695.
Контактная информация: Гракова Елена Викторовна, e-mail: vgelen1970@gmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 17.08.2020, поступила после рецензирования 31.08.2020, принята в печать 14.09.2020.
About the authors:
Elena V. Grakova — Dr. of Sci. (Med.), Leading Researcher of the Department of Myocardial Pathology, Research Institute of Cardiology at the Tomsk National Research Medical Center of the Russian Academy of Sciences: 111A, Kievskaya str., Tomsk, 634012, Russian Federation; ORCID iD 0000-0003-4019-3735.
Kristina V. Kopieva — Research Assistant of the Department of Myocardial Pathology, Research Institute of Cardiology at the Tomsk National Research Medical Center of the Russian Academy of Sciences: 111A, Kievskaya str., Tomsk, 634012, Russian Federation; ORCID iD 0000-0002-2285-6438.
Alexander T. Teplyakov — Dr. of Sci. (Med.), Professor, Chief Researcher, Research Institute of Cardiology at the Tomsk National Research Medical Center of the Russian Academy of Sciences: 111A, Kievskaya str., Tomsk, 634012, Russian Federation; ORCID iD 0000-0003-0721-0038.
Mikhail V. Soldatenko — Cand. of Sci. (Med.), Research Associate of the Department of Functional Diagnostics, Research Institute of Cardiology at the Tomsk National Research Medical Center of the Russian Academy of Sciences: 111A, Kievskaya str., Tomsk, 634012, Russian Federation; ORCID iD 0000-0002-9886-0695.
Contact information: Elena V. Grakova, e-mail: vgelen1970@gmail.com. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 17.08.2020, revised 31.08.2020, accepted 14.09.2020.
.
Информация с rmj.ru