Ключевые слова: эмпирическая терапия, синдромный поход, крупные складки кожи, болезни складок кожи, Тридерм.
Для цитирования: Устинов М.В. Эмпирическая терапия воспалительных поражений кожи крупных складок // РМЖ. 2016. № 14. С. 945–948.
Для цитирования: Устинов М.В. Эмпирическая терапия воспалительных поражений кожи крупных складок // РМЖ. 2016. №14. С. 945-948
Ustinov M.V.
Central Military Clinical Hospital named after P.V. Mandryka, Moscow
Dermatologic syndromes with similar localization and clinical manifestations, often cause difficulties in differential diagnosis. The present study addresses the problem of lesion of large skin folds, that comprises: itching of varying intensity, hyperemia, infiltration, edema, peeling, cracks, erosion, and other symptoms. Doctor with good experience can establish the diagnosis on the basis of their specificity. Clinical picture of lesions is quite similar in various diseases, that leads to diagnostic errors. Primary or secondary nature of detectable changes are not always obvious. The paper discusses aspects of application of the syndromic approach and empirical treatment of diseases with damage of large skin folds, creating difficulties for visual differential diagnosis. Fixed combinations of topical glucocorticosteroids, antibiotics and antimycotics are reviewed. Study results are presented as well as conclusions about possibility of Triderm application for empirical therapy of syndrome with large skin folds lesion.
Key words: empirical therapy, syndromic approach, large skin folds, diseases of skin folds, Triderm.
For citation: Ustinov M.V. Empirical therapy of inflammatory lesion of large skin folds // RMJ. 2016. № 14. P. 945–948.
Статья посвящена эмпирической терапии воспалительных поражений кожи крупных складок
Эмпирическая терапия – метод, наиболее часто используемый в отношении бактериальных поражений, когда этиологический агент неизвестен, его видовая идентификация затруднена или длительна, а старт лечения не может быть отложен, часто – по жизненным показаниям. Однако в широком смысле эмпирическая терапия может быть не только антибактериальной. В различных разделах медицины существуют заболевания крайне сходные не только по симптомам, но и по подходам в терапии, при этом являющиеся отдельными нозологическими единицами. Эмпирическая терапия обычно предшествует этиотропной (если такая возможна), состоит из этиологических агентов перекрывающего спектра действия и часто содержит патогенетические и/или симптоматические компоненты. Нередко терапия, начатая как эмпирическая, приводит к выздоровлению и даже затрудняет постановку окончательного диагноза.
Ориентация на определенные симптомокомплексы – синдромы – привела к появлению так называемого синдромного подхода в терапии, по сути являющегося разновидностью эмпирической терапии. Синдром представляет собой группу субъективных и объективных симптомов, т. е. жалоб пациента и симптомов, которые наблюдает врач при обследовании больного. Синдромный подход предусматривает лечение одного симтомокомплекса разных заболеваний препаратом с максимальной терапевтической широтой для данной группы болезней. Обычно синдромный подход не применяется, а иногда и недопустим, если существует лабораторно-инструментальный или другой быстрый способ постановки этиологического диагноза. Но даже экспертами ВОЗ в случаях, когда этиологическая диагностика невозможна в конкретный момент времени, допускается использование синдромного подхода к лечению, в частности широко известен синдромный подход в лечении инфекций, передающихся половым путем, блок-схемами [1]. Более того, существуют дополнительные аргументы в пользу такого подхода:
• безотлагательность лечения, т. к. медицинская помощь может быть оказана в лечебных учреждениях первичного уровня; следовательно, пациенты могут начать лечение при первом же посещении медицинского учреждения;
• более широкая доступность лечения за счет возможности предоставления его в большем количестве учреждений.
Существуют ситуации, когда синдромный подход особенно востребован, например: при недоступности специализированной медицинской помощи, пребывании на отдыхе, в условиях чрезвычайных ситуаций или военной обстановки и т. п.
В дерматовенерологии схожие по локализации и клиническим проявлениям синдромы нередко становятся причиной затруднений при дифференциальной диагностике. Предметом настоящего исследования является симптомокомплекс поражения крупных складок кожи, который включает: зуд различной интенсивности, гиперемию, инфильтрацию, отечность, шелушение, трещины, эрозии и некоторые другие нарушения, специфичность которых позволит опытному специалисту идентифицировать их как конкретное заболевание. Поражения крупных складок кожи не являются редкостью и демонстрируют определенную сезонность, чаще встречаясь в теплое время года. Несмотря на доступность исследования этиологии таких поражений, клиническая картина поражений имеет сходную симптоматику для различных заболеваний, что делает возможным диагностические ошибки, в т. ч. и по причине неоднозначности определения первичности либо вторичности выявляемых изменений.
К крупным складкам кожи традиционно относятся: подмышечные впадины, локтевые сгибы, области паховые (пахово-бедренные, пахово-мошоночные у мужчин), межъягодичная, бедренно-мошоночные у мужчин, бедренно-ягодичные, собственно промежность, подколенные и складки под молочными железами у женщин. Кроме того, тучные люди имеют крупные складки кожи, образованные складками подкожной жировой клетчатки вне указанных анатомических зон, при этом избыточная масса тела сама по себе также служит фактором риска заболеваний кожи в крупных складках.
Синдром может иметь воспалительную, грибковую или бактериальную этиологию, быть следствием хронического дерматоза, трения или раздражения. Наиболее часто встречающиеся поражения (классификация по МКБ-10):
1) инфекции кожи и подкожной клетчатки: эритразма, бактериальное интертриго;
2) другие бактериальные болезни: актиномикоз, нокардиоз;
3) микозы: дерматофитии крупных складок, кандидоз крупных складок, малассезиозы;
4) дерматиты и экземы: эритематозная опрелость, иритантный дерматит, инфекционный дерматит, атопический дерматит, реже – себорейный дерматит (в складках кожи за ушами);
5) папулосквамозные нарушения: инверсный псориаз;
6) буллезные нарушения: семейная доброкачественная хроническая пузырчатка (болезнь Хейли-Хейли);
7) болезни придатков кожи: инверсные акне, гидраденит.
В складках кожи могут быть диагностированы и другие заболевания: витилиго, опухоли кожи, кожные гемобластозы и др. Но они, равно как перечисленные бактериальные болезни и болезни придатков кожи, не удовлетворяют критерию выделения по сходности клинических симптомов и к ним не может быть применен синдромный подход, предложенный далее.
Анатомо-физиологические особенности кожи крупных складок делают ее более чувствительной к внешним воздействиям, а также создают условия для формирования особого микробиоценоза на поверхности. Как видно на карте микрофлоры кожи человека (рис. 1), флора крупных складок в норме более разнообразна, чем на гладкой коже, нередко включает условно-патогенные штаммы бактерий и грибов в виде носительства. К преобладающим резидентным видам бактерий и грибов (рис. 2) часто транзиторно присоединяются и патогенные штаммы микроорганизмов.
![Рис. 1. Карта микрофлоры кожи человека [2] Рис. 1. Карта микрофлоры кожи человека [2]](https://medblog.su/wp-content/uploads/2018/12/empiricheskaya-terapiya-vospalitelnyh-porazhenij-kozhi-krupnyh-skladok-ustinov-m-v.png)
![Рис. 2. Преобладающие виды бактерий на разных областях кожи тела человека [3] Рис. 2. Преобладающие виды бактерий на разных областях кожи тела человека [3]](https://medblog.su/wp-content/uploads/2018/12/1545010207_535_empiricheskaya-terapiya-vospalitelnyh-porazhenij-kozhi-krupnyh-skladok-ustinov-m-v.png)
Как следствие, на практике мы часто видим, что воспалительные неинфекционные дерматозы в крупных складках подвержены вторичному инфицированию, а дерматозы с инфекционной этиологией нередко приводят к выраженной фокальной воспалительной реакции. Кроме того, воспалительные и инфекционные процессы в складках кожи находятся в динамическом взаимодействии, поддерживая друг друга и формируя порочный круг в патогенезе заболеваний.
Рассматриваются основные и дополнительные сценарии, по которым преимущественно и происходит это взаимодействие, а именно:
а) основные сценарии [4, 5]:
• вторичная инфекция осложняет течение существующего первично неинфекционного дерматоза,
• первично вялая инфекция кожи вызывает неадекватный и незаконченный иммунный ответ, проявляющийся сенсибилизацией, а клинически – экзематизацией;
б) дополнительные сценарии [6]:
• инфекция может быть триггерным фактором для хронического иммунного дерматоза,
• на первично вялую длительно существующую инфекцию кожи с вялым воспалительным ответом наслаивается более агрессивная инфекция, провоцирующая выраженную воспалительную реакцию, экзематизацию.
Описанные сценарии являются классическим представлением о группе дерматозов сочетанной этиологии, что позволяет отнести к ней большинство заболеваний с синдромом поражения крупных складок. Как известно, при дерматозах сочетанной этиологии максимальной терапевтической широтой будет обладать комплекс лекарственных средств или комплексное лекарственное средство, направленные на основные общие этиопатогенетические механизмы одномоментно. Во избежание лекарственных взаимодействий и побочных эффектов при эмпирической терапии поражений кожи следует назначать только местное лечение. Учитывая спектр возможных заболеваний в крупных складках кожи, в синдромном подходе эмпирической терапии предпочтение отдают комбинации препаратов со следующими эффектами:
• противовоспалительным;
• противоаллергическим;
• противозудным;
• антипролиферативным;
• противоотечным;
• мембраностабилизирующим;
• антибактериальным;
• противогрибковым.
Данные эффекты достигаются только использованием топических глюкокортикостероидов в комплексе с местными формами антибиотиков и антимикотиков. Прикладное значение синдромного подхода эмпирической терапии заключается в том, что выделяются механизмы заболеваний (в нашем случае – с единой локализацией) и назначается препарат с учетом спектра возможных окончательных диагнозов. Предпочтение следует отдавать фиксированным официнальным топическим трехкомпонентным комбинациям, каждую из которых пациент должен получить в виде единственной упаковки – это существенно повышает комплаентность, а соответственно и итоговую эффективность терапии [7].
Топический препарат для увеличения приверженности назначенному лечению должен соответствовать следующим критериям [8]:
• мощный, достаточно быстрый терапевтический эффект;
• пролонгированное действие (кратность нанесения – не чаще 2-х раз в сутки);
• хорошая косметическая переносимость;
• минимальный риск развития системных побочных реакций.
Удовлетворяющей всему перечисленному и, как следствие, наиболее востребованной с самого момента появления на рынке, а значит, наиболее изученной, остается топическая оригинальная комбинация, включающая: глюкокортикостероид бетаметазона дипропионат, антибиотик гентамицин и антимикотик клотримазол («Тридерм®», Bayer). Популярность данного топического средства настолько велика, что его название стало нарицательным для большого направления наружных комбинированных средств, имеющих в своем составе кортикостероид и противомикробные компоненты [9]. Препарат стал эталоном в оценке других трехкомпонентных препаратов. При строгом следовании инструкции по применению препарат не только очень эффективен, но и безопасен. Дерматологи часто используют эту комбинацию для пробного или стартового лечения, когда возникают сложности с дифференциальной диагностикой воспалительных и инфицированных дерматозов вне зависимости от локализаций, что, по сути, и есть эмпирическая терапия. Но именно поражения крупных складок кожи, на наш взгляд, одна из тех локализаций, где эта тактика действительно может быть оправданна.
С целью демонстрации возможности эмпирической терапии в течение короткого периода времени на амбулаторном приеме были подряд отобраны 20 больных с поражением крупных складок кожи, удовлетворяющие следующим критериям:
• острое начало заболевания или обострение заболевания на фоне полной ремиссии;
• наличие субъективных синдромов: локальных зуда, боли, жжения, дискомфорта, влияющих на качество жизни больных;
• клинические проявления в виде: гиперемии, инфильтрации, отечности, шелушения, трещин, эрозий;
• возраст старше 2-х лет;
• отсутствие предшествующей терапии с момента начала острого заболевания и не менее 1 мес. при обострении хронического;
• строгое выполнение назначений.
Эту выборку нельзя назвать рафинированной, в процессе набора больных с поражением складок 2 пациента, выявленных в исследуемый период, не удовлетворяли ее критериям. Возраст в выборке колебался от 18 до 64 лет. Распределение больных по полу и преимущественной локализации поражений представлено в таблице 1.
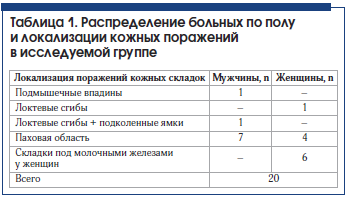
Несмотря на анамнестически и клинически очевидные диагнозы у некоторых пациентов, ни одному из них не было сделано дополнительных лекарственных назначений и была полностью исключена системная терапия. Больным рекомендовался рациональный гигиенический режим и уход за кожей пораженных зон, монотерапия одной из форм препарата (крем или мазь, в зависимости от преобладающих симптомов) оригинальной фиксированной комбинации бетаметазона дипропионата, гентамицина и клотримазола с нанесением 2 раза в сутки до полного разрешения клинической картины плюс 1–3 дня, но не более 14 дней.
Не принимая во внимание входящие предварительные диагнозы, в результате лечения у 18 из 20 пациентов в указанные сроки достигнута ремиссия, у 2-х – значительное улучшение. Средний срок достижения ремиссии – 8–10 сут, купирования субъективных симптомов – 1–3 сут с начала лечения. Констатирована высокая приверженность пациентов терапии, что объясняется выраженным эффектом уже при ее старте. Переносимость оригинальной фиксированной комбинации бетаметазона дипропионата, гентамицина и клотримазола как в форме мази, так и в форме крема не вызывала у больных замечаний, нежелательных эффектов не отмечено.
Полученные результаты позволяют сделать вывод, что в лечении дерматозов сочетанной этиологии, локализованных в крупных складках кожи, крем/мазь Тридерм является эффективным препаратом для эмпирической терапии. Длительный положительный опыт использования, высокая степень безопасности, хорошие косметические и органолептические свойства, доверие к производителю повышают комплаентность, что необходимо для получения стабильного эффекта и достижения устойчивой ремиссии при заболеваниях с различными этиопатогенетическими механизмами, но сходными клиническими симптомами и локализацией. Данной демонстрацией мы не призываем к широкому внедрению в практику дерматовенерологов синдромного подхода и эмпирической терапии с использованием трехкомпонентных топических препаратов, но вместе с тем знать о существовании такой возможности при поражении кожи крупных складок (и не только) должен каждый специалист.
Литература
1. Гладько В.В., Шегай М.М. Синдромный подход в лечении пациентов с инфекциями, передаваемыми половым путем (пособие для врачей). М.: ГИУВ МО РФ, 2005. 32 с. [Glad’ko V.V., Shegay M.M. Sindromnyy podkhod v lechenii patsiyentov s infektsiyami, peredavayemymi polovym putem (posobiye dlya vrachey). M.: GIUV MO RF, 2005. 32 s. (in Russian)].
2. Bijal Trivedi. Microbiome: The surface brigade // Nature 492. 2012. S60–S61.
3. Рудаев В.И., Куприенко О.А., Микробный пейзаж ожоговых ран: принципы лечения и профилактики гнойно-септических осложнений у обожженных на этапах оказания помощи // Презентация. Слайд № 4. 2015. [Rudayev V.I., Kupriyenko O.A., Mikrobnyy Peyzazh ozhogovykh ran: printsipy lecheniya i profilaktiki gnoyno-septicheskikh oslozhneniy u obozhzhennykh na etapakh okazaniya pomoshchi // Prezentatsiya. Slayd № 4. 2015. (in Russian)].
4. Котрехова Л.П. Диагностика и рациональная терапия дерматозов сочетанной этиологии // Consilium medicum (приложение «Дерматология»). 2010. № 4. С. 6–11 [Kotrekhova L.P. Diagnostika i ratsional’naya terapiya dermatozov sochetannoy etiologii // Consilium medicum (prilozheniye «Dermatologiya»). 2010. № 4. S. 6–11 (in Russian)].
5. Белоусова Т.А., Горячкина М.В. Алгоритм наружной терапии дерматозов сочетанной этиологии // Вестник дерматол. 2011. № 5. С. 138–144 [Belousova T.A., Goryachkina M.V. Algoritm naruzhnoy terapii dermatozov sochetannoy etiologii // Vestnik dermatol. 2011. № 5. S. 138–144 (in Russian)].
6. Устинов М.В. Выбор топического препарата для лечения сочетанных дерматозов преимущественно грибковой этиологии // Успехи медицинской микологии. Т. ХIV: матер. III Междунар. микологического форума. М.: Национальная академия микологии, 2015 [Ustinov M.V. Vybor topicheskogo preparata dlya lecheniya sochetannykh dermatozov preimushchestvenno gribkovoy etiologii // Uspekhi meditsinskoy mikologii. T. ХIV: мater. III Mezhdunar. мikologicheskogo foruma. M.: Natsional’naya аkademiya мikologii, 2015 (in Russian)].
7. Диковицкая Н.Г., Корсунская И.М., Дорджиева О.В., Невозинская З. Терапия вторичных инфекций кожи при хронических дерматозах // Эффективная фармакотерапия. Дерматология. 2014. № 2. С. 10–11 [Dikovitskaya N.G., Korsunskaya I.M., Dordzhiyeva O.V., Nevozinskaya Z. Terapiya vtorichnykh infektsiy kozhi pri khronicheskikh dermatozakh // Effektivnaya farmakoterapiya. Dermatologiya. 2014. № 2. S. 10–11 (in Russian)].
8. Коляденко В.Г., Чернышов П.В. Комбинированные препараты группы бетаметазона в лечении аллергодерматозов // Український журнал дерматології, венерології, косметології. 2007. № 1. С. 31–34 [Kolyadenko V.G., Chernyshov P.V. Kombinirovannyye preparaty gruppy betametazona v lechenii allergodermatozov // Ukraí̈ns’kiy zhurnal dermatologíí̈, venerologíí̈, kosmetologíí̈. 2007. № 1. S. 31–34 (in Russian)].
9. Тамразова О.Б., Молочков А.В. Комбинированные топические кортикостероиды в педиатрической практике: показания к применению и ошибки наружной терапии // Consilium medicum (приложение «Дерматология»). 2013. № 4 [Tamrazova O.B., Molochkov A.V. Kombinirovannyye topicheskiye kortikosteroidy v pediatricheskoy praktike: pokazaniya k primeneniyu i oshibki naruzhnoy terapii // Consilium medicum (prilozheniye «Dermatologiya»). 2013. № 4 (in Russian)].
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
Информация с rmj.ru