Введение
Псориатический артрит (ПА) — серонегативный спондилоартрит, при котором в воспалительный процесс обязательно вовлечены суставы и сухожильно-связочный аппарат [1]. В основных патогенетических механизмах развития ПА большую роль играют активация Т-лимфоцитов с последующей их дифференцировкой в Тh1 и Th17, продукция интерлейкинов 1, 6, 12, 17, 23 [2]. По данным мировых экспертов, ПА встречается с частотой около 6 случаев на 100 000 населения в год с распространенностью 1–2 случая на 1000 человек в общей популяции [3]. По мнению ведущих российских экспертов, ПА одинаково распространен среди мужчин и женщин [4]. Согласно данным литературы [5] при раннем ПА уже через 5 мес. после появления клинических симптомов у 27% пациентов наблюдаются эрозии в периферических суставах, а через 2 года после дебюта ПА — еще у 47%, поэтому современная тактика ведения больных с данной артропатией, согласно концепции treat to target (лечение до достижения цели), предусматривает как можно более раннюю диагностику и активное лечение заболевания до достижения стойкой клинико-лабораторной ремиссии или низкой активности заболевания, чему препятствуют позднее обращение пациента за медицинской помощью, трудность диагностики ПА как мультисистемной патологии, поздняя инициация базисной противовоспалительной терапии, недостаточная эффективность и индивидуальная резистентность к лекарственным средствам, а также аксиальные проявления. Все эти факторы вместе с индивидуальными особенностями пациента (восприятие болезни, генетические факторы перцепции боли, социально-культурные установки) участвуют в формировании хронического болевого синдрома (ХБС) и препятствуют достижению ремиссии. В настоящее время ХБС рассматривается как сложный многокомпонентный механизм, который эволюционно не несет адаптивной функции, а является патологическим — дезорганизует работу центральной нервной системы, приводя к сенситизации. Согласно мнению мировых авторов наблюдаемый при ревматических заболеваниях ХБС, в частности при ПА, состоит из ноцицептивного, дисфункционального и ней-ропатического компонентов [6]. Нейропатическая боль (НБ) развивается в результате морфологических и функциональных изменений периферического и центрального отделов нервной системы, может считаться осложнением хронического течения и обусловливать болевую сенсибилизацию у пациентов с ПА, имитируя недостаточную эффективность противоревматических лекарственных препаратов [7]. Высказано предположение [8], что длительная персистенция ХБС у пациентов с ПА может приводить к центральной сенситизации (ЦС), усугубляющей течение любого болевого синдрома. О распространенности НБ среди пациентов с ПА свидетельствуют не многие зарубежные исследователи: в 2019 г. НБ среди 64 пациентов с ПА выявили у 26,6%, а в исследовании 2020 г. — у 25% из 118 обследуемых с ПА [9–11]. Отсутствие крупных исследований распространенности НБ среди пациентов с ПА в России и мире, взаимосвязь НБ с активностью, длительностью, отдельными клинико-лабораторными, инструментальными показателями и качеством жизни пациентов представляют собой большой пробел в понимании полной клинической картины данного заболевания, поскольку для практической медицины важно, что в условиях прогрессирования ПА и ХБС у пациентов может снижаться эффективность противовоспалительных и обезболивающих препаратов [12] и, как следствие, возникают недостаток комплаентности, утрата доверия к традиционной медицине. На практике даже при достижении стойкой клинико-лабораторной ремиссии или низкой активности ПА пациенты продолжают жаловаться на некоторые болевые ощущения, что зачастую определяется специалистом как обострение заболевания, не подразумевая вовлечение в патологический процесс иных структур, отличных от суставного аппарата и околосуставных тканей. Отдельно следует отметить, что при ПА с ХБС наблюдается снижение качества жизни [13, 14]. Например, группа канадских авторов [15] в 2021 г. показала, что низкие показатели качества жизни могут быть предикторами прогрессирования заболевания при ПА. Таким образом, ПА, даже несмотря на своевременное применение базисной противовоспалительной и генно-инженерной биологической терапии, неотъемлемо сопровождается развитием ХБС и значительным снижением качества жизни пациента [16].
Цель исследования: определить у пациентов с ПА частоту встречаемости НБ, наличие связи между НБ и полом, активностью, стажем заболевания, центральной сенситизацией (ЦС), качеством жизни.
Материал и методы
В исследование включено 88 пациентов с ПА в возрасте старше 18 лет на момент включения в исследование, находившихся на стационарном лечении в ревматологическом отделении БУЗ УР «РКДЦ МЗ УР». Критериями включения в исследование являлись диагноз ПА по критериям CASPAR 2006 г., подписанное информированное согласие пациента на участие в исследовании. Критериями невключения были: наличие сопутствующих заболеваний, сопровождающихся ХБС иной этиологии (онкологические, метаболические, токсические, например сахарный диабет), наличие органической патологии головного мозга, психических заболеваний, соматических заболеваний в стадии декомпенсации; беременность и послеродовый период менее 6 мес. Исследование выполнялось в соответствии с этическими стандартами Хельсинкской декларации.
Клиническое обследование участников проводилось с подсчетом числа припухших суставов (ЧПС, 0–66) и числа болезненных суставов (ЧБС, 0–68). Оценка интенсивности боли проводилась с использованием визуально-аналоговой шкалы (ВАШ боли, 0–100 мм). Лабораторное обследование включало количественное определение С-реактивного белка (СРБ, мг/л). Активность ПА оценивалась по индексу Disease activity in psoriatic arthritis (DAPSA): при значениях DAPSA 0–4 балла определялась ремиссия, 4,1–14 баллов — низкая активность заболевания, 14,1–28 баллов — умеренная и ≥28,1 балла — высокая. Для выявления эрозивного периферического артрита проводили рентгенографию кистей и стоп в прямой проекции. Наличие НБ определяли с помощью русскоязычной версии опросника PainDetect (PDQ), который многократно показал надежность и валидность в работе с пациентами с ПА. НБ считали выявленной при значениях PDQ ≥19 баллов, при этом невролог проводил осмотр для исключения или подтверждения НБ [17]. ЦС определяли с помощью русскоязычной версии опросника CSI: при значениях ≥30 баллов ЦС считается выявленной и клинически значимой [18]. Качество жизни оценивали при помощи опросника The Short Form-36 (SF-36) с определением физического и психологического компонентов (ФК и ПК соответственно) здоровья. Данный опросник многократно показал надежность при использовании у пациентов с ПА [18].
Статистическая обработка проводилась с помощью программы IBM SPSS 26.0. Проверку распределения на нормальность выполняли по критерию Колмогорова — Смирнова с построением квантильных диаграмм (Q-Q Plots). Статистическую значимость различий нормально распределенных независимых переменных определяли по критерию Стьюдента для независимых выборок, нормально распределенных зависимых переменных — по критерию Стьюдента для парных выборок, для распределенных отлично от нормального переменных — по критерию Манна — Уитни для независимых и по критерию Уилкоксона — для зависимых выборок, для качественных независимых переменных — по критерию χ2 Пирсона, зависимых — по критерию Мак-Нeмара. Для всех видов анализа данных различия считали статистически значимыми при p≤0,05. Нормально распределенные показатели представлены как среднее значение (М), стандартное отклонение (СО) и 95% доверительный интервал (ДИ) (М±СО; 95% ДИ), данные, распределение которых отличалось от нормального, — как медиана (Me), 25-й, 75-й процентили и 95% ДИ (Ме [25%; 75%]; 95% ДИ).
Результаты и обсуждение
По результатам обследования было сформировано 2 группы пациентов: с НБ (группа НБ+) и без НБ (группа НБ-) (см. таблицу).
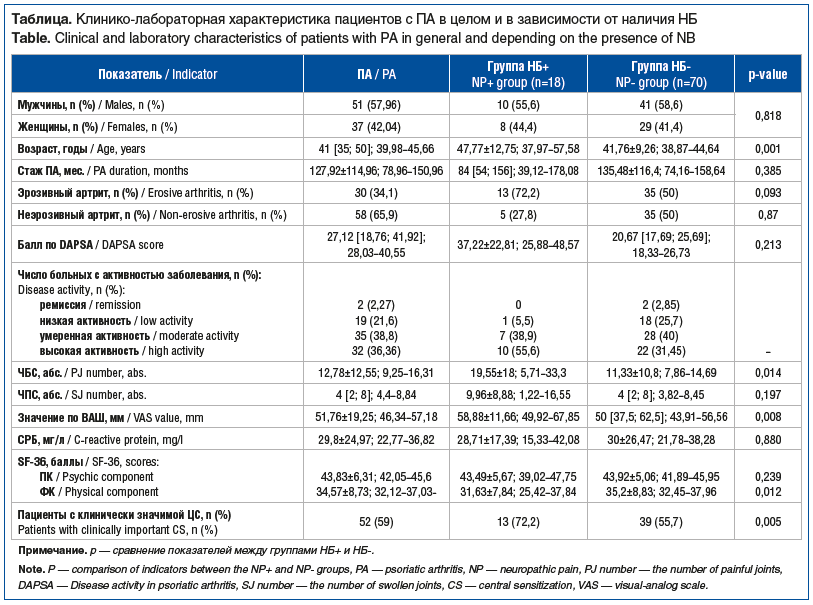
Сформированные группы были сопоставимы по полу обследованных. Группу НБ+ составили пациенты более старшего возраста (p=0,001). Разницы в длительности течения ПА в группах не обнаружено (р=0,385), однако наблюдалась тенденция к большей длительности основного заболевания среди пациентов без НБ. Группы не различались по числу пациентов с эрозивным и неэрозивным ПА. Мы не выявили статистически значимых различий средних значений индекса DAPSA (p=0,213) между группами, несмотря на прослеживаемые бóльшие показатели такового у пациентов с НБ. В группе НБ+ определены бóльшие средние значения по ВАШ боли, чем в группе НБ- (р=0,008). Среднее ЧБС у пациентов с НБ превышало таковое в группе без НБ (р=0,014). Среднее ЧПС в группах не различалось (р=0,197). Различий в средних значениях уровня СРБ в группах не обнаружено (p=0,880). У всех пациентов наблюдалось снижение качества жизни согласно опроснику SF-36, причем у пациентов группы НБ+ при сравнении с группой НБ- были снижены средние значения ФК (p=0,012), но не ПК (р=0,239). У 52 (59%) пациентов с ПА выявлена клинически значимая ЦС. Несмотря на высокую распространенность клинически значимой ЦС в обеих группах у пациентов группы НБ+ клинически значимая ЦС встречалась достоверно чаще (р=0,005).
Нами выявлена высокая распространенность НБ и ЦС среди пациентов с ПА (20,4 и 59% соответственно). НБ достоверно чаще встречалась у пациентов более старшего возраста. Среди пациентов с подтвержденной НБ среднее ЧБС и показатели ВАШ боли были достоверно больше, однако средняя длительность основного заболевания, среднее ЧПС, средние значения индекса DAPSA и значения СРБ в группе пациентов с выявленной НБ не отличались от таковых у пациентов без НБ. Схожие результаты получены в исследовании [19], показавшем отсутствие связи между длительностью ПА и НБ. Мы считаем, что нейропатический компонент ХБС ассоциирован со столь выраженным болевым синдромом, что это может несколько «завышать» активность заболевания за счет субъективного восприятия пациентом выраженности и тяжести проявлений болезни и искажать представление врача об активности заболевания или быть показателем тяжелого и неконтролируемого хронического воспаления. Иными словами, у пациентов с НБ не исключается вклад невоспалительных факторов в формирование активности болезни. Наши выводы согласуются с данными группы исследователей, показавшими присутствие НБ у 24% пациентов с ПА, и их предположением о вкладе НБ в повышение значений ВАШ боли у пациентов с ПА [19]. Мы наблюдали снижение показателей ФК и ПК качества жизни среди всех пациентов с ПА, при этом средний показатель ФК у пациентов с НБ был достоверно ниже по сравнению с таковым у пациентов без НБ, что свидетельствует в пользу более выраженного болевого синдрома у пациентов с НБ. Полученные данные соотносимы с результатами исследования зарубежных авторов, отмечавших снижение качества жизни у пациентов с НБ при ПА [20]. Интересно, что у пациентов с ПА и подтвержденной НБ клинически значимая ЦС встречалась достоверно чаще, что может говорить о существенном вкладе последней в клиническую картину ХБС при данном заболевании. Результаты нашего исследования соотносятся с недавним зарубежным исследованием [21], которое обнаружило ЦС у 42,9% пациентов с ПА, авторы также указали на искажение индекса DAPSA у пациентов с ЦС. Наши результаты позволяют предполагать у пациентов с ПА «болевую сенсибилизацию», которая требует индивидуального и междисциплинарного подхода с учетом вариабельности клиники основного заболевания.
Выводы нашей работы четко демонстрируют участие периферических и центральных нейрогенных механизмов в развитии ХБС при ПА.
Стоит указать и другую точку зрения. Так, авторы более ранней работы [22] указывают на необходимость принятия во внимание культурных и социальных факторов региона, к которым принадлежат когорты пациентов с наблюдаемой ЦС, подчеркивая именно их решающую роль, а не само бремя болезни.
Заключение
Таким образом, среди пациентов с ПА выявлена частая встречаемость НБ — 20,1%, которая может несколько «завышать» активность заболевания за счет субъективных суждений пациента о тяжести болезни, однако является показателем хронического течения воспаления и снижает качество жизни. Так, у пациентов с ПА значения ФК были достоверно ниже в группе НБ+, чем в группе НБ- (p=0,012). Более чем у половины (59%) пациентов с ПА выявлена клинически значимая ЦС (в группе НБ+ достоверно чаще, чем в группе НБ- (р=0,005)). Дальнейшее изучение данной проблемы необходимо для более точной и своевременной диагностики ПА, в том числе болевого компонента, а также для реализации персонализированного подхода в оказании медицинской помощи и оптимизации терапевтической стратегии, необходимой для поддержания достойного уровня жизни пациентов с этой патологией.
Сведения об авторах:
Акулинушкина Екатерина Юрьевна — врач-ревматолог БУЗ УР «РКДЦ МЗ УР»; 426000, Россия, г. Ижевск, ул. Ленина, д. 87Б; ORCID iD 0000-0002-9321-431X.
Иванова Лариса Владимировна — главный внештатный специалист МЗ УР по ревматологии, заведующая стационаром ревматологического отделения БУЗ УР «РКДЦ МЗ УР»; 426000, Россия, г. Ижевск, ул. Ленина, д. 87Б; ORCID iD 0000-0003-0411-6118.
Якупова Светлана Петровна — к.м.н., главный внештатный специалист МЗ РТ по ревматологии, доцент кафед-ры госпитальной терапии ФГБОУ ВО Казанский ГМУ Минздрава России; 420012, Россия, г. Казань, ул. Бутлерова, д. 49; ORCID iD 0000-0002-8590-4839.
Якупов Эдуард Закирзянович — д.м.н., профессор, директор ООО «НИМК «Ваше Здоровье»; 420097, Россия, г. Казань, ул. Достоевского, д. 52; ORCID iD 0000-0003-2965-1424.
Контактная информация: Акулинушкина Екатерина Юрьевна, e-mail: katewenterly@gmail.com.
Источник финансирования: авторы не имеют финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 20.01.2023.
Поступила после рецензирования 14.02.2023.
Принята в печать 14.03.2023.
About the authors:
Ekaterina Yu. Akulinushkina — rheumatologist, Republican Clinical and Diagnostic Center of the Ministry of Health of the Udmurt Republic; 87B, Lenin str., Izhevsk, 426000, Russian Federation; ORCID iD 0000-0002-9321-431X.
Larisa V. Ivanova — chief external specialist in rheumatology of the Ministry of Health of the Udmurt Republic, Head of the Rheumatology Department Hospital, Republican Clinical and Diagnostic Center of the Ministry of Health of the Udmurt Republic; 87B, Lenin str., Izhevsk, 426000, Russian Federation; ORCID iD 0000-0003-0411-6118.
Svetlana P. Yakupova — C. Sc. (Med.), chief external specialist in rheumatology of the Ministry of Health of the Udmurt Republic, associate professor of the Department of Hospital Therapy, Kazan State Medical University; 49, Butlerov str., Kazan, 420012, Russian Federation; ORCID iD 0000-0002-8590-4839.
Eduard Z. Yakupov — Dr. Sc. (Med.), Professor, Director, LLC «Research Medical Complex “Vashe Zdorovie»; 52, Dostoevsky str., Kazan, 420097, Russian Federation; ORCID iD 0000-0003-2965-1424.
Contact information: Ekaterina Yu. Akulinushkina, e-mail: katewenterly@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 20.01.2023.
Revised 14.02.2023.
Accepted 14.03.2023.
Информация с rmj.ru