Введение
Бронхиальная астма (БА) в настоящее время является одним из наиболее распространенных заболеваний, которым в мире страдает около 300 млн человек [1]. Развитие и прогрессирование заболевания у лиц молодого возраста отрицательно влияют на уровень трудоспособности и качество жизни, а также повышают затраты здравоохранения на решение данной проблемы. Согласно рекомендациям GINA (2019) понятие тяжести течения заболевания неразрывно связано с понятием контроля [2]. Тяжесть течения определяется по объему терапии, необходимой для достижения контроля БА, а также по активности заболевания на фоне проводимого лечения. На сегодняшний день у пациентов с БА достижение контроля является ключевой целью лечения, а также главным признаком оказания качественной медицинской помощи [2]. Однако, несмотря на значительный прогресс современной клинической фармакологии и широкую доступность препаратов, число больных с неконтролируемой БА колеблется от 40 до 67% в различных странах [3]. В России, по результатам наблюдательного исследования контроля над астмой (НИКА), полный контроль заболевания имели 23% больных БА, частичный — 35%, а у 42% пациентов имела место неконтролируемая БА [4]. Причины неудовлетворительного контроля над астмой — в низкой приверженности терапии, прежде всего обусловленной страхами пациентов перед гормональными препаратами из-за недостаточной осведомленности о действующих веществах, а также боязнью долгосрочного эффекта, появления зависимости, опасений по поводу вреда здоровью, снижения эффективности при регулярном приеме, неудобства использования ингалятора [5, 6]. Многие пациенты самостоятельно регулируют объем базисной терапии в зависимости от частоты и тяжести симптомов. Кроме того, примерно треть больных начинает применять препараты только при появлении симптомов и отменяет прием при улучшении самочувствия. В результате препараты, предназначенные для регулярного приема, используются по интермиттирующей схеме [7].
Согласно рекомендациям GINA (2020) перед постановкой диагноза или коррекцией фармакотерапии неконтролируемой БА рекомендуется оценивать приверженность пациентов лечению [8]. По определению Всемирной организации здравоохранения, приверженность рассматривается как степень, в которой действия пациента — прием лекарственных препаратов, соблюдение диеты, смена образа жизни — соотносятся со следованием рекомендациям врача [9]. Исходя из этого, приверженность подразумевает не слепое подчинение больного, а активное вовлечение его в процесс лечения. Проведен ряд исследований с целью изучения возможностей методов, способствующих увеличению приверженности больных терапии, в которых показано, что повысить приверженность лечению у больных БА проблематично даже с помощью комплекса методов [10]. Отсутствие терапии либо нерегулярный прием назначенных препаратов неизбежно приводят к тяжелым обострениям даже пациентов с легким течением астмы. Таким образом, низкая приверженность больных БА лечению и, как следствие, плохой контроль над симптомами заболевания являются на сегодняшний день ключевыми проблемами в данной области.
Цель исследования: изучить уровень контроля и приверженности лечению пациентов молодого возраста с БА легкого и среднетяжелого течения.
В задачи исследования входило: провести общеклиническое обследование пациентов с БА различной степени тяжести, оценить функциональное состояние респираторной системы у больных БА с помощью метода спирометрии, уровень контроля над симптомами заболевания с помощью опросников АСТ (Asthma Control Test — тест по контролю астмы), ACQ-5 (Asthma Control Questionnaire — опросник по контролю над астмой), а также приверженность больных БА легкого и среднетяжелого течения терапии с помощью опросника Мориски — Грина (MMAS-6) в зависимости от степени тяжести заболевания.
Материал и методы
Обследовано 146 пациентов с установленным диагнозом БА аллергического генеза легкого и среднетяжелого течения вне обострения. В основной группе обследовано: мужчин — 55 (38%), женщин — 91 (62%), медиана возраста составила 28 [24; 37] лет, медиана длительности заболевания — 5 [2; 13] лет. В зависимости от степени тяжести БА выделено 2 группы. В 1-ю группу вошли пациенты с легким течением БА, во 2-ю группу — пациенты с БА среднетяжелого течения. В 1-ю группу включено 68 больных, среди них 27 (40%) мужчин и 41 (60%) женщина, медиана возраста составила 29 [24; 37] лет, медиана длительности заболевания — 3 [1; 9] года. Во 2-й группе наблюдалось 78 человек, мужчин — 28 (36%), женщин — 50 (64%), медиана возраста составила 30 [24; 38] лет, медиана длительности заболевания — 6 [2; 14] лет.
Критерии включения: БА аллергического генеза легкого, среднетяжелого течения вне обострения; возраст от 18 и до 45 лет; возможность правильного использования базисных препаратов; адекватная оценка своего состояния (по мнению исследователя); получение информированного согласия на участие в исследовании.
Критерии исключения: БА тяжелого течения; обострение БА; наличие цереброваскулярных заболеваний (острое нарушение мозгового кровообращения, транзиторные ишемические атаки); заболевания сердца (ишемическая болезнь сердца: инфаркт миокарда в анамнезе, коронарная реваскуляризация, хроническая сердечная недостаточность IIБ и III стадий); злокачественные новообразования; тяжелая почечная и печеночная недостаточность; сахарный диабет; хроническая обструктивная болезнь легких; беременность.
Диагноз «бронхиальная астма» у всех пациентов был ранее установлен, что подтверждалось наличием медицинской документации о стационарном лечении и/или обращении за медицинской помощью в амбулаторном порядке.
Тяжесть течения заболевания фиксировалась в соответствии с медицинской документацией с последнего осмотра врача аллерголога-иммунолога. Все пациенты на момент включения в исследование находились на динамическом наблюдении и получали базисную терапию, степень тяжести заболевания оценивалась ретроспективно, исходя из необходимого для контроля симптомов и обострений объема терапии. Диагноз БА легкого течения устанавливался пациентам, у которых, по данным медицинской документации, зафиксировано достижение контроля над симптомами заболевания при приеме терапии ступеней 1 и 2, среднетяжелого течения — при достижении контроля на ступени 3 [2].
Общеклиническое обследование заключалось в опросе больного (сбор жалоб, анамнеза), получении физикальных данных (осмотр, аускультация).
Изучение анамнеза осуществлялось путем опроса больных, учитывались частота обострений, триггеры, вызывающие ухудшение состояния, объем ранее проводившегося лечения. Спектр сенсибилизации определяли на основании данных аллергологического анамнеза и результатов специфического аллергологического обследования, прежде всего, кожных тестов с аллергенами.
Оценка уровня контроля и приверженности терапии осуществлялась с помощью специализированных опросников. Анкетирование пациентов выполнялось без временного интервала между заполнением опросников.
Оценка приверженности базисной терапии осуществлялась путем устного опроса пациентов и анкетирования больных с помощью модифицированного опросника MMAS-6, по доменам «Приверженность», «Мотивация», «Осведомленность» [11]. Приверженными считались пациенты, набравшие 4 балла, неприверженными — менее 4 баллов. Количество баллов 0–1 свидетельствовало о низкой мотивации или, соответственно, низкой осведомленности, 2–3 — о высокой мотивации или высокой осведомленности.
Для оценки уровня контроля астмы использовались вопросники АСТ и ACQ-5. По шкале АСТ симптомы оценивались пациентом за 4 нед. Сумма баллов менее 20 свидетельствовала об отсутствии контроля над симптомами заболевания, 20–24 балла — о частичном контроле, при наборе пациентом 25 баллов диагностировалось контролируемое течение БА. C помощью опросника ACQ-5 уровень контроля над симптомами заболевания оценивался за последнюю неделю. О контролируемом течении астмы судили при результате менее 0,5 балла, частично контролируемая БА диагностировалась при показателе от 0,75 до 1,5 балла, набор 1,5 балла и более демонстрировал отсутствие контроля над симптомами заболевания.
После проведения анкетирования все пациенты были проконсультированы аллергологом, им были даны соответствующие рекомендации по объему базисной терапии, необходимости регулярного приема препаратов. Пациенты посетили астма-школу, где проводится обучение правильной технике ингаляции.
Изучение функционального состояния респираторной системы осуществлялось с помощью спирометрии. Исследования были проведены на установке Master Screen Body (Jaeger, Германия). Спирометрия выполнена в рамках стандартов качества исследований Европейского респираторного общества (European Respiratory Society — ERS) и Американского торакального общества (American Thoracic Society — ATS) [12, 13]. Пациенту рекомендовалось воздержаться от курения и приема кофе в день обследования. Своевременно были отменены лекарственные средства, способные повлиять на результаты теста.
В ходе работы были проанализированы следующие параметры спирометрии: форсированная жизненная емкость легких (ФЖЕЛ), объем форсированного выдоха за 1 с (ОФВ1), индекс Генслера (ОФВ1/ФЖЕЛ), объемная скорость на среднем участке кривой «поток — объем» форсированного выдоха между 25–75% выдохнутой ФЖЕЛ (СОС25–75).
Данные спирометрии оценивались c учетом требований ERS, ATS [12, 13] и Федеральных клинических рекомендаций Российского респираторного общества по применению метода спирометрии [14].
Статистический анализ данных проводился с помощью пакета программ Statistica 10.0 for Windows. Количественные значения представлены в виде медианы (Ме) и интерквартильного интервала [Q1; Q3], где Q1 —
25-й процентиль, Q3 — 75-й процентиль. Качественные переменные описаны абсолютными значениями и в виде процентных долей и их стандартных ошибок. При сравнении групп по количественным признакам применялся непараметрический U-критерий Манна — Уитни. Качественные признаки оценивались с помощью критерия χ2 с поправкой Йетса.
Результаты исследования
В группе больных с легким течением БА за 12 мес. до включения в исследование обострение заболевания наблюдалось у 78% пациентов. При оценке уровня контроля с использованием критериев GINA (2019) отмечено наличие дневных приступов затрудненного дыхания более 2 раз в неделю у большинства пациентов 1-й группы (медиана 0,71 [0,42; 1] раза в сутки). Ежедневно применяли короткодействующие β2-агонисты (КДБА) 23 (34%) пациента, 45 (66%) респондентов использовали их менее 1 раза в сутки. Необходимо отметить, что ежедневный прием КДБА в группе БА легкого течения регистрировался у больных, которые по тем или иным причинам не принимали базисную терапию. Медиана частоты потребности в КДБА в группе составила 0,72 [0,43; 1] раза в сутки. По данным опросников, отсутствие контроля над симптомами заболевания регистрировалось у 61 (90%) пациента и лишь у 7 (10%) больных отмечен частичный контроль над симптомами заболевания. Средний суммарный балл по шкале АСТ в группе больных БА легкого течения составил 17 [15; 21] баллов, по шкале АCQ-5 — 1,8 [1,4; 2,2] балла.
В группе пациентов со среднетяжелым течением заболевания имели обострение и проходили стационарное лечение за последние 12 мес. до включения в исследование все пациенты. Обращает на себя внимание то, что у всех респондентов 2-й группы регистрировались ежедневные симптомы астмы. Так, медиана дневных приступов удушья составила 1 [1; 2] раз в сутки, ночных приступов — 1 [0,1; 1,0] раз в сутки. Ежедневно применяли ситуационно КДБА все пациенты с частотой 2 [1,3; 2,5] раза в сутки. Среди пациентов с БА среднетяжелого течения регистрировалось отсутствие контроля над симптомами заболевания у 68 (87%) человек, частичный контроль отмечен у 10 (13%) больных. Средний суммарный балл по шкале АСТ составил 15 [12; 21] баллов, по шкале АCQ-5 — 2,2 [1,4; 2,8] балла.
При анализе спектра сенсибилизации чаще выявлялась поливалентная сенсибилизация к различным группам аллергенов. Моносенсибилизация выявлялась реже, чаще всего к бытовым аллергенам — у 20 (13,7%) больных. Наиболее часто в обследованных группах регистрировалась полисенсибилизация к бытовым и эпидермальным аллергенам — у 25 (17,1%) пациентов. Сенсибилизация к растительным, бытовым и эпидермальным аллергенам наблюдалась у 23 (15,8%) больных, к растительным, эпидермальным и пищевым аллергенам — у 19 (13,0%) человек, поливалентная сенсибилизация к бытовым, эпидермальным, пищевым и растительным аллергенам выявлена у 14 (9,6%) респондентов.
Известно, что ключевыми параметрами, характеризующими наличие бронхиальной обструкции, являются ОФВ1, ФЖЕЛ, индекс Генслера (отношение ОФВ1/ФЖЕЛ). По данным спирометрии, в группе больных БА легкого течения вентиляционные нарушения по обструктивному типу выявлены у 12 (18%) пациентов. При количественном анализе показателя ОФВ1 были зарегистрированы легкие нарушения проходимости дыхательных путей (НПДП) у 4 (6%) человек, умеренные НПДП — у 8 (12%) пациентов, при этом параметры ФЖЕЛ у всех обследованных находились в пределах нормальных значений, снижение показателя СОС25–75 установлено у 14 (21%) больных.
По результатам спирометрии в группе больных БА среднетяжелого течения обструктивные нарушения выявлены у 22 (28%) человек. Нарушения, соответствующие легкой степени тяжести, выявлены у 12 (15%) человек, умеренные НПДП установлены у 10 (13%) пациентов, показатель ФЖЕЛ находился в пределах нормы у всех респондентов.
Анализ приверженности проводимому лечению продемонстрировал, что большинство пациентов самостоятельно отменяют базисную терапию после улучшения самочувствия. Так, на момент обследования в обеих группах выявлен крайне низкий процент пациентов, которые постоянно получали противовоспалительную терапию. При анализе различий по исследуемым показателям, рассчитанных с помощью критерия χ2 с поправкой Йетса, выявлены значимые различия между 1-й и 2-й группой: p=0,048 при сравнении пациентов, регулярно принимавших базисную терапию, p=0,043 — в группах больных, допускавших периодические пропуски, p=0,036 — среди респондентов, не принимавших препараты (рис. 1).
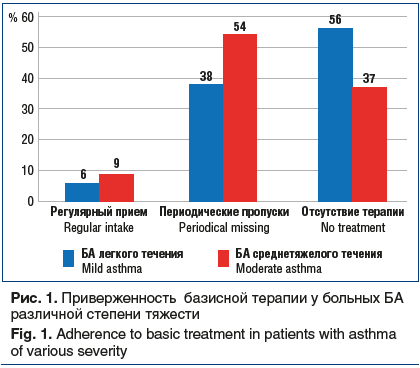
При оценке приверженности лечению в группе больных БА легкого течения с помощью опросника MMAS-6 у 94,1% больных выявлена низкая приверженность терапии, которая сформирована за счет пропуска препарата при хорошем самочувствии у 83,8% человек и невнимательности к часам приема лекарств у 60,3% респондентов. Также 18 (26,5%) пациентов пропускали следующий прием при плохом самочувствии после приема препарата. Низкая мотивация зарегистрирована у 48 (70,6%) больных, преимущественно за счет пропуска приема лекарственных препаратов у 47 (97,9%) человек и невнимательности к часам приема у 40 (83,3%) пациентов. У 45 (66,2%) респондентов отмечалась низкая осведомленность о своем заболевании.
При оценке приверженности терапии в группе больных БА среднетяжелого течения с помощью опросника MMAS-6 у 91% больных выявлена низкая приверженность терапии, которая сформирована за счет пропуска препарата при хорошем самочувствии у 79,5% пациентов и невнимательности к часам приема лекарств у 61,5% респондентов. Пропускали следующий прием при плохом самочувствии после приема препарата 19 (24,4%) человек. Низкая мотивация зарегистрирована у 61 (78,2%) больного, преимущественно за счет пропуска приема лекарственных препаратов у 54 (88,5%) человек и невнимательности к часам приема у 49 (80,3%) пациентов. У 32 (41%) респондентов отмечалась низкая осведомленность о своем заболевании (табл. 1).
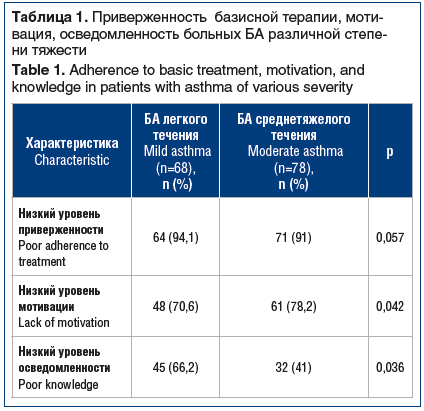
Таким образом, пациенты группы БА легкого течения были менее осведомлены о своем заболевании в сравнении с больными со среднетяжелым течением заболевания. Во 2-й группе несколько чаще встречались пациенты, имевшие низкий уровень мотивации к приему лекарств. Среди обследованных больных вне зависимости от степени тяжести отмечался крайне высокий процент больных с низкой приверженностью лечению и самостоятельно отменяющих прием базисной терапии при улучшении самочувствия. Одним из ключевых факторов, способствующих снижению приверженности лечению, является невысокий уровень знаний пациентов о заболевании и недостаточная информированность о важности регулярной базисной терапии в долгосрочной перспективе.
Заключение
Течение БА крайне вариабельно, степень тяжести заболевания может меняться на протяжении месяцев и лет. Наряду с достижением контроля над симптомами заболевания у многих больных в большей степени возникают сложности в поддержании данного состояния в течение длительного времени. Основными причинами отсутствия контроля у пациентов с БА являются: низкая приверженность регулярной базисной терапии и неправильная техника ингаляции. В настоящем исследовании вне зависимости от тяжести БА у 92% пациентов молодого возраста установлена низкая приверженность лечению. Таким образом, актуальными на сегодняшний день остаются вопросы разработки новых терапевтических подходов, которые, возможно, будут способствовать более высокой приверженности пациентов лечению.
Кроме того, у 52% больных выявлен невысокий уровень осведомленности о своем заболевании. На сегодняшний день активно функционируют школы для больных БА, целью которых является расширение знаний пациентов об астме и разъяснение факторов риска, определяющих развитие осложнений заболевания. Однако сохраняющийся низкий уровень приверженности пациентов лечению свидетельствует о том, что деятельность астма-школ оказывает умеренное положительное действие, которое длится короткий период [10].
Подводя итоги, необходимо отметить, что в настоящее время требуются разработка и совершенствование программ, направленных на поддержание уровня знания пациентов, приобщение их к проведению самооценки и самоконтроля. При этом подход к проблеме комплаентности больных молодого возраста должен осуществляться с двух сторон: как со стороны специалиста, так и со стороны пациента. Обучение основам коммуникации и мотивации, тактика персонализированного подхода и внедрение компьютерных технологий являются на сегодняшний день приоритетными задачами для здравоохранения с целью повышения приверженности лечению и контроля над симптомами БА.
Источник финансирования
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 19–315–90030.
Funding
The study is partially supported by RFBR, research project No. 19–315–90030.
Сведения об авторах:
Леонтьева Нигора Минавваровна — аспирант, младший научный сотрудник кафедры внутренних болезней и иммунологии с курсом постдипломного образования, ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого Минздрава России, 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; врач функциональной диагностики, КГБУЗ ККБ, 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 3А; ORCID iD 0000-0001-8915-5153.
Демко Ирина Владимировна — д.м.н., профессор, заведующая кафедрой внутренних болезней и иммунологии с курсом постдипломного образования, ФГБОУ ВО КрасГМУ
им. проф. В.Ф. Войно-Ясенецкого Минздрава России, 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; заведующая легочно-аллергологическим центром, КГБУЗ ККБ, 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 3А; ORCID iD 0000-0002-2186-1876.
Собко Елена Альбертовна — д.м.н., профессор кафедры внутренних болезней и иммунологии с курсом постдипломного образования, ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого Минздрава России, 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; заведующая отделением аллергологии, КГБУЗ ККБ, 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 3А; ORCID iD 0000-0003-3153-899X.
Ищенко Ольга Петровна — к.м.н., ассистент кафедры внутренних болезней и иммунологии с курсом постдипломного образования, ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого Минздрава России, 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; врач-аллерголог, КГБУЗ ККБ, 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 3А; ORCID iD 0000-0002-1784-9356.
Контактная информация: Леонтьева Нигора Минавваровна, e-mail: nigora-razzakova@rambler.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 08.06.2020, поступила после рецензирования 16.07.06.2020, принята в печать 29.07.2020.
About the authors:
Nigora M. Leont’eva — postgraduate student, junior researcher of the Department of Internal Diseases and Immunology and the Course of Postgraduate Education, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University, 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; diagnostician, Territorial Clinical Hospital, 3A, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0001-8915-5153.
Irina V. Demko — Dr. of Sci. (Med.), Professor, Head of the Department of Internal Diseases and Immunology and the Course of Postgraduate Education, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University, 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; Head of Pulmonary Allergic Center, Territorial Clinical Hospital, 3A, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0002-2186-1876.
Elena A. Sobko — Dr. of Sci. (Med.), Professor of the Department of Internal Diseases and Immunology and the Course of Postgraduate Education, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University, 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; Head of the Department of Allergy, Territorial Clinical Hospital, 3A, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0003-3153-899X.
Olga P. Ishchenko — Cand. of Sci. (Med.), Assistant of the Department of Internal Diseases and Immunology and the Course of Postgraduate Education, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University, 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; allergist, Territorial Clinical Hospital, 3A, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0002-1784-9356.
Contact information: Nigora M. Leont’eva, e-mail: nigora-razzakova@rambler.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 08.06.2020, revised 16.07.06.2020, accepted 29.07.2020.
.
Информация с rmj.ru