Введение
Согласно современным представлениям спондилоартриты относятся к неоднородной группе заболеваний, объединенных общими патогенетическими механизмами и схожими симптомами. В соответствии с современной классификацией выделяют периферический спондилоартрит и аксиальный спондилоартрит, который, в свою очередь, подразделяется на нерентгенологический аксиальный спондилоартрит и анкилозирующий спондилит (АС) [1].
Анкилозирующий спондилит — хроническое иммуновоспалительное заболевание из группы спондилоартритов, характеризующееся обязательным поражением крестцово-подвздошных суставов (КПС) и/или позвоночника с потенциальным исходом их в анкилоз, с частым вовлечением в патологический процесс энтезисов и периферических суставов [1].
В диагностике ревматических заболеваний решающее значение имеют тщательно собранные жалобы, анамнез заболевания, данные объективных методов исследования.. Особое внимание следует уделять характеру болевого суставного синдрома. Так, при ревматических заболеваниях в большинстве случаев болевой синдром имеет воспалительный характер, в то время как для дегенеративно-дистрофических процессов характерна боль механического характера. Характеристика болевого синдрома чрезвычайно важна при дифференциальной диагностике спондилоартритов и дегенеративно-дистрофического поражения позвоночника (остеохондроза). После выявления признаков спондилоартрита его целесообразно рассматривать как недифференцированный и в дальнейшем действовать в соответствии с клиническими рекомендациями.
Диагностика АС преимущественно основывается на характерных жалобах пациента, таких как боль «воспалительного» характера в нижней части спины и других отделах позвоночного столба согласно критериям ASAS (2009), и подтвержденном лучевыми методами исследования двустороннем сакроилиите [2]. При этом такие лабораторные показатели, как СОЭ и уровень С-реактивного белка (СРБ), не имеют самостоятельного диагностического значения, но необходимы для оценки прогноза заболевания и выбора тактики ведения пациента [2, 3].
Немаловажное значение в диагностике как нерентгенологического аксиального спондилоартрита, так и АС имеют внеаксиальные проявления заболевания: периферические асимметричные моноолигоартриты, энтезиты, увеиты, дактилиты [2].
Поражение периферических суставов в дебюте АС имеет неблагоприятный прогноз, и одним из его грозных факторов при АС является коксит, приводящий к развитию осложнения в виде коксартроза, как правило, с выраженным болевым синдромом, с нарушением функции тазобедренного сустава (ТБС), что в дальнейшем требует проведения эндопротезирования.
Комплексный подход к диагностике АС и его осложнений на ранних этапах заболевания позволяет в кратчайшие сроки определить тактику ведения пациента, способствуя снижению уровня инвалидизации и повышению качества жизни пациента.
Независимо от активности заболевания, наличия осложнений безальтернативным является длительный прием различных групп НПВП как в сочетании с генно-инженерными биологическими (ингибиторы фактора некроза опухоли α (иФНО-α), ингибиторы интерлейкина-17А) и синтетическими таргетными препаратами (ингибиторы янус-киназ), так и без них [3–6]. В то же время длительное применение системных кортикостероидов не рекомендовано при лечении АС независимо от наличия внеаксиальных проявлений и характера развившихся осложнений [7].
В лечении периферических артритов следует использовать сульфасалазин (в дозе до 3 г/сут) с оценкой эффективности терапии не менее чем через 3 мес. [8, 9]. При сохранении высокой активности заболевания на фоне приема НПВП и сульфасалазина в максимально переносимых дозах рекомендовано как можно раньше назначать терапию иФНО-α или ингибиторами ИЛ-17. Эффективность генно-инженерной биологической терапии выше на ранней стадии болезни и при ее высокой активности.
Следует отметить, что у пациентов с достоверным диагнозом АС при наличии быстропрогрессирующего коксита рекомендовано инициировать терапию генно-инженерными биологическими препаратами без учета активности болезни [10, 11].
Представляем клиническое наблюдение пациента с АС с двусторонним кокситом, потребовавшим выполнения тотального эндопротезирования ТБС.
Клиническое наблюдение
Пациент Ч., 34 года. Наблюдается в клинике факультетской терапии с декабря 2020 г. Поступил с жалобами на боль в левом ТБС в покое, усиливающуюся при движении, боль в правом плечевом суставе, общую слабость.
Из анамнеза известно, что в 2018 г. впервые появилась боль в левом ТБС. По данному поводу лечился и обследовался в терапевтическом отделении с диагнозом: реактивный артрит неуточненной этиологии с системными проявлениями (снижение массы тела, анемия), полиартрит, острое течение, 3-й степени активности. Из инструментальных исследований выполнена рентгенография левого ТБС — патологии не выявлено (из выписного эпикриза), по остальным исследованиям сведения отсутствуют. Проводилось лечение: преднизолон 40 мг/сут, диклофенак 150 мг/сут, азитромицин 500 мг/сут № 3 — с положительным эффектом. В дальнейшем по рекомендации врача снизил суточную дозу преднизолона до 2,5 мг. При попытке полной его отмены проявления артрита возобновились.. В динамике, несмотря на соблюдение рекомендаций (прием преднизолона, сульфасалазина 2 г/сут), рецидивировал болевой суставной синдром в ТБС, больше слева, появилась боль в плечевых суставах, стал отмечать уменьшение мышечной массы левой нижней конечности. Последняя госпитализация в терапевтическое отделение была 26.10.2020 с диагнозом: основным — реактивный артрит неуточненной этиологии, полиартрит, острое течение, 3-й степени активности; двусторонний сакроилиит; функциональная недостаточность сустава II; сопутствующим — остеоартроз правого тазобедренного сустава 2-й степени, левого тазобедренного сустава 3-й степени.
Проведено обследование, по результатам которого выявлена высокая острофазовая активность заболевания: в клиническом анализе крови — гемоглобин 124–130 г/л, лейкоциты 10,4–14×109/л, СОЭ 47–60 мм/ч, в биохимическом анализе крови — СРБ 48 мг/л, фибриноген 9,1 г/л. Также выявлены антитела (IgА) к Ureaplasma urealyticum.
По данным МРТ тазобедренных суставов (30.10.2020) выявлены изменения, характерные для двустороннего далеко зашедшего коксита с явлениями деструкции ТБС, более выраженные слева: суставная щель значительно неравномерно сужена, головка левой бедренной кости умеренно деформирована за счет уплощения суставной поверхности, по краю крыши вертлужной впадины и головки бедренной кости определяются краевые остеофиты, кортикальная пластинка по суставным поверхностям головки бедренной кости и вертлужной впадины — с наличием глубоких эрозий. Структура костного мозга головки и шейки левой бедренной кости, а также прилежащих отделов вертлужной впадины — с зонами отека трабекулярной костной ткани. Гиалиновый хрящ неравномерно истончен, визуализируется фрагментарно. В полости сустава незначительное количество выпота, синовиальная оболочка неравномерно утолщена.. Справа: хрящевой компонент истончен, МР-сигнал от него снижен, по краю крыши вертлужной впадины и головки бедренной кости определяются краевые остеофиты. Структура костного мозга головки и шейки левой бедренной кости, а также прилежащих отделов вертлужной впадины — с зонами отека трабекулярной костной ткани. Кортикальная пластинка по суставным поверхностям головки бедренной кости и вертлужной впадины — с наличием немногочисленных эрозивных дефектов.. Заключение: МР-картина остеоартроза тазобедренных суставов, справа — II стадии, слева — III стадии (снимки пациентом не представлены).
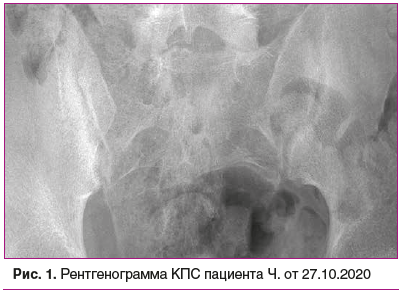
Также выполнена рентгенография КПС (27.10.2020).
На рентгенограмме (рис. 1) определяется чередование участков расширения и сужения рентгеновской суставной щели, неровность контуров КПС с обеих сторон. Выраженный субхондральный склероз подвздошной кости.. Заключение: двусторонний сакроилиит.
Проведенное лечение: преднизолон 40 мг/сут, сульфасалазин 2 г/сут — без эффекта.
При поступлении в клинику факультетской терапии Военно-медицинской академии имени С.М. Кирова в ноябре 2020 г. дополнительно выполнена рентгенография ТБС (рис. 2, А, В).
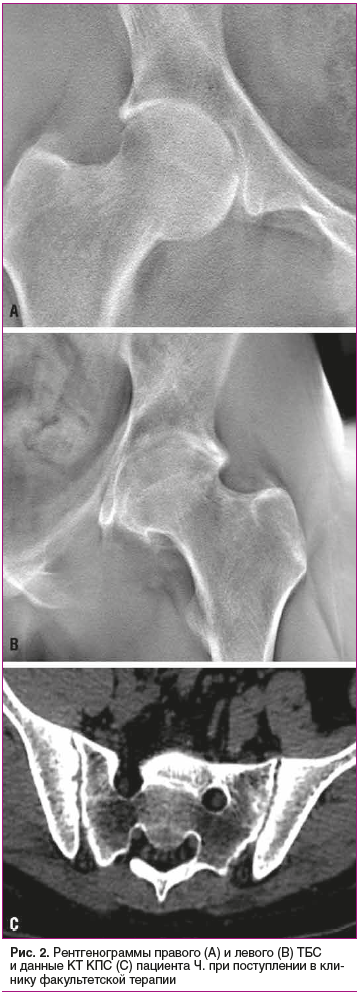
Выявлено значительное сужение суставной щели, уплощение крыши вертлужной впадины, наличие глубоких эрозий в кортикальной пластинке по суставным поверхностям головки бедренной кости и вертлужной впадины.
Также пациенту выполнена КТ КПС (рис. 2, С). На представленных томограммах визуализируется чередование участков расширения и сужения рентгеновской суставной щели, а также множественные эрозии подвздошной кости с обеих сторон.
По результатам обследования критериально установлен диагноз: анкилозирующий спондилит, развернутая стадия, активность высокая (ASDASCRP — 3,03, BASDAI — 3,6), с внеаксиальными (двусторонний коксит) проявлениями, HLA-В27-позитивный, функциональный класс 2. Осложнение: двусторонний коксартроз III стадии с преимущественным поражением левого тазобедренного сустава с выраженным болевым синдромом. Комбинированная контрактура тазобедренных суставов.
В связи с неэффективностью комбинированной терапии НПВП и БПВП (сульфасалазин в дозе 2–3 г/сут в течение 3 мес.), быстропрогрессирующим кокситом, высокой активностью заболевания пациенту инициирована генно-инженерная биологическая терапия. Для достижения быстрого эффекта и уменьшения прогрессирования заболевания выбран иФНО-α цертолизумаба пэгол в виде двух инъекций по 200 мг в первый день, на 2-й
и на 4-й неделе лечения, в дальнейшем по 400 мг 1 р/мес. подкожно.
Посредством проводимой терапии в январе 2021 г. удалось достигнуть низкой активности заболевания (ASDASCRP — 0,97, BASDAI — 2,8). После достижения низкой активности заболевания в феврале 2021 г. пациенту успешно проведено эндопротезирование левого ТБС (рис. 3).
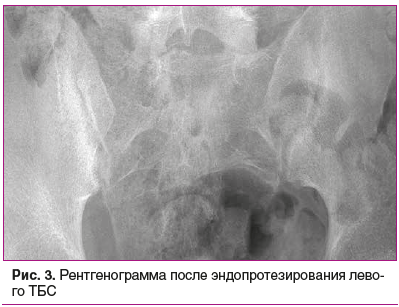
В настоящее время, согласно данным контрольного обследования, признаков прогрессирования заболевания не выявлено, клинически значительно уменьшились спондилоалгии в поясничном отделе позвоночника, увеличился объем движений в левом ТБС, острофазовая активность снизилась, продолжено динамическое наблюдение.. С учетом тяжелого поражения (анкилоз) правого ТБС в ближайшее время планируется оперативное вмешательство — тотальное эндопротезирование пораженного сустава.
Обсуждение
В рамках представленного клинического наблюдения хотелось бы акцентировать внимание на важности как можно более ранней диагностики данной патологии и своевременного назначения противовоспалительной базисной иммуносупрессивной и генно-инженерной биологической терапии, которая данному пациенту в дебюте заболевания не назначалась. Этот факт в последующем повлиял, вероятно, на быстрое прогрессирование болезни с формированием анкилоза обоих ТБС.. В конечном итоге потребовалось применение высокотехнологичных дорогостоящих методов лечения (генно-инженерная биологическая терапия, тотальное эндопротезирование суставов) с целью купирования острофазовой активности заболевания, болевого синдрома, восстановления утраченных функций ТБС. Вероятно, при более ранней диагностике данного заболевания удалось бы избежать применения тяжелого оперативного вмешательства, а также значительно уменьшить материальные затраты на лечение..
Выводы
Несвоевременное установление правильного диагноза АС приводит к быстрому прогрессированию заболевания и инвалидизации лиц молодого возраста.
Использование современных высокотехнологичных методов лечения (генно-инженерная биологическая терапия) при отсутствии эффекта от стандартной базисной терапии в сочетании с глюкокортикостероидами позволяет в сокращенные сроки замедлить прогрессирование болезни и достичь эффективного контроля над заболеванием в динамике.
Своевременно выполненное на данном этапе эндопротезирование тазобедренного сустава [12] позволило значительно улучшить качество жизни молодого пациента.
.
Информация с rmj.ru


