Результаты органосохраняющего хирургического лечения труднорубцующихся язв желудка
С.Н. Серикова
ГБОУВПО «Кубанский государственный медицинский университет» КубГМУ Минздравсоцразвития России (ректор — С.Н. Алексеенко);
МБУЗ Городская больница № 2 Краснодарское многопрофильное лечебно-диагностическое отделение (главный врач — Г.А. Пенжоян)
Резюме: Проведена комплексная оценка морфологических и функциональных результатов органосохраняющего оперативного лечения труднорубцующихся язв желудка методом гастропластики по В.И. Оноприеву в зависимости от способа её выполнения. Изучены две группы пациентов: первая группа — 74 пациента, перенёсшие гастропластику с инвагинационным корпоро-антральным анастомозом; вторая группа — 30 пациентов после гастропластики с формированием корпоро-антрального сфинктера из петли тощей кишки. Анализ исследований показал, что в течение года после операции происходит восстановление функционального состояния оперированного желудка, улучшение макро- и микроскопической структуры слизистой, что обусловлено адекватными моторной и эвакуаторной функциями вновь созданных анастомозов. В отдалённом послеоперационном периоде технология гастропластики с формированием корпоро-антрального сфинктера из петли тощей кишки имела ряд преимуществ перед своим аналогом гастропластикой с инвагинационным корпоро-антральным сфинктером. Создаваемая мышечная манжетка из петли тонкой кишки препятствует расширению желудочной трубки; обеспечивает порционное поступление пищевых масс в антральный отдел желудка, предотвращая его перегрузку. При этом наблюдалась тенденция к восстановлению пищевой рецептивной релаксации проксимального отдела желудка, что улучшало субъективный статус пациентов и повышало уровень качества жизни.
Ключевые слова: труднорубцующаяся язва желудка, гастропластика, результаты оперативного лечения.
Введение
По данным различных авторов, встречаемость труднорубцующихся язв желудка (ТЯЖ) колеблется от 10 до 23% [4,6,33,34]. Многократное не эффективное консервативное лечение ТЯЖ приводит у 8-20% пациентов к позднему обращению в хирургическую клинику уже с развившимися осложнениями [7,23]. В настоящее время нет сомнений в том, что рост экстренных операций по поводу осложнений язвенной болезни желудка (ЯБЖ) и увеличение послеоперационной летальности при кровоточащих язвах желудка напрямую зависит от снижения числа плановых оперативных вмешательств [14, 25, 31]. В условиях ургентной хирургии арсенал методов оперативного лечения ЯБЖ включает резекцию желудка, стволовую ваготомию [10,11,29], после которых у 25 — 45% пациентов развиваются пострезекционные и постваготомические расстройства, ухудшающие функциональные результаты этих вмешательств [13,19,36]. При плановом вмешательстве операцией выбора являются органосберегающие технологии. Частота рецидива язвенной болезни в опытных руках хирурга составляет 1,5 — 2% в сроки более 10 лет после операции [8,28]. В.И.Оноприевым и соавт. [21] была разработана органосохраняющая технология хирургического лечения ЯБЖ — сегментарная гастропластика (ГП), восстанавливающая и корригирующая основные функции гастродуоденального комплекса (ГДК), что улучшает субъективный статус пациентов и обеспечивает высокий уровень качества жизни (КЖ) в различные сроки после операции.
Цель исследования: дать комплексную морфологическую и функциональную характеристику результатов органосохраняющего хирургического лечения методом ГП у пациентов с ТЯЖ.
Материал и методы. Работа основана на результатах морфологических и функциональных исследований 104 пациентов с ТЯЖ (желудочные язвы, которые не показали существенной динамики заживления на фоне адекватной медикаментозной терапии в течение 8 недель при исключении их симптоматического характера), оперированных в плановом порядке в Российском центре функциональной хирургической гастроэнтерологии в 2002-2008 годы. Все пациенты получали медикаментозную терапию согласно Федеральному стандарту по ведению пациентов с ЯБЖ (№ 241 от 2004 г., № 612 от 2007 г.), включающему приём ингибиторов протонной помпы (омепразол 20 мг, эзомепразол 20 мг, рабепразол 10 мг) 2 раза в сутки в течение 8 недель. При подтверждении двумя из перечисленных методов (дыхательный, гистологический, иммуноферментный) контаминации СОЖ HP — инфекцией проводили эрадикационную терапию согласно рекомендациям Российского общества гастроэнтерологов, основанных на рекомендациях европейских консенсусов (Маастрихтское соглашение 2000 — 2005 гг.). В комплексное лечение больных включали цитопротективную терапию висмут трикалия дицитратом (120 мг 4 раза в день 4 недели), при необходимости прокинетики (домперидон) в суточной дозе 40 мг (в течение 4 недель), антациды применялись в качестве симптоматических средств «по требованию». Выделены две группы больных: первая группа — 74 пациента, перенёсшие ГП с инвагинационным корпоро-антральным анастомозом (КАА); вторая группа — 30 пациентов после ГП с формированием корпоро-антрального сфинктера (КАС) из петли тощей кишки. Показаниями к органосохраняющему хирургическому лечению ТЯЖ стали выявленные нами на этапе дооперационного обследования морфофункциональные предикторы неэффективности медикаментозного лечения: дисплазия высокой степени в дне и краях язв у 30,8% (32 чел.), пенетрация язвы у 43,3% (45), сочетание язв с кардиофундальными и фундокорпоральными грыжами пищеводного отверстия диафрагмы (ГПОД) у 26% (27), повторные кровотечения в анамнезе у 35,6% (37). Осложнения ЯБЖ, встречавшиеся у больных с ТЯЖ на момент операции (пенетрация в поджелудочную железу, печень, малый сальник) и в анамнезе (кровотечение) были сопоставимы по группам (таблица 1). Больные, поступающие на оперативное лечение по поводу таких осложнений ЯБЖ как кровотечение и прободение были исключены из исследования. Возраст пациентов был от 31 до 70 лет (средний — 54,2±11,2 года). Длительность язвенного анамнеза до операции значимо чаще была более 2 лет у 70 (67,3%) больных, анамнез ЯБЖ до 2 лет у 34 (32,7%) пациентов. По размеру ТЯЖ были в основном большими (1,1 — 3 см) у 76,9% и гигантскими (более 3 см) у 17,3% больных, медиогастральная локализация была у 99 (95,2%) пациентов, язвы кардии — у 5(4,8%) больных.
Таблица 1. Осложнения язвенной болезни желудка из анамнезу по группам
| Осложнения чел, (%) |
I А группа, n=74 чел. (%) |
I Б группа, n=30 чел. (%) |
Всего, n=104 чел. (%) |
| Кровотечение в анамнезе |
26(35,1) |
11(36,7) |
37(35,6) |
| Пенетрация |
34(45,9) |
11(36,7) |
45(43,3) |
В контрольную группу вошли 20 человек, признанные здоровыми по результатам лабораторных и инструментальных методов исследования (для установления нормативных показателей периодической моторной деятельности ГДК и определения популяционной нормы параметров КЖ). Условно — контрольная группа (20 человек) — больные с хроническими гастроэнтерологическими заболеваниями без язвенного повреждения СОЖ.
ГП по В.И. Оноприеву представляет собой способ хирургического лечения ЯБЖ, включающий сегментарную резекцию тела желудка с удалением проксимальной части малой кривизны и сохранением иннервации пилороантрального отдела. Главным отличием ГП от существовавших ранее методик является формирование арефлюксного трубчатого гастрогастрального анастомоза, выполненного двумя способами: инвагинационный КАА (Рис. 1) или КАС из петли тощей кишки (Рис. 2). Обязательным моментом ГП является восстановление замыкательной функции кардии. Это достигается путём создания новых анатомических взаимоотношений между пищеводом, кардией и желудком в форме эзофаго-кардио-гастрального клапана методом боковой инвагинации с восстановлением пищеводно-диафрагмальной, диафрагмально-фундальной связок и угла Гиса.
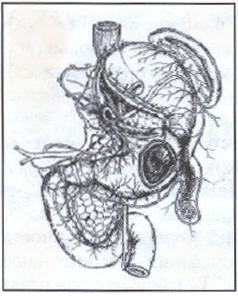
Рис. 1. Окончательный вид желудка после выполненной гастропластики с инвагинационным корпоро-антральным анастомозом по В.И. Оноприеву
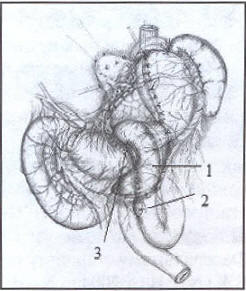
Рис. 2. Сформированы корпоро-антральный и межкишечный анастомозы. 1 — петля тощей кишки, 2 — корпоро-антральный анастомоз, 3 — межкишечный анастомоз «бок в бок»
Сроки динамического диспансерного наблюдения за прооперированными больными указаны в таблице 2. Пациентам проводилось комплексное исследование, которое включало гастродуоденоскопию, исследование желудочной секреции методом рН-метрии и аспирационно-зондовым методом, рентгенологическое исследование, исследование моторной функции желудка методом открытых катетеров и морфологическое исследование гастробиоптатов СОЖ с последующей оценкой интегральных показателей по визуально-аналоговой шкале, утверждённой решением Ш съезда Российского общества патологоанатомов 2009 г. (Российский пересмотр международной классификации OLGA-2008) [3]. Параметры КЖ пациентов оценивали по опроснику MOS-SF-36. Статистическая обработка данных проводилась с помощью программы STATISTICA 6.0.
Таблица 2. Распределение больных по длительности наблюдения после операции
| Всего
прооперировано, чел. (%) |
Сроки наблюдения |
||||
|
через 3 месяца |
через 6 месяцев |
через 1 год |
через 2-5 лет, |
через 5,1-10 лет |
|
| 1 группа-74(100) |
66(89,2) |
61 (82,4) |
58(78,4) |
44(59,5) |
39(52,7) |
| 2 группа-30(100) |
27(90,0) |
25(83,3) |
23 (76,7) |
20(63,3) |
10(33,3) |
Результаты и их обсуждение
Ранние послеоперационные осложнения, встречающиеся после хирургической технологии ГП по В.И. Оноприеву с формированием антирефлюксного гастро-гастрального анастомоза двумя способами указаны в таблице 3. Явлений несостоятельности швов и анастомозита мы не наблюдали. Летальных исходов не было.
Таблица 3. Осложнения раннего послеоперационного периода по группам
| Вид осложнений |
I A группа n=74, чел.(%) |
І Б группа n=30, чел.(%) |
| Панкреатит |
6(8,1) |
2(6,6) |
Гнойно-септические осложнения:
|
5(6,7) 4(5,4) |
3(10,0) 1(3,3) |
| Пневмония |
2(2,7) |
1(3,3) |
| Тромбофлебит подкожных вен голени |
2(2,7) |
0 |
| Всего пациентов с осложнениями |
8(10,8) |
4(13,3) |
По результатам эндоскопических исследований у пациентов с ТЯЖ до операции выявлена недостаточность нижнего пищеводного сфинктера у 100% больных и грыжи пищеводного отверстия диафрагмы (ГПОД) у 26% больных. Это способствовало развитию у всех пациентов рефлюксных поражений слизистой пищевода различной степени выраженности от неэрозивного до эрозивного эзофагита. Результаты эндоскопических исследований в течение всего периода послеоперационного наблюдения свидетельствуют о достоверном улучшении макроскопической структуры слизистой оперированного желудка, что обусловлено адекватной функцией вновь созданных анастомозов и проведённым предоперационным медикаментозным лечением. В период диспансерного наблюдения плотное смыкание кардии после операции наблюдалось у всех больных второй группы и большинства пациентов первой группы (95,5%-94,8%). Через 2-5 лет и более была выявлена недостаточность кардии у 5 (14,1 %) пациентов (4(9,1 %) чел. из первой группы и 1(5%) чел. из второй группы). В 2 случаях (1,9% от всех прооперированных пациентов) диагностирован рецидив ГПОД. Через 3 месяца после операции отмечалась положительная динамика со стороны патологически измененной слизистой пищевода: неэрозивный эзофагит диагностирован у 5(7,6%) пациентов первой группы. У 2(7,4%) больных второй эрозивный эзофагит не выявлен. Данная тенденция сохранялась и в более отдаленные сроки после операции, через два года только у 1 (2,3%) больного с рецидивом ГПОД был выявлен эрозивный эзофагит. Через три месяца после операции деструктивно-воспалительные изменения СОЖ и двенадцатиперстной кишки (ДПК) не прогрессировали, что свидетельствовало об оптимальном выборе схем предоперационной подготовки, позволивших снизить уровень хирургической агрессии и обеспечить гладкое течение послеоперационного периода. Эта тенденция сохранялась в период до 2 — 5 лет. Выявленный в этот период эрозивные гастрит (бульбит) у 5(11,4%) пациентов первой группы и 4(20%) пациентов второй был ассоциирован с Helicobacter pylori. HP — инфекция диагностирована и пролечена у 81% (60 чел.) и 70% (21 чел.) больных до операции соответственно первой и второй групп. У 1 больного из первой группы в раннем послеоперационном периоде была выявлена язва кардиальном отделе желудка, возникшая сразу после операции в результате недостаточности кровоснабжения СОЖ, связанной с ошибками мобилизации в ходе операции фундального отдела желудка, зарубцевавшаяся после назначения медикаментозной терапии.
Частота выраженного дуоденогастрального рефлюкса (ДГР), диагностированного до операции у 35,1% и 40% пациентов соответственно первой и второй групп, достоверно уменьшилась через 1 год после операции до 13,8%(8 чел.) и 4,3%(1 чел.) соответственно. Заброс желчи в просвет проксимальной культи желудка в указанные сроки после ГП выявлен не был. В отдалённом послеоперационном периоде (через 5,1-10 лет) выраженный ДГР определялся только у 6(15,4%) пациентов первой группы (у 2 из них был выявлен желчный антрофундоантральный рефлюкс). Полученные результаты свидетельствуют о выраженных арефлюксных свойствах гастрогастрального анастомоза.
Проведённое нами морфологическое исследование СОЖ у пациентов с ТЯЖ после курса предоперационной подготовки и планового органосохраняющего хирургического лечения методом ГП по В.И. Оноприеву позволило оценить эффективность комплексного лечения и осуществить мониторинг пациентов с пренеопластическими изменениями: атрофия, кишечная метаплазия (КМ). При сопоставительном анализе гистологической и гистохимической картины гастробиоптатов по группам оказалось, что статистически значимых различий между группами прооперированных пациентов не наблюдалось. До 2 лет после операции активность (в виде лейкоцитарной инфильтрации) хронического гастрита (ХГ) отсутствовала, как и до операции, что было связано с проведённым медикаментозным лечением. В обеих группах выраженность лимфоцитарной инфильтрации оперированного желудка неуклонно уменьшалась с 92,3% до операции до 56,4% — после. В более отдалённом периоде появление лейкоцитарной активности в антральном отделе желудка (АОЖ) у 40% пациентов и наличие лимфоцитарной инфильтрации у 38,8% в СОЖ было связано с рецидивом HP — инфекции или реинфекцией (через 2-5 лет у 37,8% больных, через 5,1 — 10 лет у 38,8% больных от всех наблюдаемых пациентов в указанные периоды). Наши результаты коррелируют с данными литературы о том, что со временем закономерно наблюдается реинфекция HP [5,35]. Оценка трансформации атрофии и КМ СОЖ в оперированном желудке только через 5,1 — 10 лет выявила достоверное увеличение КМ I типа (43,6% против 27,3% до операции) в АОЖ у больных первой группы, что свидетельствует о нарастании атрофических процессов в СОЖ в отдалённом послеоперационном периоде. По данным исследователей частота встречаемости КМ после резекции желудка составляет 70% и более [2,18]. Одной из причин развития и прогрессирования КМ в послеоперационном периоде является нарушение иннервации СОЖ [30].
Для объективизации результатов хирургического лечения ТЯЖ методом ГП по В. И. Оноприеву и оценки кумулятивного риска рака в резецированном желудке мы сравнили динамику степени и стадии ХГ у 49 больных (39 чел. первой группы и 10 чел. — второй) через 5,1-10 лет после операции с аналогичными показателями у пациентов с ТЯЖ до операции (104 чел.), а также с результатами гистологического исследования гастробиоптатов у обследуемых в условно-контрольной группе. При этом мы использовали визуально-аналоговую шкалу, утверждённую решением III съезда Российского общества патологоанатомов, Самара-2009 (Рис. 3). По результатам наших исследований кумулятивный риск РЖ через 5,1-10 лет после хирургического лечения методом ГП по В.И. Оноприеву не увеличивался. Статистически значимое увеличение атрофии в прооперированном желудке у 42,9% больных против 23,1 % пациентов до операции происходило за счёт хронического атрофического гастрита (ХАГ) I стадии (при этом встречаемость ХАГ III-IV стадии была сопоставима с дооперационной). Сравнительный анализ морфологических изменений СОЖ в отдалённом (через 5,1-10 лет) послеоперационном периоде с пациентами условно-контрольной группы показал, что имеющаяся трансформация СОЖ соответствуют изменениям СОЖ у больных, сопоставимых по полу и возрасту с гастроэнтерологическими заболеваниями без язвенного анамнеза.
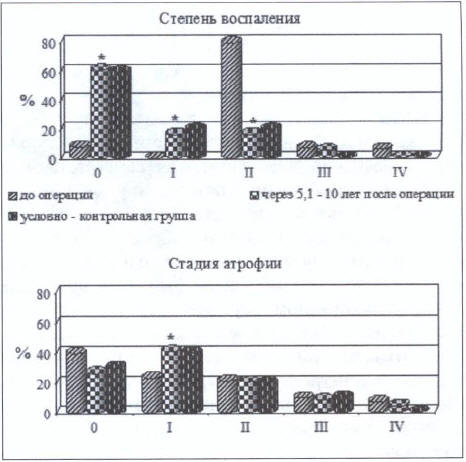
Рис. 3. Сравнительная оценка степени и стадия хронического гастрита у пациентов с ТЯЖ до, после гастропластики и условно — контрольной группой, «*» -отмечены достоверные отличия от показателей до операции (р<0,05)
Таким образом, проведенное морфологическое исследование СОЖ у пациентов с ТЯЖ в различные сроки после ГП по В.И. Оноприеву независимо от способа формирования гастро-гастрального анастомоза продемонстрировало, что комплексное медикаментозное и хирургическое лечение влияет на течение ХГ следующим образом: уменьшается выраженность активности воспаления в СОЖ, прогрессируют атрофические процессы в АОЖ, что подтверждалось достоверным увеличением частоты КМ I типа. Кумулятивный риск рака желудка в отдалённые сроки после ГП по В.И. Оноприеву не увеличивался.
Важными критериями оценки отдалённых результатов после ГП являются показатели функционального состояния ГДК По данным литературы оптимальным является такой уровень остаточной кислотности резецированного желудка, при котором сохраняется желудочный тип пищеварения в культе и минимизирована угроза появления пептической язвы [ 13,19]. Вовремя ГП по В.И. Оноприеву осуществляется деваскуляризация и денервация кислотопродуцирующей зоны по типу селективной проксимальной ваготомии и резекция проксимальной части малой кривизны желудка, это приводит к снижению желудочной секреции в теле желудка, не достигая ахлоргидрии.
У больных с ТЯЖ кислотообразование повышенной и нормальной концентрации и интенсивности было выявлено у 20,2% и 32,7% пациентов, гипоацидность в базальном и стимулированном периодах наблюдалась у 47,1% больных. Изучение кислотообразующей функции желудка методом рН-метрии по периодам наблюдения после операции (через 1 год, 2 — 5 лет, 5,1 — 10 лет) выявило достоверное снижение секреторной функции желудка, характеризующееся кислотообразование пониженной концентрации, пониженной интенсивности у 80-82% пациентов и нормальной интенсивности у 18-20% больных, т.е. кислотообразование сохраняется, но снижается его концентрация. По данным аспирационно-зондового метода продукция хлористоводородной кислоты снижается в большей степени, чем пепсина. Базальное кислотообразование отсутствовало у 10,3% (4 чел.) и 10% (1 чел.) больных из 1 и 2 групп соответственно. Гистаминорефрактерной ахлоргидрии не было ни в одном случае. Таким образом, сохранение АОЖ во время ГП является важнейшим фактором, позволяющим предотвратить развитие атрофических процессов в слизистой оболочке ФОЖ и сохранить секрецию соляной кислоты и пепсинов на оптимально низком уровне. Кроме того, в АОЖ осуществляется синтез факторов защиты, способствующих предотвращению рецидива язвообразования [17].
В органосохраняющем подходе к проблеме хирургического лечения ЯБЖ приоритетна концепция выполнения кислоторедуцирующих операций при максимальном сохранении естественных анатомических и функциональных механизмов желудочной моторики [21]. Результаты исследования моторной и эвакуаторной функций оперированного желудка играют важную роль в изучении патогенеза развития послеоперационных патологических синдромов и в достижении оптимальных результатов оперативного лечения [9,13,22]. По мнению исследователей, большинство функциональных послеоперационных расстройств обусловлено исходными нарушениями моторной деятельности желудка и ДПК, а также погрешностями техники оперативного вмешательства, связанными с нарушением иннервации АОЖ и привратника [1,15,24,32]. Н.А. Майстренко и А.А. Курыгин [16] отметили, что в послеоперационном периоде восстановление моторной активности желудка или его культи происходит медленней, чем восстановление эвакуаторной функции. K. Aonuma [27] отмечает, что при сохранении иннервации антрального отдела и привратника происходит восстановление III фазы мигрирующего моторного комплекса (ММК) в АОЖ.
При исследовании ММК оперированного желудка периодичность обнаружена у большинства пациентов: у 70 — 75% пациентов в первой группе и 86,7 — 80% больных — во второй соответственно по периодам наблюдения (через 1 год, 2 — 5 лет, 5,1 — 10 лет). Анализ полученных результатов показал, что у обследованных лиц после ГП по В.И. Оноприеву достоверно укорочен период покоя, удлинена фаза неритмической активности и уменьшено соотношение фаз покоя и активности по сравнению с группой контроля. Трансформация временных параметров при сохранении периодичности ММК, по-видимому, связанна с нарушением вагусной иннервации оперированного желудка, что подтверждается исследованиями других авторов. А.Ф. Черноусов и А.Л. Шестаков [26] отмечали изменения голодной и постпрандиальной моторной активности антрума у пациентов, перенёсших СП В.
У 54% пациентов первой группы и 70% пациентов второй после ГП отмечалось увеличение амплитуды сокращений ФОЖ, что связано с увеличением пропульсивной активности фундального отдела, необходимой для продвижения пищевых масс через желудочную трубку. Это явление отмечалось у пациентов с порционной эвакуацией бариевой взвеси при рентгенологическом исследовании и свидетельствовало о тенденции к восстановлению рецептивной релаксации ФОЖ в послеоперационном периоде.
После хирургического вмешательства важным является сохранение способности генерировать различные варианты волн в антральном отделе, обеспечивающие полноценное измельчение, перемешивание пищевых масс. Антропилорические волны давления через 1 год после ГП вне зависимости от способа формирования гастро-гастрального анастомоза были представлены следующими видами: преобладали синхронные — у 25-40% и смешанные — у 25-30%. При этом антеградные волны составили 15-10%, ретроградные — 5-10%. Такое соотношение антральных волн соответствовало их распределению в группе контроля. С увеличением сроков после оперативного вмешательства тенденция подобного распределения антральных волн давления сохранялась и свидетельствовала о нормализации антродуоденальной координации у пациентов с ТЯЖ после хирургического лечения. Признаки перегрузки АОЖ зарегистрированы через 2 — 5 лет после операции у 3(6,7%) больных первой группы в виде ослабления моторной активности со снижением амплитуды сокращений до 30 мм.рх ст. и увеличением частоты моторных волн до 3/мин. У этих пациентов отмечались жалобы на тяжесть в эпигастрии, тошноту, боли в животе; при эндоскопическом и рентгенологическом исследованиях отмечалось расширение желудочной трубки и увеличение в размерах АОЖ.
По данным рентгенологического метода исследования (Таблица 4) порционность эвакуации бариевой взвеси из ФОЖ в АОЖ наблюдалась у 90% больных второй группы в течение 10 лет динамического наблюдения, что свидетельствовало о нормализации тонуса и перистальтики кислотопродуцирующей камеры желудка у этой группы больных и достоверно отличалось по этому признаку от пациентов первой (р<0,05). У больных первой группы было отмечено уменьшение порционности темпа эвакуации бариевой взвеси через КАА от 75,9% через 1 год до 61,5% через 5,1- 10 лет, что связано с укорочение и расширение желудочной трубки в проксимальном отделе через 2 - 5 лет у 22,7% пациентов с последующей дезинвагинацией у 11,4% больных группы. Антрофундальный рефлюкс наблюдался у 6,8% пациентов 1 группы.
Таблица 4. Результаты рентгенологического исследования пищевода, желудка и двенадцатиперстной кишки в зависимости от длительности послеоперационного периода
|
Признаки |
Исходно n=74 чел. (%) |
После операции 1 группа |
Исходно n=30 чел. (%) |
После операции 2 группа, чел.(%) |
|||||
|
1 год n=58 |
2-5 лет n=44 |
5,1-10 лет n=39 |
1 год n=23 |
2-5 лет n=20 |
5,1-10 лет n=10 |
||||
| Функциональные | |||||||||
| Кардия
смыкается не смыкается |
2 (2,7) |
58 (100)* |
41 (93,2)* |
35 (89,7)* |
2 (6,7) |
23 (100)* |
23 (100)* |
23 (100)* |
|
|
72 (97,3) |
0* |
3 (6,8)* |
4(10,3)* |
28 (93,3) |
0* |
0* |
0* |
||
| ГЭР |
65 (87,8) |
0* |
3 (6,8)* |
3 (7,7)* |
26 (86,7) |
0* |
0* |
0* |
|
| ДГР |
26 (35,1) |
8 (13,)* |
7 (6,7)* |
6 (8,3)* |
12 (40) |
1 (4,3)* |
0* |
0* |
|
| Антрофундальный
рефлюкс |
— |
1 (1,7) |
3 (6,8) |
3 (7,7) |
— |
0* |
0* |
0* |
|
| Темп эвакуации из желудка | |||||||||
| нормальный |
36 (48,6) |
54 (93,1)* |
38 (86,4)* |
20 (84,6)* |
13 (43,3) |
21 (91,3)* |
20 (100)*• |
10 (100)*• |
|
| ускоренный |
8 (10,8) |
2 (3,4) |
3 (6,9) |
3 (7,7) |
4 (13,3) |
0 |
0 |
0 |
|
| замедленный |
32 (43,2) |
3 (5,1)* |
3 (6,9)* |
3 (7,7)* |
11 (36,7) |
2 (8,7)* |
0* |
0* |
|
| Порционность
эвакуации через ГГА |
— |
44 (75,9) |
28 (65,9) |
24 (61,5) |
— |
21 (91,3)• |
18 (90)• |
9 (90)• |
|
| Сопровождающие | |||||||||
| ГПОД |
17 (22,9) |
0* |
2 (4,5)* |
2 (5,1)* |
10 (33,3) |
0* |
0* |
0* |
|
Примечание: * — достоверные отличия от исходных показателей (р<0,05); • -достоверные отличия от 1 группы, ГЭР - гастроэзофагеальный рефлюкс, ДГР - дуоденогастральный рефлюкс, ГПОД - грыжа пищеводного отверстия диафрагмы, ГГА - гастрогастральный анастомоз.
Таким образом, по данным рентгенологического исследования технология ГП по В.И. Оноприеву с формированием КАС из петли тощей кишки имеет ряд преимуществ перед своим аналогом ГП с инвагинационным КАА: создаваемая мышечная манжетка из петли тонкой кишки препятствует расширению желудочной трубки; восстанавливает резервуарную функцию ФОЖ; обеспечивает порционное поступление пищевых масс в АОЖ, предотвращая его перегрузку; обладает арефлюксными свойствами, обеспечивая надежную защиту ФОЖ от действия желчи.
Параметры КЖ все шире применяются в практике отечественного здравоохранения для экспертизы и стандартизации новых методов лечения [20]. В настоящее время общепринятым является мнение, что пока не изучено влияние хирургического лечения на КЖ в послеоперационном периоде, нельзя с полной объективностью судить о достоинствах и недостатках той или иной операции [12].
При сравнении параметров КЖ в послеоперационном периоде у всех пациентов с ТЯЖ через 3 месяца после операции наблюдалось достоверное повышение КЖ по шкале «боль», через 1 год достоверно повышались параметры КЖ по всем шкалам (Рис. 4, 5). Следует отметить, что у пациентов первой группы в отдалённом послеоперационном периоде (через 1 год и более) достоверно ниже показатель психического здоровья КЖ по шкале «социальное функционирование» по сравнению с обследованными пациентами второй группы. Проведённый сопоставительный анализ параметров КЖ контрольной группы и прооперированных лиц выявил, что у пациентов первой группы в отдалённом послеоперационном периоде (через 2 — 5 лет и более) остаются достоверно ниже показатели по пяти шкалам: «физическое функционирование», «жизнеспособность», «социальное функционирование», «ролевое эмоциональное функционирование», а у больных второй группы по двум шкалам: «физическое функционирование» и «ролевое эмоциональное функционирование». Таким образом, органосохраняющая технология ГП по В.И.Оноприеву повышает уровень КЖ пациентов с ТЯЖ по всем шкалам и в большей степени у пациентов 2 группы, перенёсших ГП с формированием КАС из петли тощей кишки.
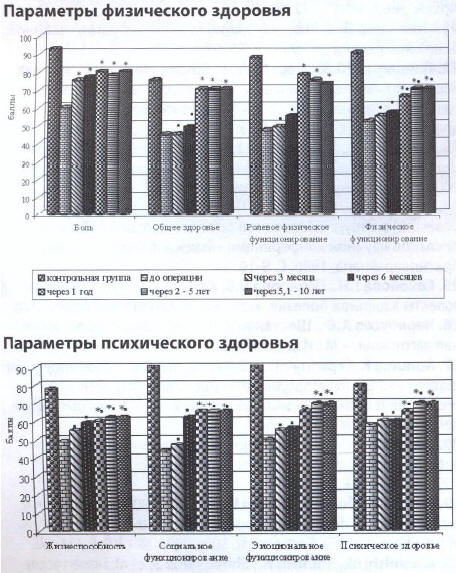
Рис. 4. Параметры КЖ больных 1 группы в различные сроки после операции по сравнению с дооперационными и контрольной группой
Примечание: «*» — обозначены отличия от показателей КЖ до операции; • — обозначены отличия от показателей КЖ контрольной группы (р< 0,05)
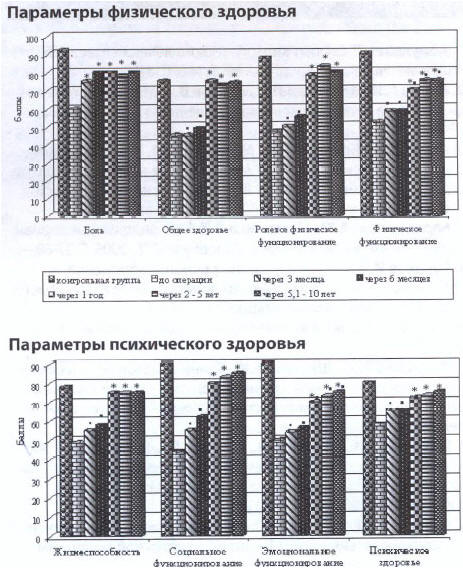
Рис. 5. Параметры КЖ больных 2 группы в различные сроки после операции по сравнению с дооперационными и контрольной группой
Примечание: «*» — обозначены отличия от показателей КЖ до операции; • — обозначены отличия от показателей КЖ контрольной группы (р< 0,05)
Заключение
Морфологическая трансформация СОЖ у пациентов с ТЯЖ после комплексного медикаментозного и хирургического лечения методом ГП по В.И.Оноприеву в течение 2 лет характеризуется уменьшением воспалительных изменений слизистой пищевода и желудка, через 5 лет и более соответствует аналогичным изменениям СОЖ у гастроэнтерологических пациентов без язвенной болезни в анамнезе, кумулятивный риск рака желудка не увеличивается.
Восстановление моторной и эвакуаторной функций оперированного желудка после ГП по В.И.Оноприеву происходит в течение 1 года и обусловлено адекватным функционированием вновь созданных анастомозов. В отдалённые сроки после операции наблюдается тенденция к восстановлению рецептивной релаксации ФОЖ. Применение ГП с формированием КАС из петли тощей кишки является эффективным методом хирургического лечения ТЯЖ.
Информация об авторе
Серикова Светлана Николаевна — канд. мед. наук, зав. гастроэнтерологическим центром поликлиники СКАЛ городской больницы № 2, врач — хирург.
Адрес для корреспонденции: 350089, г. Краснодар ул. Красных партизан 6/1, тел. 8(861) 2220009 serikovasn@mail.ru
Список литературы
- Абдуллаев Д.С. Опыт хирургического лечения язвенной болезни желудка // Хирургия.-1999. №8. С. 8-11.
- Аруин Л.И., Капуллер Л.Л., Исаков В.А. Морфологическая диагностика болезней желудка и кишечника. М.: Медицина, 1998. С. 483.
- Аруин Л.И., Кононов А.В., Мозговой С.И. Новая классификация хронического гастрита // Актуальные вопросы патологической анатомии: Материалы III съезда Российского общества патологоанатомов. Самара, 2009. Том 1. С. 5-8.
- Барановский А.Ю., Назаренко Л.И. Неблагоприятные варианты течения язвенной болезни. С.-Петербург: СПб, 2006. С. 22-68.
- Бураков И.И. Результаты долгосрочного наблюдения за больными язвенной болезнью, ассоциированной с Helicobacter pylori. После эрадикации микроорганизма // Экспериментальная и клиническая гастроэнтерология. 2002. №3. С.45-48.
- Вахрушев Я.М., Шкатова Е.Ю. Клинико-патогенетическая характеристика течения язвенной болезни с сопутствующей патологией сердечно-сосудистой системы // Практическая медицина. Казань, 2006. №4.С. 5-7.
- Гостищев В.К., Евсеев М.А., Головин Р.А. Радикальные оперативные вмешательства в лечении больных с перфоративными гастродуоденальными язвами // Хирургия. Журнал им. Н.И.Пирогова.2009. №3. С.10-17.
- Жерлов Г.К. Современные тенденции диагностики и лечения гастродуоденальных язв // Бюллетень сибирской медицины. 2003. №4. С. 5-14.
- Жерлов Г.К., Кошель А.П. и др. Анализ ближайших и отдаленных результатов органосохраносохраняющих и органомоделирующих операций в хирургии гастродуоденальных язв. // Вестник хирургической гастроэнтерологии. 2006. № 1.С. 35.
- Зайцев О.В., Тарасенко С.В., Копейкин А.А. К вопросу о тактике при острых желудочно-кишечных кровотечениях // Экспериментальная и клиническая гастроэнтерология. 2003. №1.С. 176.
- Калиш Ю.И., Турсуметов А.А. Хирургическое лечение сочетанных язв желудка и двенадцатиперстной кишки // Хирургия. 2009. №6. С. 27-30.
- Крылов Н.Н., Кузин М.И. К методике оценки результатов операций на желудке // Хирургия. 2000. №2 . С. 17-20.
- Кузин М.И. Актуальные вопросы хирургии язвенной болезни желудка и двенадцатиперстной кишки // Хирургия. 2001. №1. С. 27-32.
- Лобанков В.М. Язвенная болезнь: концепция популяцион-ной хирургической активности // Вестник хирургической гастроэнтерологии. 2010. №3. С.29-39.
- Лубянский В.Г., Леонтьев С.В., Кузнецов Г.Л. Лечение осложнений резекции желудка с сохранением привратника // Хирургия. 2002. №4. С. 40-43.
- Майстренко Н.А., Курыгин А.А. Моторно-эвакуаторные расстройства пищеварительного тракта в ранние сроки после операций на желудке // Вестн. хир. 1998. №4.С. 32-37.
- Мансуров Х.Х. Современный взгляд на некоторые спорные вопросы язвенной болезни и хеликобактерной инвазии // Клиническая медицина. 2005. №2. С.63-65.
- Минушкин О.Н., Денисов Л.Е., Бурдина Е.Г. и соавт. Helicobacter pylori после резекции желудка // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2001. №2. С. 34-37.
- Наумов В.Ф., Габдраупова С.Р., Тимошенко P.O. Адекватная коррекция функциональных структур желудка в хирургии язвенной болезни //Экспериментальная и клиническая гастроэнтерология. 2003. №3. С. 76-84.
- Новик А.А., Ионова Т.И., Денисов Н.Л. Концепция и стратегия исследования качества жизни в гастроэнтерологии //Тер. Архив. 2003. №10. С. 42-46.
- Оноприев В.И. Этюды функциональной хирургии язвенной болезни. Краснодар, 1995. — 295 с.
- Панцырев Ю.М., Чернякевич С.А., Михалев А.И. и соавт. Рациональные подходы к применению прокинетиков в хирургической клинике // Рос. журн. гастроэнтерол., гепатол., колопрктол. 2000. №3. С. 20-23.
- Саблин О.А., Ильчишина Т.А. Проблема резистентности Helicobacter pylori кларитромицину// Гастроэнтерология. №2. 2009. Приложение Consilium medicum. C.4-7.
- Саенко В.Ф., Лаврик А.С Пилоро- и антрум сохраняющие резекции в хирургии язвенной болезни желудка // Тезисы докладов научной конференции «Язвенная болезнь желудка». Краснодар-Анапа, 1996. С. 9-10.
- Соколова Г.Н., Потапова В.Б. Клинико-патогенетические аспекты язвенной болезни желудка. М.:Анахарсис, 2009. С.328
- Черноусов А.Ф., Шестаков А.Л. Селективная проксимальная ваготомия. — М.: Изд-во AT, 2001. С. 158.
- Aonuma К. Experimental studies on the gastroduodenojejunal motility and gastric emptying after duodenectomy with preservation of the total stomach and pylorus // J. Smooth Muscle Res. 1994.V. 30, №4. P. 147-64.
- Donahue P. Parietal cell vagotomy nervus vagotomy-anterectomy: ulcer surgery in the modern era //World J. Surg. 2000.V.24, №3. P. 264-269.
- Espat N.J., Ong E.S., Helton W.S. et al. 1990-2001 US general surgery chief resident gastric surgery operative experience: analysis of paradigm shift // J. Gastrointest. Surg. 2004. №4, V.8. P. 471-478.
- Kaminishi M., Shimizu N., Shimoyama S. et al. Denervation promotes the development of cancer-related lesions in the gastric remnant //J. Gin. Gastroenterol. 1997. V. 25. № 1. P. 129-134.
- Ohmann C, Imhof M., Ruppert С et al. Time-trends in the epidemiology of peptic ulcer bleeding // Scand. J. Gastroenterol. 2005.V.40. №8. C.914-920.
- Polous I.M., Borshch IV. Periodic gastric and duioenal motility in peptic ulcer pacients after selective proximal vagotomy // Lik. Sprava. 1999.V.5. P.98-101.
- Remacha ТВ., Lanas A.A., Sainz S.R. Refractory peptic ulcer: the pathogenic mechanisms Rev Esp Enferm Dig. 1995; V.87, №6. P. 453-59.
- Rodriguez H.H., Sanchez A.L. F., Quinones E. Eradication of Helicobacter pylori in peptic ulcer and chronic gastritis // A randomized clinical trial Rev Gastroenterol Мех. 1998.V.63, №1. P. 21-27.
- Rollan A., Giancaspero R., Fuster F. et al. The long-term reinfection rate and the course of duodenal ulcer disease after eradication of Helicobacter pylori in a developing country// Am. J. Gastroenterol. 2000. V. 95. P. 50-56.
- Yamaguchi Т., Ichikawa D., Kurioka H. et al. Postoperative clinical evaluation following pylorus-preserving gastrectomy// Hepatogastroenterology. 2004.V. 51, №57.P. 883-886.
Статья опубликована на сайте http://www.gastroscan.ru
материал MedLinks.ru






