Профилактика рестеноза у пациентов после чрескожного коронарного вмешательства: возможный патогенетический подход
Содержание статьи
Введение
За последнее десятилетие в России существенно снизилась смертность от сердечно-сосудистых заболеваний. Коронарное стентирование вносит существенный вклад в снижение смертности пациентов с инфарктом миокарда (ИМ) и другими формами ишемической болезни сердца (ИБС), а стентирование сонных артерий снижает риск инсульта [1]. Количество операций коронарного стентирования возрастает во всем мире: в Германии, например, выполняется 350 тыс. операций в год [2], а в США — более 1,8 млн в год [3]. В России число операций стентирования постоянно растет: в 2016 г. проведено 107 тыс. операций по установке сосудистых стентов в рамках высокотехнологичной медицинской помощи, а в 2017-м — уже 110 тыс. операций [4].
Рестеноз сосуда, возникающий в результате гиперплазии интимы в просвете стента, остается существенным осложнением стентирования. Проблема рестеноза связана с необходимостью повторного стентирования [5, 6] и, как следствие, существенно повышает затраты здравоохранения [7, 8]. Рестеноз сосуда в месте установки стента — сложный процесс, включающий воспаление, неоваскуляризацию и активацию тромбоцитов [9], и может сочетаться с обострением коморбидной патологии, ассоциированной с хроническим воспалением (например, остеоартритом (ОА)) [10].
К решению проблемы рестеноза подходят, как правило, посредством изготовления стентов из современных высокотехнологичных материалов и применения эффективной антитромботической терапии. В современных рекомендациях четко отражены позиции по антитромботической терапии как в отношении сочетания лекарственных средств разных классов, так и в отношении длительности их применения [1]. Однако проблемы, связанные с процессами воспаления и неоваскуляризации, требуют более пристального внимания.
Отметим, что использование сочетанной антитромботической терапии, включающей низкомолекулярные формы гепарина (который блокирует синтез и активность тромбина), нестероидные противовоспалительные препараты (НПВП) (ингибируют синтез тромбоксана A2) и антикоагулянты per os (снижают эффекты витамин-К-зависимых прокоагулянтов), имеет ряд ограничений [11].
Во-первых, использование такой сочетанной антитромботической терапии приводит к нарушениям гемостаза и повышению риска кровотечений. Во-вторых, при адгезии тромбина в зоне сосудистого повреждения тромбин остается устойчивым к действию гепарина и других макромолекулярных антикоагулянтов, по-прежнему стимулирует формирование тромба и гиперплазию неоинтимы (фиброзной оболочки, образующейся на внутренней поверхности сосудистого протеза в результате перерождения прорастающего в него эндотелия) [11]. В-третьих, клинические исследования показали, что некоторые НПВП могут проявлять кардиотоксические свойства, повышая сердечно-сосудистый риск.
Например, метаанализ 87 исследований показал, что общий сердечно-сосудистый риск (в т. ч. цереброваскулярный) достоверно повышался при использовании таких НПВП, как рофекоксиб (ОР 1,39, 95% ДИ 1,31–1,47) и диклофенак (ОР 1,34, 95% ДИ 1,26–1,42) [12]. Наблюдения, проводимые в течение нескольких лет за когортой пациентов со спондилоартритом (n=8140) без истории ИМ, позволили выявить 115 случаев ИМ (1,9%). Прием диклофенака был ассоциирован с 3-кратным повышением риска ИМ (ОШ 3,32, 95% ДИ 1,57–7,03) [13]. Таким образом, востребованы подходы, которые бы позволили повысить эффективность и безопасность антитромботической фармакотерапии, назначаемой до и после стентирования.
Перспективным направлением фармакологической профилактики рестеноза может являться использование хондроитина сульфата (ХС) и/или глюкозамина сульфата (ГС). Являясь основными компонентами «гелевой основы» соединительной ткани, ХС и ГС повышают ее эластичность и механическую прочность, гидратацию и накопление нутриентов, поддерживают физиологическое состояние синовиальной жидкости. Поэтому ХС и ГС широко используются в терапии ОА и других заболеваний суставов [14].
Отметим, что ОА часто является коморбидной патологией у пациентов, нуждающихся в проведении стентирования. Например, в крупномасштабном клиникэпидемиологическом исследовании пациентов с ОА (n=18 490) встречаемость ИБС и ИМ была на 30% выше, чем в контрольной группе [10]. Кроме того, хондропротекторное действие ХС и ГС — далеко не единственное фармакологическое действие этих молекул. Они также проявляют выраженное противовоспалительное действие, ассоциированное со снижением уровней биомаркеров воспаления ИЛ-1, ИЛ-6, ФНО-α и С-реактивного белка [15, 16]. Поэтому вполне естественно, что использование ХС и ГС для облегчения боли при ОА также ассоциировано и со сниженным риском сердечно-сосудистой патологии.
Например, при наблюдении за крупномасштабной когортой участников без сердечно-сосудистых заболеваний на момент начала исследования (n=466 039) в течение 7 лет было зарегистрировано 10 204 случая сердечно-сосудистых событий, в т. ч. 3060 случаев сердечно-сосудистой смерти, 5745 случаев ИБС и 3263 случая ишемического инсульта (ИИ). С поправкой на возраст, пол, индекс массы тела, этнос, диету, прием фармацевтических препаратов и другие факторы было показано, что долговременный прием ГС ассоциирован со значительно более низким сердечно-сосудистым риском (ОШ 0,85, 95% ДИ 0,80–0,90), в т. ч. со сниженным риском ИБС (ОШ 0,82, 95% ДИ 0,76–0,88), ИИ (ОШ 0,91, 95% ДИ 0,83–1,00) и общей сердечно-сосудистой смертности (ОШ 0,78, 95% ДИ 0,70–0,87) [17].
В настоящей работе представлено обоснование использования ХС и ГС для профилактики рестеноза. Рассмотрены результаты гистологических анализов рестеноза, полученные в ходе экспериментальных и клинических исследований, проведено сопоставление патофизиологии рестеноза и молекулярных механизмов действия ХС и ГС, рассмотрены возможности использования ХС и ГС для предотвращения рестеноза.
Гистологическая картина рестеноза
Экспериментальные данные
Эксперименты на модели атеросклероза на обезьянах показали, что сужение просвета после повреждения сосудистой стенки артерии связано с образованием тонких пристеночных тромбов в местах дробления атеросклеротических бляшек (2–7-й день). Отмечается интенсивная миграция лейкоцитов (2–4-й день) и α-актин-позитивных гладкомышечных клеток (ГМК) (4–7-й день) в область повреждения сосудистой стенки. Пристеночные тромбы постепенно заменяются ГМК, экспрессирующими гиалуронан и протеогликан версикан (14-й день). Экспрессия версикана отмечена по всей поверхности растущей неоинтимы (28-й день) и постепенно снижается по мере восстановления сосудистой стенки (112-й день). Экспрессия проколлагена I первоначально увеличивалась в формирующейся неоинтиме (14-й день) и снижалась через 3,5–4 мес. наблюдений. Экспрессия альфа-v-бета-3 интегринового рецептора фибриногена исходно увеличивалась в области повреждения стенки артерии (7-й день), затем существенно снижалась (28-й день). В целом гистологический анализ показал, что процесс заживления сосудистой стенки аналогичен процессу ранозаживления. Соответственно, в результате стентирования возможно формирование своего рода «рубцов», которые способствуют сужению просвета сосуда [18].
На рисунках 1 и 2 представлены микрофотографии
структурных изменений в стенке артерии после экспериментальной ангиопластики [18].
![Рис. 1. Микрофотографии структурных изменений в стенке артерии на 4-й (A, B, G), 7-й (C, D), 14-й (E, F) и 28-й дни (H, I, J , К) после экспериментальной ангиопластики [18]. Рис. 1. Микрофотографии структурных изменений в стенке артерии на 4-й (A, B, G), 7-й (C, D), 14-й (E, F) и 28-й дни (H, I, J , К) после экспериментальной ангиопластики [18].](https://medblog.su/wp-content/uploads/2019/09/profilaktika-restenoza-u-patsientov-posle-chreskozhnogo-koronarnogo-vmeshatelstva-vozmozhnyj-patogeneticheskij-podhod-gromova-o-a-torshin-i-yu-lila-a-m-nazarenko-a-g-zolotovskaya-i-a.png)
![Рис. 2. Микрофотографии повреждений интимы на 4-й день после экспериментальной ангиопластики [18]. Рис. 2. Микрофотографии повреждений интимы на 4-й день после экспериментальной ангиопластики [18].](https://medblog.su/wp-content/uploads/2019/09/1569645914_293_profilaktika-restenoza-u-patsientov-posle-chreskozhnogo-koronarnogo-vmeshatelstva-vozmozhnyj-patogeneticheskij-podhod-gromova-o-a-torshin-i-yu-lila-a-m-nazarenko-a-g-zolotovskaya-i-a.png)
Клинические исследования
Приведенные выше результаты экспериментального исследования рестеноза подтверждаются результатами гистологических исследований сосудов пациентов с сердечно-сосудистой патологией. Рестенотические поражения периферических артерий человека также характеризуются избирательными отложениями протеогликана версикана во внеклеточном матриксе (ВКМ). Например, сегменты артерий, подвергнувшихся рестенозу в течение 0,5–36 мес. после ангиопластики, были взяты у 30 пациентов при проведении атерэктомии пораженных участков. Гистохимический анализ выявил наличие отдельных зон, обогащенных ХС-протеогликаном версиканом, бигликаном (лейцинсодержащий дерматансульфатный протеогликан), другими протеогликанами и фибриллярным коллагеном. ВКМ, обогащенный версиканом, также содержал удлиненные и звездчатые ГМК, расположенные на достаточно больших расстояниях друг от друга [19].
Клинические исследования также подтвердили, что рестеноз после стентирования возникает вследствие гиперпролиферации ГМК и увеличения объема ВКМ (который составляет в среднем 50% от объема неоинтимы). Пациенты, перенесшие чрескожную транслюминальную коронарную ангиопластику (n=43), были разделены на 4 группы в соответствии со временем рестеноза после ангиопластики: 0–1 мес. (n=6), 1–3 мес. (n=12), 3–6 мес. (n=11), более 6 мес. (n=6). Пациентам была проведена коронарная атерэктомия, фрагменты сосудов с рестенозом были удалены и подвергнуты гистологическому исследованию. Большинство клеток в исследованных образцах артерий с рестенозом являлись актин-положительными ГМК. Иммуногистохимический анализ показал, что формирование «отложений» версикана было наибольшим в течение 1–3 мес. после первичной ангиопластики, т. е. именно в период наиболее активной прогрессии рестеноза [20]. Таким образом, торможение формирования рестеноза следует осуществлять именно в первые 3 мес., сразу после установки стента.
Образование сети волокон версикана при формировании неоинтимы является одной из основных причин рестеноза коронарной артерии. Изменения в структуре ВКМ, характерные для стентированных коронарных артерий, изучали посредством гистологического прокрашивания неоинтимальных протеогликанов, гиалуронана, коллагена (типа I и III), рецептора гиалуронана CD44 на образцах стентированных коронарных артерий человека, взятых post mortem (n=45). Биопсийный материал был разделен на 3 группы: 1) стенты, простоявшие 3–9 мес. (n=17);
2) стенты, простоявшие 9–18 мес. (n=19); 3) стенты, простоявшие >18 мес. (n=9).
В группах 1 и 2 окрашивание неоинтимы на версикан и гиалуронан было чрезвычайно выражено и колокализовано с α-актин-положительными ГМК, тогда как окрашивание на декорин было наибольшим в группе 3 (рис. 3, 4). Неоинтима стентов в группах 1 и 2 была в большей степени обогащена коллагеном III типа, чем неоинтима вокруг стентов в группе 3. Окрашивание на коллаген I типа было наименее выражено в стентах у пациентов группы 1 и прогрессивно усиливалось в группах 2 и 3. Плотность ГМК и степень рестеноза стента были значительно снижены в группе 3 по сравнению с группами 1 и 2. Эти наблюдения позволяют предположить, что процесс организации ВКМ в коронарных стентах человека напоминает процесс заживления раны, за ним следует неоинтимальная ретракция. Поэтому одной из целей терапии, направленной на профилактику рестеноза в месте установки стента, является снижение интенсивности роста ВКМ [21].
![Рис. 3. Окрашивание неоинтимы на α-актин, версикан и гиалуронан [21]. Рис. 3. Окрашивание неоинтимы на α-актин, версикан и гиалуронан [21].](https://medblog.su/wp-content/uploads/2019/09/1569645914_827_profilaktika-restenoza-u-patsientov-posle-chreskozhnogo-koronarnogo-vmeshatelstva-vozmozhnyj-patogeneticheskij-podhod-gromova-o-a-torshin-i-yu-lila-a-m-nazarenko-a-g-zolotovskaya-i-a.png)
![Рис. 4. Окрашивание неоинтимы при сроке стояния стента 11 мес. [21]. Рис. 4. Окрашивание неоинтимы при сроке стояния стента 11 мес. [21].](https://medblog.su/wp-content/uploads/2019/09/1569645914_295_profilaktika-restenoza-u-patsientov-posle-chreskozhnogo-koronarnogo-vmeshatelstva-vozmozhnyj-patogeneticheskij-podhod-gromova-o-a-torshin-i-yu-lila-a-m-nazarenko-a-g-zolotovskaya-i-a.png)
На рисунке 3 видно, что окрашивание неоинтимы на версикан и гиалуронан сильно выражено в стентах, стоявших в течение 3–9 мес. (группа 1) и 9–18 мес. (группа 2) и колокализовано с актин-положительными ГМК. Окрашивание на версикан и гиалуронан снижается в стентах, стоявших 48 мес. (группа 3), и ассоциировано со снижением плотности клеток неоинтимы [21].
На рисунке 4 видно, что окрашивание на гиалуронан выраженно в средней и поверхностной неоинтиме (B), а также в зоне, прилегающей к стойке стента. Окрашивание на интертрипсиновый ингибитор, который формирует поперечные сшивки гиалоуронана и усиливает взаимодействие с макрофагами, колокализовано с окрашиванием гиалуронаном (С).
Процессы накопления гиалуронана, версикана и ГМК при рестенозе сопровождаются инфильтрацией макрофагов, которая ассоциирована с увеличением толщины неоинтимы. Важно отметить, что в зоне неоинтимы окрашивание на макрофаги сочетается с окрашиванием на рецептор гиалуронана CD44 в глубине неоинтимы (рис. 5).
![Рис. 5. Стент через 11 мес. после установки [21]. Рис. 5. Стент через 11 мес. после установки [21].](https://medblog.su/wp-content/uploads/2019/09/1569645914_961_profilaktika-restenoza-u-patsientov-posle-chreskozhnogo-koronarnogo-vmeshatelstva-vozmozhnyj-patogeneticheskij-podhod-gromova-o-a-torshin-i-yu-lila-a-m-nazarenko-a-g-zolotovskaya-i-a.png)
Положительное окрашивание на CD44 присутствовало в 48% и 42% стентов в группах 1 и 2 соответственно и лишь в 12% стентов в группе 3 (P=0,0001). Толщина неоинтимы была больше в образцах с CD44-позитивными клетками (0,68±0,31 мм) по сравнению с образцами, содержащими CD44-негативные клетки (0,45±0,29 мм; P=0,0001) [21].
Таким образом, детальное гистологическое исследование процессов рестеноза указало на взаимосвязи между повреждением сосудистой стенки, воспалением, ростом неоинтимы и инфильтрацией макрофагами. Площадь неоинтимы, занятая макрофагами, была в 3 раза больше в области стентов с рестенозом, чем в области стентов без рестеноза. В неоинтиме с высоким содержанием гиалуронана, характеризующейся повышенной толщиной, плотность рецептора CD44 выше там, где выше концентрация активированных макрофагов [22]. Известно, что рецептор CD44 необходим для миграции воспалительных клеток и активации роста ГМК [23, 24]. Активация рецептора CD44 на поверхности активированных макрофагов повышает синтез провоспалительных цитокинов, усиливает дальнейшую миграцию макрофагов в зону роста неоинтимы, что повышает синтез протеогликанов, заполняющих просвет сосуда в области стента (рис. 5) [21].
Патофизиология рестеноза и молекулярные механизмы действия ХС и ГС
Итак, экспериментальные и клинические исследования показали, что характерными особенностями рестеноза являются: 1) накопление в неоинтиме протеогликана версикана; 2) гиперпролиферация ГМК; 3) инфильтрация макрофагами; 4) вовлеченность рецептора CD44 в процессы сужения просвета сосуда. Фармакологические свойства ХС и ГС, установленные в результате фундаментальных и клинических исследований, позволяют утверждать, что ХС и ГС оказывают специфическое таргетное воздействие на эти процессы.
Версикан — главный ХС-протеогликан кровеносных сосудов, часто встречающийся в интиме и адвентиции большинства артерий и вен, синтезирующийся при участии ГМК и заполняющий пространство между фибриллярными белками ВКМ [25]. Экспрессия версикана повышается при повреждениях тканей и необходима для заживления ран [26]. Как было отмечено выше, версикан интенсивно накапливается в так называемой ранней неоинтиме, формирующейся при атеросклерозе и рестенозе сосудов [27]. Накопление версикана ассоциировано с гиперпролиферацией ГМК и возрастанием уровня воспаления в области атеросклеротических поражений сосудов [28].
Накопление версикана в области рестеноза ассоциировано с активностью рецептора CD44. Во-первых, версикан может связывать и активировать рецептор CD44, причем этот процесс ингибируется молекулами ХС [29]. Во-вторых, активация рецептора CD44 связана с инфильтрацией макрофагами и повышением локального воспаления. В-третьих, блокирование рецептора CD44 специальными антителами нарушает процессы структурной организации версикана во ВКМ и тормозит гипепролиферацию неоинтимы [26].
Описанный нами на основании результатов экспериментальных и клинических исследований механизм рестеноза позволяет предположить, что адъювантная фармакотерапия ХС и ГС, начатая сразу после стентирования, может быть патогенетической. Дело в том, что действие ХС и ГС на процессы воспаления и репарации тканей высокоспецифично и обусловлено воздействием на определенные таргетные белки. Биоинформационные анализы
20 540 аннотированных белков протеома человека позволили выделить 40 белков метаболизма глюкозамина и 11 белков, вовлеченных в осуществление противовоспалительных эффектов ХС [14]. В целом ХС и ГС взаимодействуют с рецепторами CD44, TLR4 и ICAM1 на поверхности макрофагов и клеток других типов, ингибируют провоспалительный транскрипционный фактор NF-кВ и цитокиновый сигнальный путь JAK/STAT.
Основной механизм фармакологического действия ХС и ГС заключается во взаимодействии этих молекул именно с рецептором CD44 [30]. Специфически связываясь с рецептором CD44 (см. рис. 5), ХС и ГС воздействуют на внутриклеточные сигнальные процессы. Основное отличие между фармакологическими эффектами ГС и ХС заключается в том, что ХС осуществляет медленное, пролонгированное действие, а ГС позволяет достигать быстрого эффекта
(прежде всего устранение воспаления и обезболивание).
Связывание рецептора CD44 молекулами ХС и ГС способствует предотвращению деградации белка IκBα, ингибирующего провоспалительный белок NF-kB [31]. Взаимодействуя с регулятором IκBα, NF-kB не может перемещаться в клеточное ядро и активировать экспрессию
генов, участвующих в воспалительной реакции (рис. 6, 7).
NF-кВ является одним из центральных медиаторов воспаления, и его инактивация стимулирует снижение уровней биомаркеров воспаления ИЛ-1, ИЛ-6, ФНОα, С-реактивного белка и др. [32]. Более того, ГС противодействует осуществлению эффектов этих цитокинов, прежде всего ФНОα (см. рис. 6, 7). Активация молекулой ГС рецептора CD44 также приводит к снижению избыточной активности металлопротеиназ, в т. ч. за счет регуляции транскрипции соответствующих генов [15].
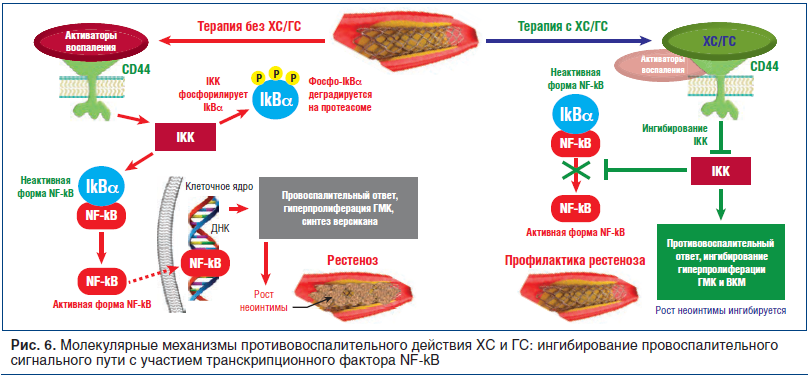
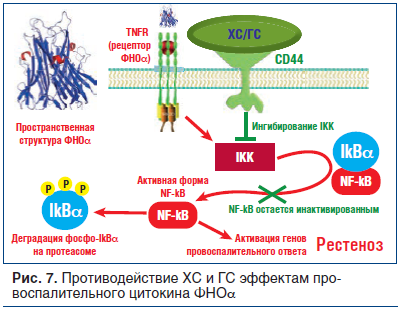
Таким образом, основной механизм фармакологического действия ХС и ГС заключается в связывании с рецептором CD44, что приводит к ингибированию сигнального пути NF-kB (как результат, к снижению неспецифического хронического воспаления). Отметим, что блокада сигнального пути NF-kB также способствует снижению гиперпролиферации ГМК и торможению роста неоинтимы вокруг стента [33]. Кроме того, фундаментальные исследования ХС и ГС указали на антигиперпролиферативный [34, 35] и слабый антитромботический [36] эффекты ГС и ХС, которые также способствуют снижению гиперплазии неоинтимы. Кроме того, использование ХС и ГС позволяет снизить потребность в НПВП [37, 38], тем самым снижая кардиотоксичность, имеющую место при применении этой группы препаратов.
Приведенные выше результаты фундаментальных исследований указывают на возможность использования ХС и ГС для торможения рестеноза. В нескольких экспериментальных исследованиях была изучена целесообразность различных способов применения ХС при проведении стентирования. Например, ХС в форме хондроитин-4-сульфата улучшает адгезию клеток эндотелия и их устойчивость к апоптозу, тем самым стимулируя заживление сосудов вокруг стентов [39]. Поэтому покрытие стентов из нержавеющей стали слоями ХС и гепарина, ковалентно связанных с со стальной подложкой золото-димеркаптосукцинатными линкерами, может использоваться для устранения тромбообразования и рестеноза, которые происходят при имплантации сердечно-сосудистых стентов. Результаты коагуляционных тестов указали на удлинение времени свертывания крови и снижение адгезии тромбоцитов на стентах, модифицированных смесями ХС и гепарина [40].
Такие покрытия можно дополнять веществами, подавляющими избыточный рост ГМК (например, сиролимусом) [41] или, наоборот, стимулирующими рост клеток эндотелия (например, эпидермальным фактором роста, ЭФР). Биоактивное покрытие стентов слоем ХС с добавлением ЭФР способствовало выживанию клеток эндотелия in vitro вследствие замедления апоптоза [42], улучшенному заживлению стента in vivo без таких неблагоприятных эффектов, как образование неоинтимы или тромбов [43].
Клинические исследования показали, что ОА способствует снижению системного хронического воспаления и болевого синдрома вследствие ингибирования сигнального пути NF-kB [14, 30]. Устойчивые клинические эффекты у пациентов с ОА достигаются на 2–4-й нед. при инъекционном введении ХС и ГС [44]. Дополнение терапии ХС пероральным приемом ГС способствует достижению устойчивой длительной ремиссии. Поэтому можно предположить, что для снижения риска рестеноза могут быть апробированы схожие режимы назначения ХС и ГС.
Такая апробация должна проводиться с использованием фармацевтических препаратов на основе высокоочищенных форм ХС (Хондрогард®) и ГС (Сустагард® Артро). Наличие в препаратах ХС и ГС посторонних примесей (особенно белкового происхождения) будет провоцировать провоспалительные реакции, препятствующие развитию желаемого фармакологического эффекта, и усиливать инфильтрацию макрофагами области неоинтимы стента. Использование ХС и ГС также позволяет снизить потребность в НПВП, тем самым снижая кардиотоксическую нагрузку.
Следует отметить, что представленный обзор не затрагивает вопросы снижения рисков рестеноза за счет внедрения новых технологий стентирования. Мы рассматривали основные патофизиологические механизмы, которые приводят к процессу рестенозирования.
Известно множество факторов риска, приводящих к рестенозу. Их можно разделить на системные (например, сахарный диабет), процедурные, связанные непосредственно с техникой стентирования, местные сосудистые детерминанты (например, извитость сосудов) [32]. В частности, показано, что пациенты с чрезмерным изгибом коронарных артерий имеют повышенный риск неблагоприятных кардиальных событий после имплантации стента [32].
Совершенно очевидно, что процесс формирования рестеноза при современных технологиях, направленных на его минимизацию, зависит от фенотипа пациента, включая индивидуальные параметры соматического статуса, преморбидный фон, а также от сопутствующей фармакотерапии, или, наоборот, от отсутствия необходимой фармакотерапии. Сегодня активно обсуждается возможность снижения риска рестеноза в зависимости от правильной оценки фенотипических особенностей пациента. Идет активный поиск биомаркеров, позволяющих осуществлять раннюю диагностику вероятного развития рестеноза [44, 45]. Остается открытым вопрос: гиперплазия интимы — это часть процесса заживления после имплантации стента или предиктор более поздних клинических рестенозов [46]? Однако уже сегодня показано, что первые 3 мес. являются наиболее критичными с точки зрения активности патофизиологического каскада, приводящего к формированию рестеноза. Это значит, что данный временной интервал и есть то самое «терапевтическое окно» для профилактики рестеноза. Именно в этот период следует активно проводить профилактические мероприятия, активные фармакологические интервенции, включая терапию ХС и ГС.
Заключение
Очевидно, что рестеноз — существенное осложнение кардиоваскулярного стентирования. Активация рецептора CD44 ассоциирована с патофизиологией рестеноза, стимулируя рост неоинтимы, инфильтрацию макрофагами области неоинтимы, гиперпролиферацию ГМК в области стента и накопление протеогликана версикана. Одновременно рецептор CD44 является таргетным белком молекул ХС и ГС, которые, взаимодействуя с рецептором CD44, способствуют инактивации провоспалительного белка NF-kB, препятствуют избыточной пролиферации ГМК в просвете стента и, как результат, могут тормозить рестеноз. Описанный механизм действия ХС и ГС открывает возможности для их применения с целью уменьшения воспалительных реакций у пациентов с сердечно-сосудистыми рисками, нуждающихся в лечении болевого синдрома, в частности, обусловленного ОА. На практике профилактика рестеноза может достигаться курсовым применением ХС и ГС в первые 3 мес. после операции. В соответствии с вышеописанными механизмами и имеющимися клиническими данными применение ХС и ГС будет способствовать не только снижению системного воспаления, но и торможению неоваскуляризации. Курсовое применение ХС и ГС должно начинаться с инъекционных форм (Хондрогард® 2 мл в/м через день, 25–30 инъекций) с последующим переходом на пероральный раствор
ГС (Сустагард® Артро 1500 мг/сут, 2–3 мес.). Курсы желательно повторять 2 раза в год.
Потенциальные ограничения
Приведенный обзор имеет ряд ограничений в части, касающейся представления клинических данных по использованию режимов применения ХС и ГС в условиях реальной клинической практики. Однако считаем, что представленная информация адресована широкому кругу специалистов, включая кардиологов, терапевтов, ревматологов, занимающихся проблемой профилактики рестеноза после проведенного стентирования, а также лечением пациентов с кардиоваскулярной патологией и наличием болевого синдрома, в частности, при ОА. Считаем, что обсуждение возможностей ХС и ГС позволит расширить показания для их применения.
Работа выполнена при поддержке грантов
РФФИ 16-29-12936, 18-07-00929, 18-07-00944.
Информация с rmj.ru





