Введение
Сохранение репродуктивного потенциала и бережное ведение каждой беременности — основная задача акушерско-гинекологической службы.
Женщина, вынашивающая ребенка, более подвержена острым респираторным заболеваниям и входит в группу риска по тяжелому течению острой респираторной вирусной инфекции [1–3]. Это связано с тем, что во время беременности возникают физиологические изменения во всех органах и системах организма, в том числе и в сердечно-сосудистой, дыхательной и иммунной. В связи с этим важно вовремя диагностировать респираторное заболевание, маршрутизировать пациентку и назначить правильное лечение.
В конце 2019 г. весь мир охватила пандемия инфекционного заболевания COVID-19, вызванного коронавирусом SARS-CoV-2 (Severe Acute Respiratory Syndrome Coronavirus 2). С момента открытия вируса он постоянно мутирует [4], что осложняет подбор эффективной терапии. В России известно около 1,5 тыс. мутаций коронавируса. В январе 2022 г. в России началась 5-я волна эпидемического подъема СOVID-19, вызванная новым высококонтагиозным штаммом вируса омикрон.
За период пандемии новой коронавирусной инфекции в 2019–2021 гг. установлено, что заболеваемость COVID-19 у беременных выше, чем в популяции в целом, а само заболевание приводит к множеству неблагоприятных исходов беременности (повышение материнской смертности относительно небеременных пациенток — 11,3% против 6,4%) [3, 5, 6]. Среди перинатальных исходов наиболее часто регистрируются дистресс-синдром плода (26,5–30,0%), низкая масса тела при рождении (25,0%), асфиксия новорожденных (1,4%)[1]. В связи с полученными данными на государственном уровне в разных странах были разработаны различные проекты, направленные на снижение материнской и перинатальной смертности от новой коронавирусной инфекции.
Ведущими специалистами здравоохранения г. Москвы было предложено изучить новые подходы в диагностике, маршрутизации, лечении новой коронавирусной инфекции у беременных и родильниц с целью уменьшения осложнений, связанных с гипериммунной реакцией организма, а также снижения частоты возникновения тяжелых форм заболевания и госпитализаций указанной группы женщин. Благодаря этому в Москве были созданы акушерский дистанционный консультативный центр (АДКЦ), где проводился мониторинг беременных пациенток, заболевших коронавирусной инфекцией, и стационары короткого пребывания (СКП) на базе двух московских городских больниц: ГБУЗ «ГКБ № 52 ДЗМ» и ГБУЗ «ГКБ № 15», где проводились обследования и лечение беременных и родильниц с высоким риском тяжелого течения заболевания. Выстроенная организационная модель направлена на выявление, наблюдение, активное мониторирование состояния беременных и родильниц с новой коронавирусной инфекцией, оказание помощи и проведение лечения на амбулаторном этапе пациенток с легким или среднетяжелым течением заболевания.
Беременные женщины — наиболее уязвимый контингент населения с ограниченным реестром разрешенных к применению препаратов, и это очень осложняет выбор метода лечения коронавирусной инфекции.
Одним из разрешенных к применению методов лечения COVID-19 является лечение моноклональными антителами — высокоперспективное направление в современной медицине.
Моноклональные антитела создавались задолго до пандемии новой коронавирусной инфекции и широко используются в лечении иммуноопосредованных заболеваний: псориаза, аутоиммунных заболеваний, ревматоидного артрита, рассеянного склероза, вирусных заболеваний и др. [7–9]. Большие перспективы эти технологии имеют и в онкологии в рамках таргетной терапии.
В 2019 г. создано огромное количество моноклональных антител для лечения COVID-19 [7]. Часть из них утратили эффективность в связи с мутациями вируса, другие же сохраняют свою эффективность и в настоящее время [8]. В середине 2021 г. в Российской Федерации было разрешено применение моноклональных антител для лечения беременных и родильниц с факторами риска тяжелого течения заболевания согласно методическим рекомендациям1 [5, 10].
Сотровимаб (VIR-7831) — рекомбинантный человеческий IgG, содержащий модификацию LS в домене Fc и способный проникать через плаценту от матери к плоду. Обладает высокой эффективностью при лечении коронавирусной инфекции [11]. Разрешение на временное обращение препарата сотровимаб в условиях пандемии выдано Минздравом России в соответствии с постановлением Правительства РФ от 03.04.2020 № 441[2].
Бамланивимаб (LY-CoV555 (LY3819253)) и этесевимаб (LY-CoV016 (LY3832479)) — моноклональные антитела, которые связываются с разными участками S-белка SARS-CoV-2.
Данные препараты показали высокую эффективность при лечении COVID-19 на ранних сроках заболевания.
Цель исследования: сравнить эффективность моноклональных антител, применяемых для лечения коронавирусной инфекции у беременных.
Содержание статьи
Материал и методы
Проведен ретроспективный анализ историй болезни 502 беременных и родильниц в возрасте от 18 до 49 лет, больных COVID-19, пролеченных моноклональными антителами с июля 2021 г. по март 2022 г. в ГБУЗ «ГКБ № 52 ДЗМ» и ГБУЗ «ГКБ № 15».
Основными критериями отбора пациенток были положительный ПЦР-тест на SARS-CoV-2, легкое и среднетяжелое течение заболевания, день болезни, наличие одного или нескольких факторов риска тяжелого течения коронавирусной инфекции: хронического заболевания легких, заболевания сердечно-сосудистой системы, артериальной гипертензии, сахарного/гестационного диабета, онкологического заболевания, ожирения (ИМТ 30 кг/м2 до беременности), хронического заболевания почек, печени, возраст 35 лет и старше.
Критериями невключения являлись отсутствие согласия на проводимое лечение и тяжелое состояние пациентки.
При поступлении в СКП пациентки предъявляли жалобы на кашель, слабость, боль в горле. Температура тела при этом не превышала 38 °C. Лечение моноклональными антителами назначалось решением врачебного консилиума на основании клинико-лабораторных и инструментальных данных. Все пациентки были информированы о проводимых методах терапии и подписывали согласие на лечение, одобренное Департаментом здравоохранения г. Москвы.
Пациентки были разделены на две группы: первую группу составили 108 пациенток, получавших препарат сотровимаб. Схема лечения: сотровимаб 500 мг + 0,9% раствор натрия хлорида 250 мл однократно в виде внутривенной инфузии длительностью 30 мин и более. Препарат не должен вводиться струйно или болюсно. После инфузии пациентка находилась под медицинским наблюдением как минимум в течение 1 ч.
Вторую группу составили 394 пациентки, получавшие комбинацию препаратов бамланивимаб и этесевимаб. Схема лечения: бамланивимаб 700 мг / 20 мл / 1 флакон + этесевимаб 1400 мг / 40 мл / 2 флакона + 0,9% раствор натрия хлорида 250 мл однократно внутривенно капельно в течение 75 мин. Комбинация лекарственных препаратов вводится под строгим контролем врача с последующим наблюдением пациентки в течение не менее 1 ч после введения.
От начала терапии за беременными и родильницами проводился ежедневный мониторинг в течение 14 дней. Лабораторные параметры контролировались на 1, 3, 7-й день от введения препарата. Выполняли общий анализ крови (с лейкоцитарной формулой), биохимический анализ крови (общий белок, АЛТ, АСТ, креатинин, мочевина, С-реактивный белок (СРБ)); коагулограмму (АЧТВ, МНО, ТВ, фибриноген), определение уровня антител (IgG, IgM ) к SARS-СоV-2 методом ИФА; мазок со слизистой носо-ротоглотки с последующим ПЦР-тестом на SARS-СоV-2. В те же сроки проводилось УЗИ легких, кроме этого, проводили УЗИ во время беременности и в послеродовом периоде.
Удаленный мониторинг осуществляли на 2, 4, 5, 6, 10, 14-й день, а также в послеродовом периоде. В течение всего периода наблюдения оценивали следующие показатели: сатурацию; динамику температуры тела, общее самочувствие пациентки. На основании данных критериев оценивали эффективность препаратов. Критериями выздоровления являлись отсутствие жалоб, элиминация вируса по данным ПЦР-исследования мазка на SARS-СоV-2, отсутствие данных за прогрессирование легочного поражения и синдрома системной воспалительной реакции. Также мы оценивали акушерские риски (синдром задержки развития плода, преэклампсия, хромосомные аномалии, пороки развития плода) и устанавливали, влияют ли коронавирусная инфекция и моноклональные антитела на их развитие. Проводилось наблюдение за развитием, состоянием плода и беременной с целью своевременного реагирования при подтверждении данных состояний.
При оценке безопасности оценивали побочные реакции, связанные с введением препаратов.
Специального отбора по сроку беременности и назначаемым препаратам не проводилось. Предварительный расчет необходимого размера выборки не проводили. Для статистического анализа данных использовали непараметрические методы описательной статистики: медиана, интерквартильный размах. Анализ данных выполнен с использованием пакета статистической программы IBM SPSS STATISTICS V-22. При сравнении количественных данных использовали U-критерий Манна — Уитни, качественных характеристик — критерий χ2 Пирсона. Различия считали статистически значимыми при p<0,05.
Результаты исследования
Практически по всем характеристикам пациентки были схожи. Средний возраст пациенток группы сотровимаба составил 31,94 года, группы бамланивимаб + этесевимаб — 33,25 года. В анамнезе у всех женщин было по 2 беременности, 0–1 родов. Доля пациенток с рвотой беременных в анамнезе в каждой группе составила по 20%. Все пациентки поступали в стационар на 4–5-й день болезни. В день поступления осуществляли введение препаратов. Оценка риска венозных тромбоэмболических осложнений во время беременности, которую проводили по шкале, предложенной RCOG в 2015 г. и утвержденной в клинических рекомендациях (протоколе лечения)[3], в группе сотровимаба составила 1,1 балла, в группе бамланивимаб + этесевимаб — 1,63 балла.
Все пациентки, получавшие терапию моноклональными антителами, имели положительный тест на РНК SARS-CoV-2, выполняемый методом ПЦР (рис. 1).
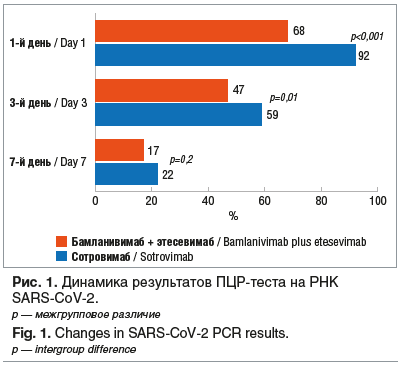
Данные диаграмм демонстрируют значительное снижение числа случаев положительного ПЦР-теста. Отсутствие 100% положительного результата ПЦР-теста на РНК SARS-CoV-2 в день проведения лечения было связано с тем, что пациентки поступали в стационар на 4–5-й день болезни. Амбулаторно выполненный тест был положительным во всех наблюдениях.
Также в обязательном порядке определялись антитела в крови, необходимые для оценки иммунного ответа на инфекцию. Иммуноглобулины класса М выявляются примерно на 7-й день от заражения, достигают пика через неделю и могут сохраняться в течение двух месяцев и более. Особенностью гуморального ответа на коронавирусную инфекцию является небольшой временной промежуток между появлением антител IgM и IgG, а иногда одновременное их формирование [8]. Как видно на рисунке 2, статистически значимых межгрупповых различий уровней иммуноглобулинов не выявлено.
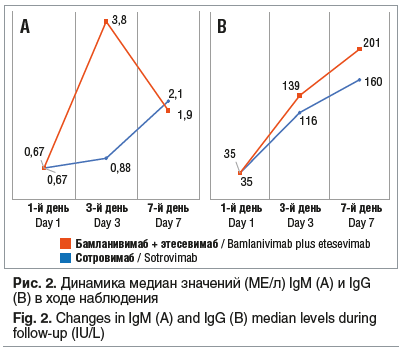
При анализе изменений других показателей крови хотелось бы отметить следующее: лимфопения и лейкопения, характерные для вирусной инфекции, не были ярко выражены у беременных. Фибриноген, повышающийся при нормальной беременности, чаще характеризовался незначительным дополнительным повышением.
При повышенном уровне СРБ при первичном обследовании пациентки отмечалось снижение его в 1,5 раза на 3-й день и значительное снижение на 7-й день от проведенной терапии (рис. 3).
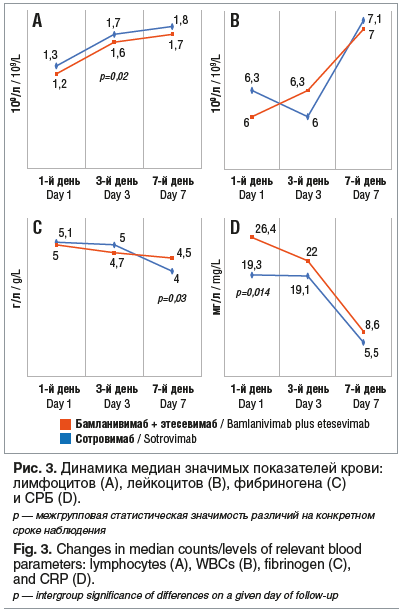
На 7-й день отмечалось повышение уровня печеночных ферментов, однако это связано не с применением данных препаратов, а с действием вируса на клетки печени. Ранее в исследованиях [12, 13] отмечено, что повышение уровня печеночных ферментов оценивается как неблагоприятный признак течения заболевания. Однако в нашем исследовании через 2 нед. после выздоровления ретроспективно отмечено снижение уровня трансаминаз без применения гепатопротекторов (рис. 4).
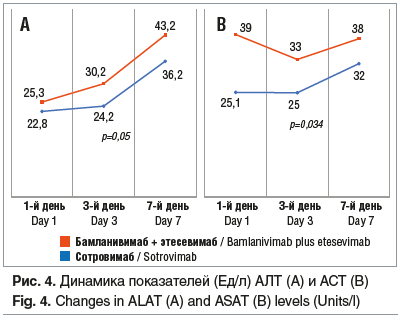
Для диагностики пневмонии мы предпочитали проводить УЗИ легких. Повреждение легких по данным УЗИ: основное поражение легких в обеих группах 1а и 2а степени либо абсолютное отсутствие повреждения легочной ткани. На рисунке 5 показана частота выявления поражения легких у пациенток на 1, 3 и 7-й день от проведенного лечения.
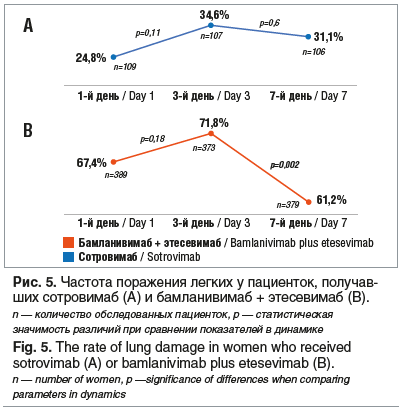
Поражение легких при отсутствии его признаков при первой явке пациентки могло проявиться на 3-й день даже при клиническом и лабораторном улучшении состояния пациентки, что говорит о том, что вирус уже находился в легочной ткани в начале лечения.
Побочных реакций в ответ на введение препаратов зафиксировано не было. При УЗИ во всех триместрах беременности, а также в послеродовом периоде плода на 3-й и 7-й день после введения препарата клинически значимых изменений (неразвивающаяся беременность, фето-фетальный синдром, неиммунная водянка плода, пороки развития плода, синдром задержки роста плода, антенатальная гибель плода, инволюция матки в послеродовом периоде), связанных с проведением терапии, не выявлено.
На момент написания статьи из 502 пролеченных пациенток известен исход беременности у 460: у 447 пациенток беременность закончилась родами. Своевременные самопроизвольные роды произошли у 259 пациенток, своевременные оперативные роды путем операции кесарева сечения — у 153, у одной пациентки проведена вакуум-экстракция плода. Преждевременные оперативные роды наступили у 20 пациенток, преждевременные самопроизвольные роды — у 14, из них 4 антенатальных гибели плода и 1 материнская смерть. Антенатальная гибель плода произошла у трех пациенток по акушерским причинам в сроке от 26 до 30 нед. беременности. Артифициальный аборт произошел у двух пациенток, самопроизвольный выкидыш — у шести пациенток и неразвивающаяся беременность — у двух. Сроки и способ родоразрешения зависели от следующих факторов: состояние беременной, срок беременности, состояние плода. Экстренное кесарево сечение проводилось при ухудшении состояния роженицы, дистресс-синдроме плода и слабости родовой деятельности. В целом COVID-19 и своевременно проведенное лечение не повлияли на акушерские исходы и тактику ведения пациенток с акушерской точки зрения, которые соответствовали таковым в общей популяции.
Установлено, что оба метода лечения имеют высокую эффективность. У части пациенток сохранялись положительный ПЦР-тест на COVID-19, катаральные явления и гипертермия не более 37,5 °С. Прогрессирования легочного поражения и синдрома системной воспалительной реакции не наблюдалось. В течение 14 дней наблюдения у 96% пациенток, получивших препарат сотровимаб, наступило выздоровление. В группе, получившей комбинацию моноклональных антител бамланивимаб + этесевимаб, эффективность за тот же период составила 89%. Акушерские осложнения (синдром задержки развития плода, преэклампсия, хромосомные аномалии, пороки развития плода, преждевременная отслойка нормально расположенной плаценты) на фоне проведенного лечения не наблюдались.
Обсуждение
Физиологические, механические и иммунологические изменения во время беременности потенциально могут повлиять на восприимчивость к SARS-CoV-2-инфекции и тяжесть ее течения во время беременности. Состояние пациенток может ухудшаться за считанные часы. Ведение и лечение беременных во время пандемии осложняет то обстоятельство, что одобрение препаратов для лечения COVID-19 было экстренным, в их испытаниях не участвовали беременные женщины, кроме того, пациентки испытывали страх перед любыми последствиями, которые могут повлиять на беременность. Полученные в ходе настоящего исследования данные согласуются с данными исследований, подтверждающих безопасность и эффективность моноклональных антител при SARS-CoV-2-инфекции [14, 15].
На основании полученных нами данных мы пришли к выводу, что применение моноклональных антител у беременных и родильниц для лечения новой коронавирусной инфекции может позволить улучшить перинатальные исходы и течение беременности при COVID-19, снизить материнскую и перинатальную смертность, число госпитализаций и осложнений, что позволит снизить материальные затраты на реабилитацию и лечение осложнений у матери и ребенка.
Заключение
Моноклональные антитела доказали свою высокую эффективность в лечении беременных и родильниц на ранних сроках заболевания COVID-19 и не оказывали отрицательного воздействия на организм матери и ребенка.
Сведения об авторах:
Поликарпова Ольга Валентиновна — врач акушер-гинеколог отделения гинекологии ГБУЗ «ГКБ № 52 ДЗМ»; 123182, Россия, г. Москва, ул. Пехотная, д. 3; ORCID iD 0000-0001-9060-3005.
Доброхотова Юлия Эдуардовна — д.м.н., профессор, заведующая кафедрой акушерства и гинекологии лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-7830-2290.
Грабовский Василий Михайлович — заместитель главного врача по акушерству и гинекологии ГБУЗ «ГКБ № 52 ДЗМ»; 123182, Россия, г. Москва, ул. Пехотная, д. 3; ORCID iD 0000-0002-7048-4827.
Шевченко Николай Алексеевич — к.м.н., заведующий отделением гинекологии ГБУЗ «ГКБ № 52 ДЗМ»; 123182, Россия, г. Москва, ул. Пехотная, д. 3; ORCID iD 0000-0001-5869-367X.
Лысенко Марьяна Анатольевна — д.м.н., главный врач ГБУЗ «ГКБ № 52 ДЗМ»; 123182, Россия, г. Москва, ул. Пехотная, д. 3; ORCID iD 0000-0002-2636-2558.
Контактная информация: Доброхотова Юлия Эдуардовна, e-mail: pr.dobrohotova@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 26.04.2023.
Поступила после рецензирования 24.05.2023.
Принята в печать 12.06.2023.
About the authors:
Olga V. Polykarpova — obstetrician and gynecologist of the Department of Gynecology, City Clinical Hospital No. 52; 3, Pekhotnaya str., Moscow, 123182, Russian Federation; ORCID iD 0000-0001-9060-3005.
Yuliya E. Dobrokhotova — Dr. Sc. (Med.), Professor, Head of the Department of Obstetrics and Gynecology of the Faculty of Medicine, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-7830-2290.
Vasiliy M. Grabovskiy — Deputy Head Doctor for Obstetrical Gynecological Service, City Clinical Hospital No. 52; 3, Pekhotnaya str., Moscow, 123182, Russian Federation; ORCID iD 0000-0002-7048-4827.
Nikolay A. Shevchenko — C. Sc. (Med.), Head of the Department of Gynecology, City Clinical Hospital No. 52; 3, Pekhotnaya str., Moscow, 123182, Russian Federation; ORCID iD 0000-0001-5869-367X.
Maryana A. Lysenko — Dr. Sc. (Med.), Head Doctor, City Clinical Hospital No. 52; 3, Pekhotnaya str., Moscow, 123182, Russian Federation; ORCID iD 0000-0002-2636-2558. Contact information: Yuliya E. Dobrokhotova, e-mail: pr.dobrohotova@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 26.04.2023.
Revised 24.05.2023.
Accepted 12.06.2023.
Информация с rmj.ru






