Для цитирования: Маркова Т.П., Чувиров Д.Г. ОРВИ: профилактика и лечение в эпидемический сезон // РМЖ. Медицинское обозрение. 2016. №3. С. 171-176
В статье рассмотрены вопросы профилактики и лечение ОРВИ в эпидемический сезон
 Для цитирования. Маркова Т.П., Чувиров Д.Г. ОРВИ: профилактика и лечение в эпидемический сезон // РМЖ. 2016. № 3. С. 171–176.
Для цитирования. Маркова Т.П., Чувиров Д.Г. ОРВИ: профилактика и лечение в эпидемический сезон // РМЖ. 2016. № 3. С. 171–176.
Распространение информации о нарастании заболеваемости острыми респираторными вирусными инфекциями (ОРВИ) в средствах массовой информации влияет на заболеваемость гриппом, по данным исследователей Шенскийского педагогического университета (Китай) и Йоркского университета Канады. Исследование проводили, сравнивая число госпитализаций с количеством сообщений в СМИ и их длительностью. Установлена связь между этими фактами с некоторой временной задержкой в 3–4 дня. Частота госпитализаций снижалась в 2 раза, если в течение 10 дней увеличивалась длительность сообщений в СМИ о гриппе. Внимание средств вещания и печатных СМИ к теме эпидемии гриппа как медицинской и социально значимой проблеме повышает осторожность людей, что ведет к уменьшению контактов и снижению заболеваемости. Проведенное исследование подтверждает значение и влияние информации в современном обществе даже на частоту заболевания гриппом [1].
22 января 2016 г. специалисты НИИ гриппа Мин-здрава России в Санкт-Петербурге объявили о начале эпидемии гриппа и ОРВИ в России, 26 января эпидемия была зарегистрирована в Москве. Идентифицирован вирус H1N1 («свиной» грипп) [2]. В различных регионах был введен режим карантина для школьников: в Адыгее, Карачаево-Черкесии, Якутске, Смоленске, Воронеже, Тамбове, Липецке, Оренбурге, Челябинске, Екатеринбурге, Ханты-Мансийске.
При массовых вспышках гриппа инфекция может охватить 5–10% населения [3, 4]. Во время эпидемии смертность в мире, обусловленная гриппом или его осложнениями, в среднем может достигать 870 случаев на 100 тыс. населения. По данным ВОЗ, развитие пандемии может быть связано с появлением нового штамма вируса (грипп типа А), против которого у людей отсутствует иммунитет. Во время прошлых пандемий гриппа было инфицировано 20–40% населения [5]. В XX в. зарегистрированы 3 пандемии, наиболее опасная из них – «испанка» (H1N1) унесла 30 млн жизней, что превысило потери во время Первой мировой войны [6]. Следующая пандемия (штамм H2N2) началась через 40 лет в Азии, в результате умерли более 1 млн человек. Третья пандемия, за 6 нед. унесшая жизни более 800 тыс. человек, была вызвана штаммом H3N2, который появился в Гонконге в 1968–1969 гг.
В последние годы в мире произошло несколько вспышек гриппа, передающегося от птиц: в Гонконге, Европе, на Дальнем Востоке. Контролировать вспышки до сих пор удавалось за счет массового забоя домашней птицы. В 2009 г. наблюдалась эпидемия, вызванная вирусом гриппа типа А (H1N1, штамм «Калифорния»), так называемого «свиного» гриппа. В России в результате анализа клинических материалов в 2009 г. от 1114 больных выявлена суммарная частота гриппа 12,6%, в т. ч. гриппа A(H1N1), A(H3N2), гриппа типа А и В – 2,9; 5,7; 1,4 и 2,5% соответственно [7].
На создание эффективной вакцины против нового штамма вируса, по данным ВОЗ, требуется не менее 5–6 мес. За это время количество заболевших может достигать нескольких миллионов, поэтому возрастает значение противовирусных препаратов и неспецифической профилактики.
Предотвращение развития пандемии необходимо обеспечивать заранее, т. к. во время эпидемии существенно возрастает расход лекарственных препаратов, потребность в первичных консультациях, число обращений к врачам, частота госпитализаций и осложнений. По прогнозам ВОЗ, при пандемии за короткий срок число посещений в поликлиниках может достигать 233 млн, поступлений в больницы – 5,2 млн, смертей – 7,4 млн [8].
Предполагают, что наиболее выраженные проявления пандемии придутся на слаборазвитые страны из-за недостаточно организованной работы системы здравоохранения. С другой стороны, будет наблюдаться недостаток вакцины, медицинского персонала, что повлечет нарушения работы здравоохранения, общественного транспорта, правоохранительных органов. Без развития пандемии в США ежегодно от гриппа умирают от 10 тыс. до 40 тыс. человек, при этом за последние 60 лет не отмечено снижения показателей смертности от гриппозной пневмонии [9].
Несмотря на успехи профилактики, объем вакцинации остается ограниченным [10, 11]. Например, в США в 1997 г. вакцинированных в возрасте до 65 лет было менее 30%. Не всегда наблюдается полное соответствие структуры вакцины циркулирующим штаммам, соответственно защитный эффект такой вакцины составляет 70–90%. В группах риска (дети, пожилые люди старше 50 лет, пациенты с сопутствующими заболеваниями, иммунодефицитами, аллергическими заболеваниями) эффективность вакцины снижается до 30–40% [12, 13].
В группах риска, для которых характерны более тяжелое течение заболевания, развитие осложнений и смертельные исходы, по рекомендациям ВОЗ вакцинация проводится только субъединичными вакцинами. У пожилых людей высок риск серьезных осложнений, приводящих к госпитализации и повышенной смертности, включая вторичную бактериальную пневмонию, обострения сопутствующих хронических заболеваний. Инактивированные противогриппозные вакцины применяются более 50 лет, они безопасны, проверены на миллионах людей. Вакцинация уменьшает число смертельных исходов, развитие и тяжесть осложнений.
Группы населения, подлежащие вакцинации [14]:
1) лица старше 65 лет;
2) больные, находящиеся в стационарах независимо от возраста;
3) беременные женщины;
4) дети до 3-х лет;
5) дети и подростки от 6 мес. до 18 лет, включая длительно получавших ацетилсалициловую кислоту;
6) лица, страдающие хроническими заболеваниями легких или сердечно-сосудистой системы;
7) лица, страдающие нарушением обменных процессов, включая сахарный диабет;
8) лица, страдающие гемоглобинопатиями (например, серповидно-клеточной анемией);
9) больные со стафилококковой инфекцией;
10) больные с иммунодефицитами (ВИЧ-инфицированные, лица, получающие иммунодепрессанты, лучевую и химиотерапию, реципиенты трансплантатов);
11) лица, относящиеся к группам повышенного риска [14]:
a) медицинские работники;
б) члены семей больных;
в) взрослые, находящиеся в контакте с детьми до 6-месячного возраста;
г) другие группы (лица, имеющие частые контакты по роду работы, часто мигрирующие внутри и вне страны, студенты).
У беременных женщин велик риск осложнений после гриппа, мертворождений и прерывания беременности, у детей при заболевании матери гриппом в момент беременности и кормления грудью повышен риск развития опухолей мозга, нейробластомы. Рекомендована вакцинация беременных женщин, если срок составляет 14 нед. в период подъема заболеваемости или эпидемии [14].
Учитывая большое количество вирусов, способных вызывать ОРВИ, заболеваемость гриппом после вакцинации должна быть подтверждена серологически.
По данным James F. Marx, отмечено снижение числа заболевших гриппом после проведения вакцинации сотрудников медицинских учреждений. В сезон 2011–2012 гг. в Калифорнии удалось вакцинировать 68% медработников. При вакцинации 90% сотрудников заболеваемость гриппом в этом штате может быть снижена на 30 тыс. случаев ежегодно, это значительный успех, учитывая 200 тыс. госпитализаций в масштабах страны по поводу гриппа ежегодно и 24 тыс. случаев смертельных исходов. Во время сезона гриппа всех врачей обязывают пройти вакцинацию или носить защитные маски. Принимаемые меры позволят защитить пациентов и снизить заболеваемость, включая население и врачей [2].
Во время эпидемии 2009 г. грипп был зарегистрирован в 214 странах, число летальных исходов составило 18 тыс. 90% заболевших были в возрасте до 65 лет, характерным признаком среди умерших было быстрое поражение легких с развитием респираторного дистресс-синдрома. У 26–38% умерших была определена вирусно-бактериальная микст-инфекция. За октябрь – декабрь 2009 г. в России переболели 13,26 млн человек, 44% из них лица 18–39 лет. По данным департамента здравоохранения г. Екатеринбурга за 2009 г., среди заболевших 91,8% составили непривитые, 100% умерших были не привиты против сезонного гриппа [15].
Проведение вакцинации не всегда возможно, особенно в группах риска: у детей, людей старше 60 лет, пациентов с сопутствующими заболеваниями, иммунодефицитами, аллергическими заболеваниями. Для группы риска характерны более тяжелое течение инфекции, развитие осложнений и смертельные исходов. У лиц преклонного возраста, пациентов с иммунодефицитом эффективность вакцинации снижается до 30–40%.
Для развития пандемии необходимо появление нового вируса, против которого в организме не сформированы структуры иммунологической памяти, вирус должен обладать высокой контагиозностью и передаваться от человека к человеку [16]. Известно более 200 респираторных вирусов, участвующих в формировании вирусно-бактериальных микст-инфекций при ОРВИ. Перечисленные факты ставят ряд задач перед исследователями и клиницистами и стимулируют получение новых противовирусных препаратов и проведение неспецифической профилактики респираторных инфекций.
Для лечения и профилактики ОРВИ назначают противовирусные препараты, учитывая клинические проявления, начало острого периода заболевания. Известно, что 95% ОРВИ имеют вирусную этиологию.
Противовирусные препараты представлены тремя группами:
1) блокаторы М2-каналов вируса гриппа типа А – римантадин, амантадин;
2) ингибиторы нейраминидазы вируса гриппа типа А и типа В – осельтамивир, занамивир;
3) другие препараты.
Белок М2 играет важную роль на ранних этапах вирусной инфекции, нарушает процесс сборки вирусных частиц и их репликацию. Римантадин обладает противовирусной активностью в отношении вируса гриппа А, уменьшает токсическое влияние вируса гриппа В. К сожалению, штаммы вируса гриппа типа А, подтипов Н1N1 и H3N2 перестали быть чувствительными к римантадину, т. е. происходит развитие резистентности к препарату [17]. Назначение препарата в острый период снижает клинические проявления ОРВИ у детей, особенно при гриппе типов А и В. Основные противопоказания к назначению римантадина: гепатит, нефрит, почечная недостаточность, тиреотоксикоз, беременность, кормление грудью. Побочные действия: аллергические реакции, боли в животе.
Осельтамивир, ингибитор нейраминидазы, активен по отношению ко всем вирусам гриппа. Показана его эффективность в отношении штаммов вируса гриппа птиц Н7 и Н9, а также H5N1. Препарат проникает во все органы и ткани, где происходит размножение вируса. Он подавляет синтез нейраминидазы – вирус не может покинуть клетку-хозяина и погибает. Осельтамивир назначают для профилактики и лечения гриппа [18–20]. Препарат быстро абсорбируется из ЖКТ и метаболизируется в осельтамивира карбоксилат. 75% принятой дозы попадает в кровоток в виде осельтамивира карбоксилата, менее 5% – в неизмененном виде.
Применение препарата разрешено взрослым и детям с года жизни, в том числе вакцинированным против гриппа в случае их заболевания, а также представителям групп риска: пожилым, пациентам, страдающим хроническими заболеваниями или одновременно принимающим несколько лекарственных препаратов.
Лечение должно начинаться в первые 40 ч после появления симптомов гриппа. Прием препарата в первые 12 ч сокращает продолжительность заболевания более чем на 3 дня по сравнению с приемом через 48 ч. У детей прием осельтамивира в первые сутки заболевания сокращает длительность симптомов на 36 ч. Препарат взрослым и детям с 8 лет назначают по 75 мг 2 раза в сутки в течение 5 дней. Детям от 1-го года – 3-х лет осельтамивир назначают в виде суспензии. С целью профилактики достаточно приема препарата по 75 мг 1 раз в сутки [19, 20].
При использовании для профилактики осельтамивир эффективен в отношении вирусов гриппа типов А и В. После контакта с больным назначение препарата снижает вероятность заболевания на 60–90%; предсезонная профилактика приводит к сходным результатам [20]. В профилактических целях прием следует начинать в первые 2 дня после контакта с инфицированным. Для профилактики осельтамивир назначают детям старше 1 года, подросткам старше 12 лет и взрослым, относящимся к группе повышенного риска инфицирования вирусом. Данных по применению препарата у беременных женщин недостаточно, его следует назначать во время беременности или кормящим матерям, если преимущества от его применения превышают потенциальный риск для плода или грудного ребенка.
Назначение осельтамивира может приводить к развитию резистентности. Изоляты вируса гриппа типа А при снижении чувствительности к осельтамивиру были исследованы в культуре in vitro, с увеличением дозы осельтамивира карбоксилата. Генетическй анализ показал, что снижение чувствительности к осельтамивиру связано с мутациями и изменением аминокислот нейраминидазы и гемагглютинина. В частности, наблюдались мутации I222T и H274Y нейраминидазы N1 вируса гриппа типа А и I222T и R292K нейраминидазы N2 вируса гриппа типа А. Для нейраминидазы N9 вируса гриппа типа А у птиц были типичны мутации E119V, R292K и R305Q; для гемагглютинина вируса гриппа типа А H3N2 – мутации А28Т и R124М, для гемагглютинина реассортантного вируса (геном состоит из генома вируса человека и птиц) человека/птиц H1N9 – мутация Н154Q [21].
Осельтамивир получили более 40 млн пациентов в 80 странах мира: в США, Японии, Канаде, Австралии, Швейцарии, странах Европы и Латинской Америки. Длительность симптомов гриппа, таких как кашель, миалгия, головные боли и лихорадка, после лечения осельтамивиром уменьшается по сравнению с плацебо на 40% (10). Частота осложнений у больных гриппом при лечении осельтамивиром снижается на 50% по сравнению с плацебо.
Занамивир – противовирусный препарат, высокоселективный ингибитор нейраминидазы (поверхностного фермента вируса гриппа), действие направлено против вирусов гриппа типов А и В. Вирусная нейраминидаза обеспечивает высвобождение вирусных частиц из инфицированной клетки, ускоряет проникновение вируса через слизистые и инфицирование клеток дыхательных путей. Активность занамивира показана in vitro и in vivo и направлена против всех 9 подтипов нейраминидаз вирусов гриппа. Развития резистентности к занамивиру не зарегистрировано. Препарат выпускается в виде порошка для ингаляций через дискхалер, биодоступность низкая (в среднем 2%). Показания – лечение и профилактика гриппа типов А и В у детей старше 5 лет и у взрослых. При лечении гриппа типов А и В взрослым и детям старше 5 лет рекомендуется назначать по 2 ингаляции (2×5 мг) 2 раза в день (суточная доза: 20 мг для взрослых, 10 мг для детей) в течение 5 дней. Для профилактики – по 2 ингаляции (2×5 мг) 1 раз в день (суточная доза 10 мг) в течение 10 дней, курс может быть продлен до месяца при опасности инфицирования. Для профилактики гриппа занамивир эффективен у детей старше 5 лет и у 67–79% взрослых, что достоверно по сравнению с плацебо.
Аллергические реакции: в редких случаях отек лица и гортани, бронхоспазм, затруднение дыхания, высыпания, крапивница. В постмаркетинговых исследованиях (преимущественно с участием детей, Япония) отмечались судорожные припадки, делирий, галлюцинации и девиантное поведение у пациентов, инфицированных вирусом гриппа и принимающих занамивир. Явления наблюдались на ранних стадиях заболевания, часто имели внезапное начало и быстрое наступление исхода. Причинно-следственная связь между приемом занамивира и вышеуказанными явлениями не была доказана [21].
Благодаря химической структуре занамивира резистентность к нему развивается в меньшей степени, чем к осельтамивиру [21, 22].
Перамивир – ингибитор нейраминидазы, новый препарат кампании BioCryst, разрешен к применению в Японии и Южной Корее, в России не зарегистрирован. В плацебо-контролируемых исследованиях с участием 427 взрослых пациентов 1 доза перамивира (300 мг) вводилась внутримышечно в течение первых 48 ч появления симптомов гриппа. Затем 14 дней пациенты вели записи о своем самочувствии. Как показали результаты испытаний, длительность острого периода гриппа уменьшалась на 22 ч (у получивших 1 дозу перамивира симптомы заболевания проходили через 113,2 ч, у получивших плацебо – через 134,8 ч). Отмечено существенное снижение выделения вируса от больного в первые 2 сут после введения препарата [23].
Американский Центр по контролю и предотвращению заболеваний (CDC) в Атланте представил рекомендации по профилактике и лечению гриппа. Для проведения профилактики рекомендована вакцинация, произведено изменение состава вакцин, направленное против H1N1 (с учетом «свиного» гриппа). Для лечения гриппа типов А и В рекомендованы ингибиторы нейраминидазы: осельтамивир, занамивир и перамивир. Лечение нужно начинать не позднее 48 ч от начала заболевания. Осельтамивир разрешен к применению Управлением по контролю за продуктами и лекарствами (FDA), США, для лечения заболевших гриппом детей в возрасте от 2 нед., беременных; CDC рекомендует также лечить детей младше 2 нед. Занамивир рекомендован для лечения гриппа начиная с возраста 7 лет. Внутривенный препарат перамивир разрешен к применению с возраста 18 лет. Особое внимание необходимо уделить группе риска (дети в возрасте младше 2-х лет, пожилые старше 65 лет, пациенты с хроническими заболеваниями, включая бронхиальную астму, сердечно-сосудистые заболевания, болезни почек и печени, диабет, болезни крови, болезни нервной системы, ВИЧ-инфицированные, беременные), а также пациентам до 19 лет, длительно получающим ацетилсалициловую кислоту, и лицам с ожирением. При выявлении резистентности к осельтамивиру и перамивиру рекомендуют введение занамивира внутривенно. Учитывая, что к амантадину и римантадину выявлен высокий уровень резистентности вируса гриппа типа А, CDC не рекомендует данные препараты к применению [24].
Представляет интерес препарат Амизон (энисамиума йодид): действующее вещество является производным изоникотиновой кислоты (N-метил-4-бензил карбамидопиридиния йодид), обладает противовирусным действием, ингибирует проникновение вируса через мембраны клеток, индуцирует синтез интерферона, лизоцима.
Препарат назначают в острый период респираторной инфекции по 0,5 г 3 раза в день (до 2 г в сутки) после еды в течение 5–7 дней. В России препарат разрешен к применению с 18 лет, однако сейчас проводятся многоцентровые рандомизированные плацебо-контролируемые клинические исследования для расширения возрастных групп и показаний: 1 – дети с 2 до12 лет, 2 – подростки с 12 до 18 лет, 3 – взрослые, профилактика гриппа и ОРВИ.
Побочные действия: ощущение горького вкуса во рту, возможно развитие отека слизистой ротовой полости, что не требует отмены препарата. Горький вкус во рту может быть связан с наличием йода в составе Амизона и возможностью выделения небольших количеств препарата со слюной; эти ощущения проходят самостоятельно и не требуют специальной терапии.
Противопоказания: беременность, возраст до 18 лет, период лактации, непереносимость компонентов препарата, йода, недостаточность лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция.
Показана чувствительность вируса гриппа типа А к Амизону, который в культуре in vitro 100-кратно угнетает репликацию подтипов вируса (H1N1, H1N1pdm09 и H3N2). Добавление Амизона в течение первых 4 ч после инфицирования приводит к снижению титра вируса более чем в 100 раз, т. е. препарат действует на начальных этапах синтеза вирусных частиц. Амизон угнетает синтез респираторно-синцитиального вируса в культуре NHBE, снижая титр вируса более чем в 100 раз, что коррелирует со снижением уровня вирусной РНК. Получены данные об активности Амизона против аденовирусов и коронавирусов. Поглощение Амизона дифференцированными нормальными бронхоэпителиальными клетками человека in vitro в культуре NHBE (normal human bronchial epithelial cells) было довольно высоким. Клетки культуры были инкубированы с вирусом гриппа типа А и осельтамивиром (контроль) или Амизоном. Амизон снижал синтез подтипов вирусов гриппа типа А, включая H1N1, имевшего мутацию H275YNA (осельтамивир-резистентный вирус). Полной блокировки синтеза вирусных частиц не наблюдалось. Противовирусный эффект Амизона выражен при низких дозах, в первые 8 ч после инфицирования культуры. Увеличение дозы Амизона не приводит к усилению эффекта [25].
Первые упоминания об Амизоне появились в 1998 г. [26]. Показан анальгезирующий, жаропонижающий, антиоксидантный эффект препарата. По противовоспалительной активности Амизон превосходит ибупрофен и не оказывает раздражающего действия на слизистую желудочно-кишечного тракта, что позволяет назначать препарат при сочетанной патологии желудка [27]. Амизон обладает антиэкссудативным действием, что позволяет уменьшить отек тканей и выраженность сосудистых воспалительных реакций за счет стабилизации мембран клеток и лизосом, торможения де-грануляции базофилов и тучных клеток и снижения выброса и регуляции медиаторов воспаления [28]. При приеме Амизона максимальная концентрация в крови достигается через 2,5 ч, период полувыведения – 14 ч, 90–95% его метаболитов выводятся с мочой [29].
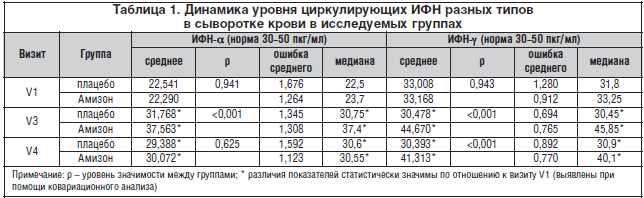
В различных исследованиях отмечена интерфероногенная активность препарата, не уступающая тилорону. Уровень ИФН-α и ИФН-γ повышаются в 2–3 раза после приема Амизона. Введение здоровым мышам Амизона приводило к активации экспрессии генов цитокинов ИЛ-1, ИЛ-2, ИЛ-12. У пациентов с ОРВИ при назначении Амизона на 7-й день приема отмечалось повышение продукции ИФН-α и ИФН-γ по сравнению с исходным уровнем и группой, получавшей плацебо (табл.1) [29].
У больных ОРВИ, включая грипп, назначение Амизона ускоряло исчезновение симптомов острого периода. Нормализацию температуры тела к 3-му дню лечения отмечали 73% пациентов, получавших Амизон в ходе клинического исследования, проведенного ФГБУ «НИИ гриппа» Минздрава России. Продолжительность лихорадки сокращалась в среднем на 1,1 дня. Улучшение самочувствия в группах, получавших Амизон и плацебо, было у 43,3 и 15% пациентов соответственно. На 7–й день приема Амизона почти все пациенты (59 человек из 60) отметили исчезновение симптомов. В группе, получавшей плацебо, в это время 37,5% пациентов испытывали недомогание и снижение активности [30].
По данным А.Ф. Фролова и соавт., Амизон может быть использован для профилактики гриппа и ОРВИ в период сезонного подъема заболеваемости. На ряде промышленных предприятий, в школах-интернатах, воинских частях Амизон получали 1869 взрослых и 625 детей и подростков в возрасте от 7 до 16 лет. Отмечено снижение заболеваемости ОРВИ в 3–6 раз по сравнению с контрольными группами. При возникновении ОРВИ инфекция протекала менее тяжело и отмечалось снижение осложнений (пневмонии, бронхиты, гаймориты). 323 взрослых и 116 подростков (военнослужащие и учащиеся воинского лицея-интерната) получали для профилактики гриппа и ОРВИ Амизон и аскорбиновую кислоту. Группа контроля (384 взрослых и 105 подростков) получала бендазол и аскорбиновую кислоту. Уровень заболеваемости был достоверно ниже у получавших Амизон взрослых в 3,6±0,2 раза, подростков – в 4,2±0,15 раза (р<0,001) [18, 19].
Повышение уровня ИФН-α отмечено в 3–4 раза при его исходном снижении и сохраняется в течение 2,0–2,5 мес. При контакте с больным гриппом или ОРВИ родственниками или при профессиональных контактах (врачи, медсестры) рекомендован прием Амизона взрослым по 0,25 г 3 раза в сутки в течение 3–5 дней, затем по 0,25 г в день на протяжении периода контактов. Аналогичные исследования были проведены в целях профилатики ОРВИ у детей [28].
Профилактический прием Амизона проводили в осеннее-зимний период члены 69 врачебных семей (272 человека, включая 205 взрослых и 67 детей и подростков). За 6 мес. наблюдения только у 4-х человек из них были зарегистрированы ОРВИ, тяжелого течения и осложнений не было отмечено. 65 человек в этих же семьях не принимали Амизон по разным причинам (возраст до 6 лет, аллергия к йоду). В этой группе грипп или ОРВИ возникли у 28 (43,1%), в том числе у 12 детей в возрасте до 6 лет. За 6 мес. наблюдения у 4-х детей зарегистрировано 2 эпизода и у 3-х детей – 3 повторных эпизода ОРВИ. Ангины отмечены у 8 человек, 6 человек из них были госпитализированы. В 28 семьях были зарегистрированы больные гриппом или ОРВИ, при этом остальные члены семей, принимавшие в этот период Амизон (85 человек, в том числе дети), не заболели. В двух из 28 семей лица, не получавшие Амизон (дети 4–х лет и 4,5 года) и контактировавшие с источником инфекции, заболели гриппом [28].
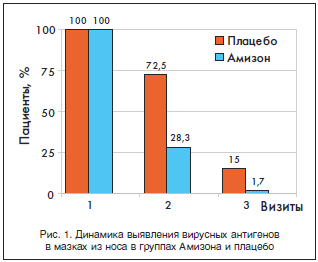
По данным клинического исследования, проведенного ФГБУ «НИИ гриппа» Минздрава России, использование препарата Амизон способствует статистически значимому сокращению продолжительности выделения вирусных антигенов из носовых смывов. Для оценки эффективности терапии препаратом Амизон был проведен иммунофлюоресцентный анализ – так, на 3–й день от начала терапии вирусные антигены определялись только в 28,3% случаев в группе пациентов, принимавших Амизон, и в 72,5% случаев в группе пациентов, получавших плацебо (рис. 1). Это говорит о том, что Амизон не только оказывает противовирусный эффект, но и позволяет не заражать окружающих [29].
Cимптоматическая терапия в острый период ОРВИ включает жаропонижающие, деконгестивные, противовоспалительные и анальгезирующие препараты. Часто один препарат обладает сочетанным действием (табл. 2).
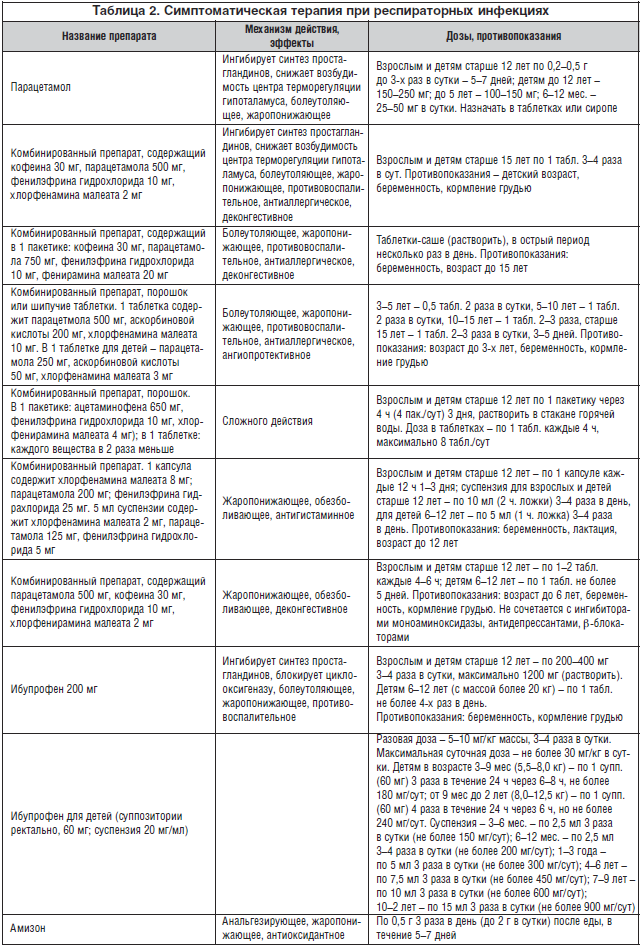
Назначение симптоматической терапии облегчает состояние пациента в острый период ОРВИ. Опубликованы данные о том, что назначение парацетамола беременным женщинам повышает риск развития бронхиальной астмы у 5% детей в дальнейшем в возрасте 3-х лет [31].
Таким образом, лечение и профилактика ОРВИ представляют комплекс методов и лекарственных препаратов, направленный на снижение частоты осложнений и смертельных исходов. Комплексное лечение может включать: противовирусные препараты (осельтамивир, занамивир, римантадин и др.); препараты, обладающие противовирусным и интерфероногенным эффектом (Амизон) и симптоматическую терапию (парацетамол, ибупрофен, комбинированные препараты). Амизон оказывает анальгезирующий, жаропонижающий, антиоксидантный эффекты, что позволяет уменьшить длительность острого периода ОРВИ и назначение других лекарственных препаратов.
Литература
1. Media coverage and hospital notifications: Correlation analysis and optimal media impact duration to manage a pandemic // Journal of Theoretical Biology. 2016. doi:10.1016/j.jtbi.2015.11.002 2.
2. www.univadis.ru. Раздел «Новости медицины». 29. янв. 2016 г.
3. Palach А.M. Tens years experience with a subunit influenza vaccine // Europ. J.of Clin. Research. 1992. Vol. 3 Р. 117–138.
4. Uphoff H., Cohen J.M., Fleming D., Noone A. Harmonisation of national influenza surveillance morbidity data from EISS: a simple index. // Euro Surveill. 2003 Jul. Vol. 8 (7). Р. 156–64.
5. Aymard M. Hospices Civils de Lyon, France. Presentation at a symposium entitled. Meeting the challenge of influenza., European Respiratory Society 1998 Annual Congress, Geneva, Switzerland.
6. Collier L. et al. Orthomyoxoviruses and influenza. Human Virology (2nd ed). Oxford: Oxford University Press, 2000. Р. 85.
7. www.gripp.ru. Раздел «Новости медицины». 28 июля 2009 г.
8. WHO checklist for influenza pandemic preparedness planning. Geneva, World Health Organization, 2005.
9. Center for Disease Control and Prevention (CDC). Prevention and control of influenza: recommendations of the Advisory Committee on Immunization Practices (ACIP) // MMWR. 2000. Vol. 49. Р. 1–38.
10. Murphy B.R.,Webster R.G. Orthomyxoviruses. In: Fields B.N. et al. editors. Fields virology, 3rd Edn. Philadelphia, USA: Lippincott–Raven, 1996. Р. 1397–445.
11. Palache AM. Influenza vaccines. A reappraisal of their use // Drugs. 1997. Vol. 54. Р. 841–856.
12. Arden N.H., Patriarca P.A., Kendal A.P. Experiences in the use and efficacy of inactivated influenza vaccine in nursing homes. In: Kendal A.P., Patriarca P.A. editors. Options for the Control of Influenza. New York; Alan R. Liss Inc. 1986. Р. 155–168.
13. Patriarca P.A.,Weber J.A., Parker R.A. et al. Efficacy of influenza vaccine in nursing homes: reduction in illness and complications during an influenza A (H3N2) epidemic // JAMA. 1985. Vol. 253. Р. 1136–1139.
14. Грипп (сезонный, птичий, пандемический) и другие ОРВИ / под ред. проф. В.П. Малого, проф. М.А. Андрейчина. М.: ГЭОТАР-МЕДИА, 2013. 319 с.
15. Таточенко В.К., Озерецковский Н.А., Федоров А.М. Иммунопрофилактика – 2014. М.: ПедиатрЪ, 2014. 199 с.
16. Kamps B.S., Hoffmann C., Preiser W. Influenza Report 2006. Available at: http://www.influenzareport.com (Accessed on 15 September 2008).
17. Киселев О.И., Деева Э.Г., Слита А.А., Платонов В.Г. Антивирусные препараты для лечения гриппа и ОРЗ. Дизайн препаратов на основе полимеразных носителей. СПб.: Время, 2000. 132 с.
18. Yen H.-L., Monto As., Webster R.G., Govorkova E.A. Virulence may determine the necessary duration and dosage of oseltamivir treatment for highly pathogenic A/Vietnam/1203/04 influenza virus in mice // J. Infect. Dis. 2005. Vol. 192. Р. 665–672.
19. Treanor J.J. et al. Efficacy and safety of the oral neuraminidase inhibitor oseltamivir in treating acute influenza: a randomized controlled trial // JAMA. 2000. Vol. 283. Р. 1016–1024.
20. Nicholson K.G. et al. Treatment of acute influenza: efficacy and safety of the oral neuraminidase inhibitor oseltamivir // Lancet. 2000. Vol. 355. Р. 1845–1850.
21. WHO. Influenza A(H1N1) virus resistance to oseltamivir – 2008/2009 Influenza season, northern hemisphere. Available at: http://www.who.int/csr/disease/influenza/H1N1webupdate20090318%20ed_ns.pdf (Accessed 12 March 2009)
22. CDC. 2008–2009 Seasonal Influenza Update. Bridges CB. Available at: http://emergency.cdc.gov/coca/ppt/Influenza-10-28-08.ppt#257,1,2008-09 Seasonal Influenza Update. (Accessed 12 March 2009.)
23. www.preparatum.ru. Раздел «Новости медицины». 8 сент. 2016 г.
24. Weekly U.S. Influenza Surveillance Report – Centers for Disease Control and Prevention, 2016.
25. Boltz D., Peng X., Muzzio M. et al. Antiviral Activity of Enisamium Against Influenza Viruses in Differentiated Normal Human Bronchial Epithelial Cells. III antivirus congress, Amsterdam, 2014, 12–14 Оct.
26. Тринус Ф.П. Фармакотерапевтический справочник. Киев: Здоров’я, 1998. 880 с.
27. Бухтіарова Т.А. Експериментальне досліження впливу нового неопіоїдного анальгетика амізону на периферичну кров та кровотворення. Ліки, 1997. Т. 6. С. 69–73.
28. Фролов А.Ф., Фролов В.М., Лоскутова И.В. Амизон: опыт применения нового украинского препарата. Укр. мед. часопис, 2000. Т. 1. С. 78–80.
29. Мельникова Т.И., Деева Э.Г., Охапкина Е.А. и др. Клиническая эффективность препарата на основе изоникотиновой кислоты в терапии гриппа и других острых респираторных вирусных заболеваний // Инфекционные болезни. 2012. № 4. С. 70–75.
30. Осидак Л.В., Еропкин М.Ю., Ерофеева М.К. и др. Грипп А (H1N1) 2009 в России. Terra Medica Nova. 2009. № 4–5. С. 6–9. / Osidak L.V., Eropkin M.Yu., Erofeeva M.K. et al. Influenza A H1N1 2009 in Russia // Terra Medica Nova. 2009. № 4–5 P. 6–9 (in Russian).
31. Prenatal and infant paracetamol exposure and development of astma; the Norwegian mother and child Cohort Study // Intern. J. of Epidemiology. 2016. doi. 10.1093/lje/dyv366/
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
Информация с rmj.ru