Нарушения в системе гемостаза и его коррекция у беременных с метаболическим синдромом
Е. И. Соколов, доктор медицинских наук, профессор, академик РАМН
И. Б. Манухин, доктор медицинских наук, профессор
А. А. Мочалов
О. Б. Невзоров, доктор медицинских наук, доцент
МГМСУ, Москва
Частота метаболического синдрома по данным различных авторов составляет 5–20% (I. Despres, A. Marette, 1994). Следует отметить, что ожирение входит в число основных компонентов метаболического синдрома, а число женщин с ожирением, включая беременных, прогрессивно возрастает.
Имеется значительное число работ, посвященных влиянию ожирения на течение беременности и родов. Однако единичные исследования посвящены изучению некоторых метаболических показателей. Так, Г. А. Чернуха (1987) показала нарушение гормонального профиля в системе гемостаза и липидного обмена у беременных с ожирением. В. Н. Серов с соавт. (2000) отметили у беременных с ожирением и дефицитом массы тела изменения метаболических процессов, в частности гипо- и дислипидемию, снижение толерантности к глюкозе.
Важным компонентом у беременных с метаболическим синдромом является нарушение кровотока в системе матери, обусловленное ожирением, нарушенной плацентарной недостаточностью, измененный гормональный профиль: повышенный уровень лептина, измененный инсулиновый коэффициент и измененный водно-электролитный баланс.
Однако в доступной нам литературе мы не нашли работ, которые бы связывали ожирение у беременных с наличием у них метаболического синдрома.
Целью нашего исследования было изучить изменения в системе гемостаза, частоту метаболического синдрома и его коррекцию у беременных с метаболическим синдромом и определить влияние этих изменений на течение беременности и родов.
Была поставлена задача выяснить патофизиологический механизм развития гиперкоагуляции крови и повреждения эндотелия у беременных женщин с метаболическим синдромом. В исследования были включены 43 беременных с метаболическим синдромом в возрасте от 27 до 37 лет в III триместре беременности, в том числе 8 беременных, у которых развился гестоз средней степени тяжести. В качестве контроля наблюдалось 15 здоровых беременных аналогичного срока беременности. Всем беременным проведено клиническое обследование с включением перорального нагрузочного теста на толерантность к глюкозе. Критериями включения беременных основной группы были: артериальная гипертезия, висцеральное ожирение, гиперинсулинемия и гипергликемия.
Лабораторные исследования
Кровь брали из локтевой вены натощак с добавлением антикоагулянта 0,6% раствора этилендиаминтетрауксусной кислоты (ЭДТА). Определяли уровень фибриногена, антитромбина III (АТ III), толерантность плазмы к гепарину, фибринолитическую активность крови, содержание тромбоксана В2, цАМФ в тромбоцитах и простациклинах. Количественные показатели агрегации тромбоцитов оценивали по спонтанной агрегации индуцированной аденозиндифосфатом (АДФ) и коллагеном, определяли инсулин крови. Для определения агрегации тромбоцитов брали кровь в пробирки, содержащие 3,8% раствор цитрата натрия в разведении 9:1. Оценку количественных характеристик скорости и интенсивность агрегации проводили на автоматическом двухканальном лазерном анализаторе агрегации с применением программного обеспечения.
Для исследования спонтанной агрегации тромбоцитов анализировали агрегационную кривую, записанную в течение 10 минут без индуктуров. В качестве индуктора агрегации использовали раствор АДФ в концентрациях 1×10-5 М, % и 1×10-7 М, %, коллаген, фактор активации тромбоцитов, адреналин 10-4 М, аггристин. Протокол исследования агрегации тромбоцитов в богатой тромбоцитами плазме включал измерение максимальной скорости агрегации в процентах. NO определялось с помощью методики определения нитритов NO2 и нитратов как продуктов метаболизма оксида азота в сыворотке крови человека методом высокоэффективной жидкостной хромотографии на приборе Shimatsu. Сыворотка крови замораживалась и хранилась при температуре -70 градусов. При проведении анализа сыворотку размораживали, разводили эквалентным количеством, буфер и белки удаляли фильтрованием через фильтр UltraFree Units на центрифуге при 5 тысячах оборотов в минуту в течение 15 минут. Количественный анализ проводили при сравнении с внешним стандартом при длине волны 214 нм с последующим учетом разведения.
Результаты исследования
Физиологическая беременность сопровождается значительными изменениями в системе гемостаза. Для решения вопроса о развитии гиперкоагуляции крови в условиях осложненной беременности мы провели исследование системы гемостаза и функциональной активности крови у беременных основной и контрольной группы. Из табл. 1 видно, что в контрольной группе уровень фибриногена 2,36, а в основной группе 3,74, толерантность плазмы к гепарину в контрольной группе равна 948,0, а в основной группе 724,0. Очень важным показателям является уровень АТ III. В контрольной группе он составляет 37,6, а в основной группе — 27,3. Увеличение уровня фибриногена в основной группе является одним из важных звеньев нарушения микроциркуляции, которая сопровождается блокадой транспорта веществ, в частности нарушения доставки к плоду кислорода, глюкозы, липидов, белков. Нарушение проницаемости мембран сопровождается при этом изменением характера окислительных процессов, в частности повышением уровня анаэробного окисления, развитием ишемических и дистрофических изменений в тканях плода.
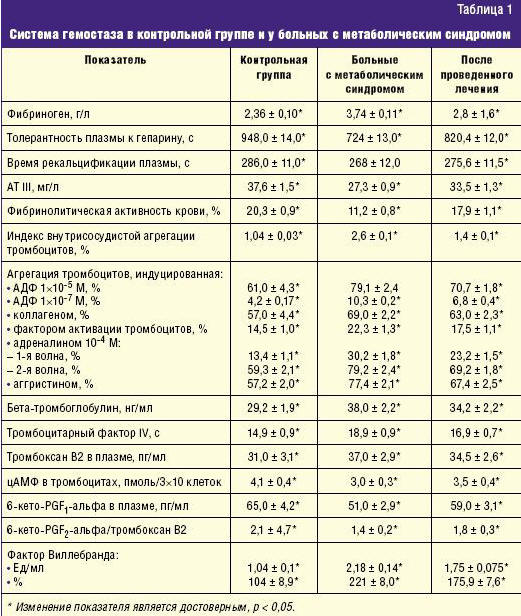
Клинически это проявляется снижением веса плода, асфиксией его. Большую опасность развития тромбозов во время беременности представляет собой сочетание высокого уровня фибриногена и сниженного показателя АТ III. Известно, что антикоагулянтная активность крови обеспечивается целым рядом биохимических факторов. Одним из наиболее активных антикоагулянтов является плазменный кофактор гепарина АТ III. Он является универсальным ингибитором почти всех ферментных факторов свертывания крови (особенно тромбина и фактора Ха). Критическое снижение уровня АТ III у беременных в основной группе вызывает преэкламптическое состояние. Сопоставляя количественные показатели агрегации тромбоцитов у здоровых женщин и у беременных с метаболическим синдромом, мы отметили существенные различия. С чем связаны эти изменения? Важную роль играют изменения физико-химических свойств тромбоцитов в условиях беременности и инсулинорезистентности.
Возникающая ишемия в органах и тканях нарушает энергетический потенциал тромбоцитов с развитием деполимеризации мембраны, соответствующей потерей клеткой одной из форм «свободной энергии», т. е. энергии трансмембранного потенциала. Агрегация тромбоцитов у больных с метаболическим синдромом, индуцированная АДФ, значительно повышается — до 79,1% (у здоровых лиц 61,0%). Достоверно повышается агрегация тромбоцитов, стимулированная коллагеном — до 69,0% (у здоровых лиц 57,0%). Коллаген-индуцированная агрегация очень важна, так как в случае незначительного морфологического изменения стенки сосуда возникают условия для образования внутрисосудистого тромбоцитарного тромба.
Повреждение эндотелия с обнажением коллагена является важным пусковым фактором агрегации тромбоцитов. При метаболическом синдроме у беременных значительно изменяется агрегация тромбоцитов под влиянием адреналина. Если у здоровых женщин с физиологической беременностью она составляет 13,4%, то при метаболическом синдроме она повышается до 30,2%. Адреналин-индуцированная агрегация тромбоцитов у беременных с метаболическим синдромом свидетельствует о резком повышении чувствительности рецепторного аппарата тромбоцитов к адреналину.
Из этого следует, что даже незначительные эмоциональные стрессы, умеренная физическая нагрузка могут провоцировать активацию агрегации тромбоцитов с возможным прогрессированием до развития преэкламптического состояния. Патофизиологической основой изменения агрегации тромбоцитов при гестозе является нарушение активности цАМФ клетки. Именно высокий уровень цАМФ тромбоцитов позволяет ему сохранить функциональную жизнеспособность: обмен веществ, энергии и обмен информации.
У беременных контрольной группы уровень цАМФ тромбоцитов составляет 4,1 пмоль (3×108 клеток), у женщин с метаболическим синдромом уровень цАМФ снижается до 3,0 пмоль (3×108 клеток). Гестоз характеризуется повышенным уровнем фибронектина, который постоянно взаимодействует с тромбоцитами. В норме его содержание составляет 4 мг × 109 клеток. В тромбоцитах он ассоциируется с альфа-гранулами и высвобождается из них после стимуляции тромбином или коллагеном, способствуя адгезии клеток коллагеном. Это играет важную роль при активации гемостатического процесса. Также при гестозе обнаруживается низкое содержание АТ III, на долю которого приходится около 80% всей первичной антикоагулянтной активности крови.
У беременных с гестозом обнаруживались высокие титры бета-тромбоглобулина и фактора IV тромбоцитов. Важную роль в предупреждении развития избыточной коагуляции крови при беременности клиницисты придают состоянию эндотелия. Антитромбогенные свойства стенки сосудов обеспечиваются воздействием целого ряда компонентов: 1) простациклина, являющегося ингибитором агрегации тромбоцитов и обеспечивающего выраженный эффект вазодилятации; 2) антикоагулянтов (АТ III и альфа-2 макроглобулин); 3) проактиватора плазминогена, вырабатывающегося в сосудах; 4) тромбомодулина, образующегося на поверхности эндотелиальных клеток. У здоровых лиц тромбоциты не прилипают к неповрежденному эндотелию. При повреждении же эндотелия тромбоциты легко прилипают к субэндотелию, что обусловлено снижением содержания глюкозоаминогликанов и простациклина, синтезируемого эндотелием. Уровень простациклина у здоровых лиц при беременности составляет 65,0 пг/мл, у беременных с метаболическим синдромом он снижается до 51,0 пг/мл.
Открытие продукции NO эндотелиальными клетками в 80-е годы еще раз подтвердило огромное морфофункциональное значение эндотелия, который ранее рассматривался как пассивная разделительная поверхность между кровью и экстравазальным пространством. NO обладает множеством функций, среди которых главными является поддержание нормальной функции сосудов и полноценная адаптация кардиоваскулярной системы к беременности. NO обладает вазодилятирующей антиагрегантной активностью, а также является ингибитором митогенеза.
Для выяснения значимости уровня NO у беременных в развитии гиперкоагуляции крови мы сопоставили его количественные показатели у беременных основной и контрольной группы. У лиц контрольной группы уровень NO составляет 23,2, а у лиц основной группы величина его снижается до 21,16. При этом очень важно отметить, что уровень NO повышается только через 6 месяцев после родов до 25,57. Это свидетельствует о том, что нарушение эндотелиальной функции обусловлено именно беременностью. У больных с гестозом происходит значительное повреждение эндотелия, увеличивается гипоксия и циркуляция свободных радикалов, а также агрессивных форм кислорода. При этом NO расходуется на связывание свободных радикалов, в результате чего страдает одна из важных его функций — вазодилятирующая и антиагрегантная.
Уровень АТ III значительно снижен, и это дает возможность увеличивать тромботическую активность крови (табл. 1). К этому же добавляется и снижение фибринолитической активности крови: если у контрольной группы она составляет 20,3%, то при метаболическом синдроме она снижается до 11,2%. Особую значимость приобретает повышение чувствительности тромбоцитов к различным агрегантам (коллагену, адреналину и АДФ), что при различных видах патологии, например гестозе, может приводить к тромботическим осложнениям. Имеет также важное значение сниженный у беременных с метаболическим синдромом цАМФ в тромбоцитах до 3×108 клеток пмоль, в то время как у лиц контрольной группы этот показатель составляет 4,1×108 клеток пмоль.
Важное значение в вопросах тромбоцитарной активности имеет сниженный уровень простоциклина (6-кето-PGF1-альфа в плазме — пг/мл), если у лиц контрольной группы выработка простоциклина составляет 65 пг/мл, то у беременных с метаболическим синдромом уровень простоциклина снижен до 51 пг/мл. Увеличивается в крови фактор Виллебранда, у беременных с метаболическим синдромом он составляет 2,18 ед/мл, а у лиц контрольной группы 1,04 ед/мл, усиливая таким образом агрегационную способность тромбоцитов. Таким образом, сочетанное воздействие высокого уровня фибриногена и увеличение агрегационной активности тромбоцитов, сочетающееся со сниженными такими показателями, как АТ III и простациклин, способствуют развитию тромбогеморрагического синдрома у беременных с метаболическим синдромом и является одним из пусковым механизмом присоединения гестоза.
С целью снижения перинатального риска и частоты возникновения других осложнений беременности у ряда больных метаболическим синдромом проводилась комплексная терапия, которая включала в себя:
- гипохлоридную белковую диету с включением продуктов, богатых «естественными» антиоксидантами (чернослив, изюм, черника, черная смородина);
- один из препаратов группы «синтетических» антиоксидантов: витамин Е (300 мг/сут), аскорбиновая кислота (100 мг/сут), глутаминовая кислота (3 г/сут);
- препараты группы мембранстабилизаторов, содержащие полиненасыщенные жирные кислоты: Эссенциале форте H по 2 капсулы — 3 раза, Липостабил по 2 капсулы — 3 раза и пищевую добавку Эйконол по 1 капсуле 1–2 раза в день;
- антикоагулянтную терапию (Фраксипарин 0,3 или 0,6 мл/сутки п/к в зависимости от показателей гемостазиограммы);
- антиагрегантную терапию — Кардиомагнил 75 мг/сут.
Больным проводилось лечение Кардиомагнилом 75 мг — 1 раз в день и Фраксипарином 0,3–1, 2 раза в день. В основе механизма действия ацетилсалициловой кислоты лежит необратимое ингибирование фермента циклооксигеназы (ЦОГ-1), в результате чего блокируется синтез тромбоксана А2 и подавляется агрегация тромбоцитов. Фраксипарин проявляет высокую способность к связыванию с белком плазмы крови AT III. Это связывание приводит к ускоренному ингибированию фактора Ха, чем и обусловлен высокий антитромботический потенциал надропарина. Антитромботический эффект надропарина включает активацию ингибитора превращения тканевого фактора (TFPI), активацию фибринолиза посредством прямого высвобождения активатора тканевого плазминогена из эндотелиальных клеток и модификацию реологических свойств крови (снижение вязкости крови и увеличение проницаемости мембран тромбоцитов и гранулоцитов). Надропарин кальций характеризуется более высокой анти-Ха-факторной активностью по сравнению с анти-IIa-факторной или антитромботической активностью и обладает как немедленной, так и продленной антитромботической активностью.
На фоне проводимого лечения отмечается улучшение состояния беременных и снижение показателей, представленных на гемостазиограмме, а также улучшение биохимических показателей у беременных с метаболическим синдромом на фоне проведенной терапии (табл. 2).
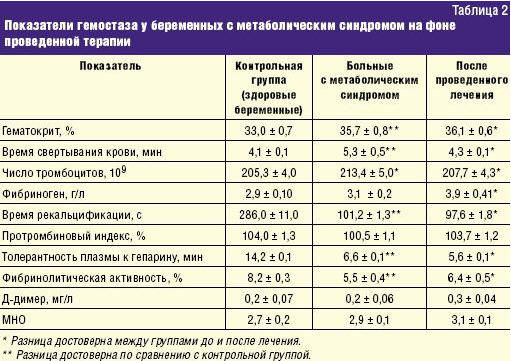
Таким образом, функциональная активность эндотелия при беременности (особенно при гестозе) резко нарушается. Оксидативный стресс во время беременности, особенно у женщин с метаболическим синдромом, стимулирует выработку эндотелина с соответствующим развитием гипертензии. Следовательно, дисфункция эндотелиальных клеток стимулирует выброс эндотелина, тромбоксана, ангиотензина II, тормозит продукцию оксида азота и приводит к ишемии плаценты, присоединению гестоза (табл. 1).
Исход беременности и родов прослежен у 58 женщин, поступивших в отделение патологии беременных родильного дома ГКБ № 70 г. Москвы. Контрольную группу составили данные течения беременности и родов у 15 женщин с метаболическим синдромом.
Анализ течения беременности у женщин с метаболическим синдромом свидетельствует о том, что беременность часто протекает с различными осложнениями, представленными в табл. 3.
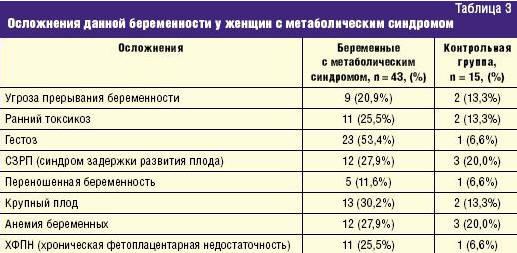
Значительный интерес представляет анализ течения родов у женщин с метаболическим синдромом. Данные представлены в табл. 4.
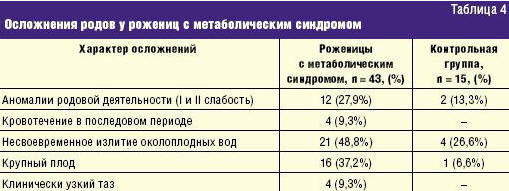
Характерной особенностью течения родов у женщин с метаболическим синдромом является несвоевременное излитие околоплодных вод, аномалии родовой деятельности, крупный плод и кровотечение в третьем периоде родов.
Так, у рожениц с метаболическим синдромом средняя величина кровотечения составила 600–900 мл (у одной роженицы из этой группы кровотечение составило 1100 мл). Во всех случаях обеспечивалось использование консервативных методов лечения.
Высокий процент кровотечений у рожениц с метаболическим синдромом возможно объяснить нарушением сократительной способности матки, о чем свидетельствует значительная частота аномалии родовой деятельности.
Особый интерес заслуживает частота оперативного родоразрешения у женщин с метаболическим синдромом. Если по родильному дому № 70 частота кесарева сечения составляет по годам 22–23%, то у женщин в нашем исследовании она составила 33,6%.
Показаниями для операции кесарева сечения были: клинически узкий таз, тяжелая форма гестоза, упорная слабость родовой деятельности, не поддающаяся медикаментозной коррекции.
Таким образом, частота метаболического синдрома у женщин с ожирением составила 89,2%. Метаболический синдром неблагоприятно отражается на течении беременности и родов, что является причиной значительного увеличения частоты оперативных вмешательств, особенно родоразрешения путем операции кесарева сечения. Проведенный анализ дает основания относить беременных с метаболическим синдромом к группе высокого риска по развитию гестоза и осложнения течения родов.
Выводы
- Метаболические изменения у женщин во время беременности (повышение уровня артериального давления, гипергликемия, инсулинорезистентность) создают угрозу развития гестоза.
- В патогенезе ДВС-синдрома (диссеминированного внутрисосудистого свертывания) у беременных с метаболическим синдромом играют роль повреждение эндотелия сосудов, повышение агрегации тромбоцитов и нарушение реологических свойств крови.
- Для лечения ДВС-синдрома у беременных с метаболическим синдромом в состав комплексной терапии необходимо включать антиагреганты и антикоагулянты. Проведение комплексной терапии с включением антиагрегантов и антикоагулянтов является патогенетически обоснованной профилактикой присоединения гестоза и позволяет не допустить или отсрочить присоединение гестоза и значительно улучшить исходы беременности и родов.
Литература
- Архипов В. В., Каюпова Г. Ф., Саматова 3. А. Течение беременности и родов, состояние плода и новорожденного у женщин с ожирением // Здравоохр. Башкортостан. 1999, № 3, с. 33–34.
- Беловицкая Н. Состояние тромбоцитарно-сосудистого звена системы гемостаза у больных ИНСД с ИБС. М., 1990, с. 144.
- Бутрова С. А. Метаболический синдром: патогенез, клиника, диагностика, подходы к лечению // Рус. мед. журн. 2001, 2, 56–60.
- Василенко А. Изменение тромбоцитарного и прокоагулянтного звеньев гемостаза у больных с артериальной гипертензией // Врачебное дело. 1992, № 8, с. 65–66.
- Гинзбург М. М., Козупица Ч. С., Крюков Н. Н. Ожирение и метаболический синдром. М., 2000, с. 14–15.
- Мамедов М. Н. Клинико-биохимические особенности и пути медикаментозной коррекции метаболического синдрома. Дисс. д.м.н. М., 2001.
- Чазова И. Е., Мычка В. Б. Метаболический синдром. 2004, с. 9.
- Чернуха Г. Е. Клиническое значение нарушений показателей гомеостаза у беременных с ожирением. Дисс. к.м.н. М., 1987.
- Bernardi F., Marcheti G., Pinotti M., Arcieri P. Factor VII gene Polymorphisms Contribute About One Third of the Factor VII Level Variation in Plasma // Atherosclerosis, Thrombosis and vascular Biology. 1996, v. 16, № 1, 72–78.
- Bray G. A. Obesity. Part I. Pathogenesis//West J. Med. 1988, v. 194, № 4, p. 429–441.
- Despres J. P. The impact of overstate on the multifactorial risk profile of abdominally obese patients // Diabetes, 1998, 48, 1, 307.
- Edwards L. E., Hellerstedt W. L., Alton I. R. et al. Pregnancy compactions and birth outcomes in obese and normal-weight woman: effects of gestational weight change// Obstet. Gynec. 1996, № 87 (3), p. 389–394.
- Galtier-Derenze F., Bringer Y. Maternal overweight and pregnancy // Diabetes Metab. 1997, v. 23, № 6, p. 192–195.
- Goldenberg R. L., Tamura T. Pregnancy weight and pregnancy outcome // JAMA. 1996, № 275 (14), p. 1127–1128.
- Stico-Rahm A., Niman В., Hamsten A., Nilsson Y. Secretion of plasminogen activator inhibitor 1 from cultudef human umbilical vein endotelian cells is included by very low density lipoprotein // Atherosclerosis. 1990, 10:1067–1073.
Статья опубликована в журнале Лечащий Врач
материал с сайта MedLinks.ru