Введение
Согласно данным литературы частота выявления пролапса тазовых органов у женщин в различных странах составляет до 60% в зависимости от экономического и социального уровня развития стран [1]. Доля пролапса тазовых органов в структуре гинекологических заболеваний в Российской Федерации составляет 39% [2]. В связи с общемировой тенденцией к повышению продолжительности жизни населения количество женщин постменопаузального возраста увеличивается [3]. При плановом осмотре во время диспансеризации у 50% женщин, выполнивших детородную функцию, выявляется пролапс тазовых органов 2–3-й степени, при этом только у 20% отмечаются выраженные клинические симптомы [4, 5]. В дальнейшем за счет развития симптоматического комплекса заболевания возникают функциональные нарушения, которые впоследствии вызывают физические и моральные страдания больных [6].
Пролапс тазовых органов связан с нарушением качества жизни пациенток. В среднем около 10% женщин пожилого возраста переносят операции в связи с наличием генитального пролапса, при этом в 30% случаев в течение нескольких лет после операции высока вероятность рецидива, что требует повторного обращения за медицинской помощью [7]. Хотя хирургическое лечение является наиболее эффективным для коррекции пролапса тазовых органов [8], высокая частота рецидивов диктует необходимость совершенствования методик оперативного лечения генитального пролапса. Целью оперативного лечения выраженного пролапса тазовых органов является восстановление правильной архитектоники органов малого таза при помощи синтетических сетчатых имплантатов и устранение функциональных нарушений органов, вовлеченных в патологический процесс [9].
К настоящему времени с развитием новых малоинвазивных технологий для коррекции генитального пролапса широкое распространение получили операции с лапароскопическим доступом. Лапароскопический доступ представляет собой современный малоинвазивный метод, который позволяет оценить степень и форму генитального пролапса, распространенность сопутствующей патологии органов малого таза, снизить риск повреждения тканей или смежных органов. Новые методики операций позволяют хирургу оперировать в бессосудистой зоне, при этом контролировать и уменьшать объем интраоперационной кровопотери, что снижает риск формирования гематом в раннем послеоперационном периоде. Ввиду отсутствия контакта инструментов со слизистой влагалища исключается развитие трофических осложнений. Кроме того, лапароскопический доступ, по сравнению с абдоминальным, снижает сроки пребывания в стационаре, имеет преимущества в сроках реабилитации и способствует достижению лучшего косметического эффекта [10].
Предложено множество способов хирургического лечения, каждый из которых, наряду с определенными преимуществами, имеет и недостатки. По данным современных источников литературы, среди операций лапароскопическим доступом для коррекции изолированных форм пролапса тазовых органов [11], например апикального, возможно использовать методику лапароскопической пектопексии. При этом виде коррекции генитального пролапса к куполу влагалища или культе шейки матки фиксируется синтетический имплантирумый материал, который располагается в поперечном направлении и фиксируется к гребенчатым связкам с обеих сторон. Данный способ оперативного вмешательства имеет дополнительные преимущества, так как гребенчатые связки являются безопасной зоной и не имеют конфликтных ситуаций со смежными полыми органами и магистральными сосудами, а также крупными нервными сплетениями. Тем не менее данный способ не позволяет корректировать задний и, частично, передний пролапс тазовых органов. Эту методику возможно использовать только после гистерэктомии для формирования точки фиксации и более эргономичного расположения синтетического имплантируемого материала, а также профилактики возможных гиперпластических процессов со стороны органов малого таза.
Помимо этого вмешательства, в последние годы наибольшее распространение получила сакровагинопексия (сакрокольпопексия) [12, 13]. К достоинствам такой операции можно отнести восстановление физиологического направления влагалищной оси и сохранение длины влагалища [14, 15]. При данном виде коррекции пролапса тазовых органов проводится продольная фиксация синтетического имплантата с последующей его установкой в пузырно-влагалищное и ректовагинальное пространства и дальнейшая фиксация конструкции из лоскутов к поперечной пресакральной связке. Данный способ обладает преимуществами при устранении апикального, заднего и, частично, переднего пролапса тазовых органов по сравнению с другими лапароскопическими методиками коррекции генитального пролапса. К возможным недостаткам сакровагинопексии относят технические сложности доступа к передней продольной связке на уровне мыса крестца у женщин с ожирением, а также при наличии спаечного процесса в брюшной полости. При этой методике высока вероятность развития люмбосакрального синдрома из-за риска повреждения надкостницы в момент фиксации имплантата к мысу крестца, с формированием сакроилеита и высокой вероятностью отрыва фиксируемого синтетического имплантата с возникновением рецидива [16].
В связи с этим сложно выделить самую эффективную и безопасную методику оперативного лечения, которая могла бы послужить руководством к действию врача [17]. В связи с этим поиск оптимальных, безопасных, эффективных, воспроизводимых хирургических методик для лечения сочетанных форм генитального пролапса актуален.
Цель исследования: оценить эффективность и безопасность комбинированной методики — пектовагинопексии и наиболее распространенной в настоящее время операции — сакровагинопексии при лапароскопическом доступе коррекции генитального пролапса.
Содержание статьи
Материал и методы
Данное исследование проводилось на базе кафедры акушерства и гинекологии № 1 Института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет) с 2020 по 2023 г. Исследование было одобрено этическим комитетом.
Критериями включения в исследование являлись: наличие у пациенток пролапса 2–4-й степени по классификации Pelvic Organ Prolapse Quantification System (POP-Q), в том числе рецидивирующих форм, наличие подписанного информированного согласия на участие в исследовании и проведение операции.
В исследование включили 32 пациентки со схожей нозологической формой генитального пролапса. На амбулаторном этапе нами проведено комплексное клиническое обследование пациенток, изучены жалобы, проведен сбор анамнеза, собраны данные о перенесенных заболеваниях, менструальной и репродуктивной функции. При объективном обследовании оценен тип телосложения, рост и масса тела, рассчитан индекс массы тела.
Для определения качества жизни мы проводили анкетирование — валидированный способ оценки дисфункции тазового дна и качества жизни пациенток по опросникам качества жизни Pelvic Floor Distress Inventory-20 (PFDI-20), Pelvic Floor Impact Questionnaire-7 (PFIQ-7) [18].
Проводили бимануальное влагалищное исследование в покое и при выполнении пробы Вальсальвы — при максимальном натуживании для определения формы и степени опущения внутренних половых органов и их отношения ко входу во влагалище. Выполняли ректальное исследование для определения степени опущения задней стенки влагалища и дифференцировки ректоцеле от энтероцеле. Результаты влагалищного исследования оценивали по классификации POP-Q [19]. Оценку по POP-Q проводили до и после операции.
Ультразвуковое исследование (УЗИ) органов малого таза проводили для верификации отделов тазового дна, которые вовлечены в пролапс тазовых органов, и оценки сопутствующей патологии (аппарат General Electric Voluson P8, США) [20, 21]. Во время исследования наблюдали за движением органов малого таза в покое, при выполнении пробы Вальсальвы и при сжатии промежности.
По результатам комплексного обследования пациентки получили рекомендации о необходимости коррекции генитального пролапса. В ходе нашего исследования с учетом имеющейся экстрагенитальной и генитальной патологии нами составлен план предоперационной подготовки, метода хирургического лечения и ведения послеоперационного периода.
Все обследуемые были разделены на 2 группы в зависимости от методики хирургического лечения. В 1-ю (основную) группу вошли 14 пациенток, у которых был применен комбинированный подход в хирургической коррекции генитального пролапса лапароскопическим доступом с продольно-поперечной фиксацией синтетических имплантатов — комбинированная пектовагинопексия. Во 2-ю (контрольную) группу вошли 18 пациенток, которым выполнена сакровагинопексия (сакрокольпопексия).
Перед госпитализацией проводили клинико-лабораторное обследование согласно стандартам оказания медицинской помощи, с определением ключевых позиций.
Оперативные вмешательства проводились на хирургической эндоскопической системе фирмы Karl Storz. Синтетический имплантируемый материал: Gynecare Gynemesh Ps и Norabsorbable Prolene Soft Mesh.
Всем пациенткам проводили предоперационную антибиотикопрофилактику за 30 мин до начала операции и профилактику венозных тромбоэмболических осложнений — компрессионный трикотаж вен нижних конечностей.
Хирургическая техника
В обеих группах операции проводили под комбинированным эндотрахеальным наркозом. Пациенток укладывали на операционном столе на спину в нижнюю литотомную позицию с максимально разведенными ногами, согнутыми в коленных суставах и уложенными на универсальные подколенники. В мочевой пузырь устанавливали трансуретрально постоянный мочевой катетер Folley 12–16 Fhench с раздуваемой манжетой. Обрабатывали операционное поле (передняя брюшная стенка, наружные половые органы и влагалище) раствором антисептика. Операционная бригада располагалась традиционно: хирург становился слева от пациентки, первый ассистент управлял лапароскопом и стоял справа от пациентки, второй ассистент располагался между ног пациентки с обеспечением промежностного доступа. В асептических условиях через параумбиликальный прокол иглой Вереша типично накладывали пневмоперитонеум СО2 (4,5 л). После этого устанавливали центральный троакар 10 мм с внутренним просветом. Мы использовали жесткую оптическую систему 0°. Пациентку переводили в положение Тренделенбурга 30–35° и проводили осмотр брюшной полости и органов малого таза. С целью улучшения экспозиции органов малого таза проводили фиксацию сигмовидной кишки к левой боковой стенке таза.
В 1-й группе пациенткам была выполнена комбинированная пектовагинопексия. Вскрывали брюшину позадиматочного пространства на 1 см от шейки матки; частично острым, частично тупым путем проводили диссекцию ректовагинального пространства до мышц, поднимающих задний проход, и их верхних пучков mm. iliococcygeus. Параллельно осуществляли мобилизацию прямой кишки с выборкой ректоцеле. Далее проводили гистерэктомию традиционным методом с удалением придатков и/или маточных труб.
Вдоль культей круглых связок матки паравезикально вскрывали листки брюшины к подвздошно-обтураторной области справа и слева. С обеих сторон выделяли нисходящие ветви лонных костей до гребенчатых связок (ligamentum pectineale). Визуализировали анатомические ориентиры с обеих сторон — гребенчатые связки и наружные подвздошные сосуды (a. femoralis, v. femoralis), сосуды, огибающие бедренную кость (a. circumflexae femoralis, v. сircumflexae femoralis).
У всех пациенток группы технический результат обеспечивался за счет комбинированной фиксации купола влагалища или культи шейки матки двумя синтетическими имплантатами к естественным физиологическим поддерживающим элементам малого таза.
Формирование поддерживающей структуры обеспечивали два синтетических лоскута. Первый имплантат, продольной формы, с выступами широким дистальным основанием крепится продольно (рис. 1А), с фиксацией отдельными швами нерассасывающейся нитью к пучкам мышц, поднимающих задний проход, с обеих сторон, а узким проксимальным основанием — к передней стенке культи шейки матки влагалища.
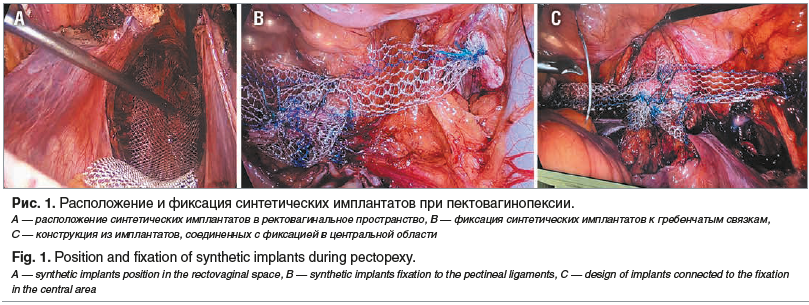
Второй, поперечный, имплантат в виде ленты 4×15 см фиксировали центральной частью также к передней стенке культи влагалища или шейки матки, а концами — к гребенчатым связкам отдельными швами нерассасывающейся нитью (рис. 1В). Причем для обеспечения физиологического положения культи влагалища или шейки матки перед этапом закрепления концов ленты второго имплантата ассистент хирурга трансвагинально фиксировал/приподнимал купол влагалища или шейку матки путем проталкивания в апикальном направлении.
Обращает на себя внимание техника выполнения операции, а именно финальные конструкции и метод установления имплантатов. Согласно нашим наблюдениям конструкция из имплантатов, соединенных с фиксацией в центральной области, образует надежную структуру, а каждый из имплантатов выполняет свою функцию поддержки органов малого таза: как вдоль (1-й имплантат), в области продольной оси сагиттальной плоскости, так и поперек (2-й имплантат), в области поперечной оси (рис. 1С). Такие действия хирурга и предлагаемая фиксация имплантатов способствуют предупреждению их смещения, скручивания и сморщивания, что повышает эффективность вновь сформированного поддерживающего аппарата малого таза, обусловливает улучшение результата операции по ликвидации пролапса и обеспечивает долговременность лечебного эффекта.
Пациенткам 2-й группы операцию проводили следующим образом. Над мысом крестца проводили вывешивание переднего листка париетальной брюшины над промонториумом, прослеживали ход магистральных сосудов (бифуркация аорты) и правого мочеточника, затем рассекали париетальную брюшину до отчетливой визуализации поперечной пресакральной связки. Частично острым, частично тупым путем формировали канал на всем протяжении от мыса крестца вдоль правой крестцово-маточной связки до ректовагинального пространства. Визуализировали анатомические ориентиры — поперечную пресакральную связку и сосуды промонториума (a. sacrales medialis, v. sacrales medialis). Вскрывали брюшину позадиматочного пространства, отступя на 1 см вниз от шейки матки; частично острым, частично тупым путем проводили диссекцию ректовагинального пространства до мышц, поднимающих задний проход, и их верхних пучков mm. iliococcygeus. Параллельно осуществляли мобилизацию передней стенки прямой кишки. Далее проводили гистерэктомию традиционным методом с удалением придатков и/или маточных труб.
Из сетчатого материала выкраивали лоскут 6×10 см, который фиксировали нерассасывающейся нитью к мышцам, поднимающим задний проход, с обеих сторон. Дополнительно выкраивали второй лоскут размером 4×10 см, который впоследствии фиксировали к передней стенке культи шейки матки. Лоскуты сшивали между собой и фиксировали к культе шейки матки тремя швами нерассасывающейся нитью. Проксимальную часть переднего сетчатого имплантата фиксировали к мысу крестца отдельным швом нерассасывающейся нитью.
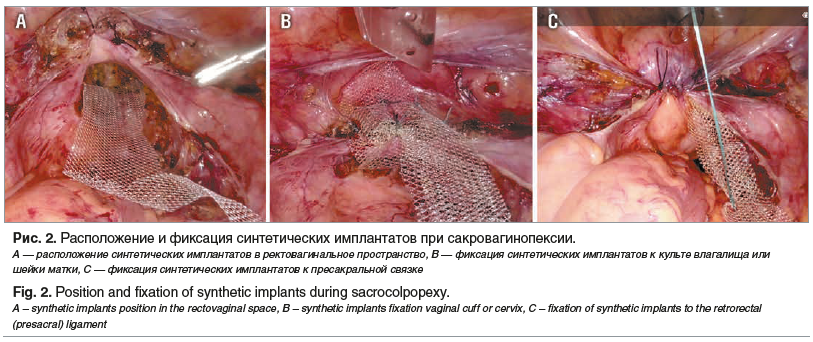
У всех пациенток группы формирование поддерживающей структуры обеспечивали два синтетических лоскута продольной формы. Первый имплантат крепился продольно широким основанием в ректовагинальное пространство (рис. 2А), фиксировался отдельными швами нерассасывающейся нитью к пучкам мышц, поднимающих задний проход, с обеих сторон, а узким проксимальным основанием — к культе влагалища или шейки матки (рис. 2В). Второй имплантат в виде ленты 4×10 см фиксировался центральной частью также к культе влагалища или шейки матки, а проксимальной частью переднего сетчатого имплантата — к пресакральной связке отдельными швами нерассасывающейся нитью (рис. 2С).
Всем пациенткам проводили перитонизацию непрерывным швом нерассасывающейся нитью с погружением всех культей и проленовых лоскутов экстраперитонеально.
В раннем послеоперационном периоде пациентки получали курс антибактериальной, анальгетической и антикоагулянтной, инфузионной и противовоспалительной терапии. Проводили спринцевание влагалища раствором фурациллина. Все пациентки были активизированы в присутствии врача и нагрузку перенесли адекватно в первые сутки после операции. Послеоперационный период протекал без осложнений и в среднем составил 7 сут.
Перед выпиской всем пациенткам было рекомендовано соблюдение лечебно-охранительного режима, диеты и режима питания, ограничение физической нагрузки, ношение компрессионного трикотажа в течение месяца, продолжение противовоспалительной терапии. Были рекомендованы осмотр гинеколога, УЗИ органов малого таза через 1 мес. после операции. Контрольные осмотры проводили через 6, 12 и 24 мес. Для оценки отдаленных результатов лечения все пациентки заполняли опросники качества жизни. Также во время каждого из осмотров изучали жалобы больных, проводили бимануальное гинекологическое исследование в покое и при натуживании для определения формы и степени опущения (проба Вальсальвы) внутренних половых органов, оценивали данные УЗИ.
Обработку полученных данных проводили с использованием пакета прикладных программ Statistica 10 (Tibco, США). Применяли стандартные методы статистической обработки данных.
Результаты и обсуждение
Средний возраст пациенток составил 64,3±5,3 года (от 46 до 73 лет). По результатам опроса длительность течения заболевания варьировала от 6 до 11 лет. По возрастному фактору, длительности заболевания, характеру и частоте сопутствующих заболеваний обе группы сопоставимы (р>0,05).
Анализ данных опроса по опросникам качества жизни позволил систематизировать жалобы пациенток и проявления генитального пролапса [18], данные представлены в таблице 1. Среди жалоб, на которые обращали внимание пациентки, наиболее частыми были тянущие боли в нижних отделах живота во время манифестации заболевания и дискомфорт, ощущение инородного тела во влагалище.

Анализ полученных измерений позволил нам систематизировать данные и выделить превалирующую степень пролапса тазовых органов [22].
Наиболее часто у пациенток регистрировали пролапс тазовых органов 3-й степени (7 (50%) и 9 (50%) в 1-й и 2-й группах соответственно), реже — 2-й степени (5 (35,7%) и 6 (33,3%) в 1-й и 2-й группах соответственно), 4-ю степень зарегистрировали у 2 (14,3%) и 3 (16,6%) пациенток из 1-й и 2-й групп соответственно.
При этом у 26 пациенток матка была сохранена (12 пациенток в 1-й и 14 пациенток во 2-й группе); у 6 пациенток было неполное выпадение культи влагалища после гистерэктомии (2 пациентки в 1-й и 4 пациентки во 2-й группе).
Объем интраоперационной кровопотери у пациенток в каждой группе составил от 50 до 100 мл. Интраоперационных осложнений не наблюдалось.
На контрольные осмотры через 1 и 6, 12 и 24 мес. пришли все пациентки. Необходимо отметить, что первичные жалобы пациенток на чувство инородного тела во влагалище более не беспокоили. Во всех случаях результат проведенного оперативного вмешательства признан положительным как по оценке пациентки, так и по оценке врача-исследователя. Отмечалось значительное улучшение показателей, отражающих состояние центрального компартмента (апикальная форма пролапса тазовых органов), а также передней и задней стенок влагалища.
Поскольку генитальный пролапс сопровождается достаточно специфичными жалобами, основным показанием для лечения будет снижение качества жизни, а не медицинские показания. Нами был проведен анализ данных функциональных результатов лечения при помощи анкетирования — данные о физическом и психическом благополучии, характере жалоб, социальной и сексуальной активности женщин свидетельствуют об улучшении качества жизни в послеоперационном периоде. В результате анализа данных опросов женщин по валидированным опросникам PFDI-20, PFIQ-7 прослеживалось существенное снижение количества баллов после оперативного вмешательства, что указывало на повышение качества жизни пациенток.
По данным УЗИ органов малого таза, а также по отсутствию mesh-ассоциированных осложнений [23] за время наблюдения, в том числе интраоперационных, можно говорить об эффективности разработанного хирургического способа лечения.
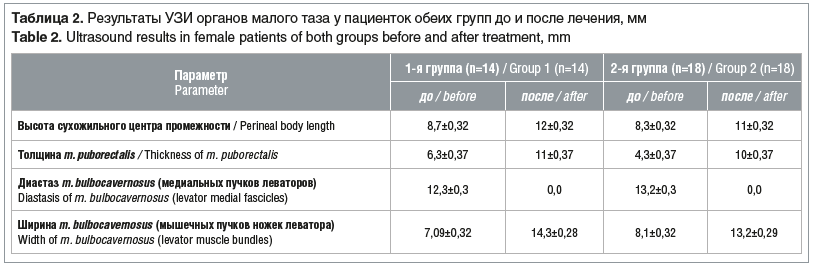
Данные трансперинеального УЗИ органов малого таза представлены в таблице 2 (во всех случаях р>0,05).
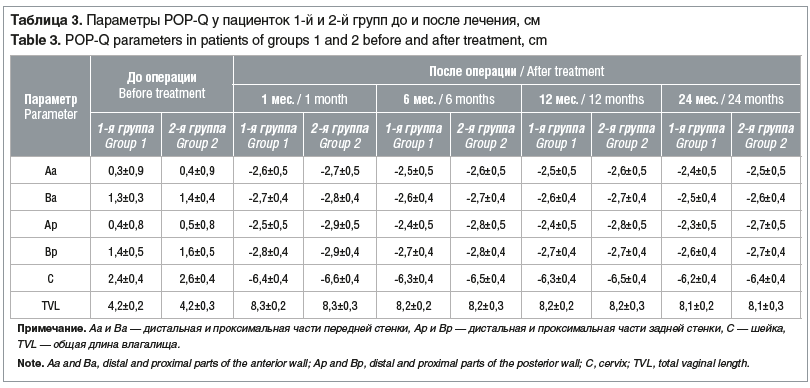
По итогам оперативного лечения нами проведен анализ клинико-анатомической эффективности лечения у пациенток обеих групп. Статистически значимой разницы (р>0,05) в результатах осмотра спустя 1, 6, 12 и 24 мес. не получено. Данные представлены в таблице 3.
На основании анализа результатов операций у пациенток 1-й и 2-й групп мы не увидели статистически значимых различий на протяжении всего периода наблюдения. Таким образом, наши данные свидетельствуют о сопоставимой эффективности обоих методов хирургического лечения пролапса тазовых органов. Исходя из результатов наблюдения, можно сделать заключение: у пациенток 1-й группы после комбинированной поперечно-продольной фиксации синтетических имплантатов достигается коррекция центрального, заднего и, частично, переднего пролапса. Формирование туннелей тупым путем в паравагинальной клетчатке в ретциево пространство к гребенчатым связкам не сопровождается кровотечением, так как крупных нервно-сосудистых пучков в данной области нет. Использование двух точек фиксации снижает риск рецидива заболевания и необходимость повторных оперативных вмешательств. Создается конструкция из двух синтетических имплантатов, соединенных в центральной области, которая образует надежную структуру и выполняет одновременно фиксирующую, подвешивающую и поддерживающую функции. В настоящее время наблюдение за пациентками продолжается в динамике, с последующей оценкой на большей выборке результатов. Мы планируем продолжить набор пациенток в исследование для детальной оценки эффективности оперативного лечения. Ввиду отсутствия контакта имплантируемого синтетического материала со слизистой влагалища мы постарались исключить развитие mesh-ассоциированных осложнений. При помощи лапароскопического доступа, по сравнению с абдоминальным, удается снизить сроки пребывания в стационаре и достигнуть лучшего косметического эффекта. Создание комплексной системы, включающей оценку анатомического результата, функционального состояния тазового дна и уровня жизни пациентки, сможет стать наиболее объективным инструментом оценки успешности лечения генитального пролапса хирургическим способом. Данные ультразвуковых параметров, а также отсутствие mesh-ассоциированных осложнений за время наблюдения, в том числе интраоперационных, свидетельствуют об эффективности разработанного хирургического способа лечения. К возможным недостаткам сакровагинопексии относят технические сложности доступа к передней продольной связке на уровне мыса крестца у женщин с ожирением, а также при наличии спаечного процесса в брюшной полости. При этой методике высока вероятность развития люмбосакрального синдрома из-за возможного повреждения надкостницы в момент фиксации имплантата к мысу крестца, с формированием сакроилеита, высокой вероятностью отрыва фиксируемого синтетического имплантата и возникновением рецидива.
Заключение
Пектовагинопексия сопоставима со считающейся наиболее распространенной в настоящее время операцией — сакровагинопексией и дает положительный эффект в коррекции генитального пролапса. Обращают на себя внимание восстановление физиологического вектора положения оси влагалища и сохранение длины влагалища в обоих представленных способах оперативного лечения. Предлагаемый способ лечения пациенток с генитальным пролапсом также обеспечивает быструю активацию и надежную реабилитацию по сравнению с уже устоявшейся методикой, что имеет не только медицинское, но и социальное значение, поскольку улучшает качество жизни пациенток.
Сведения об авторах:
Пяткина Алина Николаевна — аспирантка кафедры акушерства и гинекологии № 1 Института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0002-4260-9661.
Брюнин Дмитрий Викторович — д.м.н., профессор кафедры акушерства и гинекологии № 1 Института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0002-5969-4217.
Чушков Юрий Васильевич — к.м.н, доцент кафедры акушерства и гинекологии № 1 Института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-8125-1829.
Контактная информация: Пяткина Алина Николаевна, e-mail: patkinaalina@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 03.07.2023.
Поступила после рецензирования 24.07.2023.
Принята в печать 14.08.2023.
About the authors:
Alina N. Pyatkina — postgraduate student of the Department of Obstetrics and Gynecology No. 1, N.V. Sklifosovskiy Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0002-4260-9661.
Dmitry V. Bryunin — Dr. Sc. (Med.), Professor of the Department of Obstetrics and Gynecology No. 1, N.V. Sklifosovskiy Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0002-5969-4217.
Yuri V. Chushkov — C. Sc. (Med.), Associate Professor of the Department of Obstetrics and Gynecology No. 1, N.V. Sklifosovskiy Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0001-8125-1829. Contact information: Alina N. Pyatkina, e-mail: patkinaalina@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 03.07.2023.
Revised 24.07.2023.
Accepted 14.08.2023.
Информация с rmj.ru