Лечение больных анкилозирующим спондилитом — данные реальной клинической практики
Содержание статьи
Введение
Аксиальный спондилоартрит с рентгенологическими изменениями (р-аксСпА, син.: анкилозирующий спондилит) — это хроническое воспалительное заболевание из группы спондилоартритов, характеризующееся обязательным поражением крестцово-подвздошных сочленений и/или позвоночника с потенциальным исходом в анкилоз, с частым вовлечением в патологический процесс энтезисов и периферических суставов (М45.0 по МКБ X пересмотра) [1]. Распространенность р-аксСпА в разных странах составляет 9–30 случаев на 10 000 населения [2]. Этиология заболевания до сих пор остается неизвестной. В происхождении р-аксСпА большое значение придается генетическим факторам, в частности антигену гистосовместимости HLA-B27, который встречается у 90–95% больных, примерно у 20–30% их родственников и лишь у 7–8% лиц в общей популяции. Обсуждается роль инфекционных факторов в развитии этого заболевания [3].
Основная цель лечения больных р-аксСпА — максимальное улучшение качества жизни посредством купирования и уменьшения боли, скованности и утомляемости, улучшения или стабилизации функциональных возможностей, предотвращения или замедления структурных повреждений [1]. Желательно достижение клинико-лабораторной и магнитно-резонансной ремиссии без воспалительного структурного прогрессирования.
К лекарственным средствам, которые рекомендованы для достижения низкой активности или ремиссии р-аксСпА, относятся нестероидные противовоспалительные препараты (НПВП), анальгетики, глюкокортикоиды (локально), ингибиторы фактора некроза опухоли α (ФНОα) и интерлейкина 17А.
Следует отметить, что достижение цели лечения р-аксСпА значительно затруднено ввиду выраженного полиморфизма клинической картины заболевания (включает спондилит, сакроилиит, артрит, энтезит, внескелетные проявления, из которых наиболее часто встречается увеит), а также ввиду частых мультиморбидных состояний [2].
Препараты, рекомендованные для лечения р-аксСпА, показали высокую клиническую и лабораторную безопасность в ходе контролируемых клинических исследований. Однако эффективность и безопасность препаратов в реальной клинической практике может отличаться от таковых в клинических исследованиях, т. к. в реальной практике по сравнению с клиническими исследованиями значительно чаще встречается мультиморбидность.
Цель настоящего исследования — определить эффективность и безопасность терапии голимумабом в реальной клинической практике у больных активным р-аксСпА.
Материал и методы
Дизайн исследования. В работе представлены результаты выполнения «Программы мониторинга активности, функционального статуса и коморбидности у пациентов с аксиальными спондилоартритами Северо-Западного федерального округа (ЛАДОГА)», регистрация в ЕГИСУ АААА-А17-117100370030-9 от 03.10.2017. В статистический анализ включены 40 пациентов с р-аксСпА (соответственно критериям ASAS от 2009 г.), имеющих достоверный сакроилиит, получающих терапию голимумабом в дозе 50 мг 1 р./мес. (т. е. 28 дней) подкожно в течение 24 нед. Программа не предусматривает коррекцию схемы лечения, терапию назначает лечащий врач.
Этические аспекты. Все пациенты подписали форму информированного согласия на участие в Программе. Все данные пациентов обрабатывались в обезличенном виде. Программа одобрена комитетом по этике ФГБОУ ВО
СЗГМУ им. И.И. Мечникова.
Анализ активности болезни и коморбидности. Для определения активности заболевания использовали индексы BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) и ASDAS (Ankylosing Spondylitis Disease Activity Score) [4, 5], для общей оценки пациентом своего здоровья — визуально-аналоговую шкалу (ВАШ), для оценки функционального статуса — индекс BASFI (Bath Ankylosing Spondylitis Functional Index). С-реактивный белок (СРБ) определяли высокочувствительным методом.
Коморбидность больных оценивали с помощью кумулятивного индекса (Cumulative Illness Rating Scalefor Geriatrics) по Miller [6].
Статистический анализ проведен с использованием программ Microsoft Office Exсel 2007 (Microsoft Corp., США) и STATISTICA 8.0 (StatSoft Inc, США). Характер распределения данных оценивали графическим методом и с использованием критерия Шапиро — Уилка. При распределении признаков, отличном от нормального, результаты представлены в виде Ме [Q1; Q3], где Me — медиана, Q1 и Q3 — первый и третий квартили. При распределении данных, отличном от нормального, применяли непараметрические методы: критерий Манна — Уитни, критерий Вальда — Вольфовица, критерий χ2, критерий Вилкоксона, критерий знаков.
Результаты исследования
Клиническая характеристика пациентов на момент включения в регистр (до получения пациентом первой дозы голимумаба) представлена в таблице 1.
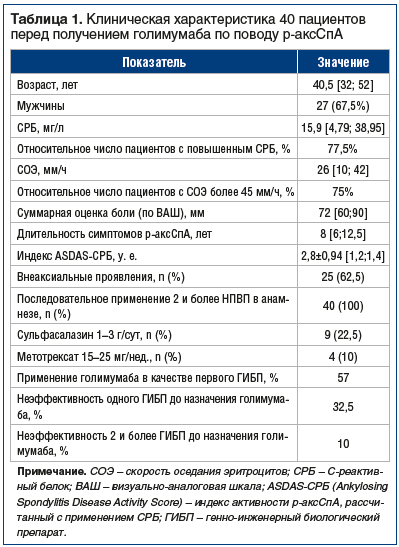
У всех пациентов до терапии голимумабом отмечалась высокая активность заболевания (см. табл. 1). Через 6 мес. после начала терапии голимумабом индекс ASDAS-СРБ снизился до 1,63±0,66 у. е. После 6 мес. непрерывной терапии голимумабом низкая активность заболевания (ASDAS<1,3) была достигнута у 12 пациентов (30%), из которых «бионаивными» являлись 10 человек (83,3% от числа достигших ремиссии и 25% от общего количества пациентов).
Средняя активность (ASDAS 1,3–2,1) сохранялась у 16 пациентов. У всех пациентов в данной группе отмечалось снижение активности заболевания: исходно ADSAS составлял 2,6±0,63, а через 6 мес. от начала терапии — 1,78±0,31.
Высокая активность заболевания (ASDAS>2,1) сохранялась у 10 пациентов (25%). У всех пациентов данной группы голимумаб являлся как минимум вторым по счету ингибитором ФНОα.
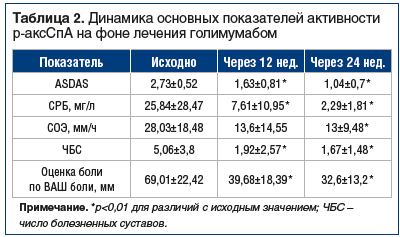
Данные таблицы 2 отражают динамику показателей воспалительной активности р-аксСпА на фоне лечения голимумабом. Достоверное снижение показателей отмечалось уже к 6-му мес. наблюдения, и в дальнейшем снижение продолжалось. Эта динамика показателей высокодостоверна (p<0,01), т. к. последующие значения заметно отличаются от исходных.
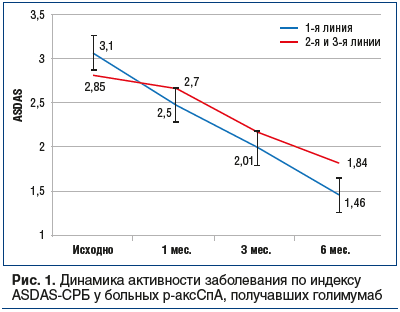
Пациенты, у которых голимумаб был вторым или третьим ГИБП, продемонстрировали меньший эффект (ASDAS в начале терапии — 2,85±0,87, через 6 мес. — 1,84±0,34). Если голимумаб был первым применяемым ГИБП, то ASDAS в начале терапии составлял 3,1±1,1, а через 24 нед. — 1,46±0,2 (рис. 1).
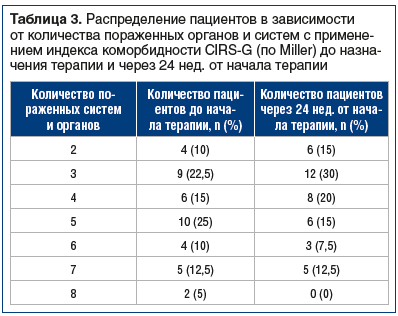
У пациентов, не достигших низкой активности заболевания, вторичный остеоартрит наблюдался в 60% случаев, сахарный диабет — в 10%, гиперурикемия выявлена в 7% случаев, артериальная гипертензия — в 17%. В ходе обследования не отмечено ни одного пациента без сопутствующей патологии. При оценке кумулятивного индекса коморбидности CIRS-G (по Miller) у всех пациентов было обнаружено как минимум два сопутствующих заболевания (табл. 3).
Чаще всего патология была связана с органами зрения (42,5%), в т. ч. со снижением уровня остроты зрения в связи с увеитами, перенесенными до начала терапии ГИБП. У пациентов, достигших ремиссии или низкой активности заболевания, выявлено снижение индекса CIRS-G (по Miller). Купирование анемии, хронического воспаления отмечено у 14 пациентов, нормализация показателей артериального давления — у 9, нормализация функциональных показателей по суставному статусу — у 40, улучшение остроты зрения — у 3, купирование симптомов депрессии — у 1, купирование симптомов гастрита и ГЭРБ — у 6.
Среди коморбидных заболеваний при р-аксСпА выделяют патологию верхних отделов желудочно-кишечного тракта (ЖКТ) в связи с длительным приемом НПВП [7–10]. В нашем исследовании частота патологии ЖКТ составляла 17,5%. При выполнении эзофагогастродуоденоскопии в 40% случаев выявлен хронический поверхностный гастродуоденит, в 13% — эрозии слизистой оболочки желудка, в 5% — рубцовая деформация стенок желудка или двенадцатиперстной кишки. Существенных различий в частоте патологии ЖКТ у больных, принимавших селективные и неселективные НПВП, не выявлено. Желудочно-кишечных кровотечений не зарегистрировано. На фоне терапии голимумабом 32 пациентам (80%) удалось снизить дозировку и кратность приема НПВП.
При оценке индексов риска возникновения значимых сердечно-сосудистых событий выявлено, что среднее значение SCORE у обследованных пациентов старше 40 лет составляло 2,82±2,81% [0,28; 3,75]. Максимальные параметры SCORE (22,43%) отмечались у пациента 60 лет с длительным анамнезом гипертонической болезни и стажем курения более 20 лет. На фоне терапии голимумабом достигнут хороший клинико-лабораторный ответ — снижение уровня ASDAS-СРБ до 1,6 (исходно ASDAS составлял 8,7).
Согласно современным рекомендациям по лечению р-аксСпА целью терапии является снижение активности заболевания и достижение клинико-лабораторной ремиссии. Терапия первой линии включает в себя НПВП, назначение которых опирается на определенные принципы:
НПВП являются препаратами первой линии у больных р-аксСпА;
НПВП вызывают замедление рентгенологического прогрессирования поражения связочного аппарата позвоночника и должны применяться длительно, в некоторых случаях — пожизненно;
р-аксСпА является, вероятно, единственным ревматическим заболеванием, при котором длительный прием НПВП патогенетически обоснован, высокоэффективен и не имеет альтернативы, кроме дорогостоящего лечения ингибиторами ФНОα; при этом заболевании к НПВП необходимо относиться как к базисным противовоспалительным препаратам;
при назначении НПВП необходимо учитывать кардиоваскулярный риск, наличие желудочно-кишечных заболеваний и заболеваний почек.
Обсуждение результатов
Главной целью терапии р-аксСпА исходя из концепции treat to target (лечение до достижения поставленной цели) является достижение стойкой ремиссии заболевания, основным критерием которой считается достоверное снижение клинической и лабораторно-инструментальной активности [11, 12]. Последние десятилетия в ревматологии ознаменовались активным внедрением в клиническую практику ГИБП, действие которых направлено на специфические звенья патогенеза ревматических заболеваний. Появление этого вида терапии расширило возможности лечения и в значительной степени способствовало пересмотру тактики ведения больных р-аксСпА [13].
Введение в лечебную практику ГИБП стало революционным, поскольку привело к беспрецедентному улучшению не только клинической симптоматики р-аксСпА, но и сдерживало рентгенологические признаки прогрессирования, способствовало существенному улучшению функций суставов и уменьшению смертности. Голимумаб — последний ингибитор ФНОα, зарегистрированный в мире и в России. Препарат представляет собой человеческие моноклональные антитела класса IgG1k, которые вырабатываются клеточной линией мышиной гибридомы, полученной с использованием технологии рекомбинантной ДНК. Голимумаб связывает и нейтрализует как растворимые, так и мембраносвязанные формы ФНОα.
Молекула голимумаба характеризуется высокой стабильностью и аффинностью к ФНОα, что обусловливает продолжительность биологического действия, поэтому инъекции голимумаба в отличие от других подкожных форм ингибиторов ФНОα проводятся реже — раз в месяц.
В ряде рандомизированных клинических исследований, таких как GO-RAISE, GO-AHEAD, GO-EASY, включая продленные фазы, при терапии р-аксСпА были продемонстрированы высокая противовоспалительная активность и высокая стабильность лечебного эффекта голимумаба [14–16].
Уже первые результаты рандомизированных клинических исследований показали, что иммуногенность голимумаба невысока и, по-видимому, не оказывает существенного влияния на результаты терапии. Это косвенно подтверждается доказанной эффективностью голимумаба при переключении с других ингибиторов ФНОα. Кроме того, при терапии голимумабом не зарегистрировано очевидных ассоциаций между образованием антител к препарату и индукцией других иммунологических нарушений, таких как инфузионные реакции и волчаночноподобный синдром.
В многочисленных клинических исследованиях и в реальной клинической практике все ингибиторы ФНОα продемонстрировали высокую эффективность в лечении р-аксСпА, однако их прямые сравнительные исследования не проводились. Поэтому выбор препарата обусловлен предпочтениями больного (подкожные или внутривенные инъекции), риском развития реинфекции, наличием специфических внесуставных признаков (увеита или воспалительных заболеваний кишечника) и сопутствующей патологии.
Заключение
Проведенное наблюдательное исследование свидетельствует о высокой симптоматической эффективности НПВП, которые являются препаратами первого выбора для большинства больных р-аксСпА. В случае их неэффективности или непереносимости альтернативой являются ингибиторы ФНОα, которые доказали свою высокую эффективность и приемлемую безопасность. Однако и их применение не всегда приводит к успешному результату по причине первичной резистентности, а нередко их эффективность снижается в ходе лечения (вторичная резистентность). В таких случаях терапия голимумабом может стать альтернативой для пациентов с р-аксСпА, у которых отсутствует ответ на лечение другими ингибиторами ФНОα. Применение ГИБП, которые способны модифицировать аутоиммунные процессы в организме путем снижения уровня провоспалительных цитокинов (ФНОα, интерлейкина 17 и др.), а также влияния на Т- и В-клеточные звенья иммунного ответа, открывает новые горизонты в лечении больных р-аксСпА. Благодаря рациональной биологической терапии возможно значительно уменьшить прогрессирование р-аксСпА, уровень инвалидизации, а также улучшить качество жизни пациентов.
Информация с rmj.ru






