Введение
Нестероидные противовоспалительные препараты (НПВП) — лекарственные средства, которые чрезвычайно часто назначают врачи различных специальностей, преимущественно терапевты, неврологи, ревматологи, ревматологи-ортопеды. Основные эффекты НПВП — жаропонижающий, анальгетический и противовоспалительный — позволяют назначать их с анальгетической целью (при зубной, головной боли), а также как жаропонижающее средство (при простудах, респираторных заболеваниях). Чаще всего используется противовоспалительное действие НПВП при ревматологических заболеваниях, распространенность которых в популяции высока: миллионы людей страдают от болей в суставах и позвоночнике при ревматоидном артрите (РА), спондилоартропатиях и остеоартрите (ОА) — наиболее частых артрологических заболеваниях [1]. Кроме того, боли в периартикулярных тканях и мышцах сопровождают многие заболевания либо возникают как самостоятельное страдание. Следует отметить, что НПВП эффективны в отношении ноцицептивной боли, а при многих заболеваниях ревматологического профиля боль формируется за счет разных механизмов и нередко включает невропатический компонент [2]. По данным Е.С. Филатовой и соавт. [2], у 43% больных РА, 37% больных ОА и 19% больных анкилозирующим спондилитом имеется компонент нейропатической боли. В таких случаях болеутоляющий эффект НПВП недостаточен, что вызывает желание повысить дозу препарата либо остановить выбор на неселективных ингибиторах циклооксигеназы (ЦОГ), которые несут повышенный риск развития осложнений. Оценка характера боли и выявление дескрипторов нейропатической боли (ощущение как при ударе током, парестезии, онемение и др.) необходимы для проведения адекватной (если необходимо, и комбинированной) терапии. Тем не менее практически все больные ревматологического профиля принимают НПВП, и притом длительно — в течение недель, месяцев и лет [3]. В связи с этим безопасность НПВП так широко обсуждается в литературе.
Переносимость различных НПВП
Те НПВП, которые используются в настоящее время в клинической практике, обладают примерно равным анальгетическим и противовоспалительным эффектом. Это продемонстрировано в большом количестве систематических обзоров и метаанализов [4–6]. Однако переносимость препаратов различной химической структуры и с различным механизмом действия существенно различается.
Серьезные побочные эффекты НПВП хорошо изучены и в значительной степени связаны с их механизмом действия [7]. Обширные фармакоэпидемиологические исследования и метаанализы задокументировали серьезные осложнения в отношении слизистой верхних отделов желудочно-кишечного тракта (ЖКТ) [8, 9] и сердечно-сосудистой системы [10–15]. Эти исследования позволили в какой-то степени оценить риск развития нежелательных явлений (НЯ) при применении тех или иных препаратов этого большого класса лекарственных средств [16]. В настоящее время стало очевидно, что основным способом профилактики НЯ, связанных с приемом НПВП, является оценка факторов риска их развития у каждого индивидуума (табл. 1) [17].
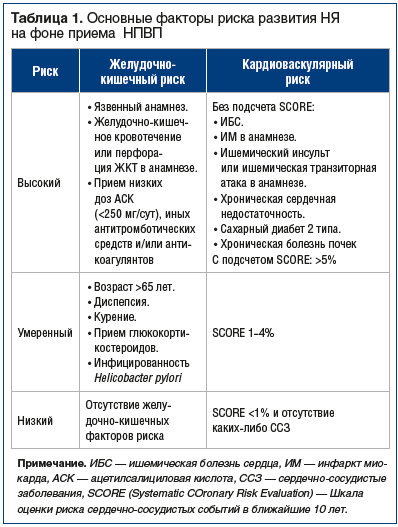
Однако оценка развития осложнений со стороны ЖКТ или сердечно-сосудистой системы существенно различается. Понятие «НПВП-гастропатия» обозначает повреждение различных отделов ЖКТ в связи с повреждающим влиянием НПВП. И основным фактором риска развития повреждения ЖКТ на фоне применения НПВП является язвенная болезнь в анамнезе, что в среднем при болезнях опорно-двигательного аппарата встречается в 5–15% случаев [18]. Риск развития кардиоваскулярных (КВ) НЯ оценивать сложнее, так как хроническое воспаление само по себе служит важным фактором риска повреждения сосудов с развитием атеросклероза и связанного с ним риска развития острых состояний: ИМ, инсульта, смерти [19–21]. Так, анализ базы данных первичной медицинской помощи в Англии на 1 475 762 человека показал, что более 50% преждевременных смертей при РА связано именно с риском развития ССЗ, что лишь частично объясняется традиционными факторами риска ССЗ [22].
Кроме того, в структуре коморбидности практически при всех хронических заболеваниях суставов ведущее место занимают именно заболевания сердечно-сосудистой системы [23, 24].
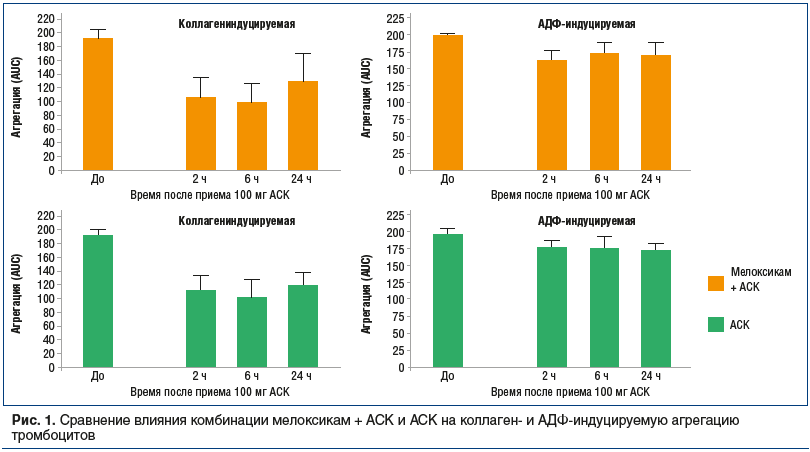
Степень повреждения ЖКТ можно снизить совместным назначением НПВП и ингибиторов протонной помпы [25]. В то же время нет убедительных доказательств того, что низкие дозы АСК снижают КВ-риск НПВП [26, 27]. Имеются данные, что сочетанный прием НПВП и низких доз АСК уменьшает риск КВ-осложнений [28] (хотя может увеличиться риск повреждения слизистой ЖКТ), что приводит к снижению частоты развития ИМ и инсульта примерно на 25% [29]. При этом известно, что ряд НПВП при одновременном с АСК назначении могут уменьшить ее кардиопротективные свойства. В основном это касается неселективных НПВП, ингибирующих ЦОГ-1 [17], в первую очередь ибупрофена. В связи с этим при необходимости одновременного назначения НПВП и АСК желательно принимать эти средства с интервалом в несколько часов. Отсутствие у селективных НПВП значимого подавления активности ЦОГ-1 и конкуренции с антитромботическим действием низких доз АСК позволяет рекомендовать именно эту группу препаратов для лечения больных с сопутствующими ССЗ. Целесообразность такого выбора показана и для коксибов [30], и для мелоксикама [31]. Было проведено специальное исследование влияния мелоксикама на дезагрегантные свойства АСК при одновременном их назначении здоровым добровольцам. По результатам этого исследования был сделан вывод, что такая комбинация не влияет на дезагрегантное действие АСК (рис. 1) [31].
При ведении пациентов с высоким риском сердечно-сосудистых событий у врачей есть выбор: не назначать НПВП или рекомендовать препарат с более низким риском. Следует подчеркнуть, что данные, касающиеся связи между приемом НПВП и риском КВ-осложнений, весьма противоречивы [32]. Увеличение частоты НЯ со стороны сердечно-сосудистой системы связывали с механизмом действия селективных НПВП — преимущественным подавлением ЦОГ-2 с нарушением баланса между антитромботическим и вазодилатирующим действием простагландина PGI2 (простациклина) и тромбоксана A2, вызывающего адгезию и агрегацию тромбоцитов (рис. 2). Однако, как показали результаты рандомизированных контролируемых исследований (РКИ) и наблюдательных когортных исследований, и неселективные, и селективные НПВП могут увеличивать риск КВ НЯ [34–36].
![Рис. 2. Влияние НПВП на сердечно-сосудистую систему [33] Рис. 2. Влияние НПВП на сердечно-сосудистую систему [33]](https://medblog.su/wp-content/uploads/2021/07/1625734477_336_kardiovaskulyarnaya-bezopasnost-nesteroidnyh-protivovospalitelnyh-preparatov-chichasova-n-v-lila-a-m.png)
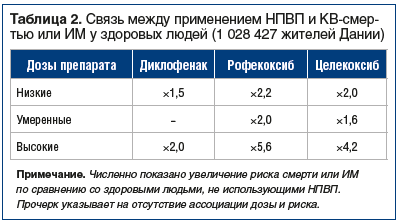
Неселективные НПВП, блокируя ЦОГ-1, способствуют дестабилизации течения артериальной гипертензии (АГ), могут приводить к задержке жидкости за счет повреждения интерстиция почек и снижению эффективности антигипертензивных препаратов [37]. Следовательно, больным с сопутствующей АГ при назначении НПВП следует рекомендовать тщательный мониторинг артериального давления, при повышенной опасности развития тромбозов (особенно при наличии их в анамнезе) необходимо дополнять лечение дезагрегантами. Следует стремиться использовать минимальные эффективные дозы НПВП, поскольку прием высоких доз ассоциируется с увеличением риска КВ-осложнений (табл. 2) [33].
Настороженное отношение к селективным ингибиторам ЦОГ-2 возникло после публикации исследования VIGOR [38]: при лечении больных РА назначение рофекоксиба приводило к достоверно большей частоте развития ИМ, чем у больных, получавших напроксен. Далее сходные данные были получены в поисковом исследовании возможного использования целекоксиба в очень высоких дозах (до 800 мг/сут) в профилактике колоректального рака [39]. Было даже высказано предположение, что КВ-осложнения — это эффекты селективных ингибиторов ЦОГ-2 как класса препаратов в целом. Однако это предположение не нашло подтверждения в дальнейших исследованиях, где целекоксиб также назначался в высоких дозах для профилактики семейного аденоматозного полипоза [40] и болезни Альцгеймера [41] и где не зарегистрировано достоверного увеличения частоты развития нежелательных КВ-событий при использовании целекоксиба в сравнении с плацебо или в сравнении с плацебо и напроксеном [41]. Более того, на фоне применения напроксена в низкой суточной дозе (440 мг) риск нежелательных КВ-событий увеличивался в 2 раза.
При всей ценности данных, полученных в РКИ, необходимо учитывать, что отбор больных для таких исследований определяется протоколом, ограничивающим включение пациентов с рядом сопутствующих заболеваний. Таким образом, больные в РКИ и больные в реальной клинической практике отличаются. Наиболее убедительные данные, дающие врачам ориентир в назначении НПВП, можно получить из когортных наблюдательных исследований.
В одно из таких сравнительных когортных исследований вошло 51 813 пациентов. Целью исследования было сравнить частоту тромботических осложнений на фоне лечения мелоксикамом (19 087 больных), рофекоксибом (15 268 больных) [42] и целекоксибом (17 458 больных) [43]. Статистический анализ проводился со стратификацией больных по полу и возрасту. Было показано, что в сравнении с мелоксикамом более высокий риск цереброваскулярных осложнений был при применении рофекоксиба (относительный риск (ОР) 1,68, 95% доверительный интервал (ДИ) 1,15–1,46) и целекоксиба (ОР 1,66, 95% ДИ 1,10–2,51). Различий по тромбоэмболическим осложнениям при использовании любого из этих трех препаратов получено не было. Прием мелоксикама или целекоксиба также не характеризовался различиями в развитии КВ-событий и периферических тромбозов.
Метаанализ данных 35 исследований (27 039 больных) подтвердил высокую безопасность мелоксикама в сравнении с неселективными НПВП или плацебо в отношении ЖКТ [44]. При оценке риска острого ИМ, застойной сердечной недостаточности, отеков и АГ у 27 039 больных с сопутствующими ССЗ на фоне приема мелоксикама в дозах 7,5–30 мг/сут (n=15 071), неселективных НПВП (11 087 пациентов получали диклофенак 100–150 мг/сут,
напроксен 500–750 мг/сут, пироксикам 20 мг/сут) и плацебо (n=736) [45] было продемонстрировано, что и в такой когорте больных мелоксикам не оказывает отрицательного влияния на течение АГ, выраженность периферических отеков и не ведет к увеличению частоты ИМ или тромбозов (табл. 3). Такие же данные получены в более позднем систематическом обзоре 19 исследований: мелоксикам продемонстрировал низкое увеличение комбинированного риска развития осложнений со стороны сердечно-сосудистой системы (ОР 1,14, 95% ДИ 1,04–1,25), поскольку он не повышал миокардиальный (ОР 1,13, 95% ДИ 0,98–1,32) или почечный (ОР 0,99, 95% ДИ 0,72–1,35) риски [46]. По сравнению с мелоксикамом комбинированный КВ-риск возрастал максимально при использовании рофекоксиба и минимально — при использовании ибупрофена [46].
![Таблица 3. Кардиоваскулярные и ренальные НЯ [44] Таблица 3. Кардиоваскулярные и ренальные НЯ [44]](https://medblog.su/wp-content/uploads/2021/07/1625734477_55_kardiovaskulyarnaya-bezopasnost-nesteroidnyh-protivovospalitelnyh-preparatov-chichasova-n-v-lila-a-m.png)
Интересны результаты рандомизированного проспективного исследования по сравнению стандартной терапии нестабильной стенокардии без изменения сегмента ST (гепарин, АСК — 1-я группа, n=60) и терапии гепарином, АСК с добавлением мелоксикама 15 мг внутривенно с переходом на пероральную форму (2-я группа, n=60). Использование комбинации с мелоксикамом привело к достоверно (р=0,007) более низкой частоте рецидивов стенокардии и развития ИМ — 15% против 38,3% при стандартной терапии гепарином и АСК [47].
Изучена связь приема НПВП с развитием венозных тромбозов (ВТ). В исследование включено 4020 больных ОА с ВТ и 20 059 больных без ВТ (группа контроля, сопоставимая по полу и возрасту) [48]. Наиболее высокий риск развития ВТ отмечен при приеме диклофенака (отношение шансов (ОШ) 1,63, 95% ДИ 1,53–1,74), несколько меньше — при приеме ибупрофена (ОШ 1,49, 95% ДИ 1,38–1,62) и еще ниже — при приеме мелоксикама (ОШ 1,49, 95% ДИ 1,11–1,50) и целекоксиба (ОШ 1,30, 95% ДИ 1,11–1,51). Повышения риска развития ВТ при приеме напроксена не отмечено.
Многоцентровое исследование по оценке риска развития острого ИМ при назначении различных (селективных и неселективных) НПВП (препарат сравнения диклофенак, риск для которого принимался за 1,0) было проведено в популяциях трех стран (Великобритании, Канады и США) [49]. Всего проанализировано 60 473 случая лечения НПВП и 248 768 случаев контроля. Во всех трех когортах больных риск ИМ при использовании мелоксикама был ниже 1,0 и колебался от 0,46 до 0,81. Целекоксиб не показал значимого увеличения риска развития ИМ по сравнению с диклофенаком, а прием рофекоксиба в когортах пациентов из Канады и США был сопряжен с повышением риска ИМ (в американской когорте повышение до 1,23, хоть и незначительное, было статистически значимым). При использовании неселективных НПВП данные в когортах несколько различались: при приеме напроксена риск был выше 1,0 в великобританской когорте и снижен в когорте больных из США, риск при приеме ибупрофена был повышен только в первой когорте. Эти данные свидетельствуют о наибольшей безопасности использования мелоксикама в сравнении с диклофенаком, а также о том, что развитие КВ-осложнений возможно при использовании любого НПВП и требует постоянного контроля со стороны пациента и врача, особенно при наличии у пациента сердечно-сосудистой коморбидности.
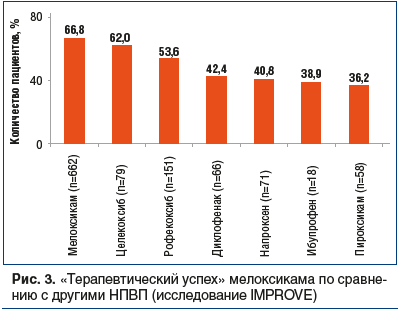
Мелоксикам уже давно с успехом используется в лечении боли и воспаления в различных структурах опорно-двигательного аппарата. Еще в начале XXI в. было проведено крупное исследование по оценке так называемого «терапевтического успеха» мелоксикама у 662 больных ОА в сравнении с 647 больными ОА, получавшими другие НПВП (исследование IMPROVE) [50]. «Терапевтическим успехом» считалось достижение клинического эффекта и отсутствие потребности в НПВП или отсутствие необходимости перехода на прием другого НПВП при завершении исследования. Таким условиям соответствовали 67% пациентов, получавших мелоксикам, и 45% пациентов, получавших другие НПВП (p<0,0005). Мелоксикам продемонстрировал и лучшую переносимость лечения: отмена из-за НЯ при приеме мелоксикама потребовалась в 12% наблюдений, при приеме других НПВП — в 20% (рис. 3).
Заключение
Эффективность мелоксикама показана в РКИ, когортных, популяционных исследованиях при хронических ревматологических болезнях, при острых болевых синдромах [51–53]. Препарат демонстрирует хорошую переносимость со стороны ЖКТ, что было показано в РКИ и подтверждено данными метаанализов и реальной клинической практики в крупных когортах больных. Большинство клинических исследований, в том числе популяционных, свидетельствуют об отсутствии у мелоксикама негативного влияния на проявления сердечно-сосудистой патологии. Однако абсолютно безопасных препаратов не существует. Для успешного и безопасного применения НПВП необходимо учитывать факторы риска развития НЯ [17] и использовать алгоритм выбора НПВП, что продемонстрировано в условиях реальной клинической практики (исследование ПРИНЦИП) [54].
.
Информация с rmj.ru





