Введение
Исследования последних лет привели к внедрению в клиническую практику лечения ревматоидного артрита (РА) и псориатического артрита (ПсА) нового класса таргетных иммуносупрессоров — ингибиторов янус-киназ (JAK), низкомолекулярных средств, прерывающих внутриклеточную передачу многих провоспалительных сигналов. Первым из препаратов этого класса для клинического применения зарегистрирован тофацитиниб, который блокирует преимущественно янус-киназу-1 (JAK1) и янус-киназу-3 (JAK3) и в меньшей степени — янус-киназу-2 (JAK2) [1].
Некоторые теоретические данные позволяют предполагать наличие у блокатора JAK-киназ тофацитиниба прямого обезболивающего эффекта. Так, продемонстрирована способность интерлейкина-6 (ИЛ-6) усиливать гипералгезию как на уровне нервных окончаний, так и на уровне центральной нервной системы. Сигнал от рецептора ИЛ-6 проводится через JAK/STAT-путь, включающий JAK1, JAK2 и транскрипционные факторы семейства STAT (signal transducer and activator of transcription) — STAT1, STAT3-молекулы, и может быть прерван тофацитинибом [2]. Блокада JAK/STAT3-пути приводит к уменьшению гипералгезии, вызванной длительной компрессией нервных окончаний [3].
A. Ogdie et al. (2020) продемонстрировали, что тофацитиниб достоверно уменьшает боль, оцененную с помощью различных опросников, у пациентов с РА, анкилозирующим спондилитом (АС) и ПсА [4]. Однако дизайн этого исследования не позволяет решить, в какой мере уменьшение боли опосредовано противовоспалительным действием препарата, а в какой — прямым анальгетическим эффектом. Известно, что и другие таргетные иммуносупрессоры купируют выраженность боли и других показателей, субъективно оцениваемых пациентами, при РА, АС и ПсА [5–8].
В то же время можно было бы предположить, что при наличии у препарата клинически значимого прямого анальгетического эффекта будет наблюдаться диспропорция между субъективными и объективными проявлениями заболевания, заметная в сравнении с эффектами других лекарств похожего действия. То есть препарат со значимым обезболивающим действием при том же уровне воспалительной активности у пациента будет демонстрировать существенно лучшую в сравнении с другими препаратами динамику субъективных симптомов заболевания.
Целью настоящего исследования стала оценка клинически значимого обезболивающего действия тофацитиниба у пациентов с РА в условиях реальной клинической практики.
Материал и методы
Были проанализированы данные пациентов с РА из Московского единого регистра артрита (МЕРА). В регистр включаются пациенты, получающие генно-инженерную биологическую или таргетную синтетическую противовоспалительную терапию за счет бюджетных средств, проживающие в Москве.
В качестве субъективных оценок рассматривались число болезненных суставов (ЧБС), индекс функциональной способности HAQ (Health Assessment Questionnaire), индекс активности заболевания RAPID3 (Routine Assessment Of Patient Index Data 3). В качестве объективных показателей воспалительной активности анализировались число припухших суставов (ЧПС), уровень С-реактивного белка (СРБ). Произведена оценка частных от деления субъективных показателей на объективные во всех возможных сочетаниях для различных таргетных препаратов, использовавшихся в изучаемой группе пациентов. Таким образом, рассчитывались следующие показатели: ЧБС/(ЧПС+1), HAQ/(ЧПС+1), RAPID3/(ЧПС+1), ЧБС/(СРБ+1), HAQ/(СРБ+1), RAPID3/(СРБ+1). Прибавление единицы к делителю применялось во избежание ошибочных и несоразмерно высоких больших значений частного при нулевых или близких к нулю значениях делителя. С учетом наблюдательного характера исследования проводился поиск конфаундеров для всех указанных отношений (частных от деления). Сравнение рассчитанных индексов на фоне лечения различными таргетными препаратами проводилось с поправкой на выявленные конфаундеры. Процесс отбора конфаундеров осуществлялся в 2 этапа: 1) предварительный отбор показателей, имеющих достоверную однофакторную связь с зависимой переменной; 2) последующий обратный пошаговый отбор переменных в рамках обобщенной линейной модели.
Результаты и обсуждение
В анализ было включено 944 эпизода лечения у 832 пациентов. Проанализированная длительность эпизодов составила 1312±1006 дней. В том числе проанализировано 93 эпизода лечения тофацитинибом, их средняя длительность составила 836±453 дня. Общая характеристика пациентов, включенных в исследование, приведена в таблице 1.

Конфаундеры, выбранные по вышеописанному протоколу, представлены в таблице 2. При анализе с поправкой на выявленные конфаундеры обнаружено, что показатели ЧБС/(ЧПС+1), HAQ/(ЧПС+1) и RAPID3/(ЧПС+1) на фоне приема тофацитиниба были достоверно ниже средних значений, полученных при применении таргетных препаратов в целом. Достоверных различий между препаратами по отношениям изучаемых субъективных показателей к уровню СРБ выявить не удалось.
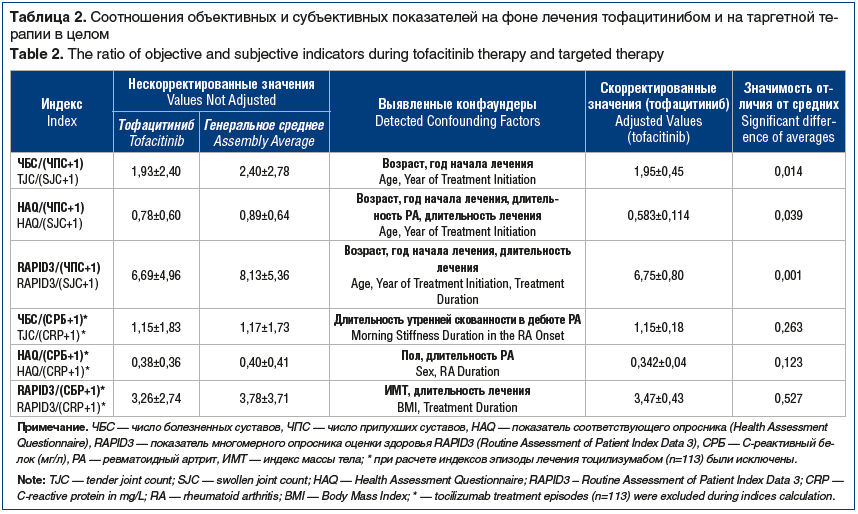
На фоне терапии тофацитинибом при том же ЧПС выявляются существенно меньшее по сравнению с другими таргетными препаратами ЧБС, меньшая выраженность функциональных нарушений, лучшая субъективная оценка общего состояния здоровья по опроснику RAPID3. Этот факт, с одной стороны, может служить косвенным подтверждением ранее предполагавшегося обезболивающего действия тофацитиниба. В таком случае этот эффект следует рассматривать как клинически значимый, поскольку он проявляется в важных для самочувствия пациента показателях.
С другой стороны, обнаруженные особенности эффекта тофацитиниба дают повод считать, что методы измерения эффективности препаратов, основанные на оценке их влияния на воспалительную активность, возможно, недооценивают действие тофацитиниба, поскольку клиническое улучшение и возрастание функциональных способностей пациента при его использовании могут быть непропорциональны достигнутому снижению воспалительной активности. По-видимому, для понимания результатов лечения тофацитинибом у пациентов с РА в качестве более корректных следует рассматривать субъективные показатели (например, RAPID3 и HAQ). Тофацитиниб не отличался от других препаратов по отношениям субъективных показателей к уровню СРБ. Возможным объяснением этого факта может быть особое действие препарата и на этот показатель. Учитывая механизм действия тофацитиниба (блокирование проведения сигнала от рецептора ИЛ-6), можно предположить, что подобно ингибиторам ИЛ-6 этот препарат способен угнетать продукцию СРБ непропорционально степени подавления воспаления. В таком случае СРБ не может рассматриваться как корректная оценка уровня воспаления при использовании тофацитиниба.
Заключение
Выраженность субъективных ощущений и функциональных нарушений у пациентов, получающих лечение тофацитинибом, может быть меньше при той же выраженности объективных признаков артрита в сравнении с таковой на фоне генно-инженерных противовоспалительных препаратов. Это означает, что клиническая эффективность препарата может недооцениваться при использовании показателей, основанных на объективных проявлениях воспаления (например, ЧПС). Полученные результаты также подчеркивают важность функциональных показателей для оценки эффекта тофацитиниба. Изучение анальгетической активности таргетных препаратов может значительно повлиять на понимание механизмов их клинической эффективности.
About the authors:
1–3 Eugenii V. Zhilyaev — Dr. of Sci. (Med.), Professor, Chief Medical Officer, Professor of the Department of Rheumatology, Leading Researcher of the Research Laboratory of Rheumatological Diseases; ORCID iD 0000-0002-9443-1164.
4,5 Galina V. Lukina — Dr. of Sci. (Med.), Professor, Head of the Research Department of Rheumatology, Head of the Moscow City Rheumatology Center; ORCID iD 0000-0001-7958-5926.
6Ekaterina N. Koltsova — Head of the Organizational and Methodological Department of Rheumatology, ORCID iD 0000-0002-5202-4878.
7Evgeniya I. Shmidt — Cand. of Sci. (Med.), Head of the Department of Rheumatology; ORCID iD 0000-0001-8814-9704.
8Karine A. Lytkina — Cand. of Sci. (Med.), Head of the Department of Rheumatology; ORCID iD 0000-0001-9647-7492.
1AO “EMC”. 35, Schepkina str., Moscow, 129090, Russian Federation.
2Russian Medical Academy of Continuous Professional Education. 2/1, Barrikadnaya str., bld. 1, Moscow, 125993, Russian Federation.
3Pirogov Russian National Research Medical University. 1, Ostrovityanova str., Moscow, 117997, Russian Federation.
4Loginov Moscow Clinical Scientific Center. 86, Entusiastov road, bld. 6, Moscow, 111123, Russian Federation.
5Research Institute of Rheumatology named after V.A. Nasonova. 34A, Kashirskoe road, Moscow, 115522, Russian Federation.
6Research Institute for Healthcare and Medical Management of Moscow Healthcare Department. 9, Sharikopodshipnikovskaya str., Moscow, 115088, Russian Federation.
7City Clinical Hospital No. 1 named after N.I. Pirogov. 8, Leninskii prospect, Moscow, 119049, Russian Federation.
8City Clinical Hospital No. 4. 25, Pavlovskaya str., Moscow, 115093, Russian Federation.
Contact information: Eugenii V. Zhilyaev, e-mail: zhilyayevev@mail.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 15.06.2020, revised 30.06.2020, accepted 16.07.2020.
.
Информация с rmj.ru






