Содержание статьи
Гастроэзофагеальная
рефлюксная болезнь и бронхообструктивный
синдром у детей — «порочный круг» или
коморбидность?
Эйберман А.С.
ФГБОУ ВО «Саратовский государственный
медицинский университет им. В.И. Разумовского»
МЗ РФ
Воротникова Наталия Анатольевна,
к.м.н., ассистент кафедры госпитальной
педиатрии и неонатологии педиатрического
факультета
Черненков Юрий Валентинович, д.м.н.,
директор клиники госпитальной педиатрии
Университетской клинической больницы № 1 им.
С.Р. Миротворцева; заведующий кафедрой,
профессор кафедры госпитальной педиатрии и
неонатологии педиатрического факультета
Эйберман Александр Семенович, д.м.н.,
профессор кафедры госпитальной педиатрии и
неонатологии педиатрического факультета
Резюме
Настоящая статья посвящена коморбидности
заболеваний органов пищеварительного тракта и
дыхательной системы у детей. Коморбидность (полиморбидность)
при патологии желудочно-кишечного тракта
достаточно широко описывается в современной
научной литературе, однако, менее изученными
представляются взаимоотношения пищеварительной
и дыхательной систем.
Цель исследования — провести анализ
эндоскопических признаков рефлюксной патологии
пищеварительного тракта у детей при
коморбидном состоянии — ГЭРБ и заболеваниях
органов дыхания, протекающих с
бронхообструктивным синдромом (БОС).
Материалы и методы. Проведено
углубленное обследование 180 детей от 6 до 16
лет с коморбидной патологией (заболевания
органов дыхания с БОС и ГЭРБ). Выполнено:
рентгенографическое исследование, спирометрия,
внутриполостная рH-метрия, ЭФГДС и УЗИ органов
ЖКТ. Для изучения морфологических особенностей
слизистой пищевода при данной сочетанной
патологии исследованы биоптаты на 1 см выше
Z-линии; одновременно проведена биопсия
слизистой антрального отдела препилорической
части желудка.
Результаты. Заболевания органов дыхания
с БОС в обследованных группах больных наиболее
часто (43,9%) сочетались с ГЭРБ в возрасте
12–14 лет. Преобладание
эндоскопически-позитивного варианта ГЭРБ 1
степени характерно для пациентов с
бронхообструктивным синдромом, обусловленного
средне-тяжелым и тяжелым персистирующим
течением БА, острым и затяжным течением
пневмонии, рецидивирующим бронхитом.
Воспалительные заболевания органов пищеварения
(хронический гастрит, хронический
гастродуоденит) при БА выявлены у 40,6%
больных, при пневмонии — у 45,7%, при
рецидивирующем бронхите — у 33,3% пациентов.
На основании данных общеморфологического
исследования биоптатов, независимо от возраста
и вида бронхо-легочной патологии, выявлено два
варианта воспаления, встречающихся чаще других
— с преобладанием изменений дистрофического
характера и с преобладанием собственно
воспаления, что в большей степени зависело от
длительности заболевания. У пациентов,
страдающих как БА, так и пневмонией с БОС,
морфологические изменения со стороны слизистой
пищевода соответствовали катаральному
характеру воспаления.
Ключевые слова: гастроэзофагеальная
рефлюксная болезнь, коморбидность,
бронхиальная астма, бронхообструктивный
синдром, рН-метрия
Конфликт интересов. Авторы заявляют об
отсутствии конфликта интересов.
Введение
Патология органов пищеварительного тракта у
детей является одной из серьезных проблем
здоровья подрастающего поколения современной
России. Особенности сегодняшней жизни, для
которой характерны стресс, нерациональное
питание, гиподинамия, повышают вероятность
заболеваний пищеварительного тракта не только
взрослых, но и детей [1] В структуре патологии
пищеварительного тракта у детей по-прежнему
высок удельный вес хронических
гастродуоденитов – от 58 до 90% [2]. В широком
спектре хронических воспалительных заболеваний
желудочно-кишечного тракта (ЖКТ), отмечаемых у
детей разного возраста, все большее место
занимают поражения пищевода, энтерологи
нередко отмечали различные аномалии и пороки
развития, травмы слизистой оболочки в
результате преимущественно термического или
химического повреждения, а также отдаленные
последствия этих повреждений, то в настоящее
время все чаще встречаются изменения слизистой
оболочки воспалительного характера [2, 3, 4],
причем воспаление пищевода сочетается с
поражением других органов и систем. На
современном этапе следует выделить отчетливую
тенденцию к нарастанию частоты ГЭРБ в
популяции [5, 6, 7]. У многих исследователей
вызывают интерес внепищеводные проявления,
которые трудно диагностируются:
кардиоваскулярная, оториноларингологическая,
стоматологическая, анемическая,
отоларингологическая «маски» рефлюксной
болезни. Наиболее многочисленной группой
заболеваний, ассоциированных с внепищеводными
проявлениями ГЭРБ, являются респираторные [8,
9].
Частота и вероятность совместного поражения
пищеварительной и дыхательной систем
объясняется общностью анатомических связей,
единством эмбриологического происхождения
бронхиального дерева и пищевода от первичной
пищеварительной трубки, единой иннервацией
веточками n. vagus, особенностями
кровоснабжения. [10]. Из этого следует, что
коморбидность в педиатрической
гастроэнтерологии не является случайной, она
может протекать по типу синтропии
(одновременное поражение органов) или
интерференции (возникновение одного
заболевания под влиянием другого) [11]. В
настоящее время широко дискутируется вопрос о
роли ГЭРБ как патогенетического фактора в
развитии заболеваний бронхолегочной системы
(бронхиальная астма, хронический кашель,
аспирационные пневмонии и др.). Легочные
проявления рассматриваются в качестве основной
«маски» ГЭРБ, при этом ГЭРБ может просто
сочетаться с легочной патологией, маскировать
и/или усугублять ее течение. По мнению ряда
авторов, наличие ГЭРБ может способствовать
формированию бронхиальной астмы (БА) и
развитию пневмонии [12, 13, 14].
Наиболее изученной является взаимосвязь между
патологическим гастроэзофагеальным рефлюксом (ГЭР)
и БА: патологический ГЭР рассматривается в
качестве триггера ночных приступов БА, вызывая
бронхоспазм [15, 16]. Коморбидность БА и ГЭРБ
сопровождается увеличением потребности в
использовании бронходилататоров короткого
действия в среднем в 1,5 раза по сравнению с
пациентами без симптомов ГЭРБ. Многие
препараты патогенетической терапии БА (бета-адреноблокаторы,
блокаторы гистаминовых и серотониновых
рецепторов, эуфиллин, НПВП, глюкокортикоиды,
транквилизаторы и др.) оказывают повреждающее
действие на слизистую оболочку пищевода,
снижают тонус нижнего пищеводного сфинктера
(НПС), замедляют перистальтику пищевода,
инициируя развитие симптомов ГЭРБ. В
результате этого формируется порочный круг
[17–20]. В то же время известно, что
адекватная терапия ГЭРБ ингибиторами протонной
помпы (ИПП) позволяет повысить контроль над
заболеванием.
В медицинской литературе доминируют две
ведущих точки зрения на механизм развития БА у
пациентов ГЭРБ: рефлекторная теория и
рефлюксная теория (микроаспирация желудочного
содержимого в легкие). Патогенез БА при ГЭРБ
обусловлен как прямым химическим повреждением
бронхолегочной ткани рефлюктатом, так и
стимуляцией рефлюктатом хеморецепторов
пищевода, которая опосредована рефлекторным
вагусным влиянием, нарушением моторики
пищевода с развитием бронхоконстрикции;
нарушением функции верхнего и нижнего
пищеводного сфинктеров; микроаспирацией
кислого содержимого в дыхательные пути,
ротоглотку, носоглотку, ротовую полость с
развитием поражений органов и тканей.
Микроаспирация – один из возможных компонентов
механизма развития рефлюкс-индуцированной БА.
Вследствие микроаспирации происходит
стимуляция кашлевого рефлекса, повышение
градиента внутрибрюшного давления, провоцируя
возникновение ГЭР, вновь запуская механизм
активации вагусных рецепторов [21, 22]. Таким
образом, с появлением рефлюкс-индуцированной
БА формируется «порочный круг» –
индуцированный рефлюксом бронхоспазм вызывает
необходимость применения лекарственных
препаратов (бета-адреноблокаторы, теофиллины),
которые еще больше понижают тонус НПС и
стимулируют усиленную секрецию соляной кислоты
в желудке. Кроме того, у больных БА растет
градиент давления между грудной клеткой и
брюшной полостью, что также способствует
рефлюксу. Применение ингаляционных
глюкокортикостероидов без спейсера приводит к
тому, что 80% ингалируемой дозы попадает в
желудок и тем самым усугубляет проявления ГЭР.
Несмотря на успехи последних лет, достигнутые
в диагностике и лечении заболеваний органов
дыхания, во всем мире отмечается тенденция к
увеличению распространенности болезней легких
и бронхов среди. По оценке ВОЗ, бронхиальной
астмой (БА) страдают около 350 миллионов
человек (Global Initiative for Asthma (GINA),
2021 [23]. Согласно результатам
эпидемиологических исследований, в Российской
Федерации распространенность БА среди детского
населения составляет около 10% [24, 25, 26].
Следует отметить, что не только БА, но и
другие заболевания органов дыхания в детском
возрасте, протекающие с признаками БОС, более
чем в 45% случаев сочетаются с патологическими
изменениями органов пищеварения [27,28].
Эффект коморбидности, порой, неблагоприятно
сказывается на течении БОС – заболевания
бронхо-легочной системы принимают упорное,
рецидивирующее течение, не поддающиеся
стандартной терапии. Многие аспекты
совместного течения патологии органов дыхания
и ГЭРБ остаются малоизученными – большинство
работ на эту тему посвящено сочетанному
течению БА и ГЭРБ, тогда как особенности
клинической картины пневмонии и бронхита с БОС
на фоне ГЭРБ практически не анализируются. До
настоящего времени остается открытым вопрос о
том, в каких случаях у детей на фоне ГЭРБ
развивается патология органов дыхания, а при
каких обстоятельствах у другой группы детей
этот процесс не реализуется.
Указанные данные с настоятельной
необходимостью требуют продолжения дальнейших
исследований, направленных на изучение причин
развития заболеваний органов дыхания,
совершенствование существующих и разработку
новых методов диагностики при сочетанном
течении заболеваний.
Цель исследования: анализ эндоскопических
признаков патологии пищеварительного тракта у
детей при коморбидном состоянии – ГЭРБ и
заболевания дыхательной системы с
бронхообструктивным синдромом.
Материалы и методы исследования
Обследование и лечение больных проводилось
в педиатрических клиниках Университетской
клинической больницы № 1 им. С.Р. Миротворцева
Саратовского ГМУ им. В.И. Разумовского.
Проведено анкетирование 180 детей в возрасте
6–16 лет с патологией дыхания,
сопровождавшейся обструктивным синдромом,
среди них выявлены дети с симптомами,
позволившими предположить у них наличие и ГЭРБ
(первый этап). На втором этапе в результате
углубленного гастроэнтерологического
обследования выделено 114 больных с сочетанным
течением заболеваний органов дыхания с БОС и
ГЭРБ и сформированы группы, представленные в
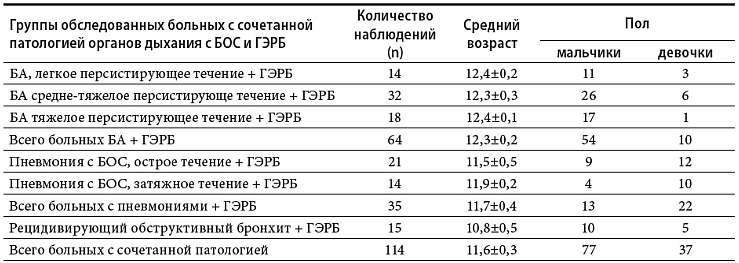
таблице 1.
сочетанным течением патологии органов
дыхания с бронхообструктивным синдромом и
ГЭРБ
Основная программа исследования пациентов с
данной коморбидной патологией включала:
общеклинические методы (изучение анамнеза
жизни и заболевания по форме 112/у,
анкетирование больных, анализ амбулаторных
карт наблюдения аллергологического центра г.
Саратова, объективное обследование). Группы
сравнения составили 93 человека: 29 больных с
изолированным течением ГЭРБ, 36 детей с
изолированным течением бронхиальной астмы (БА)
и 28 практически здоровых лиц (группа
контроля).
Инструментальное обследование пациентов с
бронхообструктивным синдромом включало
проведение рентгенографии органов грудной
клетки в 2-х проекциях; исследование функции
внешнего дыхания (спирометрия).
Углубленное обследование органов
пищеварения включало проведение:
- ультразвукового исследования органов
пищеварения с целью исключения/уточнения
патологии билиарного тракта, желчного
пузыря, поджелудочной железы (сканер
ультразвуковой диагностический “Aloka ССD
1700” с линейным датчиком с частотой
колебаний 5 МГЦ, Япония); - суточной внутрипищеводной рН-метрии
(«Гастроскан-24», «Исток-Система», г.
Фрязино); - эзофагофиброгастродуоденоскопии (ЭФГДС)
с прицельной биопсией слизистой оболочки
нижней трети пищевода (область кардиального
жома) и слизистой антрального отдела
препилорической части желудка (гастрофиброскоп
GIF–XT30, “Olympus Optical Co. Ltd”,
Япония); - рентгеноскопического исследования
органов пищеварения с сульфатно-бариевой
взвесью (выполнено четверым пациентам в
связи с отказом от ЭФГДС); - полипозиционного рентгенологического
исследования пищевода с сульфатно-бариевой
взвесью в положении Транделенбурга при
подозрении на грыжу пищеводного отверстия
диафрагмы.
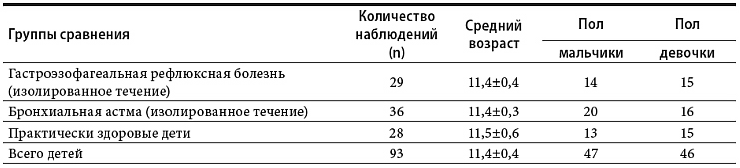
Группы сравнения были представлены 93
пациентами (табл. 2), средний возраст которых
составил 11,4 ± 0,4.
Критериями включения больных в группу
сравнения с изолированным течением ГЭРБ стало
наличие клинических симптомов данного
заболевания и эндоскопическая картина ГЭРБ.
Изолированное течение ГЭРБ 1 степени
практически в равной мере выявлялось у
мальчиков – 14 человек (48,3%) и девочек – 15
детей (51,7%). Продолжительность течения ГЭРБ
в среднем составляла от 6 месяцев до 2-х лет.
Пациентов с изолированной ГЭРБ 1 степени
беспокоили боли в эпигастрии (89,7%), тошнота
(62,0%), отрыжка воздухом (34,5%), изжога
(31,0%), рвота возникала у 13,8% пациентов.
Болезненность при пальпации в области
эпигастрия отмечали большинство обследованных
(82,7%).
группам сравнения
По данным суточной внутриполостной
рН-метрии диагностированы преимущественно
патологические кислые рефлюксы. Эндоскопически
картина слизистой оболочки пищевода
соответствовала эндоскопически-позитивному
варианту неэрозивной ГЭРБ 1 степени у 65,5%
детей и подростков, у 34,5% определялась
эндоскопически-негативная картина ГЭРБ.
Критерии включения в группу сравнения
пациентов с изолированным течением БА: наличие
типичной картины БА, с типичными приступами
удушья, экспираторной одышки и/или приступами
сухого, навязчивого кашля. Средний возраст
больных с изолированным течением БА –
11,4±0,3; мальчиков – 20 чел. (55,5%), девочек
– 16 чел. (44,5%). Диагноз «Бронхиальная
астма» устанавливался в соответствии с
рекомендациями Глобальной стратегии лечения и
профилактики бронхиальной астмы GINA (2021) и
Национальной программы «Бронхиальная астма у
детей» [29].
Группа здоровых детей – 28 человек (средний
возраст 11,5 ± 0,6). У детей этой группы
отсутствовали жалобы и объективные признаки
соматической патологии (ГЭРБ,
бронхообструктивный синдром).
Основная программа исследования пациентов с
коморбидной патологией (заболеваний органов
дыхания с БОС и ГЭРБ) включала изучение
анамнеза жизни и заболевания, сбор и оценку
генеалогического анамнеза, методы объективного
обследования; изучение, оценку антенатальных
факторов риска и особенностей перинатального
периода жизни пациентов в основной группе и в
группах сравнения. От родителей всех детей,
участвующих в исследовании, было получено
информированное согласие в соответствии с
Хельсинкской декларацией Всемирной медицинской
ассоциации 1964 г. и её последующими
редакциями, распоряжением ВАК «О порядке
проведения биомедицинских исследований у
человека», опубликованным в Бюллетене ВАК
(2002, № 3) и положением о Межвузовском
комитете по этике при Ассоциации медицинских и
фармацевтических вузов от 22.02.2006 г.
[30,31]. Анкетный опрос осуществлялся по
специально составленной форме, заполняемой
ребенком (родителями), с оценкой состояния
ребенка, динамикой и качеством симптомов
заболевания (одышка, кашель, свистящие хрипы,
качество сна и др.), наличием сопутствующей
патологии (в т.ч. первые симптомы ГЭРБ),
частоты применения и эффективности
лекарственных средств. В ряде случаев,
индивидуально, при затяжном воспалительном
процессе в бронхолегочной системе и упорном
рецидивировании бронхообструктивного синдрома
(с целью исключения легочной формы
муковисцидоза), проводился анализ потовой
жидкости на содержание хлоридов (39% больных).
С целью верификации ГЭРБ, а также выявления
воспалительных изменений органов пищеварения
проведены:
- эзофагофиброгастродуоденоскопия (ЭФГДС)
с прицельной биопсией слизистой оболочки
нижней трети пищевода (гастрофиброскоп GIF–XT
30, “Olympus Optical Co. Ltd” (Япония) –
87,7% больным. Дети и подростки основной
группы обследовались в период стихающего
обострения БА. В связи с негативным
поведением 4 больным проведено
рентгеноскопическое исследование органов
пищеварения с сульфатно-бариевой взвесью; - полипозиционное рентгенологическое
исследование пищевода с сульфатно-бариевой
взвесью в положении Транделенбурга – 8,7%
детей при подозрении на грыжу пищевода; - суточная внутрипищеводная рН-метрия
(«Гастроскан-24», «Исток-Система», Фрязино)
– 74,5%; - ультразвуковое исследование органов
пищеварения для исключения/ уточнения
патологии билиарного тракта, желчного
пузыря, поджелудочной железы (сканер
ультразвуковой диагностический “Aloka ССD
1700” с линейным датчиком с частотой
колебаний 5 МГЦ, Япония) – 100% больным.
При длительности течения ГЭРБ свыше одного
года в сочетании с повторными и/или затяжными
пневмониями проводилась консультация детского
хирурга, определялись показания к оперативному
лечению. Диагноз ГЭРБ ставился на основании
отечественных клинических рекомендаций «Гастроэзофагеальная
рефлюксная болезнь у детей», 2021, также
учитывались рекомендации Монреальского
консенсуса [32].
Оценка функции внешнего дыхания
(Спирометрия) проводилась на спирографе
“Master-ScreenRPneumo” (версия
6.0.R., 2010) – с определением объемных и
скоростных показателей: – жизненная емкость
легких (ЖЕЛ), – форсированная жизненная
емкость легких (ФЖЕЛ), – объем форсированного
выдоха за 1 секунду (ОФВ1), – максимальная
объемная скорость выдоха на уровне 25% ФЖЕЛ
(МОС25), – максимальная объемная скорость
выдоха на уровне 50% ФЖЕЛ (МОС50), –
максимальная объемная скорость выдоха на
уровне 75% ФЖЕЛ (МОС75). Полученные результаты
выражались в процентах по отношению к
расчетной должной величине (автоматический
расчет на спирографе).
Статистическая и математическая обработка
полученных результатов исследования
производилась с использованием прикладных
программ статистической обработки данных
Statgraрhica 3.0 (Manugraphica Inc. U.S.A.,
1998) и Microsoft @ Excel for WINDOWS 50 (Microsoft
Сorp.). При обработке полученных данных
проводился расчет средней М и m стандартной
ошибки среднего значения. Перед проведением
статистического исследования проводилась
проверка нормального характера распределения
признака. В зависимости от характера
распределения использовались как
параметрические, так и непараметрические
методы статистического анализа.
Результаты и их обсуждение
При сопоставлении формы патологии органов
дыхания, протекающей с бронхообструктивным
синдромом, с вариантами течения ГЭРБ
установлено, что наряду с
эндоскопически-позитивным вариантом ГЭРБ 1
степени (гиперемия, отек слизистой оболочки
нижней трети пищевода), у детей отмечалась и
эндоскопически-негативная форма рефлюксной
болезни (отсутствие эндоскопических признаков
ГЭРБ при наличии клинической картины
заболевания, верифицированной при рН-метрии).
Варианты ГЭРБ при сочетании с заболеваниями
органов дыхания с БОС, представлены в табл. 3.
эндоскопических форм ГЭРБ и виды рефлюксов у
детей с патологией органов дыхания с
бронхообструктивным синдромом
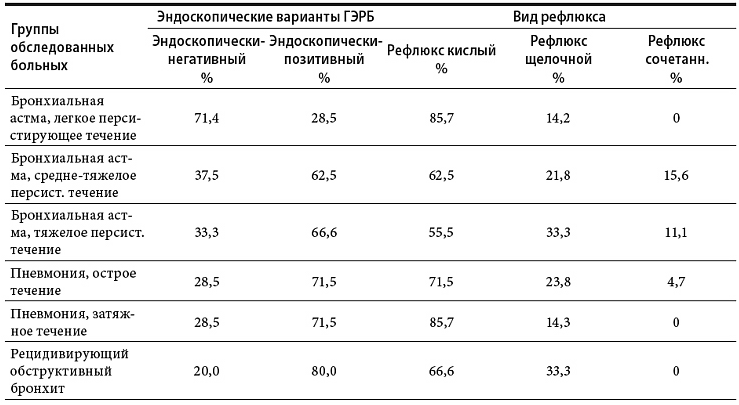
Анализ полученных данных показал, что при
легком персистирующем течении БА
эндоскопически-негативный вариант преобладал
над эндоскопически-позитивным вариантом ГЭРБ.
Эндоскопически-негативный вариант рефлюксной
болезни выявлен у 71,4% детей, а
эндоскопически-позитивный – у 28,5% больных
этой группы. Также отмечено преобладание
рефлюксов кислого характера над щелочными
рефлюксами (85,7% и 14,2% соответственно).
При средне-тяжелом персистирующем течении БА
выявлены больные как с
эндоскопически-позитивной, так и с
эндоскопически-негативной формой ГЭРБ, причем
эндоскопически-позитивный вариант ГЭРБ
несколько преобладал – диагностирован у 20
больных (62,5%), эндоскопически-негативный
вариант ГЭРБ выявлен у 12 пациентов (37,5%).
Количество кислых рефлюксов преобладало над
щелочными, 62,5% – кислых, 21,8% – рефлюксов
щелочного характера. Интересной особенностью
можно назвать наличие при средне – тяжелом
персистирующем течении БА сочетанных
(кислотно-щелочных) рефлюксов – они
диагностированы у 5 пациентов (15,6% случаев).
У детей с тяжелым течением БА наблюдалось
значительное преобладание
эндоскопически-позитивной формы ГЭРБ: данная
форма ГЭРБ встречалась в 66,6% случаев (12
чел.). Реже у этих пациентов диагностировался
эндоскопически-негативный вариант ГЭРБ – 6
детей (33,3%), т. е. у каждого четвертого
больного. В этой группе выявлено наличие трех
видов рефлюксов – кислого в 55,5% случаев,
щелочного – в 33,3%, сочетанного (смешанного)
– в 11,1% случаев, т.о., преобладали рефлюксы
кислого характера.
Обобщая сведения, касающиеся течения БА в
сочетании с ГЭРБ, можно говорить о
превалировании в этой группе рефлюксов кислого
характера, а также значительном количестве
сочетанных рефлюксов – они диагностированы у
17 человек (26,7%). При этом с возрастанием
степени тяжести БА прослеживалась тенденция
течения ГЭРБ в более тяжелом эндоскопически –
позитивном варианте, что, вероятно, могло быть
обусловлено наличием механизма так называемого
взаимоотягощения, когда наличие одного
заболевания способствовало более тяжелым
клиническим проявлениям сопутствующей
патологии.
Данные, полученные при обследовании больных с
острым течением пневмонии с БОС, указывают на
высокие показатели распространенности ГЭРБ и у
этой группы детей. Эндоскопически-позитивная
форма ГЭРБ диагностирована в 15 случаях
(71,5%), а эндоскопически-негативный вариант
рефлюксной болезни — в 6 случаях (28,5%).
Преобладали рефлюксы кислого характера – 15
человек (71,4%), щелочные рефлюксы выявлены у
5 пациентов (23,8%), и лишь в 4,7% случаев
диагностирован рефлюкс сочетанного характера.
При затяжном течении пневмонии с БОС отмечено
наличие двух форм ГЭРБ –
эндоскопически-позитивный вариант у 10 больных
(71,5%), эндоскопически-негативный – у 4
пациентов (28,5%). В этой группе чаще
встречался кислый рефлюкс – 12 случаев
(85,7%), рефлюкс щелочного характера был
выявлен в 14,3%, сочетанные рефлюксы не
диагностированы.
Таким образом, при остром и затяжном течении
пневмонии с БОС у 25 человек (71,4%) выявлен
эндоскопически-позитивный вариант ГЭРБ 1
степени, у 10 человек (28,6%) отмечалась
эндоскопически-негативная форма рефлюксной
болезни. Выявлено преобладание рефлюксов
кислого характера – 27 человек, щелочные
рефлюксы отмечены у 7 человек, сочетанный
рефлюкс установлен у 1 ребенка при остром
течении пневмонии.
При сочетанном течении рецидивирующего
обструктивного бронхита с ГЭРБ у 12 пациентов
(80,0%) выявлена эндоскопически-позитивная
форма ГЭРБ 1 степени, у 3 больных (20,0%)
диагностирован эндоскопически-негативный
вариант этой патологии. Кислые рефлюксы
встречались в 2 раза чаще щелочных: рефлюксы
кислого характера выявлены у 10 человек
(66,6%), тогда как рефлюксы щелочного
характера – у 5 обследованных (33,3%).
Сочетанные рефлюксы в этой группе не
зарегистрированы.
Суммируя полученные данные, можно заключить,
что по мере увеличения степени тяжести БА у
детей возрастала распространенность
эндоскопически-позитивного варианта ГЭРБ 1
степени. При легком персистирующем течении БА
эта форма ГЭРБ выявлялась у 28,5% больных, при
средне-тяжелом персистирующем течении БА
количество пациентов увеличилось в 2,2 раза
(62,5%), а при тяжелом течении – в 2,3 раза
(66,6%).
Высокие показатели эндоскопически-позитивного
варианта ГЭРБ 1 степени диагностированы у
пациентов с острым и затяжным течением
пневмонии – 71,5% детей, а также при
рецидивирующем обструктивном бронхите – у 80%
детей.
Эндоскопически-негативная форма рефлюксной
болезни была выявлена у третьей части
пациентов со средне-тяжелым персистирующем и
тяжелым течением БА (37,5% и 33,3%
соответственно).
Этот эндоскопический вариант ГЭРБ был
диагностирован у 28,5% пациентов с острым и
затяжным течением пневмонии, у 20% больных с
рецидивирующим обструктивным бронхитом. Более
того, по мере увеличения степени тяжести БА, у
пациентов выявлялись рефлюксы сочетанного
характера.
Для изучения морфологических особенностей
слизистой оболочки пищевода при сочетанной
патологии органов дыхания с БОС и ГЭРБ 55
пациентам (с БА – 20 человек, с острым
течением пневмонии – 10 человек, затяжным
течением пневмонии – 15 человек, с
рецидивирующим обструктивным бронхитом – 10
больных) выполнено исследование биоптатов
слизистой оболочки пищевода на 1 см выше Z–линии;
одновременно проведена биопсия слизистой
оболочки антрального отдела препилорической
части желудка.
Биоптаты фиксировали в 10% растворе формалина
в течение 24 часов с последующим промыванием
проточной водой. Депарафинированные срезы
толщиной 5–7 мкм окрашивали
гемотоксилинэозином, по методу Ван Гизона,
PAS-реакция.
При гистологическом исследовании слизистой
пищевода оценивались: характер эпителия
(плоский, цилиндрический), наличие отека и
полнокровия, вид и степень клеточной
инфильтрации, выраженность десквамации,
глубина дистрофических изменений эпителия,
наличие общих признаков атрофии, метаплазии.
Изучение вида и степени клеточной
инфильтрации, метаплазии, атрофии оценивали
как незначительное, умеренное, выраженное. На
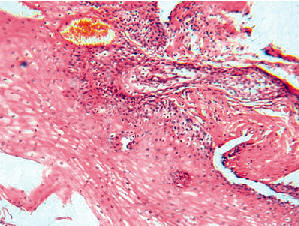
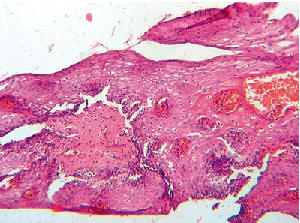
основании данных общеморфологического
исследования биоптатов, независимо от возраста
и вида бронхо-легочной патологии, выявлено два
варианта воспаления, встречающихся чаще других
– с преобладанием изменений дистрофического
характера (рисунок 1 и последующие) и с
преобладанием собственно воспаления (рис. 2),
что в большей степени зависело от длительности
заболевания.
|
|
|
Рисунок 1. Хронический эзофагит с дистрофией клеток поверхностного слоя эпителия и признаками ороговения. Очаговая дисплозия базального слоя и очаговая лимфо-гистиоцитарная инфильтрация. Окраска: гематоксилин и эозин. Ув.200 |
Рисунок 2. Хронический эзофагит с гиперплазией и очаговой дисплозией базального слоя. Резко выраженное полнокровие сосудов. Окраска: гематоксилин и эозин. Ув.200 |
У пациентов, страдавших как БА, так и
пневмонией с БОС, морфологические изменения со
стороны слизистой пищевода соответствовали
катаральному характеру воспаления. Слизистая
пищевода была гиперемирована (у 78,2% детей),
отечна (у 70,9% больных), отмечался стаз,
расширение и полнокровие венул, гиперплазия
базальной зоны (в 9% случаев), умеренная
лимфоплазмоцитарная и полиморфнонуклеарная
инфильтрация. Клеточные инфильтраты
располагались преимущественно в области
сосочков. Лимфоплазмоцитарная и эозинофильная
инфильтрация наблюдались преимущественно при
бронхиальной астме.
Склеротические изменения подслизистого слоя
выявлялись в обеих группах обследованных и
зависели от длительности анамнеза и возраста
пациентов.
В дистальном отделе пищевода был выявлен
многослойный плоский эпителий с выраженным
процессом дистрофии в основном поверхностном
эпителии пищевода.
Эрозивных проявлений, дистрофии глубоких слоев
эпителия, атрофических изменений и метаплазии
нами отмечено не было.
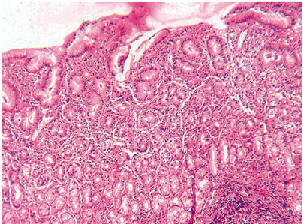
Выявленные морфологические изменения в
слизистой оболочке пищевода сочетались с
гастритом, который расценивался как
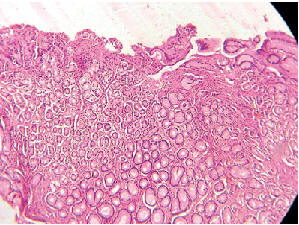
поверхностный – 92,7% (рис. 3, рис. 4), а в
единичных случаях – как гастрит с поражением
желез без атрофии (7,3%).
|
|
|
Рисунок 3. Хронический поверхностный гастрит с умеренно выраженным склерозом стромы и лимфо-гистиоцитарной инфильтрацией стромы. Признаки начинающейся атрофии желез. Окраска: гематоксилин и эозин. Ув.200 |
Рисунок 4. Хронический атрофический гастрит со склерозом стромы и умеренной лимфо-гистиоцитарной инфильтрацией. Окраска: гематоксилин и эозин. Ув.200 |
Активность гастрита по данным морфологического
исследования как в группе с пневмониями, так и
в группе больных с БА, не имела существенных
различий.
Таким образом, гистоморфологические изменения
слизистой оболочки пищевода у пациентов с БА и
пневмонией, сопровождавшихся БОС, носили
катаральный характер воспаления, которые
характеризовались отеком, полнокровием,
умеренной десквамацией эпителия,
дистрофическими изменениями,
лимфоплазмоцитарной и полинуклеарной
инфильтрацией.
Данные морфологического исследования слизистой
антрального отдела желудка у этих пациентов
свидетельствовали о поверхностной форме
гастрита без поражения желез.
Учитывая жалобы, анамнез заболевания,
параклинические данные настоящего
обследования, было отмечено, что данная
сочетанная патология, в ряде случаев,
формировалась на фоне воспалительных
заболеваний пищеварительного тракта:
хронического гастрита, хронического
гастродуоденита, хронического дуоденита, а
также язвенной болезни 12-перстной кишки
(табл. 4).
Частота встречаемости воспалительных
заболеваний желудочно-кишечного тракта у
детей с сочетанной патологией органов
дыхания с бронхообструктивным синдромом и
ГЭРБ
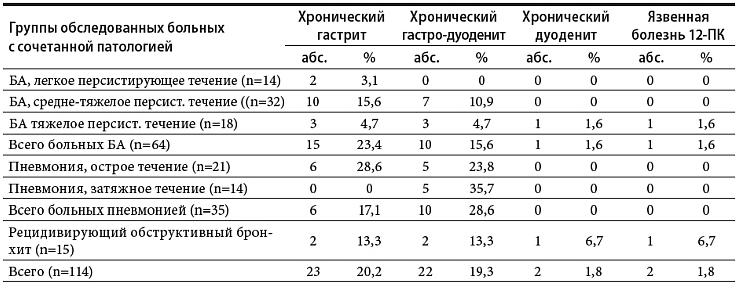
Анализируя полученные данные, следует
отметить, что у пациентов с БА сочетание ГЭРБ
с хроническими гастритами выявлено в 23,4%
случаев (15 человек), с хроническими
гастродуоденитами – в 15,6% случаев (10
человек). У 1 (6,4%) пациента вовлеченной в
воспалительный процесс оказалась лишь
слизистая оболочка 12-перстной кишки (явления
дуоденита), также у одного больного (6,4%)
диагностирована язвенная болезнь 12-перстной
кишки.
При легком персистирующем течении БА в
сочетании с ГЭРБ у двоих пациентов (3,1%)
воспалительные изменения пищеварительного
тракта были представлены только хроническим
гастритом. При сочетанном течении ГЭРБ со
средне-тяжелой персистирующей БА количество
больных с хроническими гастритами увеличилось
в 5 раз – воспалительные изменения слизистой
оболочки желудка диагностированы у 10 больных
(15,6%), а у 7 пациентов (10,9%) отмечались
явления хронического гастродуоденита. У детей
с тяжелым течением БА и ГЭРБ, помимо 3-х
случаев хронического гастрита (4,7%) и 3-х
случаев хронического гастродуоденита (4,7%),
выявлены признаки хронического дуоденита
–1,6%, и язвенной болезни 12-перстной кишки –
1,6% случаев.
В группе больных с острым течением пневмонии с
БОС и рефлюксной болезнью выявлено 6 пациентов
(28,6%) с хроническими гастритами и 5 больных
(23,8%) – с хроническими гастродуоденитами.
При затяжной пневмонии с БОС и ГЭРБ у 5
пациентов (35,7%) был установлен диагноз
хронического гастродуоденита.
Не стало исключением сочетанное течение ГЭРБ с
воспалительными заболеваниями органов
пищеварения и у детей с рецидивирующими
обструктивными бронхитами: отмечено по 2
случая хронического гастрита и хронического
гастродуоденита (13,3%) и по 1 случаю
хронического дуоденита и язвенной болезни
12-перстной кишки (6,7%).
Анализ представленных результатов
демонстрирует преобладание воспалительной
патологии органов пищеварения у больных с
сочетанным течением БА и ГЭРБ. Так у 15 детей
отмечены явления хронического гастрита, у 10
человек – хронического гастродуоденита, у
одного ребенка – хронического дуоденита.
При остром и затяжном течении пневмонии с БОС,
сочетанных с ГЭРБ, также выявлены случаи
воспалительных заболеваний пищеварительного
тракта: у 6 детей – с хроническими гастритами,
у 10 человек – с хроническими
гастродуоденитами.
Обследование больных с сочетанным течением
рецидивирующего обструктивного бронхита и ГЭРБ
выявило наличие не только воспалительных
изменений со стороны ЖКТ (2 случая
хронического гастрита, 2 случая хронического
гастродуоденита, 1 – хронического дуоденита),
но и язвенной болезни 12-перстной кишки у 1
ребенка.
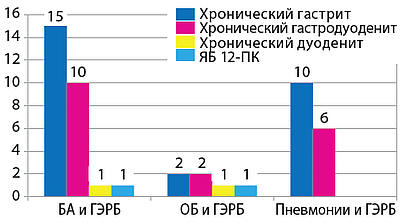
Рисунок 5. Структура воспалительных
заболеваний органов пищеварения у детей при
сочетанном течении заболеваний органов дыхания
с бронхообструктивным синдромом и ГЭРБ.
Наглядно структуру воспалительных
заболеваний желудочно-кишечного тракта у детей
с сочетанной патологией органов дыхания с БОС
и ГЭРБ иллюстрирует рис. 5.
Благодаря своевременной диагностике и
применению комплексного подхода к обследованию
пациентов с сочетанной патологией стало
возможным установление правильных диагнозов
заболеваний бронхо-легочной системы, изучение
степени морфологических изменений слизистой
оболочки пищевода и желудка, детализирование
вариантов ГЭРБ и выявление сопутствующих
воспалительных заболеваний ЖКТ.
Подводя итоги, следует отметить, что ГЭРБ на
фоне тяжелого течения БА в 3,4 раза чаще
выявлялась у мальчиков. При рецидивирующем
обструктивном бронхите ГЭРБ также чаще
развивалась у пациентов мужского пола, в то
время как при затяжном течении пневмонии с
БОС, развитие ГЭРБ в 1,9 раза чаще отмечалось
у девочек. В возрастном аспекте ГЭРБ при
бронхиальной астме чаще диагностировалась у
обследованных пациентов 12–14 лет, в связи с
чем больных этого возраста необходимо
рассматривать как группу риска по развитию
сочетанной патологии органов дыхания с БОС и
ГЭРБ.
При увеличении степени тяжести заболеваний
органов дыхания с БОС возрастало количество
детей с эндоскопически – позитивной формой
ГЭРБ 1 степени. С увеличением степени тяжести
БА увеличивалось и количество смешанных
рефлюксов. Наибольшее количество
кислотно-щелочных рефлюксов диагностировано
при БА.
Гастроэзофагеальная рефлюксная болезнь в
сочетании с заболеваниями бронхо–легочной
системы с БОС у детей в 41,2% случаев (47
чел.) развивалась на фоне воспалительных
заболеваний пищеварительного тракта –
хронических гастритов, гастродуоденитов,
дуоденитов, а в 1,8% случаев (2 чел.) – и на
фоне язвенной болезни 12-перстной кишки.
На основании изложенного выше следует
отметить, что только в результате
всестороннего, своевременного, углубленного
комплексного обследования пациентов с
применением современных диагностических
методов (суточной внутрипищеводной рН-метрии,
ЭФГДС, спирометрии) и адекватной оценки
показателей, можно выявить коморбидность
заболеваний органов дыхания с БОС и ГЭРБ уже в
детском возрасте. Коморбидность оказывает
огромное влияние на клинические проявления
заболевания – это состояние, влекущее за собой
изменение подходов к терапии сложного
пациента.
Заключение
Выявление коморбидной патологии в детском
возрасте можно назвать приоритетной задачей
здравоохранения. Полученные данные ставят
новые проблемы в диагностике коморбидных
состояний, требуют формирования
персонифицированной терапии при ГЭРБ,
воспалительных заболеваниях органов дыхания с
БОС, бронхиальной астме, а также при их
сочетании. Влияние коморбидной патологии на
клинические проявления, диагностику, прогноз
заболеваний органов дыхания и пищеварения
многогранно и неординарно. Коморбидная
патология утяжеляет течение основного
заболевания, приводит к изменению привычной
клинической картины и динамики основного
заболевания, ограничивает или затрудняет
лечебно-диагностический процесс, нередко
становясь причиной развития смертельных
осложнений и фактором риска летального исхода
[33].
С экономической точки зрения коморбидная
патология увеличивает затраты на диагностику и
лечение заболеваний, удлиняет количество
койко-дней в стационаре. Также необходимо
помнить, что коморбидность приводит к
полипрагмазии (одновременному назначению
большого количества лекарственных препаратов),
что делает невозможным контроль над
эффективностью терапии, увеличивает
материальные затраты пациентов, а поэтому
снижает их приверженность к лечению. Кроме
того, полипрагмазия может создавать
вероятность развития местных и системных
побочных эффектов медикаментов. Эти побочные
эффекты не всегда принимаются врачами во
внимание, поскольку расцениваются как
проявление одного из факторов коморбидности и
влекут за собой назначение еще большего
количества лекарственных препаратов, замыкая
еще один порочный круг. К сожалению,
полипрагмазия уже пришла и в педиатрию, а
предотвратить ее сможет лишь нацеленность на
выявление и лечение первопричины цепочки
сформировавшихся болезней.
Все вышеизложенное создает картину
своеобразного «порочного круга» взаимного
влияния этих заболеваний при их
сосуществовании, или коморбидности.
Литература | References
- Kotova E.G., Kobyakova O.S., Starodubov
V.I., Alexandrova G.A., et al. The incidence
of the child population of Russia (0–14
years) in 2020 with a diagnosis established
for the first time in life: statistical
materials. 2021. 147 P. (in Russ.) doi:
10.21045/978–25–94116–042–6
Заболеваемость детского населения России
(0–14 лет) в 2020 году с диагнозом,
установленным впервые в жизни:
статистические материалы / Е.Г. Котова, О.С.
Кобякова, В.И. Стародубов, Г.А. Александрова
и др.-М.: ЦНИИОИЗ Минздрава России, 2021. –
147 с. doi: 10.21045/978–25–94116–042–6 - Shcherbakov P.L., Lobanov Yu. F.
Pediatric gastroenterology – present and
future. Experimental and Clinical
Gastroenterology, 2011;1: 3–8. (in Russ)
Щербаков П.Л., Лобанов Ю.Ф. Детская
гастроэнтерология- настоящее и будущее.
Экспериментальная и клиническая
гастроэнтерология, 2011; 1:3–8. - Baranov A.A. Federal clinical guidelines
for the diagnosis and treatment of
gastroesophageal reflux disease in children.
2015. 27 P. (in Russ.)
Баранов А.А. Федеральные клинические
рекомендации по диагностике и лечению
гастроэзофагеальной рефлюксной болезни у
детей / А.А. Баранов, 2015. – 27 c. - Privorotsky V.F., Luppova N.E.
Gastroesophageal reflux disease in children.
In: Children’s gastroenterology, a practical
guide. Ed. I.Yu Melnikova. Moscow.
GEOTAR-Media Publ., 2018. 184–203. (in Russ.)
Приворотский В.Ф., Луппова Н.Е.
Гастроэзофагеальная рефлюксная болезнь у
детей. В кн.: Детская гастроэнтерология,
практическое руководство. Под ред. И.Ю
Мельниковой. – М.: ГЭОТАР-Медиа, 2018. – C.
184–203. - Russian Union of Pediatricians. Federal
clinical guidelines for the diagnosis and
treatment of gastroesophageal reflux disease
in children. 2016. (in Russ.)
Федеральные клинические рекомендации по
диагностике и лечению гастроэзофагеальной
рефлюксной болезни у детей / Союз педиатров
России, 2016. - Borodin D.S., Nikolskaya K.A., Bakulin
I.G. et al. Medical decision support system.
Gastroenterology: Clinical treatment
protocols. Moscow. GBU «NIIOZMM DZM» Publ.,
2021. pp. 25–41. (in Russ.)
Система поддержки принятия врачебных
решений. Гастроэнтерология: Клинические
протоколы лечения / Составители: Д.С.
Бородин, К.А. Никольская, И.Г. Бакулин и др.
– М.: ГБУ «НИИОЗММ ДЗМ», 2021. С. 25–41. - Tarasova G.N., Smirnova E.A.
Pathogenetic features of damage to the
mucous membrane of the esophagus in
gastroesophageal reflux disease. Consilium
Medicum, 2017; 8. Gastroenterology (19):
7–12. (in Russ.)
Тарасова Г.Н., Смирнова Е.А.
Патогенетические особенности повреждения
слизистой оболочки пищевода при
гастроэзофагеальной рефлюксной болезни.
Consilium Medicum, 2017; 8;
Гастроэнтерология (19):7–12. - Kornyak B.S., Kubyshkin V.A., Chernova
T.G., Azimov R.Kh. Bronchopulmonary and
laryngeal symptoms of gastroesophageal refl
ux disease: diagnosis and treatment.
Experimental and clinical gastroenterology,
2003; 1: 33–37. (in Russ.)
Корняк Б.С., Кубышкин В.А., Чернова Т.Г.,
Азимов Р.Х. Бронхопульмональные и
ларингеальные симптомы гастроэзофагеальной
рефлюксной болезни: диагностика и лечение.
Экспериментальная и клиническая
гастроэнтерология, 2003; 1: 33–37. - Zvyagintseva T.D., Chernobay A.I.
“Gastroesophageal reflux disease in
combination with bronchial asthma: common
pathogenesis and treatment tactics”. Kharkov.
– Newspaper “Medicine and Pharmacy News”
Gastroenterology (323), 2010 (thematic issue).
(in Russ.)
Звягинцева Т.Д, Чернобай А.И. «Гастроэзофагеальная
рефлюксная болезнь в сочетании с
бронхиальной астмой: общность патогенеза и
тактика лечения». Харьков. – Газета «Новости
медицины и фармации» Гастроэнтерология
(323), 2010 (тематический номер). - Asmanov A.I., Khanakaeva Z.K., Pivneva
N.D. Extraesophageal manifestations of
gastroesophageal reflux disease in the
practice of a pediatric
otorhinolaryngologist. Russian Bulletin of
Perinatology and Pediatrics, 2017; 62(6):
87–91. (in Russ.)
Асманов А.И., Ханакаева З.К., Пивнева Н.Д.
Внепищеводные проявления гастроэзофагеальной
рефлюксной болезни в практике детского
оториноларинголога. Российский вестник
перинатологии и педиатрии, 2017; 62 (6):
87–91. - Belyalov F.I. Treatment of internal
diseases in conditions of comorbidity.
Moscow. GEOTAR – Media Publ., 2019. 305 p. (in
Russ.)
Белялов Ф.И. Лечение внутренних болезней в
условиях коморбидности. – Москва: ГЕОТАР –
Медиа, 2019. 305 с. - Apenchenko Yu.S., Gnusaev S.F., Rozov
D.N., et al. The course of bronchial asthma
in combination with gastroesophageal reflux
disease in children. Bulletin of new medical
technologies, 2018; 25(3): 7–14. (in Russ.)
doi: 10.24411/1609–2163–2018–16057
Апенченко Ю.С., Гнусаев С.Ф., Розов Д.Н., и
др. Течение бронхиальной астмы в сочетании с
гастроэзофагеальной рефлюксной болезнью у
детей. Вестник новых медицинских технологий,
2018; 25(3): 7–14. (in Russ.) doi:
10.24411/1609–2163–2018–16057 - Kosarev S.S., Lopakova N.N.
Extraesophageal manifestations of
gastroesophageal reflux disease in children.
Modern problems of science and education.
2019; 5: 117. (in Russ.)
Косарев С.С., Лопакова Н.Н. Внепищеводные
проявления гастроэзофагеальной рефлюксной
болезни у детей. Современные проблемы науки
и образования. 2019; 5:117. - Alagha K., Bourdin A., Vernisse C.,
Garulli C., Tummino C., Charriot J., Gras D.
Goblet Cell Hyperplasia as a feature of
neutrophilic asthma. Clinical & Experimental
Allergу, 2019; 49 (6): 781–788. doi:
10.1111/cea.13359 - Chang A., Oppenheimer J., Kahrilas P.,
et al. On behalf of the CHEST Expert Cough
Panel. Chronic cough and gastroesophageal
reflux in children – CHEST Guideline and
Expert Panel Report, CHEST. 2019, pp.
131–140. - Abdallah A., El-Desoky T., Fathi K.,
Fawzi Elkashef W., Zaki A. Evaluation of
gastro-oesophageal reflux disease in wheezy
infants using 24-h oesophageal combined
impedance and pH monitoring. Arab J.
Gastroenterol. Pan-Arab Association of
Gastroenterology, 2017; 18 (2): 68–73. doi:
10. 1016/| j.ajg.2017.05.009 - Barfield E., Parker M.W. Management of
Pediatric Gastroesophageal Reflux Disease.
JAMA Pediatrics., 2019; 173 (5): 485–486.
doi: 10.1001/jamapediatrics. 2019.0170 - De Benedictis F.M., Bush A. Respiratory
manifestations of gastro-oesophageal reflux
in children. Arch. Dis. Child. 2018; 103
(3): 292–296. doi:
10.1136/archdischild-2017–312890 - Hu X., Lee J.S., Pianosi P.T., Ryu J.H.
Aspiration-related pulmonary syndromes.
Chest., 2015; 147 (3): 815–823. - Kolbe J. Bronchiectasis and
gastro-oesophageal reflux; Some progress but
still a long way to go. Respirology. 2015;
20 (5): 691–692. - Quitadamo P., Di Nardo G., Miele E., et
al. Gastroesophageal reflux in young
children and adolescents: Is there a
relation between symptom severity and
esophageal histological grade? J. Pediatr.
Gastroenterol. Nutr., 2015; 60 (3): 318–321. - Slater B., Rothenberg S.
Gastroesophageal reflux. Seminars in
Pediatric Surgery, 2017; 26 (2): 56–60. - Global Initiative for Asthma. Global
Strategy for Asthma Management and
Prevention, 2021. - Vishneva E.A., Namazova-Baranova L.S.,
Alekseeva A.A., et al. Actual management of
children with bronchial asthma. Pediatric
pharmacology, 2017; 14(6):443–458. (in Russ.)
doi: 10.15690/pf.v14i6/1828
Вишнева Е.А., Намазова-Баранова Л.С.,
Алексеева А.А. соавт. Актуальная тактика
ведения детей с бронхиальной астмой.
Педиатрическая фармакология, 2017;
14(6):443–458; doi: 10.15690/pf.v14i6/1828 - Bystritskaya E.V., Bilichenko T.N.
Morbidity, disability and mortality from
respiratory diseases in the Russian
Federation (2015–2019). Pulmonology,
2021;31(5): 551–562. (in Russ.) doi: 10.
18093/0869–0189–2021–31–5–551–556
Быстрицкая Е.В., Биличенко Т.Н.
Заболеваемость, инвалидность и смертность от
болезней органов дыхания в Российской
Федерации (2015–2019). Пульмонология,
2021;31(5): 551–562. doi:
10.18093/0869–0189–2021–31–5–551–556. - Zaitseva S.V., Zaitseva O.V., Lokshina
E.E., Zastrozhina A.K., et al. Severe
bronchial asthma in children. Allergology
and Immunology in Pediatrics, 2019; 3 (58):
4–14. (in Russ.)
Зайцева С.В., Зайцева О.В., Локшина Э.Э.,
Застрожина А. К., и др. Тяжeлая бронхиальная
астма у детей. Аллергология и иммунология в
педиатрии, 2019; № 3 (58): 4–14. - Simanenkov V.I., Ilyashevich I.G.,
Konovalova N.V., Tikhonov S. V. Mechanisms
of comorbidity of gastroesophageal reflux
disease and bronchial asthma. Bulletin of
the Russian Military Medical Academy, 2011;
(1): 124–128. (in Russ.)
Симаненков В.И., Ильяшевич И.Г., Коновалова
Н.В., Тихонов С.В. Механизмы коморбидности
гастроэзофагеальной рефлюксной болезни и
бронхиальной астмы. Вестник Российской
Военно-медицинской академии, 2011; №
1:124–128. - Ovsyannikov D.Yu., Eliseeva T.I., Khaled
M., et al. Comorbidity of bronchial asthma
in children: causal, complicated,
unspecified, reverse. Pediatrics, 2021;
100(2):127–137. (in Russ.) doi:
10.24110/0031–403X-2021–100–2–127–137
Овсянников Д.Ю., Елисеева Т.И., Халед М. и
соавт. Коморбидность бронхиальной астмы у
детей: причинная, осложненная, неуточненная,
обратная. Педиатрия, 2021; 100 (2):127–137.
doi: 10.24110/0031–403X-2021–100–2–127–137 - National program “Bronchial asthma in
children. Treatment strategy and prevention”
Moscow, 2017. 160 p. (in Russ.)
Национальная программа «Бронхиальная астма у
детей. Стратегия лечения и профилактика» –
Москва, 2017. – 160 с. - Drogonets Ya., Hollender P. Modern
medicine and law: translation from Slovak.
Moscow. Legal Literature Publ., 1991. 23 P.
(in Russ.)
Дрогонец Я., Холлендер П. Современная
медицина и право: перевод со словацкого. –
Москва: Юридическая литература, 1991. – С.
23. - Bulletin of the highest attestation
commission of the Ministry of Education of
the Russian Federation. 2002; 3:46–48. (in
Russ.)
Бюллетень высшей аттестационной комиссии
Министерства образования Российской
Федерации. 2002; 3:46–48. - Vakil N., van Zanten S. V., Kahrilas P.,
Dent J., Jones R.; the Global Concensus
Group. Montreal definition and
classification of gastroesophageal reflux
disease: a global evidence-based concensus.
Am. Gastroenterol, 2006; 11 (8):1900–1920. - Vertkin A.L. Comorbidity: history,
current presentation, prevention and
treatment. Cardiovascular therapy and
prevention. 2015; 14(2):74–79. (in Russ.)
doi: 10.15829/1728–8800–2015–2–74–79
Вёрткин А.Л. Коморбидность: история,
современное представление, профилактика и
лечение. Кардиоваскулярная терапия и
профилактика. 2015;14(2):74–79. doi:
10.15829/1728–8800–2015–2– 74–79
Статья опубликована на сайте
http://www.gastroscan.ru
материал MedLinks.ru





