Введение
Говоря о многообразии факторов женской инфертильности, стоит отметить значение аспекта несостоятельности ткани слизистой полости матки, что в первую очередь ассоциировано с персистирующим воспалительным процессом [1–3]. Реализация патологического процесса в эндометрии подразумевает формирование основы его структурно-функциональной недостаточности, что проявляется нарушениями субэндометриального кровотока, неполноценной регенерацией ткани, а также неадекватной рецепторной чувствительностью. В настоящее время активно изучаются особенности влияния различных факторов на результативность процесса имплантации [4]. Согласно распространенной на сегодняшний день точке зрения имплантация может быть рассмотрена как процесс, во многом сходный с воспалительным, поскольку в нем принимают активное участие сосудистые и иммунные механизмы. Ряд исследований это подтверждает, демонстрируя, что успех имплантации в том числе определяется балансом между действием провоспалительных и противовоспалительных цитокинов. Кроме того, заслуживает внимания тезис, что одним из ведущих механизмов неудач имплантации и потерь беременности становятся проблемы со стороны прокоагулянтного и антикоагулянтного звеньев гемостаза. Из-за деактивации фибринолиза по причине неадекватной реакции на влияние провоспалительных факторов на фоне микроциркуляторных расстройств, ишемизации эндометрия и прогрессирующего фиброзирования стромы и склерозирования сосудов структурно-функциональные нарушения ткани постепенно усиливаются [2]. По данным зарубежных авторов, при морфологическом исследовании сосудистые изменения в 85,7% случаев ассоциированы с хроническим эндометритом [5].
Тканевой стресс становится логичным результатом волнообразно-прогрессирующего течения заболевания и проявляется формированием стойкой эндометриальной дисфункции [6]. Указанные патогенетические закономерности в итоге реализуются в гипо- и атрофию слизистой оболочки матки. Современные исследователи полагают, что атрофию эндометрия в отсутствие классических признаков воспалительного процесса при проведении ультразвукового исследования следует трактовать как эндометриопатию [7]. Характерными для данного синдрома чертами могут быть секреторная недостаточность эпителиоцитов, снижение экспрессии рецепторов к половым стероидам с потерей или резким снижением их чувствительности, появление алло- и аутоиммунных реакций, а также наличие «тонкого» эндометрия (когда его толщина, измеренная не менее чем в двух последовательных циклах в лютеиновой фазе, составляет ≤7 мм). Интересно, что до сих пор исследователи не пришли к консенсусу относительно самого определения эндометрия как «тонкого»: неоднозначным является вопрос о том, какая его толщина может стать критичной для полноценности имплантации и прогрессирования беременности [8, 9]. Кроме того, необходимо подчеркнуть, что в нынешних условиях отечественные и зарубежные клиницисты столкнулись с некоторым парадоксом, когда ведется активное обсуждение вопросов, связанных с восстановлением репродуктивной функции, нарушения которой обусловлены эндометрио-патией («тонким» эндометрием), но состояния, обозначаемые этими терминами, не фигурируют в действующей Международной классификации болезней в качестве самостоятельных нозологических форм. При этом надо признать, что это один из главенствующих факторов, связанных с ведением данной когорты пациенток.
В отличие от этиологии и патогенеза хронического эндометрита, которые в настоящее время изучены относительно неплохо [1–3, 10], понимание закономерностей и особенностей формирования «тонкого» эндометрия является весьма дискутабельным вопросом [6–9]. Ряд отечественных ученых выдвинул концепцию развития эндометриопатии в виде «тонкого» эндометрия [7, 11, 12]. Существует мнение, что термин «хронический эндометрит» становится неуместным на определенном этапе развития патологического процесса, когда воспалительной реакции в чистом виде давно уже нет; вместо этого реализуется защитный механизм выживания клетки в изменившихся условиях в виде угнетения ее пластических факторов [7]. При этом на ультраструктурном уровне могут быть выявлены признаки остаточной воспалительной реакции, оксидативного стресса, микроциркуляторных нарушений и эндотелиальной дисфункции [13]. Обычно в этом случае патологические структурные изменения эндометрия обнаруживаются в отсутствие патогенных микроорганизмов в полости матки [14–17]. Таким образом, согласно одному из основных диалектических законов, целесообразно расценивать «тонкий» эндометрий в большинстве случаев как качественно другой, более серьезный патологический процесс в ткани, изначально запускаемый воспалением, но при этом с течением времени утративший его классические признаки и характеризующийся глубинными вторичными структурно-функциональными нарушениями [3, 7, 18]. Таким образом, феномен «тонкого» эндометрия в репродуктологии до сих пор является сложным и не до конца понятным, в связи с чем нет единых четких алгоритмов диагностики и лечения этого явления, а также общепринятых критериев готовности к беременности [6, 19].
Очевидно, что адекватная синхронизация эндометриальных рецепторов, эмбриона и желтого тела, правильный процесс трансформации слизистой полости матки — это условия успешной имплантации и прогрессирования гестационного процесса. Трансформация эндометрия происходит под контролем гормонов на фоне увеличения продукции цитокинов. Результат этого взаимодействия также определяется структурно-функциональным состоянием эндометрия в «окно имплантации» [20]. С учетом этих данных основной задачей патогенетически обоснованных лечебно-восстановительных мероприятий у женщин с эндометриальным фактором бесплодия является создание благоприятных условий для формирования оптимальных параметров толщины и структуры эндометрия, необходимых для наступления беременности [21, 22]. Включение половых стероидов (в большей степени эстрогенов) в алгоритм лечения больных с «тонким» эндометрием обусловливает вероятность реализации избыточного провоспалительного потенциала и тромбоэмболических осложнений [23], однако при этом эффективность гормональной терапии остается относительно невысокой [22, 24]. Все эти аспекты в совокупности делают необходимым поиск эффективных воздействий на несостоятельный эндометрий [19, 22].
Цель исследования: оценить эффективность комбинированной терапии комплексом противомикробных пептидов и цитокинов и природного антикоагулянта прямого действия у пациенток с эндометриальным бесплодием на фоне «тонкого» эндометрия.
Содержание статьи
Материал и методы
Работа проведена на клинической и научной базе кафедры акушерства и гинекологии в соответствии с одобренным локальным этическим комитетом ФГБОУ ВО «ПИМУ» Минздрава России клиническим протоколом, с использованием зарегистрированного в установленном порядке, сертифицированного и поверенного оборудования, участвующего в программе Федеральной системы внешней оценки качества клинических лабораторных исследований (№ 08952 в реестре ФСВОК) и Международной программе EQAS.
В настоящем исследовании приняли участие амбулаторные пациентки репродуктивного возраста с «тонким» эндометрием и ассоциированным с ним эндометриальным фактором бесплодия.
Критерии включения:
Женщины в возрасте от 19 до 45 лет включительно.
Подтвержденный в процессе УЗИ исход гипопластической формы хронического эндометрита в «тонкий» эндометрий.
Отсутствие использования в течение 2 мес., предшествующих настоящему исследованию, гормональных и антимикробных средств.
Отсутствие на момент включения в исследование показаний к проведению антибактериальной терапии.
Наличие подписанного информированного согласия пациентки на участие в клиническом исследовании.
Желание и способность пациентки выполнять требования протокола на протяжении всего исследования, заинтересованность в беременности.
Отрицательный тест на беременность для женщин с сохраненным репродуктивным потенциалом.
Критерии невключения и исключения:
Гиперчувствительность к действующему и/или любому из вспомогательных веществ препаратов.
Отягощенный аллергологический анамнез, в том числе известная аллергия к белку животного (свиного) происхождения.
Нарушение свертывающей системы крови.
Гиперпластические процессы эндометрия, синехии полости матки (до гистерорезектоскопии), генитальный эндометриоз, подслизистая миома матки, наличие субсерозных и интерстициальных миоматозных узлов больших размеров, опухоли яичников, цервикальная интраэпителиальная неоплазия 2–3-й степени, аномалии и пороки развития половых органов, непроходимость маточных труб.
Инфекции, передающиеся половым путем.
Патологические маточные кровотечения любой этиологии или аменорея.
Злокачественные новообразования, в том числе в анамнезе.
Сопутствующие аутоиммунные заболевания (системная красная волчанка, ревматоидный артрит, аутоиммунный тиреоидит, антифосфолипидный синдром и др.).
Заболевания эндокринной системы, в том числе сахарный диабет в стадии декомпенсации, выраженное ожирение (индекс массы тела ≥35 кг/м2), выраженный гипо- и гипертиреоз.
Применение исследуемых препаратов в течение 30 дней перед включением в исследование.
Прием препаратов женских половых гормонов (в том числе комбинированных оральных контрацептивов и фитоэстрогенов) в течение 2 мес. перед включением в исследование.
Необходимость назначения антибактериальной терапии.
Участие в клиническом исследовании лекарственных средств менее чем за 3 мес. до начала исследования.
Анамнез наркотической или алкогольной зависимости в течение последних 5 лет.
Добровольный отказ пациентки от участия в исследовании, любое клинически значимое состояние или сопутствующие соматические или психические заболевания или состояния, которые, по мнению исследователя, затрудняют интерпретацию результатов лечения или приводят к невозможности проведения процедур в рамках настоящего клинического исследования или представляют опасность для пациентки при ее участии в исследовании.
С учетом данных критериев в исследование было включено 25 женщин в возрасте от 24 до 43 лет. Средний возраст больных 34±1,2 года. До вступления в данное исследование все пациентки получали традиционное лечение с использованием гормональной и метаболической терапии без эффекта.
В рамках данной работы осуществлялось комплексное клинико-лабораторное и инструментальное обследование больных. Лечебно-восстановительные мероприятия проводились с применением сочетанной терапии препаратом, содержащим антимикробные пептиды и цитокины (свечи 25 ЕД вагинально и ректально, чередуя, в течение 40 дней), и препаратом с натуральными антикоагулянтами (перорально по 2 капсулы 3 р/сут в течение 20 дней).
До начала терапии и через 3 менструальных цикла после окончания лечения измерялись уровни биомаркера в менструальной крови (провоспалительный цитокин интерлейкин 6 (ИЛ-6)), толщина эндометрия (параметр М-эхо), оценивалась его эхоструктура, а также были получены данные гистероскопии и оптической спектроскопии (ОС).
Менструальную кровь забирали по ранее описанной нами методике [18]. Образец направлялся в ИФА-лабораторию, центрифугировался при 10 000 об/мин в течение 15 мин. Измерение уровня ИЛ-6 в менструальной крови проводилось методом иммуноанализа на автоматическом анализаторе Cobas 6000 (Roshe). Референтные значения (норма) для данного биомаркера, определенные нами в менструальной крови здоровых женщин-добровольцев, составляли 185–14 000 пг/мл.
Для ультразвукового исследования (УЗИ) использовались аппараты экспертного класса Voluson Е-10 Oled, Voluson E-8 с применением мультичастотных трансабдоминальных 3,5 МГц, конвексного объемного RAB 6-D, трансвагинальных 5–9 D МГц RIC датчиков (в том числе внутриполостного датчика IC5-9 с режимом ЦДК HD-Flow). В числе прочих параметров измерялась толщина эндометрия и отмечались его особенности (параметр М-эхо, эхогенность, эхоморфология), однородность, адекватность структуры дню менструального цикла. В качестве оптимальной толщины эндометрия принимались значения М-эхо 8,5–12 мм.
Гистероскопия с целью визуальной оценки состояния полости матки выполнялась в «окно имплантации» на аппарате Olimpus Visera Pro. Мини-инвазивная оценка структурно-функциональных особенностей эндометрия при помощи оптической спектрометрии проводилась на аппарате «Фотон Био» путем регистрации и анализа спектров фотолюминесценции и спектров отражения от тканей. Записанные данные в графической и цифровой форме анализировались программой аппаратного комплекса, затем вычислялись индексы оксигенации (ИО) и пролиферативной активности (ИП) эндометрия. В качестве нормальных принимались значения ИО 58–120%, ИП — 0,95–1,11 ед.
После проведения лечения в течение 6 мес. оценивались репродуктивные исходы у пролеченных пациенток. Проведены анализ и сравнение репродуктивных исходов у пациенток, получавших исследуемые препараты, с репродуктивными исходами в ретроспективной группе сравнения, которую составили бесплодные женщины с «тонким» эндометрием (n=56), получавшие традиционную циклическую гормональную терапию в виде приема эстрадиола валерата с 5-го по 25-й день менструального цикла в дозе 4–6 мг и дидрогестерона с 16-го по 25-й день менструального цикла в дозе 20 мг/сут на протяжении 3 мес., а также курс системной магнитотерапии.
Для статистической обработки результатов исследования в качестве программного обеспечения использовали пакеты прикладных программ IBM SPSS Statistics v26, Microsoft Exсel. Проверка выборок на нормальность проводилась при помощи методов Колмогорова — Смирнова и Шапиро — Уилка. Для проверки статистических гипотез использовался непараметрический критерий Уилкоксона. Распределения количественных данных, отличные от нормального, описывались с помощью медианы (Me) и квартилей в формате Me [Q1; Q3]. Для обработки частотных (качественных) переменных указывали абсолютные значения и относительные величины (%), определение статистической значимости различий проводили при помощи метода Фишера с угловым преобразованием. Данные были представлены в формате р±σр%, где р — процентная доля, σр — стандартное отклонение. В качестве порогового уровня значимости (р) принято значение 0,05, ниже которого различия расценивались как статистически значимые.
Результаты и обсуждение
Поскольку среди сравниваемых пар выборок категорий «до лечения» и «после лечения» не оказалось параметров, которые одновременно имели бы нормальность в обеих подгруппах, сравнительный анализ на различие параметров проводился по непараметрическому критерию Уилкоксона для связанных выборок.
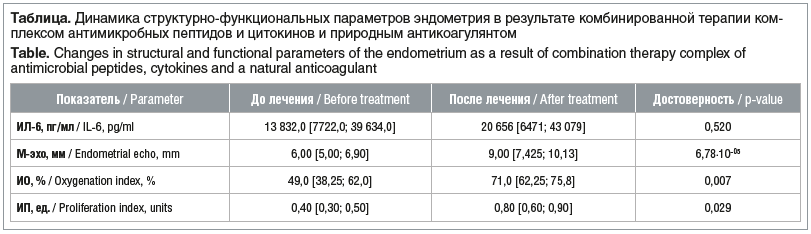
Как следует из данных таблицы, средние значения ИЛ-6 в менструальной крови больных основной группы до начала лечения составили 13 832,0 [7722,0; 39 634,0] пг/мл. После терапии по прошествии 3 мес. отмечена тенденция к увеличению данного показателя, что потенциально может стать свидетельством активизации и актуализации воспалительной реакции со стороны эндометрия («излечение через обострение») под влиянием комплекса цитокинов. Мы выяснили, что у 12 (48%) из 25 пациенток произошло увеличение показателя ИЛ-6 в 5–10 раз. Не исключено, что умеренное увеличение уровня ИЛ-6 также может быть ассоциировано с адекватностью процесса имплантации [20].
Весьма показательной оказалась динамика прироста толщины эндометрия по данным УЗ-диагностики. Так, до вступления в исследование значение параметра М-эхо у больных с «тонким» эндометрием было в среднем 6,00 [5,00; 6,90] мм. После терапии с включением комбинации препаратов с антимикробными пептидами, цитокинами и природным антикоагулянтом мы увидели рост толщины эндометрия до оптимальных значений. Кроме того, нормализация эхоструктуры эндометрия через 3 мес. по окончании лечения была зафиксирована у 18 (72%) женщин. Описанные позитивные изменения по данным УЗ-картины очевидно повышали шансы на успешную имплантацию и прогрессирование беременности, поскольку известно, что морфологические характеристики и толщина являются одними из основных определяющих признаков зрелости ткани слизистой полости матки и одновременно критериями прогноза успешного наступления беременности, на которые в настоящее время ориентируются клиницисты [20].
Что касается эндоскопического исследования, то у бесплодных больных с рецидивирующими неудачами имплантации гистероскопия с морфологическим исследованием биоптата эндометрия на сегодняшний день рассматривается как инструмент для исключения патологии эндометрия, включая хронический эндометрит, при этом данной рекомендации присвоен низкий уровень убедительности С (уровень достоверности доказательств — 5)[1] [25]. По нашим данным, при гистероскопии врач далеко не всегда имеет возможность получить визуальное подтверждение фиброзных и склеротических изменений в эндометрии. Между тем они составляют морфологическую основу «тонкого» эндометрия [18]. В связи с этим в поисках альтернативных способов оценки состояния эндометрия в ходе обследования больных нами был использован мини-инвазивный метод ОС, который был предложен В.М. Зуевым и соавт. [25].
Параметры ОС до лечения характеризовались низкими уровнями оксигенации и пролиферативной способности эндометрия, что является свидетельством глубоких структурно-функциональных нарушений при тканевом стрессе. Через 3 мес. после сочетанной терапии антимикробными пептидами, цитокинами и природными антикоагулянтами значения данных показателей статистически значимо увеличились (р=0,007 и р=0,029 соответственно), причем уровень оксигенации достиг нормальных значений и стал оптимальным (см. таблицу). Вероятно, подобный эффект стал возможен благодаря синергическому влиянию применяемых препаратов, поскольку при одновременном использовании комплекса антимикробных пептидов, цитокинов и природных антикоагулянтов обеспечивается воздействие на основные патогенетические звенья дисфункции эндометрия на фоне его гипоплазии (атрофии).
Из 25 больных основной группы, которые прошли полный курс лечения, в течение 6 мес. беременность наступила у 11 (у 9 — спонтанное зачатие, у 2 — при использовании программы экстракорпорального оплодотворения и переноса эмбриона в полость матки). На данный момент беременность прогрессирует на сроках более 30 нед. у 7 пациенток, на ранних сроках — у 2 пациенток, у 1 пациентки беременность замерла на 7 нед., еще у 1 пациентки отмечена эктопическая беременность. Раздельно анализировать репродуктивные исходы самостоятельных и индуцированных беременностей мы посчитали нецелесообразным ввиду небольшой выборки больных.
В качестве предварительного сравнения частоты наступления беременности есть смысл привести данные, полученные нами ретроспективно в предыдущих собственных исследованиях эффективности воздействия циклической гормонотерапии [18]. Так, средневзвешенное значение частоты факта установленной беременности в опытной группе больных, получавших комбинацию антимикробных пептидов, цитокинов и природных антикоагулянтов, составило 44±7,9%, тогда как в группе сравнения — 38±5,9% (р=0,2).
Лекарственный препарат, содержащий комплекс антимикробных пептидов и цитокинов, обладает противомикробным действием, антиоксидантной активностью, стимулирует регенерацию и эпителизацию раневых дефектов. Природный антикоагулянт прямого действия в виде гирудина медицинской пиявки оказывает умеренное противовоспалительное действие, замедляет и увеличивает продолжительность процесса свертывания крови, снижает адгезию тромбоцитов на эндотелии, демонстрирует фибринолитическую активность, препятствует образованию тромбов в просвете сосудов и способствует их рассасыванию.
Важно отметить, что комбинация данных лекарственных препаратов патогенетически обоснована нами с учетом взаимодополняемости известных механизмов их действия. Ранее в исследованиях отечественных ученых было убедительно показано, что эффективность экзогенной цитокинотерапии обусловлена модуляцией экспрессии факторов врожденного иммунитета в эндометрии, что способствует нормализации рецептивности и процессов ангиогенеза [26], а эффект натурального антикоагулянта прямого действия в терапии хронического эндометрита обусловил тенденцию к улучшению показателей ангиогенеза в ткани эндометрия [10].
Таким образом, проведенная нами терапия обеспечила адекватный прирост толщины эндометрия до оптимальных величин, восстановление его эхоструктуры и оптимизацию параметров оксигенации и пролиферации по данным ОС. Итогом стало наступление желанной беременности у существенного количества пролеченных пациенток, которые ранее не реагировали на традиционную терапию.
Заключение
Безусловно, это лишь предварительные результаты для когорты больных с нарушениями детородной функции на фоне «тонкого» эндометрия, необходимы дальнейшие исследования с большей выборкой пациенток и оценкой ряда дополнительных параметров — микроциркуляции, рецепторной чувствительности ткани, которые характеризуют другие звенья патогенеза эндометриальной дисфункции. Однако стоит учитывать тот факт, что ранее эти женщины безуспешно лечились с применением традиционной терапии, поэтому даже такие промежуточные итоги внушают оптимизм.
СВЕДЕНИЯ ОБ АВТОРАХ:
Мотовилова Татьяна Михайловна — д.м.н., доцент кафедры акушерства и гинекологии ФГБОУ ВО «ПИМУ» Минздрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; врач акушер-гинеколог ООО «Клиника современных технологий «Садко»; 603057, Россия, г. Нижний Новгород, ул. Бекетова, д. 13; ORCID iD 0000-0002-3795-2852.
Симакова Виктория Юрьевна — врач акушер-гинеколог ООО «Клиника современных технологий «Садко»; 603057, Россия, г. Нижний Новгород, ул. Бекетова, д. 13; ORCID iD 0009-0001-6727-3869.
Качалина Татьяна Симоновна — д.м.н., профессор кафедры акушерства и гинекологии ФГБОУ ВО «ПИМУ» Минздрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; ORCID iD 0000-0002-3459-5335.
Боровкова Людмила Васильевна — д.м.н., профессор, заведующая кафедрой акушерства и гинекологии ФГБОУ ВО «ПИМУ» Минздрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; ORCID iD 0000-0002-7643-3019.
Пономарева Ирина Владимировна — главный врач ООО «Клиника современных технологий «Садко»; 603057, Россия, г. Нижний Новгород, ул. Бекетова, д. 13; ORCID iD 0000-0001-9527-1476.
Мартьянцева Ирина Владимировна — врач диагностической лаборатории, заведующая лабораторией ООО «Клиника современных технологий «Садко»; 603057, Россия, г. Нижний Новгород, ул. Бекетова, д. 13; ORCID iD 0000-0003-4909-5250.
Круглова Ирина Александровна — врач клинической лаборатории ГБУЗ НО «Городская больница № 35» г. Н. Новгорода; 603089, Россия, г. Нижний Новгород, ул. Республиканская, д. 47; ORCID iD 0000-0001-7955-349Х.
Лазукин Валерий Федорович — к.б.н., доцент кафедры информационных технологий ФГБОУ ВО «ПИМУ» Минздрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; ORCID iD 0000-0003-0916-0468.
Богомолова Мария Дмитриевна — студентка лечебного факультета 6-го курса ФГБОУ ВО «ПИМУ» Минздрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; ORCID iD 0000-0002-8332-8049.
Казаринова Дарья Александровна — студентка лечебного факультета 5-го курса ФГБОУ ВО «ПИМУ» Минздрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; ORCID iD 0009-0004-2396-1813.
Контактная информация: Мотовилова Татьяна Михайловна, e-mail: tatyana.m.motovilova@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 23.10.2023.
Поступила после рецензирования 16.11.2023.
Принята в печать 11.12.2023.
ABOUT THE AUTHORS:
Tatyana M. Motovilova — Dr. Sc. (Med.), Associate Professor of the Department of Obstetrics and Gynecology, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; obstetrician-
gynecologist, Clinic of Modern Technologies «Sadko» LLC; 13, Beketov str., Nizhny Novgorod, 603057, Russian Federation; ORCID iD 0000-0002-3795-2852.
Victoria Yu. Simakova — obstetrician-gynecologist, Clinic of Modern Technologies «Sadko» LLC; 13, Beketov str., Nizhny Novgorod, 603057, Russian Federation; ORCID iD 0009-0001-6727-3869.
Tatyana S. Kachalina — Dr. Sc. (Med.), Professor of the Department of Obstetrics and Gynecology, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0002-3459-5335.
Lyudmila V. Borovkova — Dr. Sc. (Med.), Professor, Head of the Department of Obstetrics and Gynecology, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0002-7643-3019.
Irina V. Ponomareva — Chief Medical Officer, Clinic of Modern Technologies «Sadko» LLC; 13, Beketov str., Nizhny
Novgorod, 603057, Russian Federation; ORCID iD 0000-0001-9527-1476.
Irina V. Martiantseva — doctor of clinical laboratory science, Head of the Laboratory, Clinic of Modern Technologies «Sadko» LLC; 13, Beketov str., Nizhny Novgorod, 603057, Russian Federation; ORCID iD 0000-0003-4909-5250.
Irina A. Kruglova — doctor of clinical laboratory science, City Hospital No. 35; 47, Respublikanskaya str., Nizhny Novgorod, 603089, Russian Federation; ORCID iD 0000-0001-7955-349X.
Valery F. Lazukin — C. Sc. (Bio.), Associate Professor of the Department of Information Technology, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0003-0916-0468.
Maria D. Bogomolova — 6th year student of the Faculty of Medicine, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0002-8332-8049.
Darya A. Kazarinova — 5th year student of the Faculty of Medicine, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0009-0004-2396-1813.
Contact information: Tatyana M. Motovilova, e-mail: tatyana.m.motovilova@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 23.10.2023.
Revised 16.11.2023.
Accepted 11.12.2023.
Информация с rmj.ru






