В статье представлено описание клинического случая рецидива инсулиномы у пациентки после оперативного лечения длительно существовавшей инсулиномы без адекватного лечения. Приводятся краткие сведения об эндогенном гиперинсулинизме как проявлении инсулиномы.
Инсулинома — это самая частая нейроэндокринная опухоль (до 70–75% от общего числа), происходящая из β-клеток островков Лангерганса, неконтролируемо секретирующая в кровяное русло инсулин, что является причиной спонтанной гипогликемии. Инсулиномы встречаются редко (1–4 случая на 1 млн населения в год) и в большинстве случаев (до 90%) являются доброкачественными, злокачественные инсулиномы встречаются в 5–10% случаев. Инсулиномы чаще всего выявляются у лиц в возрасте 30–60 лет. Женщины, по некоторым данным, заболевают в 2 раза чаще мужчин, в других источниках разницы по частоте заболеваемости у мужчин и женщин не обнаружено. Помимо инсулиномы причиной эндогенного гиперинсулинизма могут быть микроаденоматоз или гиперплазия β-клеток (незидиобластоз). Инсулиномы могут быть как спорадическими (90%), так и в составе синдрома МЭН-1 (10%) (синдром Вермера — наследственный аутосомно-доминантный синдром, обусловленный опухолями или гиперплазией нескольких эндокринных желез: паращитовидной, гипофиза, клеток островков Лангерганса, надпочечников, щитовидной железы). Более чем в 90% случаев инсулинома локализуется в поджелудочной железе (ПЖ). Приблизительно в 10% случаев инсулиномы являются множественными и крайне редко (
Избыточная неконтролируемая секреция инсулина клетками аденомы, приводящая к гипогликемии, является основным механизмом патогенеза заболевания. Снижение уровня гликемии приводит к выбросу контринсулярных гормонов: норадреналина, глюкагона, кортизола, соматотропного гормона (СТГ). Клинические проявления гипогликемии в основном обусловлены выбросом адренергических медиаторов (тремор, ощущение тревоги, сердцебиение, ночные кошмары) и активацией симпатической нервной системы (потливость, чувство голода, парестезии). При дальнейшем снижении уровня глюкозы появляются симптомы гликопении (слабость, сонливость, головокружение, снижение внимания, расстройство координации движений, помутнение зрения, нервно-психические нарушения — поведенческие отклонения, в т. ч. приступы агрессии, панические состояния, спутанность сознания и амнезия, симптомы поражения периферической нервной системы: онемение верхних и нижних конечностей, парестезии), связанные с голоданием мозга, т. к. глюкоза является основным энергетическим субстратом ЦНС. Далее могут развиваться судороги и кома, что может приводить к повреждению головного мозга. Хроническая гипогликемия приводит к дистрофическим изменениям в ЦНС.
Диагностика инсулиномы может задерживаться на несколько лет с момента начала заболевания, т. к. его симптоматика неспецифична и может быть схожа с симптомами психических, сердечно-сосудистых и неврологических заболеваний. Симптомы гипогликемии купируются приемом легкоусвояемых углеводов, в связи с чем пациенты часто страдают от ожирения. Для гипогликемии, независимо от причины, характерна триада Уиппла: развитие клинических признаков гипогликемии, уровень глюкозы плазмы — 2,8 ммоль/л и ниже, обратимость симптомов при введении глюкозы [3].
Для диагностики инсулиномы применяется контрольный тест с 48–72-часовым голоданием в стационаре под медицинским контролем. Данная проба основана на том, что у людей с гиперфункцией инсулярного аппарата при прекращении поступления углеводов с пищей развивается гипогликемия. Пациенту разрешают пить только воду. Определение уровня глюкозы в крови проводят вначале через 3 ч после последнего приема пищи, а впоследствии, по мере снижения уровня глюкозы в крови, интервалы между ее исследованием сокращаются до 0,5–1 ч. Развитие гипогликемической симптоматики со снижением уровня глюкозы крови
Хирургическая резекция является основным методом лечения инсулиномы. Объем хирургического вмешательства зависит от типа, размера и локализации опухоли. При доброкачественной единичной инсулиноме маленького размера, расположенной в теле или хвосте ПЖ, возможны лапараскопическая резекция, энуклеация, частичная резекция ПЖ или средняя панкреатэктомия, которые сохраняют здоровую ткань ПЖ, таким образом снижая риск недостаточности функции ПЖ. Радикальная резекция проводится при множественных очагах, опухоли с нечеткими границами, более 4 см в диаметре или расположенной вблизи основного протока ПЖ [6]. У пациентов с высоким операционным риском, лиц пожилого возраста, при тяжелом общем состоянии пациента возможно применение менее инвазивных методов лечения: алкогольной или радиочастотной абляции, эмболизации инсулиномы.
Медикаментозная терапия, направленная на нормализацию уровня глюкозы в крови, показана в предоперационном периоде, а также для пациентов, которым не может быть проведено хирургическое вмешательство, например, с незидиобластозом, множественными инсулиномами, неоперабельной злокачественной инсулиномой, имеющим серьезные соматические противопоказания к операции, или у пациентов, которые отказываются от хирургического вмешательства. Октреотид представляет собой аналог соматостатина, который ингибирует секрецию инсулина и периферическое действие многих гормонов желудочно-кишечного тракта, в первую очередь путем активации рецепторов sst2 соматостатина, он может иметь антипролиферативный эффект, а также умеренное противоопухолевое действие на панкреатические эндокринные опухоли. Терапия может быть начата с короткодействующего октреотида 2–4 р./сут или 20–30 мг октреотида длительного действия каждые
4 нед. в течение 3–6 мес. Однако в ряде случаев применение октреотида может усугублять гипогликемическую реакцию, поскольку он наравне с подавлением продукции инсулина может угнетать секрецию глюкагона и СТГ. Другим средством, ингибирующим секрецию инсулина путем открытия АТФ-зависимых калиевых каналов в β-клетках ПЖ, является диазоксид. Кроме того, сообщалось о способности диазоксида к увеличению производства глюкозы в печени и ингибированию поглощения глюкозы [7]. Эверолимус — средство для лечения хорошо и умеренно дифференцированных недействующих панкреатических нейроэндокринных опухолей или метастатических панкреатических нейроэндокринных опухолей, относится к группе ингибиторов mTOR, блокирующих внутриклеточную протеинкиназу mTOR, которая является компонентом сигнальных путей, регулирующих выживаемость и рост клеток, а также ангиогенез [8].
Клинический случай
Пациентка К., 57 лет, поступила в отделение эндокринологии в марте 2018 г. с жалобами на выраженную общую слабость, головокружение, рвоту после приема пищи, уровень глюкозы в крови составлял 1,5 ммоль/л.
Из анамнеза известно, что с 1999 г. пациентку стали беспокоить частые, до 4 раз в день, эпизоды выраженной слабости, головокружения, которые были связаны со снижением уровня глюкозы в крови
В связи с возобновившимися симптомами пациентка обратилась за медицинской помощью. Врачами отделения, проводившими оперативное лечение, был диагностирован рецидив заболевания, по поводу которого была предложена ампутация оставшейся ПЖ, от чего пациентка отказалась. К врачам более не обращалась, терапии не получала. Гипогликемические состояния со снижением уровня глюкозы до 2–3 ммоль/л развивались ежедневно при задержке приема пищи более 4 ч, больная каждые 3–4 ч
пила сладкий чай, дробно питалась. Потери сознания на фоне гипогликемии не отмечала. С момента дебюта заболевания отметила выраженное нарастание массы тела.
В течение последнего месяца пациентка отмечала снижение аппетита, тошноту и рвоту при приеме пищи, учащение гипогликемических реакций, нарастала общая слабость, пациентка перестала подниматься с кровати. В связи с гипогликемиями до 1,5 ммоль/л, плохо поддававшимися купированию легкоусвояемыми углеводами, была госпитализирована в отделение эндокринологии.
В анамнезе: ОНМК в 2013 г. Гипертоническая болезнь. Абсцесс левой боковой поверхности шеи в ноябре 2017 г.
Гинекологический анамнез: родов — 2.
При физикальном осмотре: состояние средней степени тяжести, сознание ясное, рост — 168 см, масса тела — 114 кг, ИМТ — 40,4 кг/м2; гиперпигментация кожных покровов в области шеи; щитовидная железа не пальпируется в связи с выраженным ожирением; живот при пальпации мягкий, безболезненный, увеличен за счет подкожно-жировой клетчатки, печень выступает на 2 см из-под реберной дуги; ЧДД — 18/мин; пульс — 80/мин, среднего наполнения и напряжения, тоны сердца приглушены; АД — 120/70 мм рт. ст.
Данные лабораторных исследований (в скобках указана норма), см. также таблицу 1: гематокрит — 31,8% (33–47), гемоглобин — 109 г/л (115–160), среднее содержание гемоглобина в эритроцитах (MCH) — 27 пг (28–35), лейкоциты — 11,7 × 109 (4–10), сегментоядерные — 82% (47–72), лимфоциты — 11% (19–45), моноциты — 2% (3–12), общий белок — 53,3 г/л (66–83), мочевина — 11,1 ммоль/л (2,8–8,3), креатинин — 107,5 мкмоль/л (45–97), Na — 125 ммоль/л (135–148), К — 2,65 ммоль/л (3,5–5), Cl — 86 ммоль/л (98–106), лактат — 4,13 ммоль/л (0,5–1,6), pH крови — 7,47 (7,35–7,45), HbA1с — 4,20%, инсулин — 33,90 мкМЕ/мл (0–29,1), С-пептид — 8,78 нг/мл (0,9–7,1), глюкоза крови — 1,50 ммоль/л, индекс ИРИ / инсулин (мкМЕ/мл) / глюкоза (мг/дл) = 1,26 (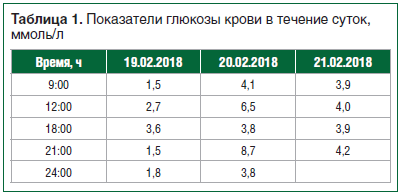
Тест с голоданием и инсулиновый супрессивный тест не проводились, т. к. даже на фоне дробного частого питания и инфузий глюкозы уровень гликемии понижался до 1,5–1,8 ммоль/л.
На ЭКГ: ЧСС — 100/мин. Синусовая тахикардия. ЭОС — горизонтальная. Изменения миокарда левого желудочка.
Рентгенограмма органов грудной клетки — без видимых патологических изменений.
УЗИ органов брюшной полости и почек: эхографическая картина стеатоза печени, ЖКБ, хронического калькулезного холецистита, диффузных изменений головки ПЖ, почек, неосложненной кисты левой почки. ПЖ — визуализируется головка (2,6 см) с нечеткими контурами, повышенной эхогенности, однородная, частично визуализируется тело железы. Селезенка не визуализируется (удалена).
Компьютерная томография брюшной полости и забрюшинного пространства, малого таза: стеатоз печени, гепатомегалия. Диффузная атрофия паренхимы ПЖ, состояние после гемипанкреатэктомии. Образования обоих надпочечников более соответствуют аденомам. Киста левой почки (Bosniak 1). ЖКБ. Образование матки более соответствует миоме.
Эзофагогастродуоденоскопия (ЭГДС): эрозивный гастродуоденит. Недостаточность кардии. Рефлюкс-эзофагит-1.
Клинический диагноз: рецидив инсулиномы поджелудочной железы. Гипогликемии рецидивирующего течения. Состояние после гемипанкреатэктомии, спленэктомии от 1999 г. Морбидное ожирение (ИМТ — 40,4 кг/м2).
Сопутствующие заболевания: ИБС: стенокардия напряжения. Гипертоническая болезнь 3 ст., риск 4, НК1. Цереброваскулярная болезнь (ЦВБ). Энцефалопатия сосудистого генеза. ОНМК от 2013 г. Эрозивный гастродуоденит. ЖКБ: хронический калькулезный холецистит. Жировой гепатоз. Киста левой почки. Нефропатия смешанного генеза. Хроническая болезнь почек (ХБП) С3а А2. Анемия легкой степени смешанного генеза. Состояние после дренирования абсцесса шейной области от 11.2017 г. Лимфоаденопатия шеи. Аденома надпочечников. Миома матки. Хронический гингивит.
Лечение пациентки началось с внутривенной инфузии 40 мл 40% раствора глюкозы и 500 мл 5% раствора глюкозы 2 р./сут, которые в дальнейшем выполнялись при появлении признаков гипогликемии, снижении уровня глюкозы крови
Применялся раствор натрия хлорида 0,9% 200 мл с 20 мл
4% раствора калия хлорида с учетом гипокалиемии, гипонатриемии вследствие потери электролитов с рвотой и на фоне инфузионной терапии раствором глюкозы (хроническая надпочечниковая недостаточность как причина гипонатриемии была исключена в связи с наличием артериальной гипертензии).
В дальнейшем использовали октреотид 0,1 мг п/к 3 р./сут ежедневно.
Была назначена индивидуальная диета: частые приемы богатой углеводами пищи каждые 3–4 ч, дополнительный прием легкоусвояемых углеводов. Панкреатин 20 000 ЕД по 1 капс. с каждым приемом пищи. Омепразол 20 мг 2 р./сут. У пациентки К. после хирургического лечения инсулиномы ПЖ в 1999 г. (гемипанкреатэктомия, спленэктомия) при обследовании были отмечены признаки рецидива заболевания. Во время обследования были выявлены признаки эндогенного гиперинсулинизма, однако визуализацию опухоли провести не удалось — при проведении трансабдоминального УЗИ и КТ брюшной полости инсулинома не была обнаружена. Пациентке проводилась симптоматическая инфузионная терапия растворами глюкозы, преднизолоном; с целью снижения эндогенной продукции инсулина проводилась терапия октреотидом с положительной динамикой в виде отсутствия эпизодов гипогликемии.
Пациентке К. было рекомендовано продолжить терапию октреотидом, наблюдаться у врача-эндокринолога амбулаторно, провести специфическое дообследование для топической диагностики инсулиномы и дифференциальной диагностики инсулиномы с микроаденоматозом, незидиобластозом: эндоскопическая ультрасонография, тонкоигольная биопсия (ТАБ) под контролем УЗИ, ангиография в сочетании с внутриартериальной стимуляцией кальцием ПЖ с последующим определением уровня иммунореактивного инсулина, после чего возобновить вопрос о повторном хирургическом вмешательстве.
При обследовании были обнаружены образования надпочечников, однако дальнейшие исследования для исключения гормональной активности данных образований, а также исключения симптоматического генеза артериальной гипертензии не проводились. Пациентке рекомендованы оценка уровня кортизола в суточной моче, в слюне или проведение ночного подавляющего теста с 1 мг дексаметазона, исследование уровня метилированных производных катехоламинов в крови или в суточной моче, а также альдостерон-ренинового соотношения в сыворотке крови с последующим решением о дальнейшей тактике ведения. С учетом наличия образований надпочечников, возможно, у данной пациентки имеет место вариант МЭН-1 синдрома (синдром Вермера), для исключения которого необходимы также исследование уровня общего и ионизированного кальция, паратгормона, пролактина, СТГ, МРТ гипофиза. По данным ЭГДС обнаружен эрозивный гастродуоденит, в связи с чем необходимо исключить гиперпродукцию гастрина. В случае обнаружения компонентов МЭН-1 синдрома рекомендуется генетическое исследование для подтверждения наличия мутаций гена супрессора MEN1, который находится на хромосоме в локусе 11q13.
В данной статье представлен нетипичный клинический случай рецидива инсулиномы. Как правило, радикальное (оперативное) лечение способствует полной ремиссии заболевания (рецидив составляет около 3%). Однако встречаются случаи неэффективности оперативного лечения при множественных аденомах или экстрапанкреатическом расположении аденомы. В данном случае гипогликемические состояния сохранились и после дистальной гемипанкреатэктомии. Несмотря на проведение оперативного лечения, в ряде случаев картина гиперинсулинизма может сохраняться, что требует дальнейшего лечения и топической диагностики источника гиперинсулинемии. Длительно существующий эндогенный гиперинсулинизм в связи с необходимостью частого приема большого количества легкоусвояемых углеводов приводит к выраженному морбидному ожирению, которое способствует развитию артериальной гипертензии, нарушениям сна вплоть до синдрома апноэ во сне, жировой неалкогольной болезни печени, ЖКБ, поражению опорно-двигательного аппарата, развитию паранеопластических процессов, что существенно снижает качество жизни пациентов, работоспособность, вплоть до инвалидизации и невозможности самообслуживания. Хронические эпизоды гипогликемии могут послужить причиной развития дистрофических изменений ЦНС, наблюдается постепенное нарастание интеллектуальных расстройств, вплоть до пресенильной деменции. В некоторых случаях у пациентов развиваются тремор, хорея, ригидность, мозжечковая атаксия и иногда симптомы вовлечения периферических мотонейронов (гипогликемическая амиотрофия).
Выводы
Для диагностики эндогенного гиперинсулинизма пациентам с симптомами гипогликемии (тремор, потливость, слабость, сонливость, головокружение, снижение внимания, спутанность сознания) проводятся определение во время приступа уровней глюкозы, С-пептида, инсулина в крови с выявлением триады Уиппла, проба с голоданием, тест с подавлением С-пептида, КТ и/или МРТ органов брюшной полости с контрастированием. При необходимости выполняются эндоскопическое и интраоперационное УЗИ, ТАБ под контролем УЗИ, ангиография с внутриартериальной стимуляцией кальцием ПЖ и определением уровня ИРИ. Необходимо исключить возможное экзогенное введение инсулина или прием препаратов сульфонилмочевины, приводящих к снижению уровня глюкозы крови.
Эпизод гипогликемии следует купировать приемом легкоусвояемых углеводов, внутривенным введением 40–100 мл 40% раствора глюкозы, при необходимости продолжить инфузионную терапию 5–10% раствором глюкозы. Применяются глюкокортикоиды парентерально или перорально.
Основным методом лечения является хирургический — резекция инсулиномы. При невозможности или неэффективности хирургического лечения применяются препараты, снижающие эндогенную секрецию инсулина: октреотид, диазоксид, эверолимус.
Информация с rmj.ru






