Дисфункция сфинктера Одди и синдром избыточного бактериального роста в кишечнике
Е. А. Лялюкова, кандидат медицинских наук, доцент
М. А. Ливзан, доктор медицинских наук, профессор
ГБОУ ВПО ОмГМА МЗ РФ, Омск
У значительной части больных после холецистэктомии развивается дисфункция сфинктера Одди (ДСО) [1, 3].
Согласно Римскому консенсусу III (2006 г.) под дисфункцией сфинктера Одди понимают нарушение его сократительной функции, препятствующее нормальному оттоку желчи и панкреатического секрета в двенадцатиперстную кишку [10].
Синдром абдоминальной боли
Считают, что в первый месяц после холецистэктомии более чем у 80% больных преобладает гипертонус сфинктера Одди, что связано с выключением регулирующей роли сфинктера Люткенса [1, 3]. Болевой синдром при наличии дисфункции сфинктеров в большинстве случаев обусловлен спазмом сфинктера Одди.
Диагностические критерии дисфункции сфинктера Одди [10]:
1) эпизоды выраженной боли, локализованной в эпигастрии или правом подреберье, в сочетании со всеми следующими признаками;
2) продолжительность 30 мин и более;
3) частота развития симптомов: 1 раз и более за последние 12 мес;
4) интенсивность боли значительная: нарушает ежедневную активность и требует обращения за медицинской помощью;
5) отсутствуют структурные изменения, которые объясняли боль.
Следует помнить, что клинические симптомы (в первую очередь абдоминальные боли) после удаления желчного пузыря наблюдаются в 70–80% случаев и могут быть обусловлены целой группой причин, среди которых наиболее значимыми являются: диагностические ошибки, допущенные на дооперационном этапе во время обследования больного и/или во время операции; обострение или прогрессирование существовавших до операции заболеваний гепатопанкреатобилиарной зоны, технические погрешности и тактические ошибки, допущенные при проведении операции [3]. Клинические симптомы могут быть обусловлены недиагностированными и некорректированными заболеваниями, существовавшими еще в предоперационный период (хронические заболевания печени, стриктуры, стенозы желчных путей, как врожденного, так и приобретенного характера, камни желчных протоков, холангит, панкреатиты, доброкачественные и злокачественные опухоли поджелудочной железы, особенно с локализацией процесса в области головки, заболевания желудка и двенадцатиперстной кишки, включая эрозивно-язвенные изменения, а также пара- и перипапиллярные дивертикулы двенадцатиперстной кишки. Ошибки, допущенные во время холецистэктомии: невыявленные камни в общем желчном протоке, повреждение протоков, оставление длинной культи пузырного протока и др. [3].
В силу указанных причин постановка диагноза «дисфункция сфинктера Одди» требует тщательного обследования больного. В качестве скрининговых диагностических методов используют лабораторные тесты (общий анализ крови, определение уровней гамма-глютамилтранспептидазы, щелочной фосфатазы, билирубина, аспартатаминотрансферазы, аланинаминотрансферазы, амилазы) и инструментальные методы диагностики (ультразвуковое исследование, эзофагогастродуоденоскопия, дуоденография). Применение высокоинформативных методов диагностики (эндоскопическая ретроградная холангиопанкреатография, магнитно-резонансная холангиография, эндоскопическая ультрасонография и др.) позволяет проводить своевременную и адекватную коррекцию анатомо-функциональных нарушений, развившихся после холецистэктомии или усугубленных ею. Для подтверждения дисфункции сфинктера Одди применяют эндоскопическую манометрию сфинктера [1, 3, 6].
В 2006 г. рабочей группой экспертов по функциональным расстройствам желудочно-кишечного тракта (ЖКТ) подготовлен Римский консенсус III, в соответствии с которым в рубрику Е «Функциональные расстройства сфинктера Одди» включены разделы: Е2 «Функциональное расстройство билиарного и панкреатического типов» [10].
Больные с билиарным типом дисфункции сфинктера Одди распределяются на три группы, представленные в таблице, тактика ведения которых существенно различается.

Аналогичная классификация используется у больных с панкреатическим типом дисфункции сфинктера Одди. В этих случаях большое значение придается не менее чем двукратному повышению уровня панкреатических ферментов в крови в период двух последовательных приступов болей, а также расширению панкреатического протока более 5 мм.
Больным 1-й группы, имеющим стеноз сфинктера Одди и высокую вероятность дисфункции сфинктера Одди (> 70%), проводится эндоскопическая сфинктеротомия без предварительного манометрического исследования, что уменьшает частоту осложнений.
У больных 2-й группы только в 50% случаев при манометрическом исследовании выявляется дисфункция сфинктера Одди. Большинство исследователей полагают, что этой группе больных необходимо провести предварительное медикаментозное лечение и лишь при его неэффективности проводить манометрию сфинктера Одди.
В 3-й группе больных причины болей в большинстве случаев обусловлены дискинезией сфинктера Одди, и, следовательно, манометрия последнего не показана.
Синдром избыточного бактериального роста и метаболизм желчных кислот в кишечнике
При наличии спазма сфинктера Одди в пищеварительный период нарушается пассаж желчи по кишечнику, сопровождающийся разнообразными проявлениями нарушения пищеварения. Нерегулярное поступление желчных кислот нарушает энтерогепатическую циркуляцию желчных кислот, переваривание и всасывание жиров, уменьшает бактерицидные свойства дуоденального содержимого, способствуя нарушению микробиоценоза тонкой кишки. В случае недостаточности сфинктера Одди, который при отсутствии резервуарной функции желчного пузыря не способен выдержать повышенное давление (более 300–350 мм вод. ст.) в общем желчном протоке, отмечается постоянное поступление желчных кислот в кишечник, что может быть причиной развития холагенной диареи [3, 12].
Следует отметить, что при обоих типах дисфункции (спазм, недостаточность) наблюдается ряд симптомов, свидетельствующих о нарушении метаболизма желчных кислот в кишечнике (диспепсический симптомокомплекс). Основная роль в развитии указанных нарушений принадлежит изменению состава кишечной микрофлоры.
У здорового человека при наличии желчного пузыря синтезированные в гепатоцитах первичные желчные кислоты экскретируются в желчь конъюгированными с глицином или таурином и по желчевыводящим путям поступают в желчный пузырь, где и накапливаются [4]. В стенках желчного пузыря происходит всасывание незначительного количества желчных кислот — около 1,3%. У здорового человека при наличии желчного пузыря основной пул желчных кислот находится в желчном пузыре и только после стимуляции пищей рефлекторно происходит сокращение желчного пузыря и желчные кислоты поступают в двенадцатиперстную кишку. Вторичные желчные кислоты — дезоксихолевая и литохолевая — образуются из первичных (холе- и хенодезоксихолевой соответственно) под воздействием анаэробных бактерий толстой кишки (рис. 1).
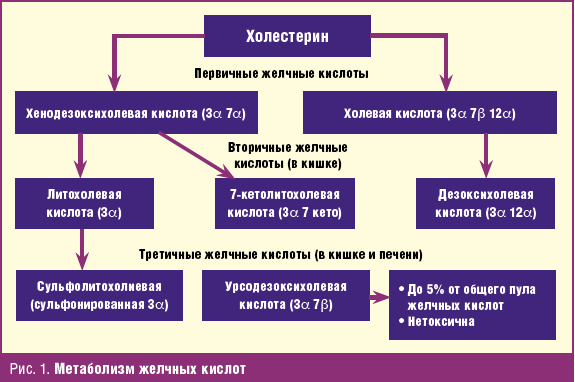
После реабсорбции вторичных желчных кислот происходит их конъюгация с глицином или таурином, и они также становятся компонентами желчи. Урсодезоксихолевая кислота (УДХК) — третичная желчная кислота не превышает 5% от всех желчных кислот организма человека и также образуется под действием ферментов микроорганизмов [13].

Из кишечника желчные кислоты с током портальной крови вновь попадают в печень, которая абсорбирует практически все желчные кислоты (примерно 99%) из портальной крови; совсем небольшое количество (около 1%) попадает в периферическую кровь (рис. 2).
Активное всасывание желчных кислот происходит в подвздошном отделе тонкой кишки, тогда как пассивная абсорбция идет за счет концентрации желчных кислот в кишечнике, поскольку она всегда выше, чем в портальной крови. В гепатоцитах токсичные свободные желчные кислоты, составляющие примерно 15% от всего количества желчных кислот, всосавшихся в кровь, превращаются в конъюгированные. Из печени желчные кислоты вновь поступают в желчь в виде конъюгатов. Подобная энтерогепатическая циркуляция в организме здорового человека совершается 2–6 раз в сутки в зависимости от режима питания; 10–15% от всех поступивших в кишечник желчных кислот после деконъюгации подвергаются более глубокой деградации в нижних отделах тонкой кишки. В результате процессов окисления и восстановления, вызываемых ферментами микрофлоры толстой кишки, происходит разрыв кольцевой структуры желчных кислот, что приводит к образованию ряда веществ, выделяемых во внешнюю среду. Учитывая, что желчные кислоты в норме предотвращают развитие избыточного микробного роста в кишечнике, у пациентов после холецистэктомии они рассматриваются также в качестве одной из причин развития данного синдрома, а также в качестве классических повреждающих факторов по отношению к слизистой оболочке желудка, пищевода, кишечника. Повреждающий эффект желчных кислот зависит не только от их концентрации, но и от конъюгации и рН окружающей среды, два последних процесса обеспечиваются микрофлорой кишечника. Желчные кислоты, обладающие детергентными свойствами, способствуют солюбилизации липидов мембран клеток поверхностного эпителия. Растворимые желчные кислоты проникают в эпителиальные клетки. Внутриклеточные концентрации желчных кислот могут в 8 раз превосходить их внеклеточные концентрации. Такое избыточное накопление приводит к повышению проницаемости мембран клеток, их разрушению, повреждению межклеточных контактов и в итоге к гибели клетки [4, 14]. Этот повреждающий эффект зависит не только от концентрации желчных кислот в рефлюксате, но и от продолжительности времени, в течение которого слизистая оболочка подвержена действию желчи. Под действием желчных кислот снижается количество фосфолипидов, теряется гидрофобность слизи [4, 9]. Конъюгированные желчные кислоты оказывают негативное влияние при кислых значениях рН, а неконъюгированные — при рН, равном 5–8. В силу указанных причин при нарушении микробиоценоза кишечника неконъюгированные желчные кислоты оказывают выраженное повреждающее действие на эпителиоциты. Зрелые и незрелые бокаловидные клетки из ткани толстой кишки здорового человека под действием желчных кислот подвергаются апоптозу.
Исследование биологических свойств бифидо- и лактобактерий показало, что популяция человеческой микробиоты оказывает многогранный спектр физиологически полезных воздействий. Применительно к обсуждаемой проблеме следует остановиться на некоторых из них.
Микрофлора кишечника принимает непосредственное участие в метаболизме и элиминации токсичных желчных кислот, в частности, холевой кислоты. В норме невсосавшаяся в дистальных отделах подвздошной кишки конъюгированная холевая кислота в толстой кишке подвергается деконъюнгации микробной холеглицингидролазой и дегидроксилированию при участии 7-альфа-дегидроксилазы [11, 12]. Образовавшаяся дезоксихолевая кислота связывается с пищевыми волокнами и выводится из организма. Большое значение имеет рН в просвете кишечника. При повышении значений рН дезоксихолевая кислота ионизируется и хорошо всасывается в толстой кишке, а при снижении — выводится. Повышение значений рН в толстой кишке приводит к повышению активности ферментов, приводящих к синтезу дезоксихолевой кислоты, ее растворимости и всасыванию и, как следствие, повышению в крови уровня желчных кислот, холестерина и триглицеридов. Одной из причин повышения рН может быть недостаток пребиотических компонентов в питании, нарушающих рост нормальной микрофлоры, в т. ч. бифидо- и лактобактерий.
Не менее важны эффекты, связанные с синтезом короткоцепочечных жирных кислот (КЦЖК) в результате анаэробного брожения доступных для бактерий ди-, олиго- и полисахаридов [11, 12]. Локально КЦЖК определяют снижение рН, обеспечивая колонизационную резистентность кишечника, принимают участие в регуляции кишечной моторики. Помимо этого КЦЖК важны для эпителия толстой кишки, т. к. именно бутират колоноциты используют для обеспечения своих энергетических потребностей. Кроме того, снижение рН, связанное с образованием КЦЖК, приводит к образованию ионов аммония из аммиака, образовавшегося в толстой кишке в процессе микробного метаболизма белков и аминокислот, который уже не может свободно диффундировать через кишечную стенку в кровь, а выводится с калом в виде аммонийных солей.
Результатом совместной симбиотической деятельности клеток эпителия кишечника и физиологической микрофлоры является формирование сложной специфической преэпителиальной структуры — слизистого барьера (биопленки, микробиологического барьера), состоящего из слизи, молекул секреторного IgA, индигенной флоры и ее метаболитов и защищающего слизистую оболочку кишечника от действия бактериальных и других токсинов физической и химической природы, включая желчные кислоты [11, 12].
Лечение пациентов с дисфункцией сфинктера Одди
Основной целью лечения больных с дисфункцией сфинктера Одди является восстановление нормального тока желчи и поджелудочного сока из билиарных и панкреатических протоков в двенадцатиперстную кишку с использованием оперативного или консервативного лечения [1–3, 5–8].
В связи с этим в задачи лечения входят:
- восстановление, а при невозможности — восполнение продукции желчи;
- восстановление тонуса сфинктерной системы;
- восстановление давления в двенадцатиперстной кишке (от этого зависит адекватный градиент давления в билиарном тракте).
Диетотерапия занимает существенное место в лечении данной категории больных. Общим принципом диеты является режим питания с частыми приемами пищи в небольшом количестве (5–6-разовое питание) с достаточным потреблением пищевых волокон, необходимых для восстановления моторно-эвакуаторной функции кишечника и коррекции микробиологических нарушений.
Для купирования болевого синдрома используют релаксанты гладкой мускулатуры, включающие несколько групп препаратов: антихолинергические средства — М-холиноблокаторы (препараты красавки, платифиллин, Метацин и т. п., в связи с выраженными побочными системными эффектами сфера применения ограничена), Бускопан (в отличие от предыдущих не проникает через гематоэнцефалический барьер и имеет низкую — 8–10% — системную биодоступность); миотропные спазмолитики: неселективные (дротаверин, отилония бромид и др.) и селективные — Мебеверина гидрохлорид [2, 5, 8].
Препаратами выбора для патогенетической терапии больных с функциональными заболеваниями билиарного тракта, безусловно, являются средства, селективно релаксирующие гладкую мускулатуру органов пищеварения, в частности мебеверин [2, 5, 8]. Преимуществом препарата является релаксирующая селективность в отношении сфинктера Одди, в 20–40 раз превышающая эффект папаверина. Мебеверин оказывает нормализующее воздействие на мускулатуру кишечника, устраняя функциональный дуоденостаз, гиперкинез, спазм, не вызывая развитие нежелательной гипотонии. Препарат у данной категории пациентов может применяться длительно, курсами в дозе 200 мг 2 раза в день.
Для лечения синдромов мальдигестии и мальабсорбции назначают препараты панкреатина (Микразим, Креон, Панзинорм форте-Н, Панцитрат и другие).
Лечение синдрома избыточного бактериального роста в кишечнике
При наличии микробной контаминации тонкой кишки необходимо проведение деконтаминирующей терапии (невсасывающиеся кишечные антибиотики — рифаксимин, или кишечные антисептики (нитрофуранового ряда — Энтерофурил, Эрсефурил, фторхинолоны и др.) с одномоментным и/или последовательным применением пробиотиков и пребиотиков (Хилак форте, Лактулоза), лекарственных препаратов на основе пищевых волокон — Псиллиум и др.). Применение про- и пребиотических препаратов улучшает метаболизм желчных кислот, стимулирует регенерацию поврежденных деконъюгированными желчными кислотами эпителиоцитов кишечной стенки [3, 11].
При наличии билиарной недостаточности назначают препараты УДХК (Урсосан). Применение препаратов в суточной дозе 10–15 мг/кг массы тела уменьшает степень билиарной недостаточности и выраженность дисхолии.
Фармакологические эффекты УДХК (Урсосана) разносторонни. Относительно рассматриваемой проблемы особое значение имеют следующие ее свойства. В первую очередь, это гидрофильность и отсутствие токсических свойств. УДХК вытесняет желчные кислоты, обладающие повреждающим действием на слизистые оболочки. При систематическом приеме УДХК становится основной желчной кислотой в сыворотке крови и составляет около 48% общего количества желчных кислот в крови, происходит дозозависимое увеличение ее доли в пуле желчных кислот до 50–75%. Это происходит, например, вследствие конкурентного захвата рецепторами желчных кислот в подвздошной кишке или за счет индукции холереза, богатого бикарбонатами, что приводит к увеличению пассажа желчи и повышенному выведению токсичных желчных кислот через кишечник. УДХК не оказывает негативного влияния на клетки (мицеллы УДХК практически не растворяют мембраны). Цитопротективные свойства УДХК имеют большое значение также с точки зрения защиты слизистой оболочки желудочно-кишечного тракта. В экспериментальных условиях УДХК продемонстрировала антиоксидантный эффект [4, 13]. Помимо этого, применение УДХК позволяет профилактировать развитие избыточного бактериального роста в кишечнике. Своевременная и правильная оценка клинической симптоматики с применением современных методов диагностики дисфункции сфинктера Одди, назначение адекватной комплексной терапии позволяют значительно улучшить самочувствие и качество жизни данной категории пациентов.
Литература
- Ардатская М. Д. Функциональные расстройства билиарного тракта (определение, классификация, диагностические и лечебные подходы) // Справочник поликлинического врача. 2010. № 7.
- Ильченко А. А. Эффективность мебеверина гидрохлорида при билиарной патологии // РМЖ. 2003. № 4.
- Ильченко А. А. Желчнокаменная болезнь. М.: Анахарсис, 2004. 200 с.
- Лапина Т. Л., Картавенко И. М. Урсодезоксихолевая кислота: влияние на слизистую оболочку верхних отделов желудочно-кишечного тракта // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2007. № 6.
- Косюра С. Д., Федоров И. Г., Ильченко Л. Ю. Применение дюспаталина в комплексной терапии функциональных расстройств билиарного тракта и дисфункции сфинктера Одди // Consilium Medicum. Гастроэнтерология. 2010. № 2.
- Лоранская И. Д., Вишневская В. В., Малахова Е. В. Билиарные дисфункции — принципы диагностики и лечения // РМЖ. 2009. № 4.
- Минушкин О. Н. Функциональные расстройства кишечника и желчевыводящих путей. Лечебные подходы, выбор спазмолитика // Лечащий Врач. 2012. № 2.
- Топорков А. С. Эффективность селективных миотропных спазмолитиков для купирования абдоминальной боли // РМЖ. 2011. № 28.
- Allen A., Flemstrom G. Gastroduodenal mucus bicarbonate barrier: protection against acid and pepsin // Am. J. Physiol. Cell Physiol. 2005. Vol. 288. P. 1–19.
- Drossman D. A. The Functional Gastrointestinal Disorders and the Rome III Process // Gastroenterology. 2006; 130 (5): 1377–1390.
- Jenkins D. J. A., Kendall C. W. C., Vuksan V. Inulin, Oligofructose and Intestinal Function // J. Nutr. 1999. Vol. 129. 1431 S–1433 S.
- Edwards C. A., Parrett A. M. Intestinal flora during the first months of life: new perspectives // British Journal of Nutrition. 2002. 88, Suppl.1. S11–S18.
- Kawamura T., Koizimi F., Ishimori A. Effect of ursodeoxycholic acid on water immersion resistant stress ulcer of rats // Nippon Shokakibyo Gakkai Zasshi. 1989. Vol. 86. P. 2378–2388.
- Stein H. J., Kauler W. K., Feussner H., Siewert J. R. Bile acids as component of the duodenogastric refluate: detection, relationship to bilirubin, mechanism of injury, and clinical relevance // Hepatogastroenterology. 1999. Vol. 46. P. 66–73.
Статья опубликована в журнале Лечащий Врач
материал MedLinks.ru







