Содержание статьи
Бета-адреноблокаторы — возможности оптимизации терапии хронической сердечной недостаточности в амбулаторных условиях
Е. С. Жубрина
Ф. Т. Агеев, доктор медицинских наук, профессор
ИКК им. А. Л. Мясникова ФГБУ РКНПК МЗ РФ, Москва
Положительное влияние терапии бета-адреноблокаторами на течение и прогноз хронической сердечной недостаточности (ХСН), одного из самых распространенных, прогрессирующих и прогностически неблагоприятных заболеваний сердечно-сосудистой системы, многократно было продемонстрировано в крупных мультицентровых рандомизированных исследованиях, что позволило отнести их к IА классу доказанности. Однако это утверждение не может быть отнесено ко всему классу препаратов, а касается лишь тех представителей, которые доказали свою клиническую эффективность в таких исследованиях, как CIBIS II, MERIT-HF, SENIORS, COPERNICUS, что в свою очередь позволило разграничить так называемые «рекомендованные» и «нерекомендованные» для лечения ХСН бета-адреноблокаторы [1, 2]. К первым в итоге были отнесены карведилол, бисопролол, небиволол и метопролола сукцинат. Эффективность же других препаратов в отношении ХСН не доказана или ставится под сомнение в связи с недостаточностью данных по этому вопросу.
В реальной клинической практике частота назначения бета-адреноблокаторов до сих пор остается неприемлемо низкой и не превышает 70% [3]. Но даже если бета-адреноблокатор все же назначен больному с сердечной недостаточностью, то в подавляющем большинстве случаев выбор падает на препараты, эффективность которых при ХСН не доказана или сомнительна (чаще всего атенолол или метопролола тартрат). В России, как и в Европе, процент больных с сердечной недостаточностью, принимающих «рекомендованные» бета-адреноблокаторы, не превышает 30% [4, 5].
Повышение приверженности врачей принятым рекомендациям, в том числе и в отношении назначения рекомендованных для лечения ХСН бета-адреноблокаторов вместо препаратов без доказанной эффективности, в рамках повышения качества медицинской помощи является одним из перспективных направлений в современной медицине. Однако недостаток исследований по прямому непосредственному сопоставлению различных препаратов одного класса оставляет открытым вопрос об оправданности такой тактики медикаментозной терапии в клинической практике.
Кроме того, наблюдаются существенные различия по влиянию на сердечно-сосудистую систему даже между представителями данного класса лекарственных препаратов с доказанной эффективностью, что диктует необходимость разработки тактики лечения больных, основанной на определении предпочтительности препарата в зависимости от клинической ситуации.
В этом аспекте целью настоящей работы стало оценить клинический, гемодинамический и нейрогуморальный эффекты перевода больных с ХСН с терапии «нерекомендованными к применению» бета-адреноблокаторами (атенолол или метопрола тартрат) на бисопролол или небиволол в амбулаторной практике, а также сравнить эффективность небиволола и бисопролола у больных ХСН.
Материалы и методы исследования
В исследование было включено 67 больных старше 18 лет с умеренно выраженной ХСН (II–III функциональный класс по классификации Нью-Йоркской Ассоциации кардиологов (NYHA), вне зависимости от фракции выброса левого желудочка по данным эхокардиографии (Эхо-КГ), и находящихся на длительной (более 6 месяцев) стандартной терапии, рекомендованной для лечения ХСН, в отсутствие декомпенсации в течение 2 недель до включения в исследование. Перевод больных на исследуемый препарат осуществлялся на этапе рандомизации. В исследование не включались больные с недавно перенесенным обострением сердечной недостаточности (менее чем за 2 недели до начала исследования); значимыми поражениями клапанов сердца; констриктивным перикардитом или гемодинамически значимым перикардиальным выпотом; гипертрофической или рестриктивной кардиомиопатией; легочным сердцем или другими заболеваниями, связанными с изолированной правожелудочковой недостаточностью; острым коронарным синдромом, инсультом или реваскуляризацией миокарда менее чем за 3 месяца до включения больного в исследование; сахарным диабетом 2-го типа, требующим инсулинотерапии, или сахарным диабетом 1-го типа; с другими состояниями, сопровождающимися повышением активности маркеров фиброза (заболевания соединительной ткани, онкологические, ревматологические заболевания, выраженный фиброз печени, легких).
Всем больным, вошедшим в исследование, исходно, а также спустя 6 месяцев с момента начала терапии было проведено клиническое и инструментальное обследование, включавшее в себя определение функционального класса (ФК) ХСН с измерением дистанции, преодолеваемой больными в течение 6-минутного теста ходьбы, оценку тяжести клинического состояния (шкала оценки клинического состояния, ШОКС) и качества жизни (Миннесотского вопросника качества жизни), трансторакальную Эхо-КГ и определение уровня N-концевого фрагмента предшественника мозгового натрийуретического пептида (NT-proBNP), а также маркеров синтеза (С-концевого пропептида проколлагена I типа, CICP) и распада (С-концевого телопептида коллагена I, CITP) коллагена I типа в сыворотке крови. Уровень NT-proBNP в плазме был определен методом электрохемилюминисценции с помощью анализатора Elecsys 1010 фирмы Roche Hitachi. Для определения содержания маркеров фиброза также в обоих случаях применялся ферментный иммунологический метод исследования. При этом для определения уровня CICP использовались наборы реактивов фирмы Quidel (CICP enzyme immunoassay), а для CITP — фирмы Roche Diagnostics (Elecsys бета-CrossLaps/serum assay).
Статистическую обработку полученных результатов проводили с помощью пакета программ Statistica 6.0 (StatSoft, USA) и SPSS 11.5 for Windows (SPSS Inc.USA) и использованием стандартных алгоритмов вариационной статистики.
Исследование состояло из периодов скрининга, рандомизации, индивидуального подбора доз бисопролола или небиволола и периода длительного наблюдения. Продолжительность исследования составила 6 месяцев с момента приема первой дозы одного из исследуемых препаратов. Больные были рандомизированы: 32 — в группу небиволола (Небилет, фармацевтическая фирма «Берлин Хеми/ А. Менарини») и 35 — в группу бисопролола (Конкор, фармацевтическая фирма «Никомед»). Титрование дозы препаратов начиналось с 1,25 мг с последующим возможным, при хорошей переносимости, двукратным увеличением дозы препарата до рекомендованного уровня 10 мг каждые 2–4 недели. Критериями хорошей переносимости являлись стабильное клиническое состояние, нормальной уровень артериального давления (АД) и частоты сердечных сокращений (ЧСС), отсутствие побочных эффектов. При развитии гипотонии (систолическое АД менее 80 мм рт. ст) и выраженной брадикардии (ЧСС менее 50 ударов в минуту) доза бета-адреноблокатора уменьшалась до предыдущей. Коррекция доз других препаратов, в т. ч. мочегонных, ингибиторов ангиотензинпревращающего фермента (АПФ) или блокаторов рецепторов ангиотензина II, антагонистов альдостерона, сердечных гликозидов, допускалась только в случае прогрессирования ХСН или тенденции к артериальной гипертензии.
Средняя доза препаратов составила: 6,48 ± 3,34 мг для небиволола и 6,78 ± 3,34 мг для бисопролола. Уровень целевой дозы был достигнут у 48% больных.
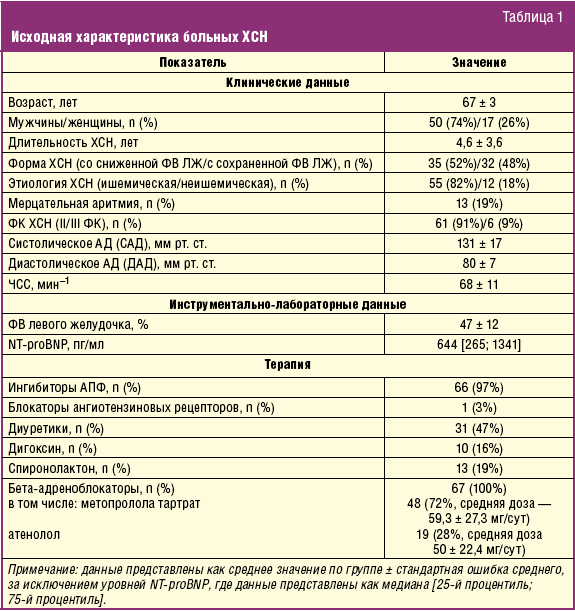
Результаты
Как следует из табл. 1, контингент больных, включенных в исследования, соответствовал типичному контингенту больных амбулаторной практики: средний возраст пациентов составил 67 лет, среди больных несколько преобладали мужчины, доминировала ишемическая этиология сердечной недостаточности, у около 20% больных имела место мерцательная аритмия. Большинство пациентов находились во II ФК ХСН (по NYHA). При этом по данным Эхо-КГ около половины больных имели сохраненную фракцию выброса (ФВ) левого желудочка. Обращает на себя внимание исходно невысокая средняя ЧСС. Однако это объясняется, прежде всего, довольно длительной предшествующей терапией бета-адреноблокаторами, пусть даже без доказанной эффективности.
Влияние перевода больных ХСН с терапии нерекомендованными к применению бета-адреноблокаторов на небиволол и бисопролол на клинико-функциональный статус, качество жизни, ФВ левого желудочка и уровень NT-proBNP представлено в табл. 2.
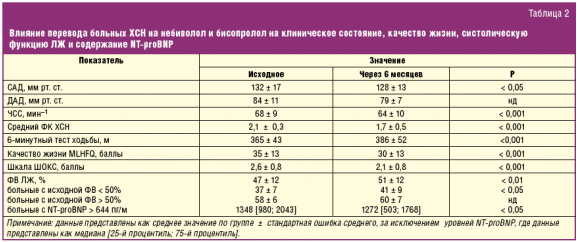
За время исследования снижения ФК ХСН (по классификации NYHA) удалось достичь у 22 (35%) больных. Ухудшение ФК было отмечено только у одного пациента. Перевод больных ХСН на небиволол или бисопролол сопровождался достоверным уменьшением среднего ФК ХСН и снижением тяжести клинического состояния, а также увеличением дистанции 6-минутного теста ходьбы. Кроме того, перевод пациентов на исследуемые препараты ассоциировался с улучшением качества жизни. Несмотря на то, что среди всех больных содержание NT-proBNP практически не изменилось, в подгруппе больных с исходно высоким содержанием этого пептида (то есть превышающим медиану — 644 пг/мл) было отмечено достоверное его снижение (р < 0,05 по сравнению с исходным значением).
На фоне проводимой терапии имело место клинически незначимое снижение уровня артериального давления и достоверное урежение ЧСС в среднем на 4 мин-1, что составило 6,4%.
Связь между снижением ЧСС и динамикой основных клинических и инструментально-лабораторных показателей при переводе больных ХСН на небиволол и бисопролол представлена в табл. 3. Учитывая имевшее место дополнительное снижение ЧСС (хотя и незначительное, всего на 4 удара в мин), отмечавшееся при переводе больных на небиволол и бисопролол, нами был проведен корреляцонный анализ связи (ассоциации) между дополнительным снижением ЧСС и динамиками функционального класса, дистанции 6-минутного теста ходьбы, уровня NT-proBNP и фракции выброса левого желудочка. Достоверной связи между снижением ЧСС и динамикой основных клинических и лабораторно-инструментальных показателей установлено не было.
Сравнительное влияние небиволола и бисопролола на клинико-функциональный статус, качество жизни, ФВ левого желудочка, уровень NT-proBNP и баланс маркеров синтеза и распада коллагена I типа у больных ХСН представлено в табл. 4.

За время исследования между группами небиволола и бисопролола отсутствовали какие-либо достоверные различия по влиянию на клиническое состояние, качество жизни, функцию левого желудочка, скорость распространения пульсовой волны (СПВ) и уровень NT-proBNP. Единственным исключением явилось достоверно более выраженное снижение уровня маркера синтеза коллагена I типа (СICP) у больных в группе небиволола по сравнению с группой бисопролола: на –12,8% против –1,4% соответственно, р < 0,01 (рис.). Влияние на уровень маркера распада коллагена С-концевого телопептида коллагена I (СITP) не было отмечено ни в одной из групп терапии.
Следует отметить, что с целью более точного описания состояния коллагенового обмена нами были проанализированы не только уровни каждого из маркеров фиброза, но и рассчитаны отношения СIСP/CITP для каждой группы больных. Снижение этого соотношения в динамике более точно свидетельствует в пользу уменьшения интенсивности фиброобразования и наоборот. При этом только на фоне терапии небивололом имело место достоверное снижение данного отношения в сторону его уменьшения.

Обсуждение полученных результатов
На сегодняшний день эффективность основных классов лекарственных препаратов, рекомендованных для лечения ХСН, не вызывает сомнения, а показания к их применению четко определены. Однако результаты лечения все еще остаются неудовлетворительными. В этом аспекте данное исследование представляется очень актуальным, являясь, по сути, моделью тактики ведения больных ХСН в повседневной практике. Действительно, на сегодняшний день бета-адреноблокаторы относятся к основным средствам лечения ХСН. Однако, как нами было указано ранее, в реальных клинических условиях больные если и получают терапию бета-адреноблокаторами, то предпочтение отдается, как правило, препаратам, эффективность которых в настоящее время не доказана (метопролола тартрат, атенололол) [5]. Таким образом, перед врачом встает очень важный с практической точки зрения вопрос: насколько положительное действие бета-адреноблокаторов, доказанное в крупных исследованиях, можно экстраполировать на весь класс этих препаратов? Если да, то больного с ХСН по идее можно лечить любым бета-адреноблокатором, рассчитывая при этом на «класс-эффект» равно эффективных препаратов. Если же способность бета-адреноблокаторов улучшать прогноз зависит прежде всего от фармакокинетических и фармакодинамических особенностей отдельных представителей этого класса препаратов, то в таком случае необходимо переводить всех больных с сердечной недостаточностью на прием препаратов с доказанной эффективностью. К сожалению, на сегодняшний день мы располагаем данными лишь единичных исследований по непосредственному сопоставлению различных бета-адреноблокаторов у больных с ХСН, в том числе сравнению рекомендованных и нерекомендованных к применению бета-адреноблокаторов. Так, в небольшом исследовании S. Nodari и соавт. показали, что прием небиволола у больных с артериальной гипертензией и диастолической сердечной недостаточностью сопровождался более выраженным улучшением допплеровских показателей трансмитрального диастолического кровотока и увеличением потребления кислорода на пике нагрузки по сравнению с атенололом [6]. В 2003 г. были опубликованы данные исследования COMET — крупнейшего на сегодняшний день проспективного испытания по сравнению различных бета-адреноблокаторов у больных с сердечной недостаточностью. В этом многоцентровом исследовании применение карведилола — альфа-1-, бета-1-, бета-2-блокатора — у больных с хронической сердечной недостаточностью II–III ФК сопровождался достоверным снижением риска смерти на 17% по сравнению с метопролола тартратом (метопрололом короткого действия) [7]. А. Go и соавт. в рамках ретроспективного анализа оценили риск смерти у 8 тысяч больных, которым после госпитализации по поводу обострения сердечной недостаточности были назначены те или иные бета-адреноблокаторы [8]. Риск смерти оказался ниже у больных, принимавших атенолол или карведилол по сравнению с больными, находившимися на терапии метопролола тартратом или вообще не принимавшими бета-адреноблокаторы. В другом ретроспективном исследовании с участием 12 тысяч больных с сердечной недостаточностью J. Kramer и соавт. не выявили достоверных различий между рекомендованными и нерекомендованными к применению бета-адреноблокаторов по влиянию на однолетнюю выживаемость [9].
В рамках настоящей работы нами впервые была проведена попытка комплексной оценки целесообразности перевода больных ХСН на рекомендованные при этом заболевании бета-адреноблокаторы небиволол или бисопролол. Результаты настоящего исследования позволили продемонстрировать, что такая тактика ведения больных в амбулаторных условиях полностью оправдана и позволяет улучшить не только качество жизни больных ХСН, но и их функциональное состояние (снижение ФК ХСН, увеличение дистанции, преодолеваемой пациентами во время 6-минутного теста ходьбы). Кроме того, перевод больных на небиволол или бисопролол позволяет добиться роста сократимости миокарда и снижения уровня NT-proBNP у больных с исходно высоким его содержанием. Последний не только является независимым предиктором прогноза у больных ХСН, но высоко коррелирует с тяжестью этого заболевания, отражая степень дисфункции левого желудочка [10–12]. При этом показано, что чем тяжелее дисфункция левого желудочка, тем большего эффекта можно ожидать от терапии бета-адреноблокаторами [13]. Отсутствие же достоверной динамики в подгруппе больных с исходно более низким уровнем NT-proBNP, вероятнее всего, обусловлено тем, что на фоне хорошей базисной терапии ХСН у больных со стабильным нетяжелым течением заболевания вклад оптимизации терапии бета-адреноблокаторами будет незначительным.
Принято считать, что снижение ЧСС является главным фактором улучшения клинического состояния больных ХСН, а степень снижения ЧСС высоко коррелирует с прогнозом у этих больных [14]. Это, с одной стороны, не позволяет исключить, что достигнутые в ходе исследования положительные эффекты небиволола и бисопролола связаны именно с пусть незначительным, однако достоверным снижением ЧСС в среднем на 4 уд./мин–1. Тем не менее, исходная средняя частота сердечных сокращений в большинстве проведенных ранее клинических исследованиях, демонстрирующих преимущества хронотропного влияния бета-адреноблокаторов при ХСН, превышала 80 мин–1, в то время как в настоящем исследовании она не достигла 70 мин–1. Кроме того, результаты такого крупного исследования, как BEAUTIFUL, также продемонстрировали, что данная закономерность в большей степени справедлива в отношении больных, исходное ЧСС которых превышает 70 мин–1 [15]. При этом в настоящее время остается спорной целесообразность дотитрования дозы бета-адреноблокаторов, если до этого уже было достигнуто значимое снижение ЧСС. Тот факт, что в нашем случае исходное значение ЧСС было относительно низким (среднее значение составило 68 мин–1), свидетельствует о том, что проводимая ранее терапия нерекомендованными к применению бета-адреноблокаторами уже привела к значительному снижение уровня ЧСС. Тем не менее, нами был проведен корреляционный анализ связи между снижением ЧСС и основными клинико-лабораторными показателями (снижение среднего ФК ХСН, увеличение дистанции 6-минутного теста ходьбы, увеличение ФВ левого желудочка и снижение уровня NT-proBNP) у больных ХСН при переводе на небиволол или бисопролол. Отсутствие достоверности в данном случае указывает, прежде всего, на то, что исследуемые препараты оказывали собственное влияние на течение сердечной недостаточности, не связанное с их хронотропными эффектами.
Другим крайне важным с практической точки зрения вопросом, поставленным нами в рамках проводимого исследования, была сравнительная эффективность в отношении ХСН двух представителей II и III поколений бета-адреноблокаторов бисопролола и небиволола. Бисопролол представляет собой «чистый» высокоселективный блокатор бета-1-адренорецепторов, в то время как небиволол сочетает в себе не только наиболее селективные среди всех представителей этого класса бета1-блокирующие, но и NO-моделирующие свойства. Именно с наличием у небиволола способности активировать NO-синтетазу и, таким образом, приводить к повышению синтеза оксида азота эндотелиальными клетками как сосудов, так и эндокарда, связывают в настоящее время его выраженное положительное влияние на функцию эндотелия и снижение интенсивности оксидативного стресса [16, 17]. А наибольшая селективность в отношении бета-1-рецепторов позволяет наиболее эффективно использовать этот препарат у больных с высоким риском развития побочных эффектов бета-адренергической блокады, таких как развитие бронхоспазма, метаболического синдрома, дислипидемии и т. д. [18]. Эффективность применения обоих препаратов у больных ХСН основывается на результатах двух крупных мультицентровых плацебо-контролируемых рандомизированных исследований CIBIS II и SENIORS. В исследование CIBIS II с бисопрололом было включено 2647 пациентов с тяжелой ХСН III–IV ФК по NYHA и ФВ левого желудочка, не превышающей 35% [19]. Пациенты были рандомизированы в группу терапии бисопрололом или плацебо. Первичной конечной точкой явилась общая смертность, вторичные конечные точки включали в себя госпитализацию по любому поводу, смертность по сердечно-сосудистым причинам и комбинацию сердечно-сосудистой смертности и госпитализации по сердечно-сосудистым причинам. Исследование было приостановлено досрочно в связи с достижением достоверных положительных результатов в группе бисопролола. При среднем периоде наблюдения 1,3 года было показано, что присоединение к терапии бисопролола достоверно снижало общую смертность на 34% (11,8% в группе бисопролола против 17,3% в группе плацебо), а внезапную на 44% (3,6 против 6,3%). Кроме этого, уменьшалось на 20% количество госпитализаций и на 29% смертей по сердечно-сосудистой причине.
В другое плацебо-контролируемое многоцентровое исследование SENIORS с небивололом была включена особая группа пациентов — 2111 больных ХСН старше 70 лет при средней длительности наблюдения в 21 месяц [20]. Несмотря на то, что терапия исследуемым препаратом не продемонстрировала достоверного снижения смертности, она была сопряжена с достоверным снижением комбинированного показателя госпитализаций и смертей на 14%. Кроме того, имело место весьма значительное снижение риска внезапной смерти на 33%, а также достоверно на 16% уменьшились риск смерти и число госпитализации из-за сердечно-сосудистых осложнений. Исследование критиковали в связи с отсутствием достоверного снижения смертности. Однако необходимо принять во внимание, что помимо «возрастной» группы пациентов в исследование включались больные с фракцией выброса левого желудочка > 35%, доля которых составила 36%, и в большинстве случаев больные были не очень тяжелыми: 57% имели ХСН II ФК по NYHA. Проведенный впоследствии дополнительный ретроспективный анализ в подгруппе больных в возрасте 70–75 лет и при исходной ФВ левого желудочка менее 35% показал снижение риска смертности на 38%, что является сопоставимым с другими бета-адреноблокаторами с доказанной эффективностью. Полученные результаты позволили экспертам Европейского и Российского обществ кардиологов включить небиволол в стандарты лечения ХСН, в том числе и у особой группы больных пожилого возраста.
Нами в рамках представленного исследования впервые была проведена попытка прямого клинического сравнения небиволола и бисопролола. И было показано, что оба препарата имеют сопоставимую эффективность в отношении улучшения клинического состояния, качества жизни, повышения толерантности к нагрузкам, функционального состояния миокарда левого желудочка и динамики уровня NT-proBNP у больных ХСН за исключением влияния на маркеры баланса коллагена I типа. Действительно, только небиволол, но не бисопролол, продемонстрировал способность ингибировать процессы синтеза миокардиального коллагена, что отразилось в достоверном снижении уровня маркера синтеза коллагена I CICP, а также соотношения маркеров синтеза/распада коллагена — CICP/CITP.
Результаты настоящего исследования не показали значимого влияния терапии «чистого» бета-адреноблокатора бисопролола на содержание маркеров обмена коллагена I типа. Тем не менее, дизайн исследования не позволил полностью определить роль бета-адренергической блокады в регуляции синтеза коллагена, так как препараты назначались не на «чистом» от бета-адреноблокаторов фоне, а вместо длительно (более 6 месяцев) принимаемых различных препаратов этого класса в рамках стандартной терапии ХСН. С другой стороны, полученное нами в ходе исследования значимое снижение уровня маркера синтеза коллагена CICP на фоне терапии небивололом, а также динамика соотношения CICP к CITP четко указывают на, как минимум, преимущество этого препарата, определяемое, по всей видимости, прежде всего его способностью увеличивать высвобождение NO, который, как было экспериментально показано, является достаточно мощным ингибитором синтеза коллагена [21–23]. Этот факт нашел подтверждение и in vivo, демонстрируя, что небиволол, в отличие от метопролола, способен улучшать не только эндотелий-зависимую вазодилатацию, дисфункцию левого желудочка и выживание мышей в постинфарктном периоде, но и оказывает более выраженный эффект на гипертрофию кардиомиоцитов и интерстициальный фиброз по данным гистоморфометрического анализа [24]. В этой связи небиволол представляется уникальным препаратом по отношению к влиянию на синтез коллагена, так как сочетает в себе бета-блокирующие и NO-модулирующие свойства. Этот факт, вероятно, будет иметь особое значение, прежде всего у больных ХСН с сохранной систолической функцией левого желудочка, сопровождающейся гипертрофией миокарда и выраженной диастолической дисфункцией левого желудочка. Таким образом, выявленное в настоящее время различие между небивололом и бисопрололом способности подавлять синтез коллагена может стать основой для усовершенствования рекомендаций по лечению больных ХСН с учетом состояния процессов обмена коллагена в миокарде и антифибротических свойств бета-адреноблокаторов, используемых в лечении таких больных.
Заключение
Результаты проведенного исследования показали целесообразность незамедлительного перевода больных ХСН в условиях амбулаторной практики с терапии нерекомендованными к применению бета-адреноблокаторами на небиволол или бисопролол. При этом, несмотря на продемонстрированную сопоставимую эффективность обоих препаратов в отношении клинико-функционального, гемодинамического и нейрогуморального статуса больных ХСН, учитывая выявленный антифибротический эффект, назначение небиволола является более предпочтительным у пациентов ХСН в условиях повышенного фиброобразования в миокарде.
Литература
- Национальные рекомендации ВНОК И ОССН по диагностике и лечению ХСН (третий пересмотр) // Сердечная недостаточность. 2010; 11 (57); 3–62.
- ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012. The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology // Eur Heart J. 2012; 33; 1787–1847.
- De Groote P., Isnard R., Assyag P., Clerson P., Ducardonnet A., Galinier M., Jondeau G., Leurs I., Thebaut J., Komajda M. Is the gap between guidelines and clinical practice in heart failure treatment being filled? Insights from the IMPACT RECO survey // Euro J Heart Fail. 2007; 9 (12); 1205–1211.
- Shah S. M., Carey I. M., DeWilde S. et al. Trends and inequities in beta-blocker prescribing for heart failure // Brit J Gen Pract. 2008; 58; 862–869.
- Смирнова Е. А., Якушин С. С. Анализ пульс урежающей терапии хронической сердечной недостаточности. Сборник тезисов «Сердечная`2012 недостаточность», 2012; 52 c.
- Nodari S., Metra M., Dei Cas L. Beta-blocker treatment of patients with diastolic heart failure and arterial hypertension. A prospective, randomized, comparison of the long-term effects of atenolol vs. nebivolol // Eur J Heart Fail. 2003; 5; 621–627.
- Poole-Wilson P., Swedberg K., Cleland J. et al. for the COMET Investigators. Comparison of carvedilol and metoprolol on clinical outcomes in patients with chronic heart failure in the Carvedilol Or Metoprolol European Trial (COMET); randomised controlled trial // Lancet. 2003; 362; 7–13.
- Go A., Yang J., Gurwitz J. et al. Comparative effectiveness of different beta-adrenergic antagonists on mortality among adults with heart failure in clinical practice // Arch Intern Med. 2008; 168; 2415–2421.
- Kramer J., Curtis L., Dupree C. et al. Comparative effectiveness of бета-blockers in elderly patients with heart failure // Arch Intern Med. 2008; 168; 2422–2428.
- Lee S., Stevens T., Sandberg S. et al. The potential of brain natriuretic peptide a biomarker for New York Heart Association class during the outpatient treatment of heart failure // J Card Fail. 2002; 8; 149–154.
- Koglin J., Pehlivanli S., Shwaiblmair M. et al. Role of brain natriuretic peptide in risk stratification of patient with congestive heart failure // J Am Coll Cardiol. 2001; 38; 1934–1941.
- Betenncourt P. Nt-proBNP and BNP; biomarker for heart failure management // Eur J Heart Fail. 2004; 6; 359–364.
- Olsson J., Swedberg K., Cleland J. et al. Prognostic importance of plasma NT-pro BNP in chronic heart failure in patients treated with a бета-blocker; Results from the Carvedilol Or Metoprolol European Trial (COMET) trial // Eur J Heart Fail. 2007; 9; 795–801.
- McAlister F. A., Wiebe N., Ezekowitz J. A., Leung A. A., Armstrong P. W. Meta-analysis; beta-blocker dose, heart rate reduction, and death in patients with heart failure // Ann Intern Med. 2009; 150 (11); 784–794.
- Fox K., Ford I., Steg G. et al. On behalf of the BEAUTIFUL investigators. Heart rate as a prognostic risk factor in patients with coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL); a subgroup analysis of a randomized controlled trial // Lancet. 2008; 372; 817–821.
- Бубнова М. Г. Плейотропные эффекты суперселективного b1-блокатора небиволола при лечении артериальной гипертонии и ее осложнений // Cons. Med. Репринт. 2004; с. 3–10.
- Jgnarro L. J. Experimental evidences of nitric oxide-dependent vasodilatatory activity of nebivolol, a third-generation beta-blocker // Blood Press Suppl. 2004; 1; 2–16.
- Мареев В. Ю., Арболишвили Г. Н. Проблемы и перспективы бета-адреноблокаторов в ХХI веке; возможные позиции небиволола // Сердце. 2007; 6 (5); 240–249.
- CIBIS-II Investigators and Committees. The Cardiac Insufficiency Bisoprolol Study II (CIBIS-II); a randomised trial // Lancet. 1999; 353; 9–13.
- Flather M., Shibata M. et al. Randomized trial to determine the effect of nebivolol on mortality and cardiovascular hospital admission in elderly patients with heart failure (SENIORS) // Eur Heart J. 2005; 26; 215–225.
- Kolpakov V., Gordon D., Kulik T. Nitric oxide-generating compounds inhibit total protein and collagen synthesis in cultured vascular smooth muscle cells // Circ Res. 1995; 76; 305–309.
- Rizvi M., Myers P. Nitric oxide modulates basal and endothelin-induced coronary artery vascular smooth muscle cell proliferation and collagen levels // J Cell Mol Cardiol. 1997; 29; 1779–1789.
- Westermann D., Riad A., Richter U. et al. Enhancement of the endothelial NO synthase attenuates experimental diastolic heart failure // Baisic Reaserch in Cardiology. 2009; 104 (5); 499–509.
- Sorrentino S. A., Doerries C., Mohmand W. et al. Abstract 1869; Effect of Nebivolol vs. Metoprolol on Endothelial Function, Endothelial Progenitor Cell Mobilization and Left Ventricular Remodeling and Dysfunction Early After Myocardial Infarction Circulation. 2006; 114; II.
Статья опубликована в журнале Лечащий Врач
материал MedLinks.ru






