Введение
Хроническая обструктивная болезнь легких (ХОБЛ) и бронхиальная астма (БА) — бронхообструктивные заболевания (БОЗ), которые являются распространенными причинами заболеваемости и смертности в общей популяции. Многочисленные исследования демонстрируют высокую встречаемость сердечно-сосудистой патологии среди пациентов с ХОБЛ и БА [1–3]. Среди лиц пожилого возраста ХОБЛ выявляется у каждого 4-го больного артериальной гипертензией (АГ) [4], которая является одним из ведущих факторов риска развития таких сердечно-сосудистых заболеваний (ССЗ), как ишемическая болезнь сердца (ИБС), нарушения ритма сердца (НРС), хроническая сердечная недостаточность (ХСН), а ее распространенность в России, по данным ЭССЕ-РФ3, достигает 53,9% взрослого населения [5]. ССЗ широко распространены и среди пациентов с БА, а их сочетание способствует более частым обострениям и снижению уровня медикаментозного контроля БА [6]. Наличие сопутствующих ХОБЛ или БА у кардиологических пациентов может затруднять выбор фармакотерапии ССЗ. В связи с актуальностью проблемы в некоторых клинических руководствах по ведению как ССЗ, так и БОЗ появились разделы, посвященные ведению пациентов с сочетанной кардиореспираторной патологией. Например, в ведущем документе Глобальной стратегии диагностики, лечения и профилактики ХОБЛ1 особое внимание уделено внелегочным сопутствующим заболеваниям, в особенности сердечно-сосудистой патологии, что обусловлено ее доказанным влиянием на тяжесть течения и прогноз при ХОБЛ. Наличие сопутствующих БОЗ влияет и на выбор фармакотерапии ССЗ. Так, лечение АГ у больных ХОБЛ сопряжено с риском нежелательных респираторных реакций, в основном бронхообструкции, индуцированной β-адреноблокаторами (ББ) и, реже, ингибиторами ангиотензинпревращающего фермента (иАПФ). Для оптимизации лечения этих пациентов Российским медицинским обществом по артериальной гипертонии (РМОАГ) совместно с Российским респираторным обществом (РРО) были опубликованы рекомендации по диагностике и лечению пациентов с АГ и ХОБЛ [4], согласно которым применение кардиоселективных ББ при стабильном течении ХОБЛ допустимо и обосновано при наличии кардиоваскулярной патологии (ИБС, ХСН, фибрилляция предсердий), требующей их применения в рамках комбинированной фармакотерапии. При этом селективные ББ не только обеспечивают кардиопротекцию, но и способствуют снижению частоты обострений ХОБЛ. Так, метаанализ 20 исследований (n=237 709) показал, что применение ББ у пациентов с ХОБЛ и ССЗ ассоциировано со снижением риска обострений ХОБЛ (отношение шансов (ОШ) 0,76; 95% доверительный интервал 0,62–0,92; p=0,005) и снижением смертности (ОШ 0,50, p<0,00001) [7]. Важным является и их сочетание с базисной терапией ХОБЛ — ингаляционными β2-агонистами, так как кардиоселективные ББ, уменьшая частоту сердечных сокращений (ЧСС), смягчают потенциальные кардиальные побочные эффекты β-агонистов (тахикардию), что позволяет продолжать необходимую бронхолитическую терапию без повышенного риска со стороны ССЗ. В руководствах по лечению ХОБЛ также указывается, что преимущества кардиоселективных ББ при ХСН перевешивают потенциальные риски, даже у пациентов с тяжелой ХОБЛ [8]. Таким образом, назначение кардиоселективных ББ пациентам с ХОБЛ и ССЗ для лечения АГ, в том числе ИБС, НРС, ХСН, является обоснованным. Однако, несмотря на рекомендации и данные многих исследований об их относительной безопасности, лишь 33% пациентов с ХОБЛ, нуждающихся в назначении ББ, получают их на практике [9]. Из-за опасений по поводу потенциальной бронхоконстрикции врачи избегают назначений кардиоселективных ББ при ХОБЛ. Так, в ретроспективном исследовании 1603 пациентов с ХОБЛ и инфарктом миокарда в анамнезе, 55% пациентов, которым были показаны ББ, их недополучали [10]. В другом исследовании было установлено, что 64% пациентов с ИБС без ХОБЛ получали ББ, в то время как среди больных ИБС с ХОБЛ их назначали только 16%. Диагноз ХОБЛ был указан как причина отказа от ББ у 33% пациентов с ССЗ, а врачи некардиологических специальностей назначали ББ на 40% реже при наличии ХОБЛ, несмотря на показания [11]. Все эти исследования указывают на недостаточное назначение селективных ББ в лечении пациентов с кардиореспираторной патологией.
В то же время у больных БА широкое применение кардиоселективных ББ до сих пор ограничено клиническими руководствами, рекомендовано рассматривать их назначение в индивидуальном порядке у каждого отдельного пациента2.
Применение иАПФ у пациентов с АГ и ХОБЛ не рекомендуется в качестве терапии первой линии. Данное ограничение обусловлено риском развития брадикининового кашля — нежелательной лекарственной реакции, способной существенно снижать качество жизни и затруднять своевременную диагностику обострений респираторной патологии. Вместе с тем при условии хорошей переносимости и отсутствии противопоказаний, включение иАПФ в состав комбинированной антигипертензивной терапии представляется допустимым [4]. Препаратами выбора у больных АГ и БОЗ являются антагонисты кальция (АК) и блокаторы ангиотензина II (БРА). Они благоприятно переносятся кардиологическими больными с ХОБЛ и БА, отмечается улучшение сердечно-сосудистых и легочных показателей.
Высокая частота сочетания АГ и БОЗ диктует необходимость разработки алгоритмов, повышающих приверженность врачей актуальным рекомендациям. Для этого необходима проспективная оценка современной врачебной тактики при помощи проведения кардиореспираторного скрининга с ответом на вопрос о структуре назначений кардиотропных препаратов у пациентов в зависимости от наличия БОЗ.
Цель исследования: изучить особенности назначения терапии кардиоселективными ББ, АК, иАПФ и БРА у больных эссенциальной АГ, в том числе с ИБС, НРС, ХСН в сочетании с БОЗ (ХОБЛ и БА) и без БОЗ.
Содержание статьи
Материал и методы
В период с 2017 г. по 2019 г. на базе Института клинической кардиологии им. ак. А.Л. Мясникова ФГБУ «НМИЦК им. ак. Е.И. Чазова» Минздрава России был проведен набор пациентов для участия в проспективном когортном исследовании. Критериям включения соответствовали 1000 больных в возрасте 18 лет и старше с верифицированным диагнозом эссенциальной АГ. Из исследования исключались пациенты в остром периоде инфаркта миокарда, нарушения мозгового кровообращения, с признаками острой респираторной вирусной инфекции, кровохарканьем или массивным легочным кровотечением, а также лица с отягощенным аллергологическим анамнезом (непереносимость сальбутамола) и противопоказаниями к проведению спирометрии.
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good ClinicalPractice) и принципами Хельсинкской декларации. Исследование одобрено локальным этическим комитетом НМИЦК им. ак. Е.И. Чазова Минздрава России по вопросам этики и медицинским исследованиям в клинической кардиологии (протокол № 222). Все участники исследования предоставили информированное согласие.
Всем пациентам выполнено комплексное пульмонологическое обследование, включавшее спирометрию с бронходилатационным тестом при поступлении и выписке. Исследование проводилось в соответствии с рекомендациями Европейского респираторного общества с помощью аппарата Super Spiro (Micro Medical Ltd., Великобритания). Анализировали следующие функциональные параметры: индекс Генслера (отношение объема форсированного выдоха за 1-ю секунду (ОФВ1) к форсированной жизненной емкости легких (ФЖЕЛ), ОФВ1% от должного. Участники, у которых по результатам спирометрии были выявлены отклонения от референтных значений, направлялись на консультацию к пульмонологу для уточнения диагноза и решения вопроса о коррекции либо инициации базисной терапии ХОБЛ и/или БА.
В работе применяли стандартизированные респираторные опросники при поступлении и выписке: опросник CAT3, суммарный балл по которому отражает влияние ХОБЛ на жизнь пациента: 0–10 — незначительное, 11–20 — умеренное, 21–30 — сильное, 31–40 — чрезвычайно сильное; шкала mMRC4, которая оценивает выраженность одышки от 0 (отсутствие, кроме интенсивной нагрузки) до 4 (одышка при минимальной активности).
В первые сутки госпитализации пациентам проводили суточное мониторирование АД (СМАД), оценивали следующие параметры: среднесуточное систолическое АД (ср. сут. САД, мм рт. ст.), среднесуточное диастолическое АД (ср. сут. ДАД, мм рт. ст.), среднесуточная частота сердечных сокращений (ср. сут. ЧСС, в 1 мин).
Статистическая обработка данных. Для проверки статистических гипотез о виде распределения использовали тест Колмогорова — Смирнова. В качестве описательной статистики параметрических параметров использовали среднее значение и стандартное отклонение (M±SD), непараметрических — медиану и квартили (Ме [Q1; Q3]). Для сравнительной статистики использовали критерий Стьюдента. Сравнение переменных, имеющих отклонение от нормального распределения в исследуемых группах, проводили с помощью непараметрического критерия Манна — Уитни. Для выявления взаимосвязей между показателями рассчитывали коэффициент корреляции Пирсона, а при непараметрическом распределении выборки или для качественных признаков — коэффициент ранговой корреляции Спирмена. Уровень значимости для всех использованных критериев р<0,05. Статистическую обработку данных проводили с использованием приложения Microsoft Excel и пакета статистического анализа данных Statistica 10 для Windows (StatSoft Inc., США).
Результаты исследования
При сравнении характеристик групп кардиологических больных (табл. 1) выявлены статистически значимые различия по возрасту, полу и сопутствующей патологии.
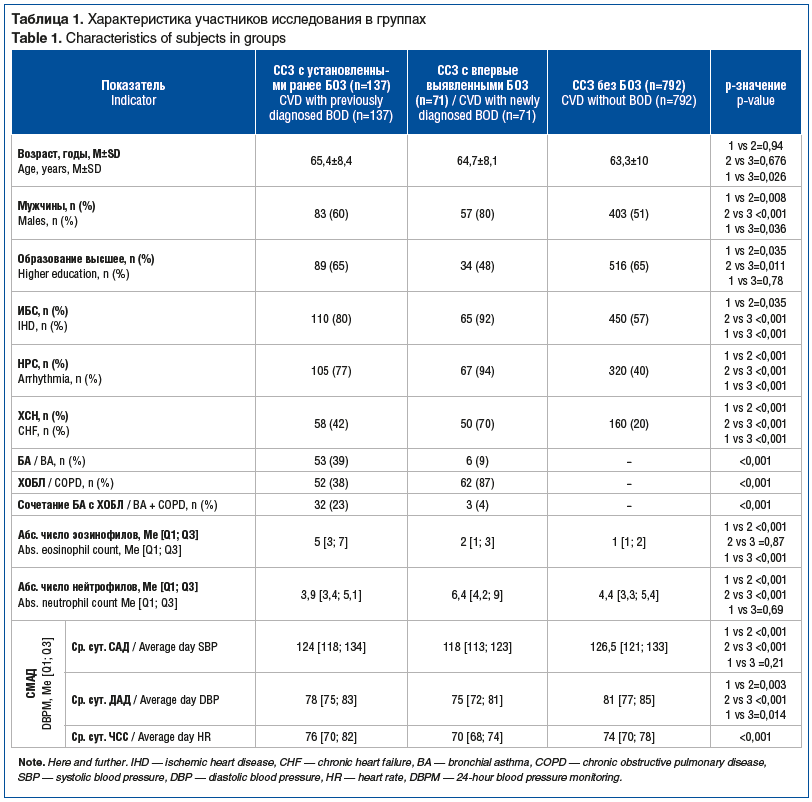
Пациенты без БОЗ были достоверно моложе пациентов с БОЗ. В группе пациентов с ССЗ и впервые диагностированными БОЗ достоверно преобладали мужчины, в этой группе также реже других встречались пациенты с высшим образованием. Частота сопутствующих ИБС, НРС и ХСН была достоверно выше у пациентов с впервые выявленными БОЗ (p<0,05). Наименьшая частота этих заболеваний зафиксирована в группе пациентов без БОЗ (р<0,05). В группе пациентов с ССЗ и установленными ранее БОЗ преобладали больные с БА (в том числе в комбинации с ХОБЛ), тогда как среди впервые выявленных случаев достоверно чаще диагностировали ХОБЛ (p<0,001). По результатам анализа крови абсолютное число нейтрофилов было достоверно выше среди больных ССЗ с впервые выявленными БОЗ, а абсолютное число эозинофилов — среди больных с установленными ранее БОЗ. По данным СМАД показатели ср. сут. САД и ДАД были достоверно ниже у больных с впервые выявленными БОЗ (p<0,05), среднесуточная ЧСС была выше у больных с установленными ранее БОЗ (p<0,001).
В рамках исследования оценивалась фармакотерапия ССЗ: частота назначений кардиоселективных ББ, АК, иАПФ, БРА при поступлении и выписке (после дообследования) в группах кардиологических больных с наличием БОЗ и без БОЗ.
Так, после дообследования частота назначений кардиоселективных ББ в группе больных ССЗ с установленными ранее БОЗ достоверно увеличилась с 31 до 55% (р<0,001), в то время как в группе ССЗ с впервые выявленными БОЗ отмечалась лишь статистически незначимая тенденция к увеличению (р=0,7), а в группе ССЗ без БОЗ отмечалось достоверное увеличение частоты назначений кардиоселективных ББ с 51 до 78% (р<0,001). Данные отражены на рисунке 1.
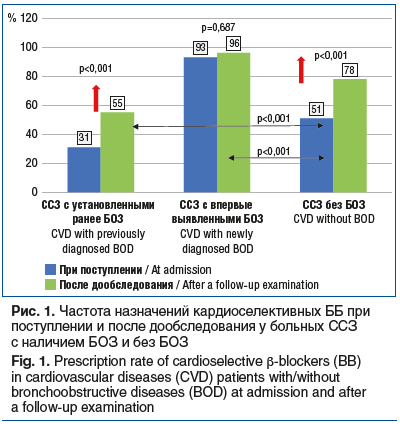
Таким образом, кардиоселективные ББ назначались больным ССЗ без БОЗ достоверно чаще, чем больным ССЗ с установленными ранее БОЗ, и достоверно реже, чем больным ССЗ с впервые выявленными БОЗ (р<0,001). После дообследования наиболее высокая частота применения кардиоселективных ББ сохранялась среди больных ССЗ с впервые выявленными БОЗ (р<0,001).
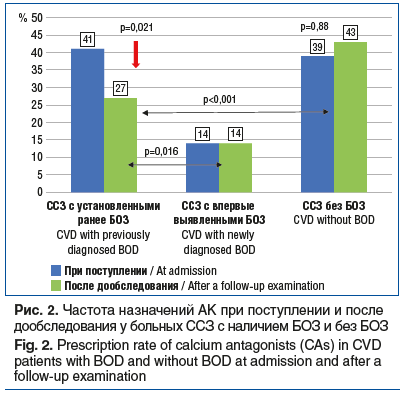
Изучение динамики назначений АК при поступлении и после дообследования в группах больных ССЗ с наличием БОЗ и без БОЗ показало, что после дообследования частота назначений АК в группе больных ССЗ с установленными ранее БОЗ достоверно снизилась с 41 до 27% (p=0,021). В то же время в группах ССЗ с впервые выявленными БОЗ и ССЗ без БОЗ статистически значимой динамики не выявлено (p<0,05) (рис. 2). Таким образом, после дообследования АК назначались больным ССЗ с установленными ранее БОЗ достоверно чаще, чем с впервые выявленными БОЗ (р=0,016), и достоверно реже, чем больным ССЗ без БОЗ (р<0,001). После дообследования наиболее высокая частота применения АК наблюдалась среди больных ССЗ без БОЗ (р<0,001).
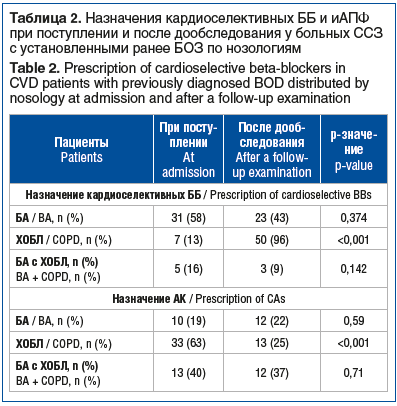
Детальный анализ группы больных ССЗ с установленными ранее БОЗ по нозологиям (ХОБЛ, БА и сочетание БА с ХОБЛ) показал, что частота назначений ББ у больных ХОБЛ достоверно увеличилась с 13 до 96% (р<0,001), а у больных ССЗ с БА и сочетанием БА с ХОБЛ отмечалась статистически незначимая тенденция к снижению частоты назначений ББ с 58 до 43% и с 16 до 9% соответственно (p>0,05) (табл. 2). Частота назначений АК у больных ХОБЛ достоверно снизилась с 63 до 25% (р<0,001), а у больных ССЗ с БА и сочетанием БА с ХОБЛ статистически значимой динамики не выявлено (p>0,05) (табл. 2). При аналогичном детальном анализе группы больных ССЗ с впервые выявленными БОЗ достоверной динамики частоты назначений ББ и АК по нозологиям ХОБЛ, БА и сочетанию БА с ХОБЛ не выявлено.
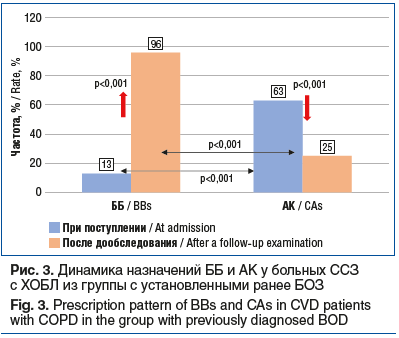
Отдельный субанализ продемонстрировал, что при поступлении у больных ССЗ с ХОБЛ из группы установленных ранее БОЗ частота назначений кардиоселективных ББ была достоверно ниже, чем АК (13% против 63%, р<0,001), а после дообследования, напротив, частота назначений кардиоселективных ББ стала выше, чем АК (96% против 25%, р<0,001) (рис. 3). При этом случаев отмены кардиоселективных ББ не отмечалось, в то время как снижение частоты назначений АК обусловлено исключительно их отменой у 21 пациента (из них 2 случая замены АК недигидропиридинового ряда на ББ).
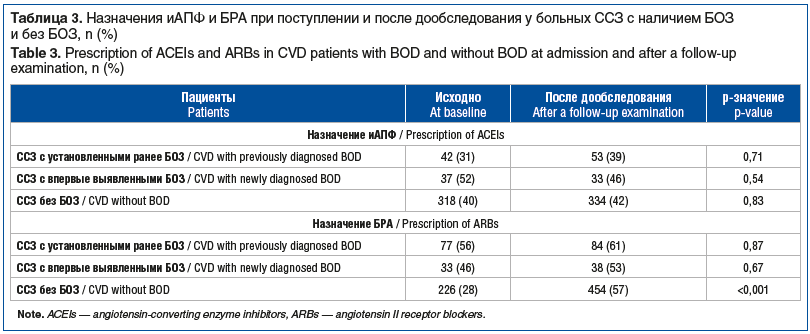
В исследовании изучалась динамика назначений блокаторов РААС (иАПФ или БРА) при поступлении и после дообследования в группах больных ССЗ с наличием БОЗ и без БОЗ. Сравнение частоты назначений иАПФ показало отсутствие статистически значимой динамики во всех группах (табл. 3). В отношении БРА также не выявлено достоверной динамики в группах ССЗ с БОЗ, однако у больных ССЗ без БОЗ, напротив, наблюдалось статистически значимое увеличение частоты назначений с 28 до 57%, p<0,001 (табл. 3). Таким образом, после дообследования частота назначений блокаторов РААС (иАПФ и БРА) в группе ССЗ с установленными БОЗ составила 100%, в группе ССЗ с впервые выявленными БОЗ — 99%, в группе ССЗ без БОЗ — 99%.
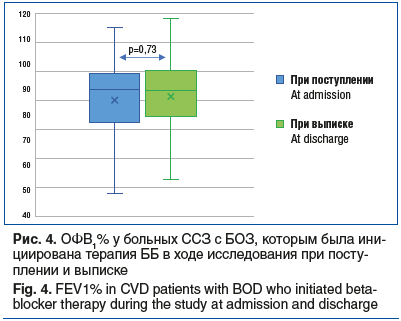
Проводился анализ спирометрического показателя ОФВ1% и результатов респираторных опросников САТ и mMRC при поступлении и выписке среди пациентов с ССЗ с БОЗ, которым была инициирована терапия кардиоселективными ББ в ходе исследования, включивший 47 пациентов с ХОБЛ. При динамической оценке не выявлено статистически значимого снижения ОФВ1% на фоне лечения (р=0,73). При сравнении показателей на момент поступления и при выписке зафиксирована достоверная положительная динамика по респираторному опроснику САТ (р=0,038), в то время как по опроснику mMRC статистически значимой динамики не наблюдалось (р=0,091) (табл. 4, рис. 4).
![Таблица 4. Динамика ОФВ1% и результатов респиратор- ных опросников у пациентов ССЗ с БОЗ, которым была инициирована терапия ББ в ходе исследования, Ме [Q1; Q3] Table 4. Changes in FEV1% and respiratory questionnaire scores in CVD patients with BOD who ini Таблица 4. Динамика ОФВ1% и результатов респиратор- ных опросников у пациентов ССЗ с БОЗ, которым была инициирована терапия ББ в ходе исследования, Ме [Q1; Q3] Table 4. Changes in FEV1% and respiratory questionnaire scores in CVD patients with BOD who ini](https://medblog.su/wp-content/uploads/2026/04/1775828455_542_Bezopasnost-i-dinamika-naznacheniya-kardio-selektivnyh-adrenoblokatorov-u-patsientov-s-arterialnoj.png)
Обсуждение
Коморбидность ССЗ и БОЗ характеризуется не только высокой распространенностью, но и значительным уровнем гиподиагностики БОЗ у кардиологических больных, что обусловлено схожестью клинических проявлений этих заболеваний [12, 13]. Выполненный нами ранее анализ выявил, что у кардиологических пациентов доля недиагностированных случаев БОЗ достигает 57% для ХОБЛ, 10,2% для БА и 74,3% для их сочетания [14]. Внедрение простых скрининговых опросников на этапе поступления в кардиологический стационар позволяет увеличить выявляемость БОЗ и снизить расходы системы здравоохранения на проведение диагностических исследований за счет своевременного выполнения при необходимости компьютерной спирометрии у кардиологических пациентов [15]. Так, в ходе настоящей работы среди 1000 пациентов с ССЗ у 71 пациента диагноз БОЗ был верифицирован впервые, 137 больных имели установленные ранее БОЗ, 792 больных не имели сопутствующих БОЗ по результатам пульмонологического обследования.
Сопутствующие БОЗ оказывают влияние и на назначение фармакотерапии имеющегося ССЗ. Так, несмотря на важную роль кардиоселективных ББ в лечении ССЗ, их применение у пациентов с ХОБЛ часто ограничивается. В недавно проведенном исследовании, включавшем 1084 больных с ХОБЛ после острого коронарного синдрома (ОКС), кардиоселективные ББ назначались только в 49,8% случаев, несмотря на то, что ранняя терапия данными препаратами была связана с улучшением результатов лечения ОКС в стационаре [16]. Частота назначения ББ также была значительно ниже и у пациентов с СН и ХОБЛ, зарегистрированных в регистре REPOSI (Италия): из 942 пациентов с СН только 47,1% получали лечение ББ; также стоит отметить, что пребывание в стационаре не повлияло на коррекцию терапии у данных пациентов (при поступлении ББ: 36,9% против 51,3%; при выписке: 38,0% против 51,7%) [17]. Причиной служат опасения по поводу потенциального риска бронхоспазма и ослабления действия базисной терапии бронходилататорами [11]. В то же время актуальные исследования у больных с кардиореспираторной патологией свидетельствуют о безопасности селективных ББ: они не повышают риск обострений, а, напротив, улучшают выживаемость после инфаркта миокарда при сопутствующей ХСН и даже ассоциированы с лучшим прогнозом при фибрилляции предсердий по сравнению с альтернативной терапией АК [18]. В ходе проведенной нами работы исходно высокая частота назначений ББ больным ССЗ с впервые выявленными БОЗ была, вероятнее всего, обусловлена как наиболее высокой коморбидностью ИБС, НРС и ХСН в этой группе, так и назначением ББ до верификации диагноза БОЗ. Сохранение высоких показателей назначений кардиоселективных ББ, а также замена недигидропиридиновых АК на ББ после дообследования у больных ССЗ с впервые выявленными БОЗ объясняется преобладанием ХОБЛ, которая, в соответствии с клиническими рекомендациями, не является противопоказанием к назначению ББ на фоне базисной терапии ХОБЛ [4]. В то время как в группе пациентов с ССЗ и ранее установленными БОЗ доминировали больные БА (в том числе в сочетании с ХОБЛ), что накладывало более строгие ограничения на инициирование терапии ББ и объясняет низкую частоту их назначений после дообследования, поскольку широкое применение ББ у больных БА до сих пор ограничено клиническими руководствами2. Это объясняет и отсутствие динамики по назначению АК в подгруппах пациентов с изолированной БА и с сочетанием БА и ХОБЛ ввиду предпочтительного использования врачами препаратов недигидропиридинового ряда с доказанным профилем безопасности у пациентов с БА [4].
На втором месте по ограничению к использованию у пациентов с ССЗ и БОЗ стоят препараты из группы иАПФ. Это связано с их нежелательным эффектом, обусловленным блокировкой распада брадикинина и накоплением его в тканях дыхательных путей, что может приводить к развитию сухого кашля, отеку слизистой, что особенно опасно на фоне существующего БОЗ [19]. В связи с этими рисками предпочтительными препаратами в лечении ССЗ чаще становятся БРА. Это было отмечено и в нашем исследовании, где, несмотря на то, что при поступлении частота применения БРА в группе пациентов с ССЗ без БОЗ была ниже, чем в группах пациентов с БОЗ, после дообследования во всех трех группах этот показатель превысил 50%, в итоге блокаторы РААС стали доминирующим по частоте назначений классом кардиологических препаратов. Проведенный нами анализ демонстрирует, что инициация терапии кардиоселективными ББ у пациентов с кардиореспираторной патологией не ассоциируется с клинически значимым ухудшением бронхиальной проходимости. Отсутствие статистически значимого снижения ОФВ1% на фоне инициальной терапии кардиоселективными ББ у 47 пациентов с сочетанием ССЗ и ХОБЛ согласуется с данными более крупных исследований и метаанализов, которые подтверждают безопасность применения кардиоселективных ББ у данной категории больных [20–22]. Эти препараты, обладая значительно более высоким сродством к β1-адренорецепторам, чем к β2-адренорецепторам бронхов, минимально влияют на показатели спирометрии, что позволяет преодолеть традиционные опасения врачей относительно риска развития бронхоспазма.
Особого внимания заслуживает выявленная в нашем исследовании положительная динамика качества жизни, по данным респираторного опросника CAT. Достоверное снижение итогового балла (с 6 [4; 10] до 5 [4; 6], р=0,038) свидетельствует об уменьшении влияния симптомов ХОБЛ на повседневную жизнь пациентов. Хотя абсолютное изменение может показаться небольшим (не достигающим минимальной клинической значимости), оно отражает статистически значимое улучшение с учетом исходно низких значений и может быть связано не только с основным лечением ХОБЛ, но и с благоприятным воздействием ББ на симпатическую активность и, возможно, системное воспаление [21, 23]. В отличие от CAT, оценка по модифицированной шкале одышки (mMRC) не показала статистически значимой динамики (р=0,091), что, вероятно, обусловлено исходно легкой степенью одышки. Шкала mMRC, оценивающая одышку по пяти градациям, является более грубым инструментом по сравнению с CAT, который охватывает более широкий спектр симптомов (кашель, продукция мокроты, стеснение в груди, сон, энергичность) и их влияние на функциональную активность [24].
Таким образом, наличие ранее установленной ХОБЛ у пациентов с ССЗ ассоциировалось с недостаточным назначением кардиоселективных ББ на госпитальном этапе. Проведенное дообследование позволило это нивелировать и назначать кардиоселективные ББ по показаниям. Инициирование терапии кардиоселективными ББ не сопровождалось ухудшением клинической симптоматики (по данным респираторных опросников) и не приводило к снижению функциональных показателей спирометрии, что подтверждает возможность их применения у больных с ССЗ и ХОБЛ.
Заключение
Кардиореспираторный скрининг больных ССЗ способствовал увеличению выявляемости БОЗ (ХОБЛ, БА), что привело к коррекции терапии ССЗ и БОЗ. Блокаторы РААС (иАПФ/БРА) стали доминирующим классом кардиологических препаратов во всех исследуемых группах, а после дообследования больным с установленной ранее ХОБЛ стали активно назначать кардиоселективные ББ, в то время как больные с впервые выявленной ХОБЛ получали их ранее в полном объеме до момента диагностики БОЗ, то есть в условиях отсутствия настороженности врачей в отношении усугубления бронхообструкции.
Таким образом, наличие ранее установленной ХОБЛ ассоциировано с исходным недоназначением ББ у больных ССЗ, однако после дообследования эта тенденция нивелируется без отрицательного влияния на респираторную функцию и симптоматику. Кардиореспираторный скрининг помогает не только эффективно диагностировать БОЗ у кардиологических пациентов, но и контролировать лечение сочетанной кардиореспираторной патологии.
Инициация терапии кардиоселективными ББ у кардиологических больных с ХОБЛ на фоне базисной терапии ХОБЛ не сопровождалась снижением ОФВ1 и не ухудшала клиническую симптоматику, что подтверждает возможность использования данной стратегии и необходимость преодоления терапевтической инертности в реальной клинической практике.
Сведения об авторах:
Климова Анна Алексеевна — соискатель отдела гипертонии, врач-кардиолог приемного отделения ФГБУ «НМИЦК им. ак. Е.И. Чазова» Минздрава России; 121552, Россия, г. Москва, ул. Академика Чазова, д. 15а; ORCID iD 0000-0001-8320-3054
Смолякова Екатерина Владимировна — к.м.н., ассистент кафедры факультетской терапии и профессиональных болезней ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; научный сотрудник лаборатории клинической пульмонологии ФГБУ «НИИ пульмонологии» ФМБА России; 115682, Россия, г. Москва, Ореховый б-р, д. 28, стр. 10; ORCID iD 0000-0002-1904-5319
Амбатьелло Лали Гурамовна — к.м.н., старший научный сотрудник, отдел гипертонии ФГБУ «НМИЦК им. ак. Е.И. Чазова» Минздрава России; 121552, Россия, г. Москва, ул. Академика Чазова, д. 15а; ORCID iD 0000-00031138-3361
Чазова Ирина Евгеньевна — д.м.н., профессор, академик РАН, руководитель отдела гипертонии ФГБУ «НМИЦК им. ак. Е.И. Чазова» Минздрава России; 121552, Россия, г. Москва, ул. Академика Чазова, д. 15а; ORCID iD 0000-0002-9822-4357
Зыков Кирилл Алексеевич — д.м.н., член-корреспондент РАН, профессор РАН, заведующий кафедрой факультетской терапии и профболезней ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; заместитель директора по научной и инновационной работе ФГБУ «НИИ пульмонологии» ФМБА России; 115682, Россия, г. Москва, Ореховый б-р, д. 28, стр. 10; руководитель лаборатории иммунопатологии сердечно-сосудистых заболеваний,
главный научный сотрудник ФГБУ «НМИЦК им. ак. Е.И. Чазова» Минздрава России; 121552, Россия, г. Москва, ул. Академика Чазова, д. 15а; ORCID iD 0000-0003-3385-2632
Контактная информация: Климова Анна Алексеевна, е-mail: ruanna89@mail.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 11.01.2026.
Поступила после рецензирования 03.02.2026.
Принята в печать 27.02.2026.
About the authors:
Anna A. Klimova — External Doctorate Student of the Department of Hypertension, Cardiologist at the Admission Department, Acad. E.I. Chazov National Medical Research Center of Cardiology; 15A, Academician E.I. Chazov str., Moscow, 121552, Russian Federation; ORCID iD 0000-0001-8320-3054
Ekaterina V. Smolyakova — C. Sc. (Med.), Teaching Assistant at the Department of Faculty Therapy and Occupational Diseases, Russian University of Medicine; 4, Dolgorukovskaya str., Moscow, 127006, Russian Federation; Scientific Officer at the Laboratory of Clinical Pulmonology, Research Institute of Pulmonology of the Federal Medical Biological Agency of Russia; 28, bldg. 10, Orekhovyy blvrd., Moscow, 115682, Russian Federation; ORCID iD 0000-0002-1904-5319
Lali G. Ambatiello — C. Sc. (Med.), Senior Scientific Officer, Department of Hypertension, Acad. E.I. Chazov National Medical Research Center of Cardiology; 15A, Academician E.I. Chazov str., Moscow, 121552, Russian Federation; ORCID iD 0000-00031138-3361
Irina E. Chazova — Dr. Sc. (Med.), Professor, Academician of the Russian Academy of Sciences, Head of the Department of Hypertension, Acad. E.I. Chazov National Medical Research Center of Cardiology; 15A, Academician E.I. Chazov str., Moscow, 121552, Russian Federation; ORCID iD 0000-0002-9822-4357
Kirill A. Zykov — Dr. Sc. (Med.), Corresponding Member of the Russian Academy of Sciences, Professor of the Russian Academy of Sciences, Head of the Department of Faculty Therapy and Occupational Diseases, Russian University of Medicine; 4, Dolgorukovskaya str., Moscow, 127006, Russian Federation; Deputy Director for Scientific and Innovative Work, Research Institute of Pulmonology of the Federal Medical Biological Agency of Russia; 28, bldg. 10, Orekhovyy blvrd., Moscow, 115682, Russian Federation; Head of the Laboratory of Immunopathology of Cardiovascular Diseases, Chief Scientific Officer of Acad. E.I. Chazov National Medical Research Center of Cardiology; 15A, Academician E.I. Chazov str., Moscow, 121552, Russian Federation; ORCID iD 0000-0003-3385-2632
Contact information: Anna A. Klimova, e-mail: ruanna89@mail.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 11.01.2026.
Revised 03.02.2026.
Accepted 27.02.2026.
1Global Initiative for Chronic Obstructive Lung Disease. Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. 2026. (Electronic resource.) URL: https://goldcopd.org/ (access date: 20.12.2025).
2Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention, 2024. Update May 2024. (Electronic resource.) URL: www.ginasthma.org (access date: 20.12.2025).
3COPD Assessment Test. 2022. (Electronic resource.) URL: https://www.catestonline.org/ (access date: 20.12.2025).
4mMRC (Modified Medical Research Council) Dyspnea Scale. (Electronic resource.) URL: https://www.mdcalc.com/calc/4006/mmrc-modified-medical-research-council-dyspnea-scale (access date: 20.12.2025).
Информация с rmj.ru