Введение
5 мая 2023 г. глава Всемирной организации здравоохранения (ВОЗ) Тедрос Адханом Гебрейесус объявил, что инфекция, вызванная новым коронавирусом SARS-CoV-2 (COVID-19), больше не является мировой чрезвычайной угрозой, пандемия имеет «тенденцию к снижению», однако это не означает, что вирус перестал представлять опасность [1]. Во всем мире по-прежнему существуют пробелы в знаниях об эпидемиологии, клинических проявлениях, наиболее эффективных методах терапии и исходах COVID-19 среди новорожденных. Опубликованные данные далеко не однозначны.
Входные ворота SARS-CoV-2 — эпителий верхних дыхательных путей и эпителиоциты желудка и кишечника, имеющие рецепторы ангиотензинпревращающего фермента II типа (АПФ2). Начальным этапом заражения является проникновение вируса в клетки-мишени, имеющие рецепторы АПФ2. Клеточная трансмембранная сериновая протеаза типа 2 способствует связыванию вируса с АПФ2, активируя его S-протеин, необходимый для проникновения SARS‑CoV‑2 в клетку. Таким образом, при COVID-19 может развиваться не только поражение дыхательных путей, но и гастроэнтероколит, что особенно характерно для детей раннего возраста. В процессе развития инфекции могут поражаться эндотелий сосудов, а также миокард, почки и другие органы, в том числе иммунокомпетентные. При критическом течении COVID-19 развивается патологическая активация врожденного и приобретенного иммунитета, дисрегуляция синтеза провоспалительных, иммунорегуляторных, антивоспалительных цитокинов и хемокинов, в том числе интерферонов (ИФН) α и β, ИФН-γ-индуцируемого белка 10, а также маркеров воспаления (С-реактивный белок (СРБ), ферритин). «Цитокиновый шторм» при тяжелом течении COVID-19, как правило, приводит к развитию острого респираторного дистресс-синдрома (ОРДС) как проявления тяжелого диффузного альвеолярного повреждения, полиорганной недостаточности, и может быть причиной летального исхода[1].
Источником инфекции для новорожденного может стать больной человек, в том числе находящийся в инкубационном периоде заболевания, особенно в первые и последние два дня болезни, или бессимптомный носитель SARS-CoV-2. При выделении групп риска по COVID-19 важен учет эпидемиологического анамнеза: новорожденные от матерей с подозреваемым или подтвержденным диагнозом COVID-19; контактировавшие с больными, имеющими респираторные симптомы и/или лихорадку, в течение 14 дней до начала заболевания; с подтвержденным или подозрительным контактом в анамнезе в течение 14 дней до начала заболевания [2].
Вопрос о возможности трансплацентарной или с грудным молоком передачи вируса SARS‑CoV‑2 долго оставался дискутабельным[2] [3]. Обсервационное когортное исследование в трех больницах Нью-Йорка (США) показало, что у 120 новорожденных от мам с положительным результатом на SARS-CoV-2 при родах, протестированных через 24 ч жизни, не было положительного результата. У 79 младенцев были сделаны тесты методом полимеразной цепной реакции (ПЦР) в возрасте 5–7 дней и у 72 новорожденных — в возрасте 14 дней: все они также были отрицательными, хотя 68 (83%) младенцев находились в одной комнате со своими матерями и 64 (78%) ребенка находились на грудном вскармливании [3]. В методических рекомендациях Минздрава России «Особенности клинических проявлений и лечения заболевания, вызванного новой коронавирусной инфекцией (COVID-19) у детей» (2020) указывается, что доказательств внутриутробной инфекции, вызванной вертикальной передачей инфекции от матери к ребенку, не обнаружено, все случаи считаются приобретенными после рождения[3]. Однако анализ 37 публикаций в PubMed (с января 2020 г. по июль 2021 г.) подтверждает возможность трансплацентарной передачи вируса от матери плоду [4]. По результатам исследований, вирус SARS-CoV-2 был выявлен в единичных образцах грудного молока [5]. Систематический обзор риска вертикальной передачи SARS-CoV-2, включающий 156 новорожденных (из которых 24,7% недоношенных), проведенный J. Chi et al. [5], показал, что риск инфицирования составил 3,2% (5 детей). В крупном обзоре K. More et al. [6], включающем 1134 наблюдения, перинатальная передача вируса SARS-CoV-2 произошла у 106 (8%) детей, горизонтальная передача — у 21 (1,5%) новорожденного. Никакой связи инфицирования со способом родоразрешения или видом кормления отмечено не было. Клинически большинство случаев заболеваемости было связано с недоношенностью и перинатальными событиями.
Опубликованы и продолжают появляться новые противоречивые отечественные и зарубежные исследования, подтверждающие отсутствие риска [7] или возможность вертикальной передачи SARS-CoV-2 от больных матерей [8, 9]. Весьма вероятны и прямые вирусные поражения плаценты, в единичных наблюдениях показана возможность внутриутробного инфицирования, клиническое значение которого требует дальнейшего изучения. При анализе деятельности родильных домов инфекционного профиля г. Алматы (Казахстан) в период с марта 2020 г. по май 2021 г. указывается частота перинатального инфицирования новорожденных — 10,6% [10]. Перинатальные исходы COVID-19 у 8485 беременных пациенток, рожениц и родильниц в Сибири и на Дальнем Востоке с 11 марта по 25 декабря 2020 г. составили 148 (6,2%) SARS-CoV-2-положительных новорожденных [11]. По данным наблюдения 64 родов, у пациенток с подтвержденным диагнозом COVID-19 с марта по август 2020 г. в Клинической инфекционной больнице им. С.П. Боткина (Санкт-Петербург) у 23,4% новорожденных лабораторно был подтвержден COVID-19 (обнаружение РНК SARS-CoV-2 в мазке из носоглотки или в анализе кала), причем у 42,7% новорожденных положительный мазок из носоглотки был получен в первые 48 ч после рождения [12]. Анализ времени заболевания COVID-19 среди 39 новорожденных с 11 марта 2020 г. по 25 декабря 2021 г. в Хабаровском крае показал, что возраст на момент диагностики составил: до 10 дней — 13% всех зарегистрированных, от 10 до 20 дней — 36%, от 20 до 28 дней — 51% заболевших, средний возраст заболевших составил 19±2,5 дня [13].
COVID-19 у новорожденных
Клинические проявления
Клинические проявления COVID-19 неспецифичны, особенно у недоношенных детей, часто маскируются под ОРДС [14]. Инкубационный период инфекции колеблется от 2 до 14 дней, хотя чаще всего составляет 3–7 дней4 [15]. Гипоксемия у матери, вызванная тяжелой инфекцией, может привести к внутриутробной гипоксии плода и асфиксии новорожденного при рождении, преждевременным родам и другим перинатальным рискам. У инфицированных новорожденных в начале заболевания в основном отмечаются симптом угнетения центральной нервной системы, интоксикационный синдром со снижением аппетита, диспепсические и респираторные проявления (заложенность носа, ринорея), возможна умеренная лихорадка, диарея4 [15].
Критериями для предположительного диагноза неонатальной инфекции COVID-19 могут являться: хотя бы один клинический симптом, включая нестабильную температуру тела, низкую активность, плохое питание, одышку; изменения на томограмме грудной клетки, показывающие аномалии, включая односторонние или двусторонние изменения по типу «матового стекла»; наличие среди членов семьи или лиц, осуществляющих уход за больным, людей с подтвержденной инфекцией COVID-19, тесный контакт с людьми с подтвержденной инфекцией COVID-19 или с тяжелой пневмонией[4].
По данным результатов анализа случаев COVID-19 среди новорожденных, в 20–37% случаев течение заболевания расценивалось как легкое с изолированными назофарингеальными проявлениями и гипертермией без пневмонии, нормальным уровнем С-реактивного белка, но в ряде случаев отмечалось повышение ферритина, лактатдегидрогеназы, лимфоцитоз и лейкопения [15, 16]. В недавних исследованиях выявлено, что количество вирусной РНК SARS-CoV-2 на слизистой оболочке носоглотки у новорожденных выше по сравнению с детьми более старшего возраста и не связано с тяжестью течения заболевания, наличием поражения легочной ткани, что, очевидно, связано с особенностями иммунного ответа в неонатальном периоде [17]. Рентгенологические данные COVID-19 неспецифичны и включают односторонние или двусторонние инфильтраты, в некоторых случаях отмечается симптом «матового стекла» или уплотнение с окружающими тяжами. Описаны случаи отсутствия явных признаков пневмонии, которые являются определяющими признаками инфекции у взрослых, а также бессимптомного носительства SARS-CoV-2 у новорожденного ребенка после оперативного вмешательства [18]. В одной из публикаций говорится о бессимптомной форме COVID-19 у детей с 2-месячного возраста с постоянно положительным результатом теста ректальных мазков на SARS-CoV-2 при отрицательном результате тестирования мазков из носоглотки, что свидетельствует о вероятности фекально-орального механизма передачи вируса [14].
По мере прогрессирования заболевания (обычно в течение недели) нарастают цианоз, одышка, а также другие симптомы дыхательной недостаточности и токсикоза, снижается двигательная активность, нарастает беспокойство. В тяжелых случаях (до 6% детей) описано развитие критической формы COVID-19 с прогрессирующим мультисистемным воспалительным синдромом, отсутствие эффекта от масочной кислородотерапии и в течение 1–3 дней отмечается прогрессирование дыхательной недостаточности, нарастание метаболического ацидоза, развитие септического шока, синдрома диссеминированного внутрисосудистого свертывания [15, 19].
Отмечено более тяжелое клиническое течение заболевания в неонатальном периоде по сравнению с детьми других возрастов с вовлечением как верхних, так и нижних дыхательных путей, гораздо более короткое время от появления симптомов до смерти (медиана 2,5 дня) и более длительное время от появления симптомов до выписки (медиана 23,5 дня) [20].
По данным анализа 28 наблюдений новорожденных с COVID-19, с июня по декабрь 2020 г. в инфекционном отделении патологии новорожденных Городской Ивано-Матренинской детской клинической больницы г. Иркутска у 46,5% детей отмечалось бессимптомное течение заболевания, у 50% детей — клиника пневмонии. Причем у новорожденных, поступивших из дома после контакта с семейными случаями COVID-19, отмечались более тяжелые проявления заболевания [21]. В инфекционном отделении СПб ГБУЗ «ДГБ св. Ольги» в период с мая по июль 2020 г. легкие формы заболевания зарегистрированы у 76% новорожденных, среднетяжелые — у 12%, тяжелые — у 12%, преобладал семейный контакт (76% наблюдений) [22].
D.H. Kim [23] отмечает, что смертность у новорожденных с COVID-19 в большинстве случаев ассоциирована с сопутствующей патологией или осложнениями основного заболевания (пневмония, сепсис, системный воспалительный синдром).
В 2022 г. описано первое клиническое наблюдение у недоношенного новорожденного ребенка в России с врожденной инфекцией, вызванной вирусом SARS-CoV-2, клинически проявившейся дыхательной недостаточностью в связи с пневмонией, потребовавшей проведения искусственной вентиляции легких (ИВЛ) в течение 2 сут, ИВЛ в режиме СРАР до 14-х суток жизни, затем ребенок был переведен на оксигенотерапию через назальные канюли до 20-х суток жизни. После двух курсов антибактериальной терапии выписан домой на 27-е сутки жизни в удовлетворительном состоянии [24].
Выздоровление у младенцев с COVID-19, по наблюдениям отечественных авторов, наступает на 9–28-е сутки жизни в зависимости от тяжести заболевания [15]. Отличительной особенностью новой коронавирусной инфекции у детей является то, что они часто очень долго выделяют вирус — более 14 дней [2, 14].
Всплеск случаев COVID-19 у детей наблюдался во время пятой волны (вызванной геновариантом SARS-CoV-2 Omicron) пандемии COVID-19 в период с декабря 2021 г. по декабрь 2022 г., несмотря на то, что во время этой волны пандемии в большинстве случаев заболевание протекало более легко.
У новорожденных с перинатальным контактом были обнаружены признаки мультисистемного воспалительного синдрома с повышенными уровнями маркеров воспаления и полиорганной, особенно сердечной, дисфункцией, которая была описана как мультисистемный воспалительный синдром у новорожденных (Multisystem inflammatory disease in neonates, MIS-N) [25].
Содержание статьи
Диагностика
Диагноз устанавливается на основании данных клинического обследования, эпидемиологического анамнеза и результатов лабораторных исследований.
Этиологическая лабораторная диагностика включает прямые методы: выявление РНК SARS-CoV-2 с применением метода амплификации нуклеиновых кислот (МАНК) (основной) и выявление антигенов SARS-CoV-2 c применением иммунохроматографических методов; непрямые методы: выявление Ig классов А, M и G к SARS-CoV-2. Новорожденный может получить антитела класса G от больной матери, поэтому требуется определение их уровня в динамике.
Общий и биохимический анализы крови неспецифичны, однако необходимы для оценки органной дисфункции, риска развития осложнений и прогнозирования исхода заболевания. Как при любых вирусных инфекциях, возможны лейкопения, лимфопения, тромбоцитопения. Ферритин и СРБ как белки острой фазы воспаления дают информацию о тяжести течения заболевания и прогнозе [26]. СРБ является основным лабораторным маркером активности процесса в легких, коррелирует с объемом поражения легочной ткани, прогнозом при пневмонии, однако у новорожденных целесообразно определять его не ранее 6 ч после рождения при подозрении на внутриутробное инфицирование (норма не более 0,5 мг/л у новорожденных), затем повторить через 24–48 ч. Уровень СРБ в сыворотке при первоначальном обследовании младенца с подозрением на любую инфекцию с поздним началом (более 72 ч жизни) вряд ли будет считаться достаточно точным [26]. Концентрация СРБ увеличивается у большинства пациентов с COVID-19 одновременно с увеличением концентрации интерлейкина (ИЛ) 6 и скорости оседания эритроцитов. Ферритин повышается у новорожденных более чем до 600 мкг/л при неблагоприятном течении заболевания. Нарастание прокальцитонина отмечается при присоединении бактериальной инфекции и также коррелирует с тяжестью течения, распространенностью воспалительной инфильтрации и прогнозом [25, 27].
В связи с тем, что при COVID-19 в неонатальном периоде возможны тяжелые поражения микроциркуляторного русла в виде распространенной тромботической микроангиопатии, тромбозами крупных артерий и вен, обязательно исследование коагулограммы (активированное частичное тромбопластиновое время, протромбиновое время, протромбиновое отношение и/или % протромбина по Квику, фибриноген, D-димер количественным методом). У новорожденных с подтвержденным диагнозом COVID-19 содержание D-димера в крови выше [27]. Повышенный уровень D-димера рассматривается как фактор риска и тяжелого течения заболевания и смерти.
Лучевая диагностика патологии органов грудной клетки новорожденных с предполагаемым/установленным COVID-19 включает обзорную рентгенографию легких, компьютерную томографию (КТ) легких и ультразвуковое исследование (УЗИ) легких и плевральных полостей [28–30]. Стандартная рентгенография имеет низкую чувствительность в выявлении начальных изменений в первые дни заболевания и не может применяться для ранней диагностики. КТ имеет высокую чувствительность в выявлении характерных изменений в легких еще до появления положительных лабораторных тестов на инфекцию с помощью МАНК. При среднетяжелом и тяжелом течении болезни до 80% случаев протекают с пневмонией, подтвержденной на рентгенограмме органов грудной полости и/или при КТ легких [14]. УЗИ легких становится все более популярным методом в неонатологии, в том числе и в случаях новой коронавирусной инфекции [28, 30]. Будучи щадящим методом, УЗИ не требует дополнительной седации, что важно при обследовании глубоко недоношенных детей. Это исследование отличается высокой чувствительностью в выявлении интерстициальных изменений и консолидаций в легочной ткани при субплевральном расположении, однако поскольку при COVID-19 очаги чаще расположены в периферических отделах, увидеть их вполне реально [6, 30]. Еще очень важный в практике момент — у реконвалесцентов изменения на КТ сохраняются довольно долго, а сонографические признаки регрессируют в сроки, сопоставимые с клиническими данными [30]. E.R. Stoicescu et al. [30] провели анализ 7 статей, в которых обсуждался метод УЗИ легких у новорожденных с диагнозом COVID-19, подтвержденным ПЦР с обратной транскрипцией или IgM-тестами. Обзор доказывает эффективность портативного УЗИ легких у 58 детей, из которых 15% новорожденных были недоношенными, 85% родились в срок. Обследование новорожденных с известной/предполагаемой пневмонией, вызванной COVID-19, по возможности начинается с применения УЗИ легких, плевральных полостей и средостения, при наличии клинических показаний продолжается с использованием рентгенографии и/или КТ органов грудной клетки. Следует подчеркнуть, что все выявляемые при лучевых исследованиях признаки, включая КТ-симптомы, не являются специфичными для какого-либо вида инфекции и не позволяют установить этиологический диагноз1 [29, 30].
Лечение
Основным подходом к терапии COVID-19, в том числе у новорожденных, должно быть упреждающее назначение лечения до развития полного симптомокомплекса жизнеугрожающих состояний, а именно пневмонии, ОРДС, сепсиса. Опыт лечения новорожденных с COVID-19 на сегодняшний день еще недостаточен и требует дальнейших исследований, основанных на доказательной медицине [5, 31].
Известно, что главными факторами противовирусной защиты являются факторы врожденного иммунитета — цитокины, а именно ИФН I типа (ИФН-α, ИФН-β) — полифункциональные регуляторы гомеостаза и модуляторы адаптивного иммунного ответа [32].
Клиническим рекомендациям по использованию препаратов ИФН для профилактики и лечения новой коронавирусной инфекции предшествовали многочисленные экспериментальные исследования по оценке чувствительности вируса SARS-CoV-2 к ИФН. В 2003 г. во время вспышки атипичной пневмонии экспериментальное исследование на модели макаки-резус выявило, что рекомбинантный человеческий ИФН-α-2b может ингибировать репликацию вируса SARS-CoV-2 и тем самым предотвратить инфекцию [33]. В последующих зарубежных исследованиях установлено, что рекомбинантный ИФН-α-2b эффективно снижает уровень инфицирования не только вирусом гриппа, аденовирусом, респираторно-синцитиальным вирусом, но и SARS-CoV-2 [34]. По данным литературы, именно ИФН I типа синтезируются практически всеми клетками организма при вирусной инвазии и обладают выраженным противовирусным эффектом в отношении большинства ДНК/РНК-содержащих вирусов, являясь «медиаторами» иммунитета [32]. Продолжающиеся экспериментальные работы подтвердили высокую чувствительность SARS-CoV-2 в культуре клеток к ИФН I типа: количество вируса в инфицированных клетках, обработанных ИФН I типа, было в 1000–10 000 раз ниже, чем в таких же инфицированных, но предварительно не обработанных клетках [35]. Доказано, что SARS-CoV-2 под воздействием клеточной протеазы ТМРRSS2 присоединяется к АПФ2, только когда рецептор находится в неактивном состоянии. По результатам современных исследований установлено, что ИФН увеличивает количество рецепторов АПФ2, которые обеспечивают проникновение вируса в клетку. Однако одновременно он активирует неактивные АПФ2, тем самым предотвращая присоединение вируса к рецептору, и снижает его возможность прохождения через клеточную мембрану [36]. Таким образом, увеличивая экспрессию рецепторов АПФ2 и переводя их в активированное состояние, ИФН повышает толерантность к SARS-CoV-2 (рис. 1).
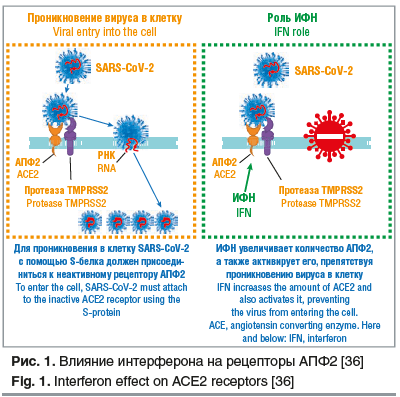
Полученные экспериментальные данные о высокой чувствительности вируса SARS-CoV-2 к ИФН I типа, а также имеющийся опыт многолетнего применения рекомбинантных ИФН для профилактики и лечения различных респираторных вирусных инфекций позволили обосновать их применение и в условиях пандемии COVID-19. Клинические исследования, проведенные в Китае, показали выраженное угнетение выработки эндогенного ИФН у пациентов при воздействии SARS-CoV-2, что диктует интерферонозамещение с применением высоких доз [36].
Были установлены минимальные количества ИФН в периферической крови или легких больных с тяжелой формой COVID-19, причем около четверти пациентов, находящихся в критическом состоянии, абсолютно не продуцировали ИФН, что могло привести к выраженной виремии и тяжелому течению заболевания [37]. Очевидно, что низкий уровень ИФН-α в плазме крови можно рассматривать как прогностический маркер риска развития критического состояния у пациента и показание к использованию в комплексной терапии COVID-19 препаратов ИФН-α [37]. Таким образом, по данным многочисленных экспериментальных и клинических исследований, нарушение регуляции системы ИФН, включающей в себя гены ИФН и их рецепторы, сами ИФН, специфические клеточные рецепторы и ферментные системы, является одной из ключевых детерминант патогенеза COVID-19, определяет характер течения и прогноз заболевания [32–37].
Извлечение из временных методических рекомендаций «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)», версии 16, 17 (2022), 18 (2023)»: «… в качестве противовирусной терапии детей с COVID-19 в случаях заболеваний среднетяжелой и легкой степени тяжести рекомендуются препараты ИФН-α, при тяжелой степени тяжести используются внутривенные иммуноглобулины, а ИФН-α может снизить вирусную нагрузку на начальных стадиях болезни, облегчить симптомы и уменьшить длительность болезни»[5],[6].
По мере роста кишечной трубки ребенка уровень представительства АПФ2 в тонком и толстом кишечнике будет заведомо выше, чем в легочной ткани или эпителиальном пуле назофарингеальной системы, что обусловливает особую тропность SARS-CoV-2 к желудочно-кишечному тракту (ЖКТ). По данным, представленным R. Zang et al. [38], вирус обнаруживали в кале детей в течение нескольких недель после исчезновения симптомов COVID-19, поскольку SARS-CoV-2 может дольше сохраняться в энтероцитах, чем в клетках эпителия респираторного тракта (до 28 дней против 14 дней). Новые вирусные частицы выходят в межклеточное пространство, попадают в просвет кишки и, следовательно, могут оставаться в каловых массах, в связи с чем считается, что кишечный эпителий может быть источником повторного инфицирования [14]. В связи с вышесказанным, «обосновано применение препаратов ИФН-α в свечах, особенно с антиоксидантами, которые обеспечивают системное действие препарата, могут способствовать сокращению периода выделения вируса SARS-CoV-2 с фекалиями»6 (рис. 2). [39].
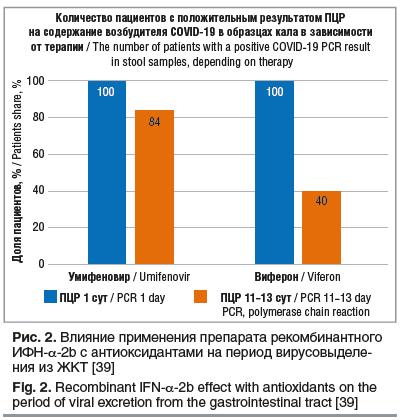
Накоплен большой опыт применения препарата рекомбинантного ИФН-α-2b с антиоксидантами (Виферон®) в терапевтически эффективных дозах в различных формах (суппозитории, гель, мазь) и комбинациях при вирусных инфекциях, в том числе COVID-19, у детей и беременных как с целью лечения, так и с целью профилактики [22, 40–45]. В инфекционном отделении СПб ГБУЗ «ДГБ св. Ольги» 16 новорожденных с COVID-19 в комплексной терапии получали рекомбинантный ИФН-α-2b с антиоксидантами в суппозиториях с хорошим клиническим эффектом [22]. Неинъекционная системная форма препарата рекомбинантного ИФН-α-2b с антиоксидантами (ректальные суппозитории) удобна для применения у новорожденных, в том числе недоношенных младенцев. Антиоксиданты (α-токоферола ацетат и аскорбиновая кислота), входящие в состав препарата, за счет связывания активных форм кислорода оказывают аттенуирующее действие на течение острого воспалительного процесса при вирусной инфекции, обладая противовоспалительным, мембраностабилизирующим и регенерирующим свойствами [42].
В 2021 г. опубликован метаанализ 21 исследования эффективности и безопасности использования препарата рекомбинантного ИФН-α-2b с антиоксидантами в суппозиториях (Виферон®) у новорожденных, в том числе родившихся недоношенными, для профилактики и лечения различных перинатальных и неонатальных инфекций вирусной и бактериальной этиологии за период 1985–2021 гг. [43]. В исследования включены 950 пар «мать — новорожденный», 1315 доношенных и недоношенных младенцев, родившихся на 24–28-й неделе гестации. Всем назначался препарат рекомбинантного ИФН-α-2b с антиоксидантами в форме ректальных суппозиториев, а также геля в возрастных дозировках. Беременные получали по 1 суппозиторию 500 000 МЕ 2 р/сут курсом 10 дней, от 1 до 5 курсов терапии, а в 1 случае женщине дополнительно назначался местно гель. Новорожденным детям назначались суппозитории 150 000 МЕ 2 р/сут курсом 5–10 дней. При тяжелом течении врожденной инфекции у младенцев препарат исследования использовался в дозе 500 000 МЕ 2 р/сут в течение 5 дней, а затем 150 000 МЕ 2 р/сут еще 5 дней. Применение изучаемого препарата ИФН-α-2b с антиоксидантами способствовало сокращению на 2,4 дня длительности нахождения пациентов на ИВЛ, на 14 дней — пребывания в палате/отделении интенсивной терапии, на 16 дней — в отделении патологии новорожденных и недоношенных детей. Естественно, в основной группе наблюдения сокращались период интоксикации, длительность антибактериальной терапии (от 6,9 дня у доношенных до 9,1 дня у недоношенных) и длительность парентерального питания. Кроме того, ускорялась элиминация возбудителя, в 3 раза снижались частота и длительность вирусо- и бактерионосительства, в 2,5 раза — частота развития госпитальной инфекции. Важным результатом применения препарата Виферон®, по данным метаанализа, является снижение риска летальных исходов в 3–4,2 раза [43].
В 2023 г. опубликованы результаты открытого сплошного проспективного рандомизированного клинического исследования эффективности и безопасности комбинированной терапии среднетяжелой формы COVID-19 у новорожденных препаратом рекомбинантного ИФН-α-2b с антиоксидантами (Виферон®) в виде геля и ректальных суппозиториев, проведенного на базе Межрайонной детской клинической больницы № 1 (Красноярск) [44]. Основная группа в составе комплексной терапии получала исследуемый препарат ИФН-α-2b суппозитории ректальные 150 000 МЕ 2 р/сут в сочетании с гелем 36 000 МЕ/г, наносимым на слизистую оболочку носовых ходов 5 р/сут, в течение 10 дней. Младенцам контрольной группы назначался препарат ИФН-α-2b в виде назальных капель 10 000 МЕ/мл по 1 капле в каждый носовой ход 5 р/сут. Комбинированная терапия препаратом ИФН-α-2b с антиоксидантами статистически значимо сокращала продолжительность заболевания, способствовала более быстрому разрешению пневмонии (медиана 10 дней в основной группе против 16 дней в группе сравнения, p<0,05), уменьшала время элиминации SARS-CoV-2 со слизистой носоглотки младенцев (медиана 5 дней в основной группе против 9,5 дня в группе сравнения, p<0,05), что в конечном итоге приводило к сокращению сроков госпитализации (медиана 10 дней в основной группе по сравнению с 15 днями в группе сравнения, p<0,05). Нежелательные эффекты изучаемого препарата зарегистрированы не были. Доказанные эффективность и безопасность комбинированной противовирусной терапии изучаемым препаратом на основе рекомбинантного ИФН-α-2b в комплексе с антиоксидантами, суппозитории ректальные в сочетании с гелем, позволили исследователям рекомендовать данную схему для широкого внедрения в неонатальную практику при лечении новорожденных с COVID-19 [44].
Возможность ректального пути введения ИФН-α-2b, обеспечивающего быстрый терапевтический эффект, важна именно для новорожденных, особенно недоношенных детей, имеющих проблемы перорального приема препаратов, а также проблемы всасывания через незрелый ЖКТ. Наличие в препарате Виферон® высокоактивных антиоксидантов — витамина Е (α-токоферола ацетат) и витамина С (аскорбиновая кислота) в терапевтически эффективных дозах важно для осуществления мембраностабилизирующего эффекта, снижения инактивации ИФН продуктами перекисного окисления липидов, активирующегося в ходе инфекционного процесса, и улучшения взаимодействия ИФН с клеточными рецепторами [42, 45].
Фармакологические свойства препарата в виде геля «сопоставимы с таковыми у противовирусных препаратов системного действия и заключаются в иммуномодулирующем, противовирусном и антипролиферативном эффектах» [46].
Исследования по оценке эффективности использования ИФН в терапии и профилактике новой коронавирусной инфекции у детей, в том числе новорожденных, продолжаются в настоящее время во всем мире, в том числе и в нашей стране.
Антибактериальная терапия показана только при наличии признаков присоединения к COVID-19 бактериальной инфекции или их сочетания при рождении. Рекомендуются защищенные аминопенициллины (амоксициллин/клавуланат, амоксициллин/сульбактам), реже — азитромицин. Поддерживающая терапия — восполнение потерь жидкости и дезинтоксикация являются неотъемлемой частью терапии среднетяжелых и тяжелых форм болезни. Объем вводимой жидкости должен строго контролироваться. В тяжелых случаях развития ОРДС инфузия должна быть максимально продуманной, поскольку избыток жидкостей неблагоприятно действует на новорожденного пациента с легочно-сердечной недостаточностью. Оксигенотерапия показана во всех случаях гипоксемии (SpО2≤94%) при клинически выраженной дыхательной недостаточности. Системные кортикостероиды оправданы только при развитии ОРДС, надпочечниковой недостаточности, развитии гемофагоцитарного синдрома (цитопения, высокий уровень ферритина на фоне сниженного показателя фибриногена) в дозировках, соответствующих этим состояниям[7].
Таким образом, особую важность на сегодняшний день приобретают вопросы, касающиеся прежде всего рационального выбора противовирусной терапии у новорожденных детей, поскольку именно неонатальный период и младенчество ограничивают или полностью исключают применение многих лекарственных препаратов для лечения COVID-19 из-за противопоказаний и возможности развития нежелательных реакций.
Профилактика
Неспецифическая профилактика COVID-19 у новорожденных представляет собой мероприятия, направленные на предотвращение распространения инфекции: ранняя диагностика и активное выявление инфицированных беременных и родильниц, в том числе с бессимптомными формами; разобщение ребенка и больной матери сразу после рождения; соблюдение правил личной гигиены и использование средств индивидуальной защиты мамой: орошение слизистой оболочки полости носа изотоническим раствором хлорида натрия; использование лекарственных средств для местного применения, обладающих барьерными функциями (например, рекомбинантный ИФН-α-2b с антиоксидантами, гель или мазь (Виферон®) и пр.
Перспективным направлением благоприятного влияния на неспецифический иммунитет ребенка с целью профилактики и снижения тяжести протекания острых респираторных инфекций является применение пробиотиков [47]. Очень важно профилактировать нарушение микробиома кишечника у детей, получающих антибактериальную терапию. В выводах по исследованию бактериальной колонизации кишечника новорожденных высказывается предположение, что здоровый микробиом кишечника может защищать от COVID-19 [47].
Описан успешный опыт применения местных форм препарата рекомбинантного ИФН-α-2b с антиоксидантами (Виферон® гель для наружного и местного применения 36 000 МЕ/г) в профилактике ОРВИ в период пандемии COVID-19. Весной 2020 г. на базе МОНИИАГ проведено открытое проспективное сравнительное исследование интраназального применения описанного препарата у 227 пар «мать — новорожденный» [48]. Первая группа пациентов профилактически применяла гель в соответствии с инструкцией к препарату 2 р/сут в течение 1 мес.; 2-я группа — с нарушением рекомендуемой схемы (например, применяли нерегулярно или только при заболевании), 3-я группа (контрольная) не применяла лекарственный препарат. У новорожденных детей применение изучаемого препарата приводило к уменьшению числа эпизодов ОРВИ в 2,5 раза по сравнению с контролем (7,9 и 20,2% соответственно, р<0,05); статистически значимому уменьшению выраженности клинических симптомов (уровня гипертермии и ее продолжительности, ринореи, кашля (р<0,05)) и, соответственно, сокращению длительности заболевания (в среднем на 3 дня). Статистически значимых различий между описанными показателями во 2-й и 3-й группах не установлено, что диктует необходимость соблюдения схем применения, изложенных в инструкции к препарату. Случаев COVID-19 среди новорожденных и их матерей, принимавших гель интраназально, на фоне пандемии не зарегистрировано. Хорошая переносимость препарата, отсутствие побочных эффектов отмечены у всех пациентов в исследовании, что очень важно для новорожденных младенцев с чувствительной слизистой оболочкой носовых ходов [48]. Данное исследование обосновало необходимость применения препарата рекомбинантного ИФН-α-2b с антиоксидантами в виде геля с целью профилактики новой коронавирусной инфекции и других ОРВИ начиная с неонатального периода.
В ГУЗ «СОИКБ имени Н.Р. Иванова» (Саратов) с апреля 2020 г. по февраль 2021 г. у новорожденных, имеющих контакт по COVID-19, использовали 2 схемы применения ИФН-α-2b с антиоксидантами (Виферон®) курсом 7 дней: назально в комбинации с ректальным применением (125 младенцев) и только назально (110 новорожденных). В первой группе COVID-19 развился у 4 (3,2%) контактных новорожденных, во второй — у 13 (11,8%), что показало снижение риска развития инфекции почти в 4 раза при сочетанном применении ИФН-α-2b в свечах и геле для слизистой носа [48]. Данное исследование очень важно для новорожденных, имеющих особенности врожденного иммунитета, в частности цитокинового статуса, предрасполагающие к развитию инфекции: низкий уровень продукции фактора некроза опухоли α, ИЛ-12 и ИФН-γ, низкий уровень экспрессии рецепторов к цитокинам на поверхности Т- и В-лимфоцитов (например, рецепторов к ИЛ-2, ИЛ-6, ИЛ-7 и ИНФ-γ) [32]. Поскольку в среднем у 50% инфицированных COVID-19 заболевание протекает бессимптомно, а практически у 80% пациентов с наличием клинических симптомов — в легкой форме ОРВИ, очень важна профилактика инфицирования контактных, особо незащищенных категорий детей неонатального периода, например, препаратом ИФН-α-2b в виде геля для слизистых и суппозиториев (Виферон®). Препарат в виде геля «обладает выраженным местным иммуномодулирующим действием и способствует увеличению локально образующихся антител класса секреторных IgA, препятствующих фиксации и размножению патогенных микроорганизмов на слизистых оболочках, что обеспечивает эффективность препарата для профилактики вирусных и других заболеваний» [42, 45, 49].
Препараты ИФН в различных формах выпуска (топические, ректальные) в качестве профилактического и лечебного средства при COVID-19 включены во все методические рекомендации по профилактике, диагностике и лечению новой коронавирусной инфекции, утвержденные Минздравом России, в том числе в последней, 18-й версии1-6.
Прогноз
SARS-CoV-2 во время беременности может воздействовать на развитие плода с помощью многих механизмов. Кроме плацентарных изменений не исключены возможные отдаленные последствия воздействия тяжелого острого респираторного синдрома, обусловленного SARS-CoV-2, во время беременности на развитие нервной системы плода [31]. Не было обнаружено свидетельств увеличения частоты грубых задержек в развитии среди младенцев, подвергшихся гестационному контакту с SARS-CoV-2. Однако метаанализ трех исследований, выполненный в соответствии с кокрейновскими протоколами, показал более низкие показатели в области мелкой моторики и личностно-социальной сферы ASQ-3 среди детей, матери которых переболели COVID-19 в разные сроки беременности [31]. В целом в детской популяции отмечен более благоприятный прогноз при COVID-19, чем у взрослых, однако описаны случаи тяжелого MIS-N и мультисистемного воспалительного синдрома детей с развитием аневризм коронарных артерий, сердечной дисфункции и мультиорганных воспалительных проявлений [25]. Выздоровление у новорожденных при легком течении преимущественно происходит в период от 1–2 нед. до 28 сут в зависимости от тяжести новой коронавирусной инфекции [15]. Описан случай благоприятного исхода у самого маловесного больного COVID-19, младенца 29 нед. гестации в Малайзии, который получил терапию сурфактантом, 14 дней находился на ИВЛ и выписан домой на 54-е сутки жизни [50].
Заключение
Таким образом, подтверждены риски инфицирования плода и новорожденного при перинатальном контакте и грудном вскармливании. Отмечена неспецифичность клинических проявлений COVID-19 с преобладанием бессимптомных и легких форм болезни в неонатальном периоде, особенно у недоношенных детей, с длительным выделением вируса с фекалиями. В редких случаях возможно развитие тяжелого MIS-N. Методические рекомендации, утвержденные Минздравом России, рекомендуют в качестве противовирусной терапии детей с COVID-19 при среднетяжелой и легкой степени тяжести препараты ИФН-α с антиоксидантами, особенно в свечах, которые обеспечивают «системное действие препарата, могут способствовать сокращению периода выделения вируса SARS-CoV-2 с фекалиями».
Многочисленные исследования подтверждают эффективность и безопасность применения препарата ИФН-α-2b в комплексе с антиоксидантами (витамины Е и С), суппозитории ректальные в сочетании с гелем, в лечении и профилактике COVID-19 у новорожденных, в том числе недоношенных. Ѓ
СВЕДЕНИЯ ОБ АВТОРАХ:
Панова Людмила Дмитриевна — д.м.н., профессор кафедры госпитальной педиатрии ФГБОУ ВО БГМУ Минздрава России; 450008, Россия, Уфа, ул. Ленина, д. 3; ORCID iD 0000-0001-7570-7420
Хисматуллина Зарема Римовна — д.м.н., профессор, заведующая кафедрой дерматовенерологии ФГБОУ ВО БГМУ Минздрава России; 450008, Россия, Уфа, ул. Ленина, д. 3; ORCID iD 0000-0001-8674-2803
Гурова Зухра Гельмешариповна — к.м.н., врач акушер-гинеколог, главный врач ГБУЗ РБ ГКПЦ г. Уфы; 450065, Россия, г. Уфа, ул. Кольцевая, д. 131; ORCID iD 0000-0002-9535-3014
Панов Павел Владимирович — к.м.н., врач-неонатолог, ООО «Клиника «Мать и Дитя»; 450077, Россия, г. Уфа, Лесной пр-д, д. 4.
Галеева Алина Анваровна — врач-неонатолог, заведующая обсервационным отделением новорожденных ГБУЗ РБ ГКПЦ г. Уфы; 450065, Россия, г. Уфа, ул. Кольцевая, д. 131.
Хамматшина Алсу Рифовна — врач-неонатолог ГБУЗ РБ ГКПЦ г. Уфы; 450065, Россия, г. Уфа, ул. Кольцевая, д. 131.
Идрисова Алиса Фуатовна — врач неонатолог-реаниматолог, заведующая отделением реанимации и интенсивной терапии новорожденных ГБУЗ РБ ГКПЦ г. Уфы; 450065, Россия, г. Уфа, ул. Кольцевая, д. 131.
Контактная информация: Панова Людмила Дмитриевна, e-mail: panov_home@ufacom.ru
Прозрачность финансовой деятельности: авторы не имеют финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 05.03.2025.
Поступила после рецензирования 28.03.2025.
Принята в печать 22.04.2025.
ABOUT THE AUTHORS:
Lyudmila D. Panova — Dr. Sc. (Med.), Professor of the Department of Hospital Pediatrics, Bashkir State Medical University; 3, Lenin str., Ufa, 450008, Russian Federation; ORCID iD 0000-0001-7570-7420
Zarema R. Khismatullina — Dr. Sc. (Med.), Professor, Head of the Department of Dermatovenerology, Bashkir State Medical University; 3, Lenin str., Ufa, 450008, Russian Federation; ORCID iD 0000-0001-8674-2803
Zukhra G. Gurova — C. Sc. (Med.), obstetrician-gynecologist, Chief Medical Officer, City Clinical Perinatal Center of Ufa; 131, Koltsevaya str., Ufa, 450065, Russian Federation; ORCID iD 0000-0002-9535-3014
Pavel V. Panov — C. Sc. (Med.), neonatologist, Clinic «Mat’ i Ditya» LLC; 4, Lesnoy Proezd str., Ufa, 450077, Russian Federation.
Alina A. Galeeva — neonatologist, Head of the Neonatal Observational Department, City Clinical Perinatal Center of Ufa; 131, Koltsevaya str., Ufa, 450065, Russian Federation.
Alsu R. Hammatshina — neonatologist, City Clinical Perinatal Center of Ufa; 131, Koltsevaya str., Ufa, 450065, Russian Federation.
Alisa F. Idrisova — neonatologist and intensive care physician, Head of the Neonatal Intensive Care and Intensive Care Unit, City Clinical Perinatal Center of Ufa; 131, Koltsevaya str., Ufa, 450065, Russian Federation.
Contact information: Lyudmila D. Panova, e-mail: panov_home@ufacom.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 05.03.2025.
Revised 28.03.2025.
Accepted 22.04.2025.
[1] Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)». Версия 16 (18.08.2022). (Электронный ресурс.) URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/060/193/original/%D0%92%D0%9C%D0%A0… (дата обращения: 24.12.2024).
[2] Методические рекомендации «Организация оказания медицинской помощи беременным, роженицам, родильницам и новорожденным при новой коронавирусной инфекции COVID-19». Версия 4 (05.07.2021). (Электронный ресурс.) URL: https://www.consultant.ru/law/hotdocs/70077.html (дата обращения: 20.12.2024).
[3] Методические рекомендации Минздрава России «Особенности клинических проявлений и лечения заболевания, вызванного новой коронавирусной инфекцией (COVID-19) у детей». Версия 2. (03.07.2020). URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/050/914/original/03062020_дети_COVI… (дата обращения: 20.12.2024).
[4] Методические рекомендации Минздрава России «Особенности клинических проявлений и лечения заболевания, вызванного новой коронавирусной инфекцией (COVID-19) у детей». Версия 2. (03.07.2020). URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/050/914/original/03062020_дети_COVI… (дата обращения: 20.12.2024).
[5] Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)». Версия 17 (14.12.2022). (Электронный ресурс.) URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/061/252/original/%D0%92%D0%9C%D0%A0… (дата обращения: 24.12.2024).
[6] Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)». Версия 18 (26.10.2023). (Электронный ресурс.) URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/064/610/original/%D0%92%D0%9C%D0%A0… (дата обращения: 24.12.2024).
[7] World Health Organization (2020). Clinical management of severe acute respiratory infection (SARI) when COVID-19 disease is suspected: interim guidance, 13 March 2020. World Health Organization. (Electronic resource.) URL: https://iris.who.int/handle/10665/331446 (access date: 24.12.2024).
Информация с rmj.ru






