Место ХОБЛ в развитии и прогрессировании коморбидности
А. С. Скотников*, кандидат медицинских наук
О. М. Дохова**
Е. С. Шульгина***
* ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
** ГБУЗ ГП № 6 Филиал № 4 ДЗМ, Москва
*** КГБУЗ ДГКБ № 9, Хабаровск
В сложившихся условиях «популярности» темы коморбидности, обусловленной
обилием больных с сочетанной патологией, большинство терапевтических научных
школ рассматривает конкретные нозологии, в т. ч. и хроническую обструктивную
болезнь легких (ХОБЛ), в тесной связи с другими часто встречающимися социально
значимыми заболеваниями [1–6].
Концепция локального воспаления при ХОБЛ как субстрата для развития
системного воспаления сегодня распространена и среди пульмонологов [7–9], при
этом роль последнего в отсроченном негативном влиянии на реологические свойства
крови [10], прогрессирование атеротромбоза [11], усугубление эндотелиальной
дисфункции [12], процессы канцерогенеза [13], углеводные и липидные нарушения
[14], аутоиммунные процессы [15], гемопоэз [16], синтез коллагена [17] и т. д.
широко исследована и продолжает изучаться. Однако в отечественной литературе до
сих пор очень трудно найти практические наблюдения за собственными больными,
указывающие на причастность ХОБЛ к степени тяжести и срокам возникновения
основных инвалидизирующих нозологических единиц клиники внутренних болезней.
С данной целью авторы провели работу по изучению взаимосвязи давности и
тяжести имеющейся ХОБЛ со сроками развития коморбидной патологии. Из 206
амбулаторных пациентов (средний возраст 66,1 ± 10,2 года), прикрепленных к
нескольким городским поликлиникам Москвы и Хабаровска, страдающих ХОБЛ вкупе с
другими хроническими заболеваниями, ХОБЛ в 43,2% случаев (n = 89)
манифестировала себя хронологически ранее остальных нозологий, а в 56,8% случаев
(n = 117) — позднее или одновременно с ними.
Таким образом, ХОБЛ как второе или последующее заболевание в структуре
хронологической коморбидности развивается на 13,6% чаще, чем ХОБЛ в качестве
первой болезни.
По данным амбулаторных карт в целом и листов для записи заключительных
(уточненных) диагнозов в частности, 206 коморбидных больных ХОБЛ разделили на
две группы. В группу «А» включили 89 (43,2%) пациентов (средний возраст 64,3 ±
11,2 года), у которых ХОБЛ в структуре коморбидности развилась хронологически
ранее основного и большинства сопутствующих заболеваний. В группу «Б» вошли 117
(56,8%) пациентов (средний возраст 67,9 ± 13,2 года), у которых диагноз ХОБЛ был
установлен позднее основного и большинства сопутствующих заболеваний.
Все пациенты независимо от первоочередности манифестации клинических
симптомов ХОБЛ имели схожие факторы риска развития как хронической бронхиальной
обструкции, так и других неинфекционных социально значимых заболеваний (табл.
1).
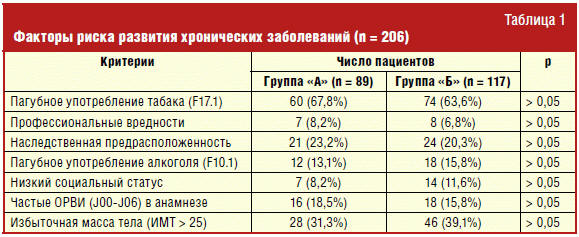
Как видно из данных, представленных в табл. 1, предпосылки для развития ХОБЛ
у пациентов сравниваемых групп были сопоставимы. Из всех факторов риска, которые
удалось установить по данным медицинской архивной документации, 65,1% больных (n
= 134) имели длительный стаж интенсивного курения, а 7,3% (n = 15) —
профессиональные вредности (загазованность или запыленность рабочего помещения,
работа с лакокрасочными материалами и т. д.). Кроме того, 21,8% больных (n = 45)
характеризовались наследственным анамнезом ХОБЛ (J44.1), бронхэктатической
болезни (J47), бронхиальной астмы (J45.9) или эмфиземы легких (J43), при этом
14,6% больных (n = 30) страдали хронической алкогольной интоксикацией, а 10,2%
пациентов (n = 21) обладали низким социальным статусом. Также 16,5% больных ХОБЛ
(n = 34) часто (более 4 раз в год) переносили острые респираторные вирусные
инфекции (ОРВИ), а 35,9% пациентов (n = 74) имели избыточный вес. Удельный вес
гиподинамии и хронического стресса у коморбидных больных ХОБЛ установить не
удалось, т. к. данные об этих факторах риска в подавляющем большинстве случаев
отсутствовали в амбулаторных картах.
Таким образом, в популяции имеет место общность факторов риска,
предрасполагающих к развитию и прогрессированию как ХОБЛ, так и других
хронических социально значимых заболеваний, что делает невозможным выявление
отдельной патогенетической роли каждого из них и диктует необходимость
комплексного подхода к больному уже на этапе коррекции предрасполагающих и
провоцирующих факторов.
Однако прогностическая значимость отдельных факторов риска в отношении
развития ХОБЛ тесно связана со временем их появления (табл. 2).
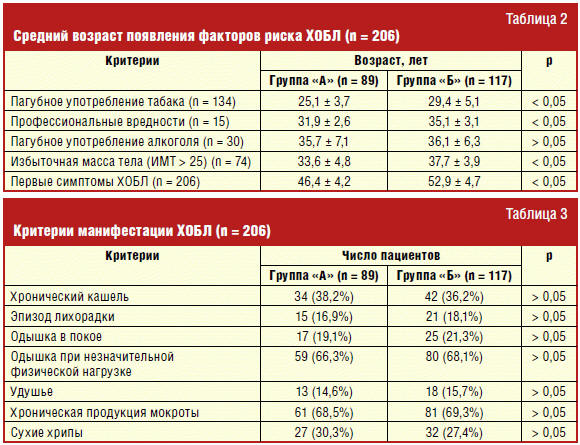
Как видно из данных, представленных выше, пациенты группы «А» начали курить
раньше пациентов группы «Б» в среднем на 4,3 года (14,6%) (p < 0,05), а
пристрастились к алкоголю раньше в среднем на 0,4 года (1,1%) (p > 0,05)
соответственно. Кроме того, пациенты группы «А» в среднем на 3,2 года (9,1%)
раньше (p < 0,05) подверглись воздействию профессиональных вредностей
респираторной системы, а также в среднем на 4,1 года (10,9%) раньше (p < 0,05) у
них появился избыточный вес. При этом для данной выборки больных (n = 206) время
до развития ХОБЛ от начала курения в среднем составило 22,5 года, от начала
пагубного пристрастия к алкоголю — 13,8 года, от начала воздействия
профессиональных вредностей — 16,2 года, а от появления избыточного веса — 13,9
года.
Таким образом, одним из наиболее агрессивных и длительно воздействующих
факторов риска ХОБЛ является пагубное пристрастие к табаку, при этом время
действия других предрасполагающих факторов примерно сопоставимо, а их
последовательное присоединение ускоряет темпы развития ХОБЛ.
Кроме того, средний возраст развития первых симптомов ХОБЛ прямо
пропорционально зависит от времени появления и начала воздействия на организм
данных факторов риска, при этом каждые 4 года их более ранней манифестации
приближают развитие ХОБЛ в среднем на 6,5 лет (p < 0,05), а, следовательно,
каждый год — на 1,6 года (p < 0,05).
В этой же части работы выявлена схожесть первых патогномоничных симптомов и
жалоб больных ХОБЛ (n = 206), когда-то послуживших поводом для обращения к
участковому терапевту (табл. 3).
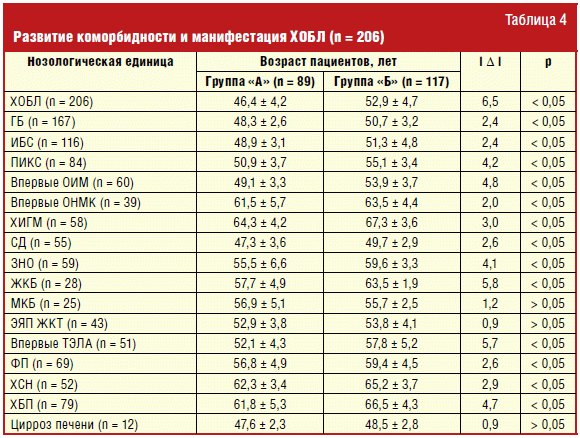
Как следует из табл. 3, наиболее частыми первыми симптомами ХОБЛ являлись
хроническая продукция мокроты (68,9%), одышка при умеренной физической нагрузке
(67,5%), хронический кашель (36,9%) и сухие хрипы (28,6%). Достоверных различий
по частоте их выявления получено не было.
Таким образом, первые клинические проявления ХОБЛ схожи у обеих групп больных
независимо от времени манифестации данного заболевания.
Как указывалось ранее, средний возраст пациентов группы «А» составил 64,3 ±
11,2 года, а пациентов группы «Б» — 67,9 ± 13,2 года. Вместе с тем первые
симптомы ХОБЛ у пациентов группы «А» появились в среднем в 46,4 ± 4,2 года, а у
пациентов группы «Б» — в 52,9 ± 4,7 года. Таким образом, на момент включения в
исследование пациенты группы «А» страдали ХОБЛ около 17,9 года, а пациенты
группы «Б» — примерно 15 лет соответственно. Согласно амбулаторной медицинской
документации, у всех 206 пациентов кроме ХОБЛ имела место хроническая
сопутствующая патология, средний возраст развития которой представлен в табл. 4.
Как указывалось ранее, пациенты группы «А» до развития ХОБЛ в среднем
возрасте 46,4 ± 4,2 года не имели какой-либо хронической соматической патологии.
Как следует из табл. 4, в относительно короткое время после развития ХОБЛ у
данных пациентов манифестировали сахарный диабет (СД), гипертоническая болезнь
(ГБ), ишемическая болезнь сердца (ИБС) и цирроз печени (в среднем через 0,9;
1,9; 2,5 и 1,2 года соответственно), впервые случились острый инфаркт миокарда (ОИМ)
и тромбоэмболия легочной артерии (ТЭЛА) (в среднем через 2,7 и 5,7 года
соответственно). Более того, у пациентов группы «А» в среднем спустя 4,5 года
после манифестации ХОБЛ развился постинфарктный кардиосклероз (ПИКС); через 17,9
года — хроническая ишемия головного мозга (ХИГМ); через 9,1 года —
злокачественные новообразования (ЗНО) различных локализаций; через 11,3 года —
желчнокаменная болезнь (ЖКБ); через 10,4 года — фибрилляция предсердий (ФП);
через 10,5 лет — мочекаменная болезнь (МКБ); через 6,5 лет — эрозивно-язвенные
поражения желудочно-кишечного тракта (ЭЯП ЖКТ); через 15,9 года — хроническая
сердечная недостаточность (ХСН); через 15,4 года — хроническая болезнь почек (ХБП);
а через 15,1 года впервые случилось острое нарушение мозгового кровообращения (ОНМК).
У пациентов группы «Б» за 2,2, 1,6, 3,2 и 4,4 года до развития ХОБЛ в среднем
возрасте 52,9 ± 4,7 года уже манифестировали ГБ, ИБС, СД и цирроз печени
соответственно. Как следует из табл. 4, в ближайшее время после вовлечения ХОБЛ
в коморбидную сосудистую патологию, у данных пациентов впервые случились ОИМ и
ТЭЛА (в среднем через 1,0 и 4,9 года соответственно), а также были
диагностированы МКБ и ЭЯП ЖКТ (в среднем через 2,8 и 0,9 года соответственно).
Более того, у пациентов группы «Б» в среднем через 2,2 года после присоединения
ХОБЛ развился ПИКС; через 14,4 года — ХИГМ; через 6,7 года — ЗНО различных
локализаций; через 10,6 года — ЖКБ; через 6,5 лет — ФП; через 12,3 года — ХСН;
через 13,6 года — ХБП; а спустя 10,6 года впервые случилось ОНМК.
Таким образом, сроки прогрессирования коморбидности при ХОБЛ зависят как от
условий возникновения самой ХОБЛ, так и от наличия патологии, предшествующей
развитию ХОБЛ.
Так, на 6,5 лет более ранняя манифестация ХОБЛ приближает развитие первого в
жизни ОИМ на 4,8 года (p < 0,05); первого ОНМК — на 2,0 года (p < 0,05); а
первой ТЭЛА — на 5,7 года (p < 0,05). Следовательно, каждый год более раннего
возникновения ХОБЛ приближает развитие первого в жизни ОИМ на 0,7 года; первого
ОНМК — на 0,3 года; а первой ТЭЛА — на 0,9 года.
Ситуация, подобная связи ХОБЛ с развитием сосудистых катастроф, наблюдается и
в отношении появления большей части хронических соматических заболеваний. Так,
на 6,5 лет более ранняя манифестация ХОБЛ на 4,2 года ускоряет сроки развития
ПИКС (p < 0,05); на 3,0 года — ХИГМ (p < 0,05); на 4,1 года — ЗНО разных
локализаций (p < 0,05); на 5,8 года — ЖКБ (p < 0,05); на 2,6 года — ФП (p <
0,05); на 2,9 года — ХСН (p < 0,05); а также на 4,7 года — ХБП (p < 0,05).
Следовательно, каждый год более раннего возникновения ХОБЛ приближает развитие
ПИКС на 0,7 года; ХИГМ на 0,5 года; ЗНО — на 0,6 года; ЖКБ — на 0,9 года; ФП —
на 0,4 года; ХСН — на 0,4 года; а ХБП — на 0,7 года, что доказывает важную роль
ХОБЛ в развитии и прогрессировании коморбидности.
Тем не менее, выявленная прогностическая значимость ХОБЛ не находит отражения
в структуре клинического диагноза (табл. 5). Как следует из данных,
представленных в табл. 5, у пациентов группы «А» частота развития ГБ была выше
на 11,5% (p < 0,05), ПИКС — на 17,3% (p < 0,05); ЗНО различных локализаций — на
8,9% (p < 0,05), а ХСН — на 11,0% (p < 0,05), чем у больных ХОБЛ группы «Б».
Кроме того, у пациентов группы «А» в анамнезе было на 7,6% (p < 0,05) больше
перенесенных ОНМК, на 23,2% больше (p < 0,05) — пневмоний и на 14% больше (p <
0,05) — ОИМ, возникших впервые в жизни.
Таким образом, первоочередное формирование ХОБЛ играет одну из
предрасполагающих ролей в последующем развитии повторных пневмоний, ЗНО, а также
ГБ и ее осложнений (ОИМ, ОНМК, ПИКС, ХСН).
С другой стороны, у пациентов группы «Б» на 12,1% выше (p < 0,05) была частота развития ИБС; на 6,1% выше (p < 0,05) — ХИГМ; на 5,5% выше (p < 0,05) — СД; на 10,1% выше (p < 0,05) — ХБП; на 5,6% выше (p < 0,05) — ФП; на 6,1% выше (p < 0,05) — ЖКБ и на 5,5% выше (p < 0,05) — МКБ. Также у пациентов группы «Б» в анамнезе было на 8% (p < 0,05) больше случаев ТЭЛА.
Таким образом, развитие ХОБЛ на фоне имеющихся ИБС, ГБ, СД, и ХИГМ оказывает
отягощающее влияние на их течение и частоту возникновения ФП, ТЭЛА и ХБП. В то
же время наличие таких клинических состояний, как ожирение, цирроз печени и ЭЯП
ЖКТ, не зависит от времени появления ХОБЛ (p > 0,05).
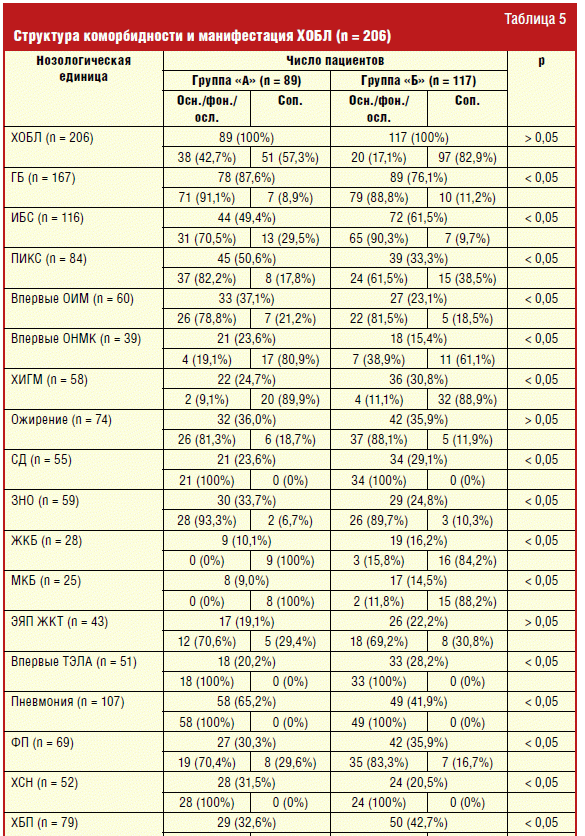
Как следует из табл. 5, если ХОБЛ возникала хронологически ранее других
нозологических единиц в структуре коморбидности, то клиницисты относили диагноз
ХОБЛ к сопутствующим заболеваниям более чем в половине случаев (57,3%). В
ситуациях же, когда ХОБЛ манифестировала себя позднее основного заболевания,
диагнозу ХОБЛ отводили место в рубрике сопутствующей патологии в 82,9% случаев.
Таким образом, независимо от времени и условий развития ХОБЛ, врачи в 71,8%
случаев (n = 148) расценивают ХОБЛ в качестве сопутствующей коморбидной
патологии, при этом в рубрику основного (фонового) заболевания клиницисты
зачастую относят сосудистую (ИБС, ГБ, СД, ХИГМ) или онкологическую (ЗНО)
патологию.
Другой немаловажной задачей работы было изучение особенностей течения и
прогрессирования коморбидной патологии в зависимости не только от времени
манифестации, но и от тяжести ХОБЛ, которую определяли по числу документированно
подтвержденных обострений данного заболевания в течение одного календарного
года. В последующем вышеописанные 206 пациентов были ретроспективно
перегруппированы в две когорты. Когорта «1» включила в себя 133 (64,6%) пациента
с ХОБЛ (средний возраст 68,3 ± 12,5 лет) с редкими обострениями (0–1 раз в год).
В когорту «2» вошли остальные 73 (35,4%) пациента (средний возраст 63,9 ± 13,8
года), относящиеся к устойчивому во времени фенотипу ХОБЛ — «пациент с частыми
обострениями» (более 2 раз в год).
Среднее число обострений в когорте «1» составило 1,4 в год, а в когорте «2» —
3,1 в год. Разница в среднем количестве обострений ХОБЛ в год между пациентами
когорты «1» и когорты «2» составила 1,7 эпизода в год. Спектр коморбидной
патологии у данных пациентов в зависимости от времени манифестации ХОБЛ
представлен в табл. 5, однако частота встречаемости отдельных нозологических
единиц, составляющих сочетанную патологию, в зависимости от тяжести течения ХОБЛ
приобрела другой вид (табл. 6).
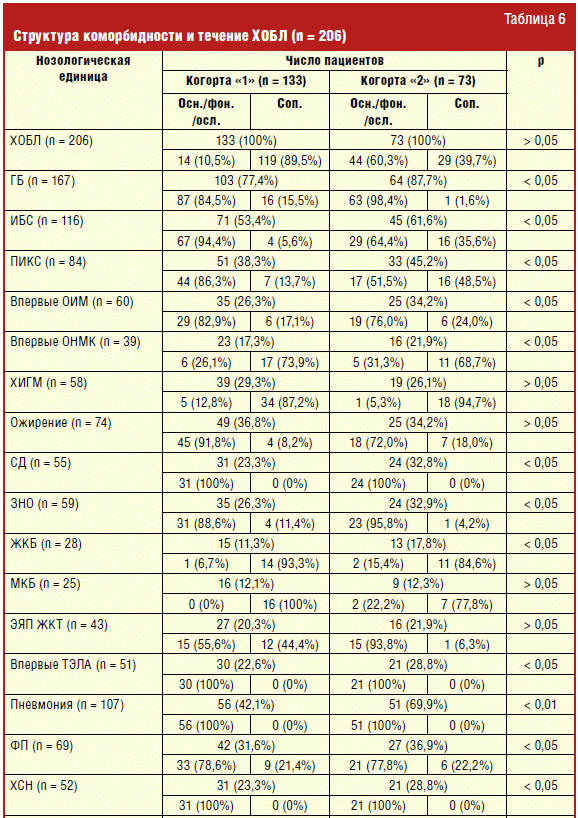
Как следует из данных, представленных в табл. 6, у пациентов с частыми
обострениями ХОБЛ на 10,3% чаще (p < 0,05) встречалась ГБ; на 8,2% чаще (p <
0,05) — ИБС; на 11,9% чаще (p < 0,05) — ПИКС; на 9,5% чаще (p < 0,05) — СД; на
6,6% чаще (p < 0,05) — ЗНО; на 6,5% чаще (p < 0,05) — ЖКБ; на 5,3% чаще (p <
0,05) — ФП; на 5,5% чаще (p < 0,05) — ХСН; на 6,4% чаще (p < 0,05) — ХБП.
Кроме того, у пациентов когорты «2» на 5,9% выше, чем у пациентов когорты «1»
(p < 0,05), была частота развития впервые в жизни возникшего ОИМ; на 4,6% выше (p
< 0,05) — первого ОНМК; на 6,2% выше (p < 0,05) — первой ТЭЛА; на 27,8% выше (p
< 0,01) — повторных пневмоний.
Таким образом, ХОБЛ с частыми обострениями способствует развитию большинства
нозологических единиц (ГБ, ИБС, ПИКС, СД, ХСН, ФП, ХБП, ЗНО и ЖКБ) в структуре
хронической соматической патологии, а также приводит к возникновению большего
числа острых событий (ОИМ, ОНМК, ТЭЛА, пневмонии). В то же время наличие таких
клинических состояний, как ХИГМ, ожирение, МКБ, цирроз печени и ЭЯП ЖКТ, не
зависит от тяжести течения ХОБЛ (p > 0,05).
Кроме того, как следует из табл. 6, клиницисты относили диагноз ХОБЛ с
частыми обострениями в рубрику сопутствующего заболевания в 39,7% случаев, что
на 17,6% реже (p < 0,05), чем в случаях с ранней манифестацией ХОБЛ, и на 43,2%
реже (p < 0,01), чем в ситуациях с ее возникновением хронологически позднее
большинства нозологий.
В ситуациях же, когда течение ХОБЛ характеризовалось редкими обострениями,
данному диагнозу отводили место в рубрике сопутствующей патологии в 89,5%
случаев, что на 6,6% чаще (p > 0,05) случаев поздней манифестации ХОБЛ.
Таким образом, конструкция клинического диагноза коморбидного больного ХОБЛ в
большей степени зависит от тяжести течения данного заболевания, чем от времени и
условий его возникновения, при этом временное расположение данной нозологии в
рубрике основного заболевания наблюдается либо в случаях ее тяжелого
рецидивирующего течения, либо в периоды обострения.
С учетом разницы в среднегодовом количестве обострений ХОБЛ между пациентами
когорт «1» и «2», в табл. 7 представлен средний возраст развития хронических
соматических заболеваний и острых клинических состояний у пациентов с разной
степенью тяжести ХОБЛ.
Как видно из табл. 7, у пациентов с частыми обострениями ХОБЛ средний возраст
развития большинства сопутствующих заболеваний ниже, чем таковой у пациентов с
редкими обострениями ХОБЛ.
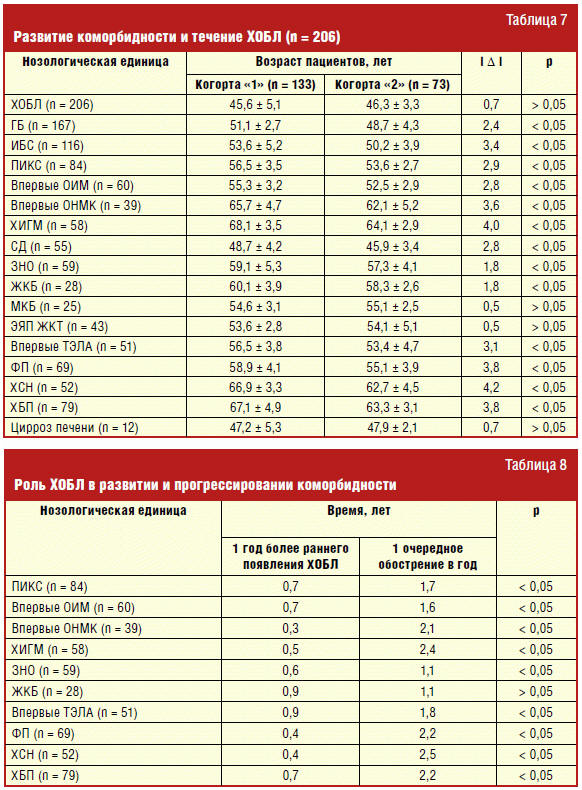
Так, средний возраст манифестации ГБ у больных когорты «2» меньше данного
показателя в когорте «1» на 2,4 года (p < 0,05); ИБС — на 3,4 года (p < 0,05);
ПИКС — на 2,9 года (p < 0,05); ХИГМ — на 4,0 года (p < 0,05); СД — на 2,8 года (p
< 0,05); ЗНО — на 1,8 года (p < 0,05); ЖКБ — на 1,8 года (p < 0,05); ФП — на 3,8
года (p < 0,05); ХСН — на 4,2 года (p < 0,05); ХБП — на 3,8 года (p < 0,05). При
этом пациенты со впервые в жизни возникшими ОИМ, ОНМК и ТЭЛА в когорте «2» были
младше таковых в когорте «1» на 2,8 (p < 0,05), 3,6 (p < 0,05) и 3,1 года (p <
0,05) соответственно.
В то же время развитие таких клинических состояний, как МКБ, цирроз печени и
ЭЯП ЖКТ, не зависят от тяжести течения ХОБЛ (p > 0,05).
Сравнение удельного веса времени и условий манифестации ХОБЛ, а также тяжести
ее течения в отношении прогностической значимости развития заболеваний в
структуре коморбидности представлено в табл. 8.
Как следует из данных, представленных в табл. 8, каждое обострение ХОБЛ в
течение одного года приближает развитие ГБ на 1,4 года; ИБС — на 2 года; ПИКС —
на 1,7 года; ХИГМ — на 2,4 года; СД — на 1,6 года; ЗНО — на 1,1 года; ЖКБ —
также на 1,1 года; ФП — на 2,2 года; ХСН — на 2,5 года; ХБП — на 2,2 года. Кроме
того, одно обострение ХОБЛ в течение года приближает развитие первого в жизни
ОИМ на 1,6 года; первого ОНМК — на 2,1 года; первой ТЭЛА — на 1,8 года.
Таким образом, значимость каждого обострения ХОБЛ в отношении сроков развития
и прогрессирования коморбидной патологии выше, чем прогностическая роль каждого
года более ранней манифестации данной болезни.
Тяжесть течения ХОБЛ значимее условий ее манифестации для приближения ПИКС —
на 58,8% (p < 0,05); ХИГМ — на 79,2% (p < 0,05); ЗНО — на 45,5% (p < 0,05); ФП —
на 81,8% (p < 0,05); ХСН — на 84,0% (p < 0,05); ХБП — на 68,8% (p < 0,05).
Подобная тенденция отмечена также для «сосудистых катастроф» — тяжесть ХОБЛ
прогностически значимее времени ее развития для первого в жизни ОИМ — на 56,3% (p
< 0,05); первого ОНМК — на 85,7% (p < 0,05); а также первой ТЭЛА — на 50,0% (p <
0,05). Для ЖКБ, МКБ, цирроза печени, ХАИ, ЭЯП ЖКТ статистически значимых
результатов касательно преимуществ течения ХОБЛ над временем ее манифестации
получено не было (p > 0,05).
При анализе табл. 8 также обращает на себя внимание отсутствие данных о
прогностической роли ХОБЛ в отношении развития ГБ, ИБС и СД. Этот факт
объясняется отсутствием между пациентами групп «1» и «2» сравнительной
информации о влиянии времени возникновения ХОБЛ на развитие коморбидности, ввиду
наличия данных заболеваний у большинства больных из группы «2» еще до
манифестации у них ХОБЛ.
Еще одной отличительной чертой, согласно табл. 8, является обнаруженная
схожесть прогностического влияния ХОБЛ (рассчитанного как по времени
возникновения, так и по тяжести) на развитие ряда заболеваний в структуре
коморбидности, среди которых ФП и ХСН (0,4 года); впервые ОИМ, ПИКС и ХБП (0,7
года); впервые ТЭЛА и ЖКБ (0,9 года); впервые ОИМ и СД (1,6 года); ФП и ХБП (2,2
года) и т. д.
Таким образом, авторами было доказано, что сроки развития коморбидной
патологии зависят не только от времени манифестации ХОБЛ, но и от тяжести ее
течения, при этом самой неблагоприятной группой в отношении прогноза развития и
интенсивности прогрессирования коморбидности являются больные с ранним
появлением ХОБЛ и фенотипом «пациент с частыми обострениями» (более 2 раз в
год).
Литература
-
Чучалин А. Г., Цеймах И. Я., Момот А. П., Мамаев А. Н., Карбышев И.
А., Костюченко Г. И. Изменения системных воспалительных и гемостатических
реакций у больных с обострением хронической обструктивной болезни легких с
сопутствующими хронической сердечной недостаточностью и ожирением //
Пульмонология. 2014. № 6. С. 25–32 -
Задионченко В. С., Адашева Т. В., Ли В. В., Жердева Е. И., Малиничева
Ю. В., Нестеренко О. И., Павлов С. В. Артериальная гипертензия и
хроническая обструктивная болезнь легких — проблемы выбора терапии // Лечащий
Врач. 2012. № 7. С. 77–81. -
Лазебник Л. Б., Конев Ю. В., Ефремов Л. И. Полиморбидность в
гериатрической практике: количественная и качественная оценка // Клиническая
геронтология. 2012. № 1–2. С. 36–42. -
Дворецкий Л. И., Чистякова Е. М. Остеопороз у больных ХОБЛ:
коморбидность или системное проявление? // Consilium medicum, 2007. № 12. С.
42–48. -
Белялов Ф. И. Двенадцать тезисов коморбидности // Клиническая
медицина. 2009. № 12. С. 69–71 -
Насонов Е. А., Гордеев А. В., Галушко Е. А. Ревматические
заболевания и мультиморбидность // Терапевтический архив. 2015. № 5. С. 4–9. -
Зайцев А. А., Безлепко А. В., Синопальников А. И. Диагностика и
фармакотерапия ХОБЛ: основные положения // Фарматека. 2015. № 4. С. 18–24. -
Гайнитдинова В. В., Авдеев С. Н. Ремоделирование крупных
периферических артерий у больных хронической обструктивной болезнью легких и
при ее сочетании с артериальной гипертензией // Пульмонология. 2015. № 1. С.
50–57. -
Чучалин А. Г., Авдеев С. Н., Айсанов З. Р., Белевский А. С., Лещенко
И. В., Мещерякова Н. Н., Овчаренко С. И., Шмелев Е. И. Федеральные
клинические рекомендации по диагностике и лечению хронической обструктивной
болезни легких // Пульмонология. 2014. № 3. С. 15–36. -
Калюжин В. В., Сибирева О. Ф., Беспалова И. Д., Калюжина Е. В., Ткалич
Л. М., Милованова Т. А., Осихов И. А., Мурашев Б. Ю. Протромботический
статус у пациентов с метаболическим синдромом: связь с воспалением //
Терапевтический архив. 2013. № 10. С. 29–33. -
Провоторов В. М., Будневский А. В., Семенкова Г. Г., Шишкина Е. С.
Провоспалительные цитокины при сочетании ИБС и ХОБЛ // Клиническая
медицина. 2015. № 2. С. 5–9. -
Мамаева М. Г., Собко Е. А., Крапошина А. Ю., Соловьева И. Л., Логачева
Н. С., Эйдемиллер Н. С., Кузьминова Т. Н., Салмина А. Б., Демко И. В.
Клинико-патогенетические аспекты формирования артериальной ригидности и
ремоделирования левых отделов сердца при сочетании хронической обструктивной
болезни легких и ишемической болезни сердца // Пульмонология. 2014. № 5. С.
5–9. -
Лаптева Е. А., Лаптева И. М., Харевич О. Н. Системные эффекты
ХОБЛ на этапах ее прогрессирования // Казанский медицинский журнал. 2013. № 5.
С. 605–609. -
Будневский А. В., Овсянников Е. С., Чернов А. В., Дробышева Е. С.
Диагностическое значение биомаркеров системного воспаления при ХОБЛ //
Клиническая медицина. 2014. № 9. С. 16–21. -
Боташев А. А., Терещенко О. А., Сергиенко В. И., Петросян Э. А.
Современные взгляды на патогенетическую взаимосвязь между системным
воспалением и иммунной системой при желчном перитоните, осложненном
абдоминальным сепсисом // Иммунология. 2013. № 3. С. 164–167. -
Дыгай А. М. Воспаление и гемопоэз. Томск: Изд-во Томского ун-та,
1992. -
Насонов Е. Л., Попкова Т. В., Новикова Д. С. Кардиоваскулярные
факторы риска при ревматических заболеваниях: связь с воспалением // Consilium
medicum. 2010. № 2. С. 112–118.
Статья опубликована в журнале
Лечащий Врач
материал MedLinks.ru






