Введение
Периферическая язва роговицы (ПЯР) относится к острым воспалительным заболеваниям, при которых образуются язвенные дефекты в эпителии и подлежащей строме перилимбальной зоны роговицы [1]. В зарубежных публикациях наиболее часто встречается термин «периферический язвенный кератит», распространенность этого заболевания в популяции составляет 0,2–3 на 1 млн населения [2, 3]. Причиной периферического поражения роговицы могут быть различные неинфекционные факторы, реже — инфекционные. Более половины случаев ПЯР относится к неинфекционным и ассоциированы с системными аутоиммунными заболеваниями соединительной ткани: ревматоидным артритом (РА), системной красной волчанкой, узелковым полиартериитом, системными васкулитами [1, 4, 5]. Особым видом ПЯР является язва Мурена, которая развивается в результате аутоиммунного изолированного воспаления в ткани роговицы [6]. В ряде случаев возможно образование язвенных дефектов на фоне краевого кератита, ассоциированного с блефаритами, розацеа (33%) и другими дерматологическими, неврологическими заболеваниями, а также в исходе глазной хирургии [7]. Среди инфекционных заболеваний, которые могут привести к возникновению ПЯР, упоминают герпес, туберкулез, сифилис, болезнь Лайма, грибковые и паразитарные инфекции [8]. По данным N. Sharma et al. [2], инфекционные ПЯР составляют 19,7% среди всех случаев заболевания, в большинстве (73,3%) случаев они вызваны бактериальными патогенами [2].
Развитие воспаления в периферической зоне роговицы определяется особенностями ее гистологического строения и иммунного ответа. Особенностями периферии роговицы являются бóльшая в сравнении с центральными отделами толщина, более плотные контакты эпителиальных клеток с базальной мембраной и стромой и плотная упаковка стромального коллагена, наличие резервуара стволовых клеток эпителия роговицы, высокая митогенная активность эндотелиальных клеток и сниженная плотность чувствительных нервных окончаний. С точки зрения развития иммунного воспаления наибольший интерес представляет особенность кровоснабжения роговицы. Известно, что роговица относится к тканям, обладающим иммунной и антигенной привилегией, механизм которой сложен и многообразен. Одним из ключевых моментов иммунной привилегии является отсутствие в роговице кровеносных и лимфатических сосудов и, соответственно, прямой связи с органами иммунной системы. В отличие от бессосудистой центральной части роговицы, лимб и периферия получают питание из капиллярных аркад, которые внедряются на 0,5 мм в ткань роговицы. Это способствует отложению иммунных комплексов и других крупных молекул: IgM, компонентов комплемента C1 и комплексов антиген — антитело на периферии роговицы. При ПЯР в ассоциации с ревматическими заболеваниями (РЗ) аутоантигены (ревматоидный фактор, антинуклеарные и антицитоплазматические антитела) приводят к активации резидентных лимбальных макрофагов, клеток Лангерганса и антигенспецифичных Т-лимфоцитов (CD4+), продуцирующих медиаторы воспаления. Образующиеся аутоантитела к коллагену, ламинину и другим белкам роговицы, а также молекулы металлопротеиназ ММР-1 и ММР-8, продуцируемые нейтрофилами и фибробластами, разрушают роговичную ткань [1, 4, 6, 7, 9, 10]. Индуцировать аутоиммунное воспаление в роговице может травма или хирургия глаза.
Клинические проявления неинфекционного кератита и язвы роговицы, включая ПЯР, имеют ряд общих признаков с инфекционными кератитами и дегенерациями роговицы. Ввиду частой встречаемости инфекционных заболеваний глаза в повседневной практике офтальмолога нередки случаи ошибок в диагностике и лечении пациентов. С учетом острого течения, быстрого лизиса стромы и образования перфорации роговицы аутоиммунные ПЯР могут привести к потере зрения, что определяет актуальность дальнейшего изучения этого заболевания.
Цель исследования: описать клинические симптомы ПЯР, определить связь с РЗ, особенности течения и оценить эффективность терапии.
Содержание статьи
Материал и методы
Под наблюдением на клинических базах кафедры офтальмологии ФГБОУ ВО ЮУГМУ Минздрава России находилось 32 пациента с ПЯР на фоне системных заболеваний соединительной ткани, в том числе 9 (28,1%) мужчин и 23 (71,9%) женщины, средний возраст 59,3±9,4 года. Исследование одобрено локальным этическим комитетом ФГБОУ ВО ЮУГМУ Минздрава России. Набор участников осуществлен по мере обращаемости методом сплошной выборки, оформлено информированное согласие на участие в исследовании.
Офтальмологический диагноз устанавливали на основании жалоб и анамнеза заболевания, сопутствующие системные заболевания диагностировали по данным медицинской документации. Офтальмологическое обследование включало определение максимально корригированной остроты зрения (МКОЗ), биомикроскопии переднего и заднего отрезка глаза, определение чувствительности роговицы. Диагностика степени ксероза глазной поверхности проводилась на основании пробы Ширмера с применением тест-полосок и расчета времени разрыва слезной пленки (ВРСП) по тесту Норна с применением красителя флуоресцеина натрия. Параллельно на основании количества точек и зон окрашивания роговицы оценивали степень повреждения ее эпителия и истинный размер дефекта.
Для исключения инфекционной природы кератита проводили бактериологическое исследование мазков с поверхности язвы и конъюнктивы, микроскопию ресниц для выявления клещей демодекса, при подозрении на герпес — ПЦР соскоба роговицы. Ассоциацию с системными заболеваниями устанавливали на основании данных медицинской документации и углубленного лабораторного и клинического обследования, совместно с терапевтом и ревматологом.
В зависимости от степени тяжести поражения роговицы офтальмологическое лечение проводилось амбулаторно или стационарно. Системную базисную терапию РЗ назначал ревматолог, системную терапию глюкокортикостероидами (ГКС) при тяжелом течении ПЯР с угрозой перфорации роговицы — офтальмолог.
Результаты исследования статистически обработаны с использованием пакета программ IBM SPSS Statistics 22.
Результаты исследования
При обращении к офтальмологу пациенты предъявляли жалобы на светобоязнь и боли в глазу — 23 (71,9%) наблюдения, покраснение глаза — 18 (56,2%), снижение зрения вдаль и вблизи — 29 (90,6%), слизисто-гнойное отделяемое из глаза — 8 (25%). На основании анамнеза и данных медицинской документации выявлено, что 7 (21,9%) пациентов амбулаторно получали лечение с диа-гнозом «синдром «сухого глаза» (ССГ), в том числе ассоциированный с РА — 5 (15,6%), с синдромом Шегрена — 2 (6,2%).
Ревматологическое заболевание установлено у 24 (75%) пациентов: РА — у 18 (56,2%), болезнь Шегрена — у 2 (6,2%), гранулематоз с полиангиитом — у 3 (9,4%), эозинофильный васкулит (синдром Чарга — Стросса) — у 1 (3,1%). По назначению ревматолога пациенты получали преднизолон 5–7,5 мг/сут (4 (12,5%)), метотрексат 10–15 мг/нед. (9 (28,1%)) либо их сочетание (7 (21,9%)), адалимумаб (2 (6,2%)), ритуксимаб (2 (6,2%)), что, однако, не предотвратило поражение роговицы. Ранее не обращались к ревматологу 8 (25%) пациентов, однако на основании лабораторных данных и углубленного обследования совместно с ревматологом им выставлены диагнозы: гранулематоз с полиангиитом (1 (3,1%)), РА (2 (6,2%)), псориатический артрит (2 (6,2%)), реактивный артрит (3 (9,4%)).
При оценке офтальмологического статуса установлено: МКОЗ при обращении: светоощущение — у 3 (9,4%) пациентов; 0,01–0,1 — у 12 (37,5%); 0,1–0,5 — у 10 (31,2%) и 0,5–1,0 — у 7 (21,9%). При биомикроскопии перикорнеальная инъекция глаза отмечена у 13 (40,6%) пациентов, расширение и извитость эписклеральных сосудов в зоне, примыкающей к дефекту роговицы, без классической перикорнеальной инъекции по окружности лимба — у 9 (28,1%). Более выраженная гиперемия и извитость глубоких сосудов эписклеры с ее инфильтрацией имели место у 10 (31,2%) пациентов, в том числе с признаками некроза склеры — у 2. В периферических участках роговицы в 2–3 мм от лимба располагались полупрозрачные светло-серые овальные или серповидные инфильтраты с дефектом эпителия и стромы роговицы (рис. 1).
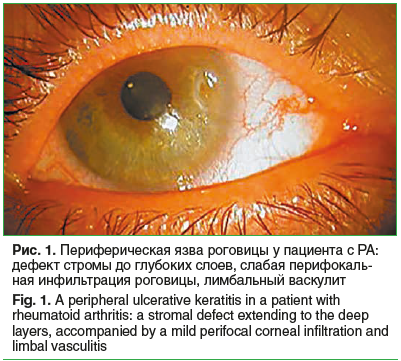
Периферическая язва чаще выглядела как ступенчатый или ровный овальный дефект стромы размерами от 3 до 6 мм, реже в виде полумесяца более 6 мм длиной — в 4 (12,5%) случаях. Глубина дефекта на 1/3 стромы отмечена в 37,5% случаев, до глубоких слоев стромы — в 7 (21,8%). Овальный дефект, практически без видимой перифокальной инфильтрации роговицы и инъекции глаза, наблюдался у 4 (12,5%) пациентов. В 9 (28,1%) случаях, помимо инфильтрации и изъязвления, в периферических участках определялись рубцовые помутнения и истончение ткани роговицы, свидетельствующие о перенесенных ранее подобных процессах. Преимущественная локализация ПЯР наблюдалась в зоне открытой глазной щели с височной стороны, реже — с носовой. У 6 (18,7%) пациентов при первичном обращении выявлена перфорация роговицы. Признаки бактериального инфицирования язвы в виде ярко выраженной перикорнеальной инъекции, слизисто-гнойного отделяемого из конъюнктивальной полости и интенсивно серой или желтой инфильтрации вокруг язвенного дефекта определялись у 5 (15,6%) пациентов. Воспалительная клеточная реакция в передней камере 1+, мелкие преципитаты на эндотелии роговицы и задние синехии выявлены у 3 (9,4%) пациентов. Изменения на парном глазу отмечены у 18 (56,2%) пациентов в виде периферических васкуляризованных помутнений и локального истончения роговицы по периферии. Двусторонние язвы роговицы выявлены в 3 (9,4%) случаях при эозинофильном васкулите и полиангиите с гранулематозом.
Исследование слезопродукции выявило снижение пробы Ширмера до 6±2 мм. Более значимыми были изменения стабильности слезной пленки: ВРСП по Норну на глазу с ПЯР определялось в пределах 2±1 с, на парном глазу — 4±3 с. Накопление флуоресцеина соответствовало зоне дефекта роговицы, а множественные точки прокрашивания роговицы были выявлены на обоих глазах в зоне от центра к нижнему сектору роговицы (рис. 2).
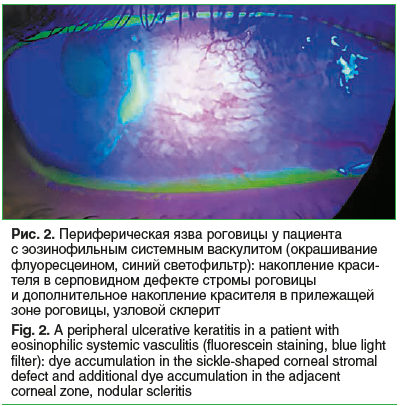
Лечение зависело от тяжести и скорости прогрессирования ПЯР. Амбулаторно лечение проведено 13 (40,6%) пациентам с поверхностными, медленно прогрессирующими ПЯР. Алгоритм лечения включал инстилляции пиклоксидина 0,05% 2 р/сут с целью профилактики инфицирования, дексаметазона 0,1% от 2 до 4 капель в день коротким курсом до 2 нед., с дальнейшим переходом на циклоспорин А 0,05% 2 р/сут. Для ускорения заживления язвенного дефекта назначали гель декспантенола 5% (Корнерегель®) 3 р/сут — днем и перед сном. Дополнительно через 2 ч назначали менее вязкие бесконсервантные слезозаместители на основе гиалуроната натрия 0,1–0,24%, в том числе комбинированные с гепарином 1300 ЕД 3–4 р/сут. Покрытие роговицы мягкой контактной линзой выполнено у 7 пациентов, однако в 2 случаях на 4–5-е сутки отмечено появление густого слизистого отделяемого и усиление инфильтрации вокруг дефекта, что было расценено как инфицирование, это послужило показанием для отмены линзы и назначения инстилляций 0,3% левофлоксацина. Скорость рассасывания отека, инфильтрации в роговице и заживление язвенного дефекта варьировали от 2 до 4 нед.
Лечение в условиях офтальмологического стационара (ГБУЗ ОКБ № 3 г. Челябинска) получали 19 (59,4%) пациентов. Показанием для госпитализации была неэффективность амбулаторной терапии по месту жительства или первичное обращение пациента с глубоким дефектом роговицы или ее перфорацией. Локально назначали антибактериальные препараты, инстилляции 0,1% дексаметазона 4 р/сут с постепенным снижением, инъекции под конъюнктиву дексаметазона 2 мг, а случае инфицирования — цефтриаксона 100 мг. Нестероидный противовоспалительный препарат (НПВП) бромфенак 0,09% назначали 2 р/сут при выраженном болевом синдроме у пациентов с сочетанием ПЯР и склерита. Системные ГКС в дополнение к базисной терапии назначались в зависимости от тяжести поражения глаза и соматического статуса пациента: перорально преднизолон с дозы 1 мг/кг в сутки либо внутривенная пульс-терапия (метипред по 1000 мг в течение 3 сут), с переходом на прием преднизолона внутрь в дозе 0,5 мг/кг и постепенным снижением до поддерживающей дозы 7,5 мг/сут в течение 3 мес. Назначение слезозаместительной и репаративной терапии соответствовало амбулаторному этапу. Восполнение дефекта роговицы на фоне консервативного лечения достигнуто у 6 (18,7%) пациентов к 7–12-м суткам.
Показаниями к хирургическому вмешательству были глубокий язвенный дефект стромы роговицы, образование десцеметоцеле или перфорация язвы. С учетом экстренности ситуации выбор вида кератопластики зависел от наличия донорского материала. Тектоническая кератопластика аутоконъюнктивой и амниотической оболочкой выполнена 4 (12,5%) и 3 (9,4%) пациентам соответственно, передняя послойная кератопластика консервированной донорской роговицей с последующей тарзорафией — 5 (15,6%). Дальнейшее лечение соответствовало амбулаторному этапу.
В результате консервативного лечения достигнуто формирование рубцовых помутнений роговицы с обильной васкуляризацией. При осмотре пациентов через 3–6 мес. после хирургической пластики дефекта роговицы также обнаружено обильно васкуляризованное рубцовое помутнение роговицы, в том числе рубец, сращенный с радужкой (4 (12,5%)). Неблагоприятный исход с перфорацией роговицы и склеры и развитием эндофтальмита с последующей энуклеацией глазного яблока отмечен у 1 (3,1%) пациентки с ПЯР в сочетании с некротизирующим склеритом на фоне впервые диагностированного полиангиита с гранулематозом. МКОЗ в результате лечения зависела от степени прозрачности оптических сред глаза и степени вторичного астигматизма и составила: светоощущение — у 2 (6,3%) пациентов, 0,01–0,1 — у 11 (34,4%), 0,1–0,5 — у 10 (31,2%), 0,5–1,0 — у 8 (25%).
Обсуждение
В настоящее исследование включены только пациенты с ПЯР на фоне системных аутоиммунных заболеваний соединительной ткани, при этом наиболее частая ассоциация ПЯР была установлена с РА (56,2%), что согласуется с опубликованными ранее данными [1, 11]. Из особенностей течения ПЯР на фоне РЗ следует отметить быстрый кератолиз роговицы, вплоть до перфорации (18,7%), двустороннее поражение глаз и сочетание со склеритом (31,2%), реже — с передним увеитом. Наблюдаемые изменения перилимбальных сосудов ряд авторов описывают как некротизирующий васкулит передних цилиарных артерий (перилимбальный артериит) [1, 7].
Периферические язвы роговицы при РЗ необходимо дифференцировать с другими неинфекционными поражениями периферии роговицы, в частности с розацеа-кератитом, краевым кератитом с изъязвлением, а также с кератитами и язвами роговицы при вирусной и бактериальной инфекции, что может быть затруднительно при вторичном инфицировании ПЯР на фоне аутоиммунного процесса. Диагноз «язва Мурена» устанавливается при исключении всех других этиологических факторов. Помимо заболеваний воспалительной природы, ПЯР следует дифференцировать с дегенерациями роговицы: краевой дегенерацией Терриена, пеллюцидной краевой дегенерацией, лимбальным пояском Фогта, дегенерацией Зальцмана и другими, для которых характерно бессимптомное течение с периферическим истончением стромы роговицы при интактном эпителии, а основными жалобами являются снижение зрения и искажение предметов [1].
Выбор противовоспалительной терапии при ПЯР вызывает определенные трудности. С учетом необходимости быстрого подавления аутоиммунного ответа в остром периоде ПЯР назначение ГКС локально и системно является патогенетически обоснованным. Однако локальное использование ГКС вызывает активную дискуссию среди офтальмологов, так как известно, что дексаметазон, ингибируя пролиферацию фибробластов, замедляет восполнение и эпителизацию дефекта роговицы и даже может ускорить ее перфорацию [9]. Однако, как отмечено в наших наблюдениях, в ситуации аутоиммунного васкулита и склерита в сочетании с ПЯР кратковременное локальное применение ГКС блокирует активацию иммунных клеток и, соответственно, продуцируемых провоспалительных цитокинов, антител, металлопротеаз, что останавливает кератолизис. Попытки лечения исключительно репаративными и слезозаместительными препаратами, как правило, остаются безуспешными, что нашло подтверждение в нашем исследовании: большинство пациентов до госпитализации в стационар получали трофическую терапию. Исследования эффективности и безопасности раннего назначения ГКС при лечении бактериальных язв роговицы показали, что в результате блокирования воспаления снижается активность коллагенолизиса и быстрее сокращается размер язвенного дефекта, уменьшается ангиогенез, формируется структурный рубец [12]. Однако при назначении ГКС важно исключить герпетическую и грибковую этиологию кератита. ГКС обладают наиболее быстрым иммуносупрессивным эффектом, но при продолжении лечения рекомендуется длительное локальное применение иммуносупрессантов, к которым относится циклоспорин А 0,05–0,1%, его терапевтический эффект развивается через 1–2 мес. Назначение НПВП при ПЯР не является методом выбора. Известно, что НПВП обладают цитотоксическим воздействием на клетки эпителия и могут вызывать безболезненный лизис роговицы, особенно у пациентов с сухим кератоконъюнктивитом и РА, поэтому применять их также следует с большой осторожностью и непродолжительно, преимущественно у пациентов с сопутствующим склеритом [13]. В зарубежных рекомендациях также указывается на эффективность применения ингибиторов коллагеназы или ингибиторов коллагеназосинтетазы (раствор ацетилцистеина 20%), однако они не представлены в Российской Федерации, а по данным зарубежных коллег, не обладают значимым эффектом в отношении торможения распада коллагеновых волокон [9, 11]. По нашим наблюдениям, при тяжелом течении ПЯР с угрозой перфорации наиболее значимой была терапия высокими дозами системных ГКС, в результате чего на 2–3-и сутки останавливалось прогрессирование лизиса роговицы и начиналось медленное восполнение дефекта. Для предотвращения рецидивов ПЯР, а также сопутствующего склерита и увеита важно ведение пациента совместно с ревматологом, подбор базисной терапии, а в ряде случаев и назначение генно-инженерных биологических препаратов [4, 14].
Практически у всех пациентов с ПЯР выявлено умеренное снижение количества слезы при проведении пробы Ширмера и нарушение стабильности слезной пленки, соответствующие тяжелой степени роговично-конъюнктивального ксероза. Нарушение секреции основной и добавочных слезных желез при РЗ убедительно доказано в ранее проведенных исследованиях и является одним из проявлений синдрома Шегрена. В связи с этим назначение постоянной слезозаместительной терапии — обязательный компонент терапии [4, 8]. Кроме того, значимое влияние на скорость заживления роговицы оказывает репаративная терапия. При отсутствии признаков инфицирования ПЯР назначение репаративных гелей и мазей можно начинать с первого дня лечения. В нашем исследовании применялся 5% гель декспантенола (Корнерегель®), преимуществами которого являются высокая концентрация декспантенола, гелевая основа (карбомер) и нетоксичный консервант (цетримид). Ранее в эксперименте и клинической практике показана способность декспантенола стимулировать регенерацию поврежденной роговицы, активировать пролиферацию клеток эпителия глазной поверхности и репарацию стромы роговицы [15, 16]. В исследованиях B.I. Weimann et al. [17] доказан дозозависимый эффект D-пантотената кальция и установлено, что максимальная стимуляция пролиферации и ускорение миграции кератоцитов в область раны роговицы отмечаются при применении препарата в концентрации от 5 до 10%. Декспантенол также обладает небольшим противовоспалительным эффектом и влияет на архитектуру формирующейся ткани, делая ее более организованной [16]. Применение в качестве основы карбомера обеспечивает слезозаместительную функцию. Взаимодействуя со слоем муцина и молекулами воды за счет ионизированных участков молекулы, карбомер восполняет водно-муциновый слой прекорнеальной слезной пленки [18].
Большую проблему представляет быстрое формирование глубоких дефектов и перфорации роговицы при аутоиммунных ПЯР. По наблюдениям большинства авторов, сквозная кератопластика часто не обеспечивает длительного эффекта, так как продолжение иммуноопосредованного воспаления может приводить к отторжению трансплантата, образованию язвенного дефекта на трансплантате или по его краю, в связи с чем шире применяются различные методики тектонической кератопластики [1, 19, 20].
Заключение
Периферические язвы роговицы относятся к тяжелым клиническим проявлениям поражения органа зрения при РЗ. Наиболее частой причиной развития ПЯР является РА. При постановке диагноза большое значение имеют учет соматической патологии, двустороннее обследование глаз, проведение лабораторной диагностики и консультации ревматолога. Клиническое течение ПЯР характеризуется быстрым прогрессированием с лизисом стромы и угрозой перфорации роговицы, может сопровождаться явлениями перилимбального васкулита, склерита и переднего увеита. Установлено умеренно выраженное снижение слезопродукции и более значимое снижение стабильности слезной пленки, что является показанием для постоянного применения слезозаместителей и репаративных препаратов. Противовоспалительное лечение ПЯР должно сочетать системную и локальную иммуносупрессивную терапию с применением ГКС в экстренных ситуациях. При быстром лизисе роговицы и ее перфорации срочное выполнение кератопластики (в виде передней послойной либо тектонической) доступными материалами позволяет сохранить глазное яблоко и зрительные функции.
Сведения об авторе:
Дроздова Елена Александровна — д.м.н., профессор, заведующая кафедрой офтальмологии ФГБОУ ВО ЮУГМУ Минздрава России; 454092, Россия, г. Челябинск, ул. Воровского, д. 64; ORCID iD 0000-0002-1799-211X.
Контактная информация: Дроздова Елена Александровна, e-mail: dhelena2006@yandex.ru.
Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов: отсутствует.
Статья поступила 12.03.2024.
Поступила после рецензирования 02.04.2024.
Принята в печать 24.04.2024.
About the author:
Elena A. Drozdova — Dr. Sc. (Med.), Professor, Head of the Department of Ophthalmology; South Ural State Medical University; 64, Vorovskiy str., Chelyabinsk, 454092, Russian Federation; ORCID iD 0000-0002-1799-211X.
Contact information: Elena A. Drozdova, e-mail: dhelena2006@yandex.ru.
Financial Disclosure: the author has no a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 12.03.2024.
Revised 02.04.2024.
Accepted 24.04.2024.
Информация с rmj.ru


