Введение
Острый тонзиллофарингит (ОТФ) — одна из самых частых причин боли или значительного дискомфорта в горле у детей и взрослых и, соответственно, обращений на амбулаторный прием [1–3]. Чаще ОТФ вызывают разнообразные вирусы или вирусно-бактериальные миксты, также он может быть обусловлен ассоциациями бактерий и даже специфической бактериальной инфекцией [4, 5]. Не вдаваясь в подробности патогенеза ОТФ и опираясь на данные проведенных исследований [6, 7], можно заключить, что допускается в миксте «постепенный переход от преобладающей этиологической роли вирусов к бактериям», а в бактериальных ассоциациях — изменение патогенности «условных» микробов, что может зависеть от многих факторов (возраст больного, коморбидный фон, социально-бытовые условия, низкий санитарно-гигиенический уровень, тесный контакт с бессимптомным носителем или больными орофарингеальной инфекцией, домашними животными (млекопитающими), проживание в «закрытых» коллективах, наличие ятрогенно обусловленной или связанной с коморбидностью иммунокомпрометации).
Тонзиллофарингит, имеющий рецидивирующее течение и приводящий к развитию хронического тонзиллита, признан актуальной медико-социальной проблемой: больной зависим от системы здравоохранения и имеет низкое качество жизни с потенциальным риском проведения оперативного вмешательства, в том числе необоснованного [8, 9]. Согласно представлениям, распространенным в мировом медицинском сообществе, рецидивирующий ТФ — это многофакторное заболевание с «повторяющимися эпизодами острой бактериальной инфекции небных миндалин и бессимптомными или «малосимптомными» интервалами между ними», т. е. рецидив ТФ считают самостоятельным эпизодом, не связанным с предыдущим [9]. Единого мнения о частоте рецидивов нет: одни авторы считают, что диагноз рецидивирующего ТФ может быть выставлен в случае не менее двух эпизодов обострения в течение года, другие клиницисты считают, что их должно быть не менее 4–5 и даже более в течение одного года на протяжении как минимум двух лет, причем каждый эпизод должен быть подтвержден и зафиксирован в медицинской документации[1] [9, 10]. Четких диагностических критериев, характеризующих «эпизод», на текущий момент времени также нет, поэтому решить данную задачу в реальной практике помогает консультация ЛОР-врача, которая позволяет исключить хронический тонзиллит и стадию его обострения (декомпенсации) и, соответственно, подтвердить наличие у пациента очередного острого стрептококкового эпизода ТФ.
Отечественные оториноларингологи считают рецидивирующим только тот ТФ, при котором доказана стрептококковая этиология рецидива, а после антибиотикотерапии подтверждается эрадикация стрептококка группы А (СГА) отрицательным тестом на стрептококк [10, 11].
Несмотря на очевидные доказательства положения о СГА как факторе риска возникновения рецидива ТФ у детей и подростков, особенно у генетически предрасположенных (имеющих семейный отягощенный «ревматический анамнез»), следует отметить, что в микробиологии рецидива у взрослых пациентов молодого возраста, как считает ряд авторов [10, 12], диагностическая значимость СГА может снижаться, а роль других патогенов требует уточнения. При этом безусловно важным является состояние системы иммунитета пациента. Так, имеются отдельные сведения о роли условно-патогенных и комменсальных микроорганизмов в модуляции деятельности иммунной системы у часто болеющих детей и подростков [13–16]. Особый интерес вызывает работа J.M. Dan et al. [17] о состоянии иммунитета у этих больных, трактующая рецидивирующий ТФ как генетически обусловленное заболевание, связанное с иммуносупрессией: авторы сообщают, что у пациентов младше 12 лет с рецидивирующим тонзиллитом наблюдаются некоторый (преимущественно субклинический) дефицит антител и аномальная функция Т-клеток.
Кроме того, известно, что в патогенезе как острого, так и хронического воспаления важную роль играют процессы свободнорадикального окисления. Обзор литературы показал, что значительное количество работ посвящено роли оксида азота (NO), состоянию антиоксидантной системы и эффективности применения препаратов с антиоксидантной активностью в комплексной терапии именно в острой фазе ТФ [18–20]. Однако исследований, показывающих стабильность или напряженность нитрозивного статуса в более отдаленные сроки у этой категории больных, найдено не было.
Итак, остаются открытыми вопросы в отношении этиологических особенностей видового состава флоры из зева у взрослых пациентов молодого возраста, состояния иммунитета и возможных проявлений окислительного стресса в промежутках между рецидивами ТФ, а также возможностей терапевтической профилактики частых рецидивов.
Цель исследования: провести диагностику этиологии, иммунного и нитрозивного статусов при рецидивах ТФ у молодых пациентов (от 18 до 44 лет) и оценить эффективность иммунокоррекции рекомбинантным интерфероном альфа-2b с антиоксидантами.
Содержание статьи
Материал и методы
Протокол исследования был одобрен локальным этическим комитетом ФГБОУ ВО КубГМУ Минздрава России (протокол № 24 от 13.05.2024). Исследование проведено с соблюдением этических принципов Хельсинкской декларации.
На первом этапе проведен ретроспективный анализ глубиной 3 года медицинских документов 594 пациентов c уточненным диагнозом ОТФ, получавших консультативную помощь и амбулаторное лечение в пяти городских поликлиниках Краснодара, являющихся базовыми для кафедры поликлинической терапии ФГБОУ ВО КубГМУ Минздрава России.
На втором этапе из общего объема амбулаторных карт отобраны 60 карт пациентов с рецидивирующим ТФ. Из них 20 (33,3%) мужчин (средний возраст 32,6±10,32 года) и 40 (66,7%) женщин (средний возраст 31,3±12,45 года). Частота рецидивов ТФ, зафиксированная в медицинских документах, составила 3–6 эпизодов в год. Выполнено проспективное сравнительное открытое нерандомизированное клиническое исследование-наблюдение. Предварительный расчет выборки не проводился. Из вышеуказанной когорты больных (n=60) 46 пациентов дали согласие на клиническое обследование и наблюдение, и из них сформированы основная группа — 25 пациентов, средний возраст 30,8±8,3 года, и группа сравнения — 21 пациент, средний возраст 28,6±6,4 года. Группа «условно здоровых» добровольцев (n=20; возраст 22,8±2,6 года) сформирована из лиц, проходивших диспансеризацию в базовых поликлиниках, и выделена с целью определения нормативных показателей исследуемых параметров иммунного и нитрозивного статусов.
Критерии включения: получение добровольного информированного согласия пациента на исследование; возраст от 18 до 44 лет; заключение ЛОР-врача об отсутствии у больного признаков декомпенсации хронического тонзиллита в момент включения в исследование и подтверждение острого эпизода ТФ стрептококковой этиологии экспресс-тестом, а также отсутствие изменений миндалин между эпизодами ОТФ по данным дневников наблюдения в амбулаторной карте; частота рецидивов 3 и более в году с указанием на стрептококковую этиологию предыдущих рецидивов; глубина ретроспективного анализа — 2 года.
Для группы здоровых добровольцев — сведения о регулярном прохождении диспансеризации с 18-летнего возраста и отсутствии патологии небных миндалин, а также другой ЛОР-патологии и хронических заболеваний бронхолегочной системы.
Критерии невключения: курение; подтверждение методом ПЦР вирусной этиологии ОТФ (гриппа — H1N1, коронавирусной инфекции — SARS-CoV-2); наличие уточненного диагноза «хронический тонзиллит» или «фарингит» и «хронический риносинусит», множественного кариеса, тяжелых хронических соматических заболеваний в стадии обострения (хронический обструктивный бронхит, хроническая обструктивная болезнь легких, артериальная гипертензия, ишемическая болезнь сердца, кардиомиопатии, хроническая сердечная недостаточность), аутоиммунных патологий и атопических заболеваний (поллиноз, атопический дерматит, астма), геморрагического синдрома, сахарного диабета 1 и 2 типов, вирусных инфекций (рецидивирующий herpes zoster, вирусные гепатиты, ВИЧ-инфекция), туберкулез, онкологическая патология, а также терапия иммунотропными препаратами в течение 6 мес. до включения в исследование.
Группы были репрезентативны по полу и возрасту. Пациенты предупреждены о тактике поведения при подозрении на возникновение очередного рецидива ТФ (срочная консультация, исключение самостоятельного приема антибактериальных препаратов и антисептиков перед исследованием). Диагноз «рецидив ТФ» подтверждал ЛОР-врач после осмотра. Часть больных была консультирована инфекционистом.
В первый день посещения врача проводили забор пробы (мазок из зева) для микробиологического и вирусологического исследования и дополнительно использовали «стрептотест» — иммунохроматографический экспресс-тест («РЭД стрептококк А», производитель — ООО «РЭД», Россия) для подтверждения стрептококкового ТФ и раннего начала антибактериальной терапии. Контролировали точность соблюдения техники забора материала из зева согласно стандарту[2]. Всех пациентов оценивали по шкале Мак-Айзека [21]. Проводили антибактериальную терапию в соответствии с актуальными клиническими рекомендациями1, а также применяли локальные антисептики, нестероидные противовоспалительные средства как жаропонижающие и обезболивающие. По окончании терапии осуществляли контроль эрадикации СГА с помощью иммунохроматографического экспресс-теста.
Исходной точкой наблюдения была стадия «клинического выздоровления» (через 10 дней после окончания антибиотикотерапии) с отсутствием признаков временной утраты трудоспособности. Всем участникам исследования выполняли общий анализ крови и мочи, ЭКГ, стандартное биохимическое исследование крови и иммунограмму, а также оценивали уровни сывороточных иммуноглобулинов и суммарный уровень метаболитов NO.
Пациентам основной группы назначали иммуномодулятор — человеческий рекомбинантный интерферон альфа-2b c антиоксидантами (токоферол ацетат 0,055 г, аскорбиновая кислота 0,0081 г, натрия аскорбат 0,0162 г) в виде ректальных свечей (Виферон®) по 500 000 МЕ 2 р/сут в течение 10 дней. Такая схема иммунокоррекции была основана на анализе литературы, доказывающем эффективность применения препарата в данной дозе как у детей старшего возраста, так и у взрослых при комплексном лечении различных вирусно-бактериальных инфекций респираторного тракта и ЛОР-органов [22, 23], и проводилась в стадии клинического выздоровления, а не в острой фазе ТФ. Модифицированный режим назначения препарата до 10 дней выбран на основе доказательств его большей клинической эффективности при частых респираторных эпизодах [24] и определен нами с учетом имеющихся в этот период достоверных изменений иммунного статуса в группах наблюдения по отношению к здоровым. Пациенты группы сравнения не получали иммуномодулятор. Лабораторное тестирование иммунного и нитрозивного статусов осуществляли исходно, через 1 и 3 мес. (непосредственное наблюдение). Срок проспективного наблюдения составил 12 мес.
Оценку иммунного статуса и этиологическую верификацию рецидива проводили следующим образом: для бактериологических посевов с миндалин на флору и чувствительность микроорганизмов к антибиотикам использовали стандартизированные питательные среды Весton Dickinson (США). Идентификацию микроорганизмов осуществляли на газовом хроматографе Agilent (США). Чувствительность к антибиотикам определяли на бактериологическом анализаторе той же фирмы. Вирусологическое исследование проводили методом ПЦР с использованием методики Real Time PCR System в режиме реального времени с помощью прибора Applied Biosystems 7300 для выявления наиболее частых возбудителей ОТФ (грипп, парагрипп, коронавирус, аденовирус, вирус Эпштейна — Барр, вирус герпеса, респираторно-синцитиальный вирус, риновирус).
Стандартное иммунологическое исследование включало оценку показателей периферической крови, популяционный и субпопуляционный состав лимфоидных клеток крови (CD3+, CD4+, CD8+, CD4+/CD8+, CD19+ и естественных киллеров (NK-клеток; CD16+)) методом проточной цитометрии. Анализ пробы крови проводили на цитометре Epics PROFILE-II (Cultronics) (FC 500 Beckman Coulter, США). Уровни сывороточных иммуноглобулинов (IgA, IgМ, IgG) определяли с помощью иммуноферментного анализа по стандартной методике.
Оценку нитрозивного статуса проводили по интегральному показателю — суммарному уровню метаболитов NO. Сумму метаболитов NO — нитратов/нитритов (NO2-+NO3-) в плазме крови определяли с помощью реакции Грисса спектрофотометрическим методом. Нитраты восстанавливали до нитритов с последующим диазотированием по общепринятой методике с использованием фотоэлектрического калориметра (Германия). Получали суммарное значение NO2-+NO3-, выраженное в мкмоль/л.
Эффективность иммунокоррекции оценивали по частоте рецидивов ТФ на протяжении последующих 12 мес. по отношению к исходным данным.
Для статистической обработки данных использовали пакет программ Microsoft Excel, 2019. С целью определения статистической однородности основной и контрольной выборок проведена проверка их принадлежности к одной генеральной совокупности по параметрическому критерию χ2 для наиболее значимых свойств указанных выборок. Различия между средними величинами по критерию Стьюдента считали статистически значимыми при р<0,05.
Результаты исследования
В когорте больных ОТФ (n=594) удельный вес пациентов с рецидивирующим течением составил 10,1% (n=60). Анализ протоколов микробиологических исследований при рецидиве (эпизоде) ТФ у включенных в исследование пациентов (n=46) показал, что в 23,9% (n=11) случаев высевался только один бактериальный возбудитель, а именно стрептококк: β-гемолитический стрептококк группы А (S. pyogenes, СГА; n=5) или β-гемолитический стрептококк группы G (S. dysgalactiae ssp. dysgalactiae, СГG; n=4), или α-гемолитический стрептококк (S. anginosus; n=2).
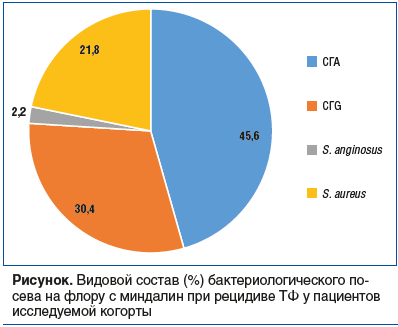
У большинства пациентов (n=35; 76,1% случаев) при оценке видового состава флоры выявлена ассоциация двух микроорганизмов, из них: СГА + СГG (n=15; 42,9% случаев); СГА + S. аureus (n=13; 37,1% случаев); СГG + S. aureus (n=7; 20,0% случаев).
В целом в этиологической структуре рецидива ТФ (см. рисунок) лидировали СГА и СГG.
Грибковая флора (Candida albicans) встречалась в 4 (8,6%) случаях. При верификации вирусов было определено следующее: вирус Эпштейна — Барр выявлен у 1 (2,3%) пациента, вирус герпеса человека 6-го типа — у 2 (4,3%), риновирус — у 25 (54,3%), аденовирус — у 3 (6,5%), а у 15 (32,6%) пациентов вирусы не определялись.
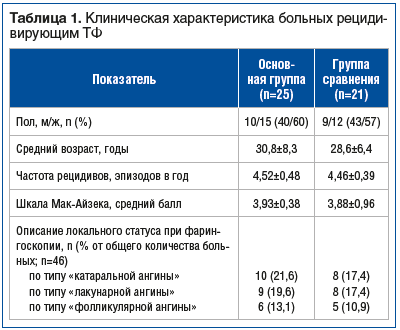
Как видно из таблицы 1, достоверных различий по частоте рецидивов ТФ, среднему баллу шкалы Мак-Айзека между группами наблюдения не было (р>0,5). Отмечено, что врачи амбулаторного звена по-прежнему описывают локальный статус при фарингоскопии как признаки «катаральной ангины» (гиперемия миндалин и небных дужек, отсутствие налетов или «нитевидные» белесоватые налеты), «лакунарной ангины» (на поверхности миндалин в лакунах гной, налеты) или «фолликулярной ангины» (гиперемия и увеличение миндалин, нагноение фолликулов). В этой структуре лидировала так называемая «катаральная ангина» — 39,1%, затем следовала «лакунарная» — 36,9% и «фолликулярная» — 24,0%. Это указывает на то, что рецидив ОТФ часто может сопровождаться незначительными признаками локального воспаления без выраженного отека и налетов на миндалинах.
В исходной точке наблюдения при исследовании показателей периферической крови концентрация лейкоцитов у пациентов с рецидивирующим ТФ в основной группе и группе сравнения практически не отличалась от параметров здоровых людей (7,12±0,60×109/л и 7,21±0,63×109/л против 6,68±0,55×109/л; р>0,5), так как пациенты в группах сравнения находились в стадии клинического выздоровления. В то же время в лейкоцитарной формуле этих пациентов имелись особенности: средняя концентрация палочкоядерных нейтрофильных лейкоцитов не отличалась от параметров нормы, но все же по сравнению со здоровыми людьми данный показатель в исходной точке наблюдения был более высоким в обеих группах (р<0,05), причем в основной группе через 3 мес. после иммунокоррекции препаратом рекомбинантного интерферона альфа-2b с антиоксидантами различия по данному параметру со здоровыми полностью нивелировались (3,8±0,4% против 3,2±0,3%; р>0,5).
При анализе лимфоидной популяции прослеживалась аналогичная, но с обратным знаком картина, т. е. у больных обеих групп с рецидивирующим ТФ имела место относительная (по сравнению со здоровыми людьми) лимфопения (26,1±2,6% и 25,4±2,4% против 34,4±1,8%; р<0,05), которая полностью нивелировалась также к 3-му месяцу наблюдения. Однако следует отметить, что абсолютной лимфопении ни на одном сроке наблюдения не отмечалось, кроме того, данный параметр никогда не выходил за пределы физиологической нормы и, соответственно, является отражением повышения концентрации нейтрофильных гранулоцитов.
При исследовании популяционного и субпопуляционного состава лимфоидных клеток у больных с рецидивирующим ОТФ (табл. 2) обнаружены существенные отличия в сравнении со здоровыми. Так, у этих пациентов определялось достоверное (р<0,01) снижение абсолютной концентрации Т-лимфоцитов (СD3+), относительной и абсолютной концентрации субпопуляции Т-хелперов (CD4+; р<0,05–0,01), снижение соотношения CD4+/CD8+ (р<0,05) и повышение относительного содержания естественных клеток-киллеров (CD16+; р<0,01). Таким образом, исходно в группах сравнения подтверждена дисфункция иммунной системы, хотя больные считались клинически излеченными.
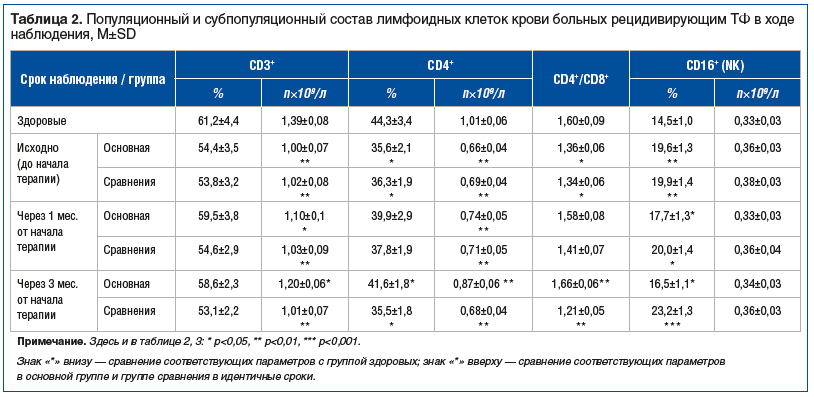
Далее, к концу 1-го месяца в группах сравнения стали намечаться положительные тенденции в отношении нормализации вышеперечисленных показателей, а именно увеличилась относительная концентрация CD3+, CD4+, CD16+, соотношение CD4+/CD8+, и эти показатели практически не отличались от параметров здоровых. Однако по-прежнему более низкими (по отношению к здоровым) оставались абсолютные значения CD3+ и CD4+ (р<0,05–0,01). Отмечено, что содержание естественных клеток-киллеров CD16+ в основной группе уже не отличалось от здоровых, а в группе сравнения, не получавшей иммунокоррекции, их относительное содержание было достоверно выше по отношению к основной группе (20,0±1,4% против 17,7±1,3%; р<0,05). К окончанию 3-го месяца наблюдения отмечено еще большее нарастание концентрации NK-клеток (CD16+) в группе сравнения по отношению к основной группе (23,2±1,3% против 16,5±1,1%; р<0,05), в то время как в основной группе этот показатель не отличался от показателя здоровых.
Анализ иммунограммы по окончании наблюдения в целом показал, что практически все значения CD3+ и CD4+ (абсолютные и относительные величины) в основной группе были статистически значимо лучше (р<0,05–0,001), чем в группе сравнения. Следует отметить, что соотношение CD4+/CD8+, или так называемый иммунорегуляторный индекс, используемый как один из показателей эффективности лечения инфекционной патологии, был достоверно выше в основной группе — 1,66±0,06 против 1,21±0,05 в группе сравнения (р<0,01).
Можно заключить, что к 3-му месяцу в группе сравнения, не получавшей препарат рекомбинантного интерферона альфа-2b с антиоксидантами, сохранялась дисфункция иммунитета: наблюдалась реверсия исследуемых основных показателей иммунограммы к исходным значениям, и они достоверно отличались от показателей иммунограммы пациентов основной группы и здоровых людей (р<0,05–0,001).
Существующий способ диагностики признаков хронизации неспецифического воспалительного процесса, заключающийся в количественном определении уровней IgG, IgM, IgA в сыворотке крови, не выявил статистически значимых исходных различий у пациентов и здоровых (табл. 3). Однако у пациентов групп сравнения иммунный статус все же отличался от нормального некоторым снижением концентрации IgA и повышением — IgG и IgM, что указывало на напряженность в первую очередь местного иммунитета.
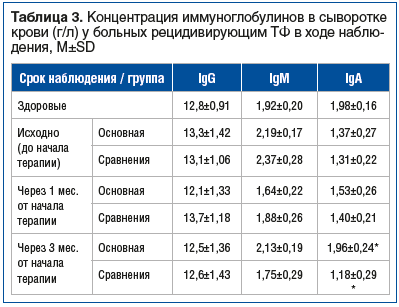
Как видно из таблицы 3, к концу 1-го месяца в обеих группах наблюдения наметились положительные тенденции в изучаемых параметрах, более выраженные в основной группе, но не достигшие статистической значимости. Через 3 мес. в основной группе концентрации IgA были достоверно выше, чем в группе сравнения, и они уже не отличались от показателей здоровых, что являлось показателем улучшения состояния местного иммунитета.
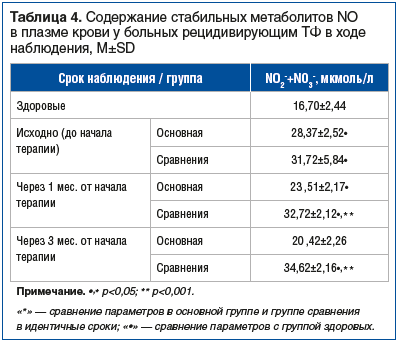
В исходной точке исследования достоверных отличий в суммарном уровне метаболитов NO (NO2—+NO3—) между группами наблюдения не было (28,37±2,52 мкмоль/л против 31,72±5,84 мкмоль/л; р>0,5) (табл. 4), но по отношению к здоровым этот критерий был достоверно выше (в 1,7–1,9 раза) (р<0,001), что косвенно указывает на активность радикал-формирующей способности нейтрофилов. Через 1 мес. в основной группе, получавшей препарат рекомбинантного интерферона альфа-2b с антиоксидантами, произошло достоверное снижение уровня метаболитов NO (NO2-+NO3-) по отношению к группе сравнения (р<0,05), а к 3-му месяцу данный показатель не отличался от значений здоровых (p=0,26). Эти положительные изменения доказывают нормализацию нитрозивного статуса у больных ТФ при применении препарата рекомбинантного интерферона альфа-2b с антиоксидантами (Виферон®).
Важным критерием эффективности проводимой иммунокоррекции больных с повторяющимися эпизодами ОТФ явилась частота рецидивов в течение последующих 12 мес. Так, в основной группе, где проводилась терапия рекомбинантным интерфероном альфа-2b с антиоксидантами, частота рецидивов достоверно снизилась с 4,52±1,18 до 2,04±0,19 (р<0,05), а в группе сравнения достоверных изменений частоты рецидивов отмечено не было (4,56±1,16 случая против 3,42±0,19 случая; р=0,33).
Обсуждение
Полученные результаты относительно частоты встречаемости рецидивирующего течения ТФ, а это 10,1%, соответствуют данным литературы [8, 9, 17]. Понимание ведущей роли определенных патогенов в рецидивах ТФ — априори главный шаг в решении проблемы эффективности этиотропного лечения у данного контингента больных и сдерживания резистентности к антибиотикам. Согласно полученным результатам оценки видового состава флоры из зева у взрослых молодых пациентов актуальными штаммами (по убыванию) были СГА, далее СГG и S. aureus, что несколько противоречит мнению ряда ученых [6, 8, 10, 11] об этиологии ОТФ у взрослых, но следует заметить, что в данных исследованиях у больных не было частых рецидивов в анамнезе. По итогу работы чаще всего определялись микробные ассоциации (76,1% от общего количества случаев; n=46). Коинфицированность СГА с другими микробами у этих больных была следующей: СГG — в 42,9% случаев (или 32,6% от общего числа больных), СГА + S. аureus — в 35,8% случаев (или 28,3% от общего числа больных) соответственно. Заметим, что определение в ротоглотке S. аureus у взрослых клиницисты чаще расценивают как носительство, относя его к условным патогенам, а СГG считают комменсальной флорой.
Однако доказано, что при определенных условиях данные микроорганизмы могут проявлять патогенные свойства подобно СГА [4, 13, 14], и эти патогенетические взаимосвязи требуют уточнения. Дискуссия о корреляции вышеуказанной микрофлоры с рецидивирующим течением ТФ и хронизацией процесса в миндалинах продолжается. Значение СГА как единственного важного фактора риска рецидивов ТФ определено [8, 9], так как доказана его внутриклеточная персистенция, обусловленная незавершенным фагоцитозом вследствие недостаточности клеточного звена системного иммунитета. А вот о роли S. аureus в микробной ассоциации СГА + S. aureus высказываются противоположные мнения, но большинство авторов [4, 25, 26] указывают на значимость этого симбиоза в развитии хронического тонзиллита, утверждая, что «данные патогены активно колонизируют в ротоглотке у пациентов с хроническим тонзиллитом даже вне обострения» и их удельный вес в микробиоте значителен и составляет 40–42% (S. аureus) и 60–62% (СГА). Подобные тенденции в видовом составе бактериологических посевов с миндалин наблюдались и в нашем исследовании (симбиоз СГА + S. аureus определен в каждом третьем случае). В противовес этому найдены доказательства, что у детей и подростков с частыми эпизодами ОТФ при увеличении возраста, а также при развитии признаков хронического тонзиллита начинают определяться не только СГА, но и гемолитические стрептококки других групп (СГВ, СГС, СГG, СГF и «негруппируемые» типы) [15, 26–29]. Необходимо отметить, что на современном этапе СГG считается комменсалом человека, т. е. бессимптомно колонизирующим ротоглотку. В то же время появляются статьи с указанием на то, что у контингента больных из группы риска, в том числе имеющих дисфункцию иммунитета, СГG может вызывать ОТФ, клинически сходный с СГА-ТФ [6, 28, 29]. Известно, что СГG имеет большое сходство с СГА в части общих факторов вирулентности, является родственным видом, и на данном этапе времени инфекционисты причисляют его к «новым патогенам человека». Описаны вспышки СГG-ТФ в «закрытых» учреждениях, а его роль в развитии острой ревматической лихорадки и хронической ревматической болезни сердца пока не доказана, но продолжает активно обсуждаться [30]. В нашем исследовании СГG встречался в микробных ассоциациях с СГА почти в каждом втором случае (43,2%). Таким образом, результаты исследования позволяют полагать, что имеется своеобразие этиологических черт рецидивирующего ТФ у молодых пациентов.
Справедливости ради следует заметить, что все же чаще ОТФ вызывают вирусно-бактериальные ассоциации. Взаимодействия коинфицирующих агентов разнообразны и сложны. Безусловно, на первый план выходит их взаимное влияние на клетки иммунной системы и изменение «инфекционности» возбудителей в этой ассоциации [4]. Для уточнения этиологии рецидивов ОТФ мы исключили значимые вирусные коинфицирующие агенты (гриппозную и коронавирусную инфекции), так как они существенно влияют на иммунную систему человека, вызывая реинфекции. Все остальные выявленные респираторные вирусы являлись малопатогенными, а одним случаем подтверждения вируса Эпштейна — Барр можно пренебречь. Соответственно полагаем, что в нашем исследовании иммуносупрессирующая роль вирусных агентов не так уж значима. В то же время, говоря о влиянии на иммунитет бактериальных коинфицирующих агентов, заметим, что на имеющиеся нарушения гуморального ответа иммунной системы у пациентов с СГА-ТФ указывали М.М. Евсикова и соавт. [11]. Значительное количество работ, посвященных детям с частыми острыми респираторными эпизодами в сочетании с ТФ, также демонстрируют наличие у них дисрегуляторных процессов в системе иммунитета и, в частности, в интерфероновом статусе, а их авторы приводят результаты эффективности иммунореабилитации с использованием интерферонотерапии [16, 23, 31].
Особенность настоящей работы заключалась в том, что исходной точкой оценки иммунного и нитрозивного статусов была стадия клинического выздоровления после ОТФ (по окончании антибиотикотерапии), но и в этот период у всех больных выявлены признаки дисфункции иммунитета и антиоксидантной защиты. «Светлый промежуток» между рецидивами в группах наблюдения составлял в среднем 2,5 мес., и, соответственно, оценка иммунитета и уровня суммарных метаболитов NO проводилась непосредственно в течение 3 мес. Наблюдение за группой сравнения, не получавшей препарат рекомбинантного интерферона альфа-2b с антиоксидантами, показало, что, несмотря на улучшение некоторых показателей иммунограммы, к 3-му месяцу все же отмечалась реверсия большинства исследуемых параметров к исходным значениям. В то же время пациенты основной группы, получавшие препарат Виферон® в ректальных суппозиториях по 500 000 МЕ 2 р/сут 10 дней, к 3-му месяцу имели показатели иммунного статуса, не отличающиеся от здоровых. В большинстве исследований, проведенных in vitro и in vivo, показано, что интерфероны I типа демонстрируют антибактериальные свойства [32]. Соответственно, включение в комплексную терапию препарата интерферона α обусловлено его иммуномодулирующими и опосредованными антибактериальными свойствами. Интерфероны I типа увеличивают экспрессию рецепторов главного комплекса гистосовместимости I типа на всех видах клеток, тем самым улучшая распознавание инфицированных клеток цитотоксическими Т-лимфоцитами, активируют натуральные киллеры, стимулируют активность дендритных клеток и пролиферацию B-клеток. Все эти факторы усиливают фагоцитарные и цитотоксические реакции в зоне воспалительного очага и способствуют эффективной элиминации инфекционного агента [31].
Известно, что показатель суммарного количества метаболитов NO (NO2-+NO3-) в крови является на современном этапе «убедительным маркером содержания NO в организме» и «интегральным метаболическим параметром» нитрозивного статуса, коррелирующим с рядом патологических состояний, связанных с воспалением [18]. В исходной точке наблюдения у больных рецидивирующим ТФ выявлен более высокий суммарный уровень метаболитов NO. Это указывает на адаптационные процессы, компенсирующие «патологическую недостачу биоактивного NO» в организме больных, так как основные факторы, влияющие на его уровень (курение, возраст старше 45 лет и хронические заболевания), были исключены. Из препаратов интерферона был выбран Виферон® благодаря наличию в своем составе комплекса высокоактивных антиоксидантов — α-токоферола ацетата и аскорбиновой кислоты, что важно для коррекции процессов свободнорадикального окисления, сопровождающих рецидивирующий ТФ. В нашем исследовании при назначении больным рекомбинантного интерферона альфа-2b с антиоксидантами отмечена положительная динамика этого параметра с нормализацией уровня NO2-+NO3- к 3-му месяцу наблюдения, что указывает на устранение дисбаланса прооксидантной и антиоксидантной систем.
Ограничения исследования. Из-за сложности в рутинной практике объективного подтверждения рецидива ТФ без консультации ЛОР-врача и определения частоты инфекционных (стрептококковых) эпизодов в предшествующие годы (часто «стрептотест» не проводится) данный фрагмент работы выполнен на небольшой группе пациентов, что затрудняет экстраполяцию полученных результатов в отношении этиологии рецидива ТФ на генеральную выборку, хотя этиологические особенности рецидива ТФ у взрослых больных молодого возраста определенно имеются. Роль СГG в этиологии рецидивирующего ТФ необходимо продолжить изучать, уточняя факторы, способствующие его патогенности. Дальнейшие исследования будут направлены на продолжение формирования большей выборки больных, в том числе с целью изучения иммунного и нитрозивного статусов при последующих рецидивах ТФ у пациентов после иммунокоррекции препаратом Виферон® по предложенной схеме.
Выводы
В этиологической структуре рецидивирующего ТФ у взрослых молодого возраста определено следующее: лидируют стрептококки — СГА (45,6%), СГG (30,4%) и превалируют (в 76,1% случаев) микробные ассоциации. У пациентов из общей когорты выделялись практически в каждом третьем случае СГА + СГG (32,6% случаев) и СГА+ S. аureus (28,3% случаев).
Уточнены некоторые патогенетические механизмы, обусловливающие рецидивирующее течение ТФ у больных молодого возраста: в стадии клинического выздоровления у них отмечаются признаки дисфункции систем иммунитета и антиоксидантной защиты, что является обоснованием для применения иммуномодулятора с антиоксидантами.
Нарушения иммунного статуса у больных рецидивирующим ТФ проявляются более низкими (в сравнении со здоровыми) значениями CD3+, CD4+, CD4+/ CD8+, концентрации IgA и повышением уровня CD16+ (р<0,05–0,001).
Дисфункция нитрозивного статуса у данной категории больных определена на основании достоверно более высоких уровней суммарного количества метаболитов NO (NO2-+NO3-) по отношению к здоровым (р<0,05).
Доказан непосредственный эффект на иммунный и нитрозивный статусы препарата рекомбинантного интерферона альфа-2b с антиоксидантами в свечах по предложенной схеме: к 3-му месяцу основные показатели иммунограммы и иммунорегуляторый индекс (CD4+/CD8+) в основной группе не отличались от нормы. Препарат имел также антиоксидантный эффект, подтверждением чего было снижение суммы активных метаболитов NO (NO2-+NO3-) к 3-му месяцу наблюдения до уровня здоровых (p=0,26).
Профилактический эффект препарата рекомбинантного интерферона альфа-2b с антиоксидантами заключался в достоверном уменьшении частоты рецидивов ТФ в основной группе в 2 раза (р<0,05).
[1] Министерство здравоохранения Российской Федерации. Клинические рекомендации. Острый тонзиллит и фарингит. 2024. (Электронный ресурс.) URL: https://diseases.medelement.com/disease/острый-тонзиллит-и-фарингит-кр-рф-2024/18281 (дата обращения: 16.11.2025).
[2] Российские рекомендации по клинической микробиологии. Микробиологическое исследование биоматериалов со слизистой зева и задней стенки. 2025. (Электронный ресурс.) URL: https://fedlab.ru/upload/medialibrary/e47/0q8j626uiqr522hqilxuizd1e5x75uan/Микробиологическое%20иссл… (дата обращения: 12.10.2025).
Информация с rmj.ru






