Содержание статьи
Дифференцированная лечебная тактика ведения пациенток с
эндометриоидными кистами яичников и бесплодием
Т. В. Клинышкова*, доктор медицинских наук, профессор
О. Н. Перфильева**
Н. Б. Фролова***, кандидат медицинских наук
* ГБОУ ВПО ОмГМА МЗ РФ, Омск
** ООО «Клиника доктора Шаталовой. Гинекологическая эндокринология и
репродукция», Омск
*** НУЗ «Отделенческая клиническая больница на станции Омск-Пассажирский», Омск
Проблема совершенствования диагностики и оптимизации лечения женщин с
гормонально-ассоциированными заболеваниями репродуктивной системы является
весьма актуальной, особенно при планировании деторождения [1–4]. К числу
последних относится генитальный эндометриоз, который имеет тенденцию к росту,
особенно среди женщин, не реализовавших репродуктивную функцию, в том числе по
причине бесплодия [5–7]. По данным Росстата, заболеваемость эндометриозом
выросла с 376 до 435 на 100 тыс. женщин с 2009 по 2013 гг.
Эффективность использования различных методов лечения эндометриоза,
ассоциированного с бесплодием, в аспекте восстановления репродуктивной функции
активно обсуждается в отечественной и зарубежной литературе. Частота наступления
беременности при эндометриоз-ассоциированном бесплодии имеет широкий диапазон
(от 8,9% до 74%) [7, 8], при распространенной форме генитального эндометриоза —
эндометриозе яичников — она составляет 20–53%, включая применение методов
вспомогательных репродуктивных технологий [1, 9, 10]. Несмотря на многочисленные
исследования, отсутствуют убедительные доказательства преимущества ведущего
хирургического метода лечения эндометриоза яичников в преодолении бесплодия,
отсутствует единое мнение по вопросам гормонотерапии [4, 11, 12]. Учитывая
высокую частоту редукции овариального резерва при хирургическом лечении
эндометриом, намечается изменение тренда в пользу консервативного подхода к
лечению [13, 14]. В соответствии с международным консенсусом по эндометриозу
(2013), отечественными рекомендациями по ведению больных эндометриозом (2013)
признается целесообразность в ряде случаев эмпирической терапии без
лапароскопической верификации диагноза с целью сохранения овариального резерва,
в то время как результаты оценки ее эффективности не получили широкого
обсуждения в литературе [15–17].
Цель исследования — оценить эффективность эмпирической терапии и
хирургического лечения с последующей гормонотерапией у пациенток с
эндометриоидными кистами яичников, ассоциированными с бесплодием, на основании
изучения частоты наступления беременности.
Материалы и методы исследования
В проспективное сравнительное исследование включена 61 пациентка
репродуктивного возраста с эндометриоидными кистами яичников (ЭКЯ) на фоне
бесплодия. Все пациентки в зависимости от дифференцированной лечебной тактики
ведения были разделены на две группы: 1-я группа (n = 13) получала гормональное
лечение диеногестом по стандартной схеме в течение 6 месяцев (эмпирическая
терапия); 2-я группа (n = 48) — двухэтапное лечение (хирургическое лечение с
последующей гормональной терапией в очередном цикле). В качестве эмпирической
терапии был выбран пероральный прогестаген четвертого поколения — диеногест,
обладающий высокой селективностью к прогестероновым рецепторам, коротким
периодом полувыведения (9–11 часов), высокой биодоступностью (90%), отсутствием
негативных метаболических и сосудистых эффектов. Диеногест обладает
антипролиферативным, антиангиогенным, противовоспалительным, иммуномодулирующим
действием, не уступая по эффективности агонистам гонадотропин-рилизинг-гормона (аГн-РГ).
Диеногест способствует апоптозу гранулезных клеток растущего фолликула и
подавлению уровня гипофизарных гормонов фолликулостимулирующего гормона (ФСГ) и
лютеинизирующего гормона (ЛГ), ведущих к ановуляции; при сохранении выраженного
антипролиферативного эффекта умеренно подавляет продукцию эстрадиола, позволяя
избежать развития симптомов эстрогенного дефицита и способствуя долгосрочной
терапевтической стратегии [18]. Диеногест назначался в дозе 2 мг/сутки в
непрерывном режиме в течение 6 месяцев.
Второй этап комбинированного лечения пациенток 2-й группы проводился в
очередном менструальном цикле с использованием: 1) внутримышечных инъекций
депо-формы аГн-РГ, которые вводились один раз в 28 дней с 2–4 дня цикла в
течение 3 месяцев (поскольку длительный курс терапии может способствовать
снижению овариального резерва), формируя гипоэстрогенное состояние,
сопровождающееся атрофическим изменением эндометриоидных очагов [18]; 2)
диеногеста в дозе 2 мг/сутки в непрерывном режиме в течение 6 месяцев; 3)
комбинированных оральных контрацептивов (КОК) в непрерывном режиме 6 месяцев,
опосредованно (через блокаду гонадотропин-релизин-гормонов) подавляющих
циклическую секрецию гипофизарных гормонов ФСГ и ЛГ и приводящих к ановуляции,
децидуализации стромы и атрофии очагов эндометриоза [18].
В зависимости от исходов восстановления фертильности после завершения терапии
пациентки с эндометриозом яичников и бесплодием разделены на 2 группы: 1-я
группа (n = 28) — пациентки с наступившей беременностью, 2-я группа (n = 33) —
пациентки с отсутствием беременности.
Критерии включения в исследование разработаны в соответствии с
дифференцированной тактикой ведения. Критерии включения в 1-ю группу:
репродуктивный возраст, эндометриоз-ассоциированное бесплодие, первичная и
рецидивирующая ЭКЯ менее 3 см, сниженный овариальный резерв (ФСГ более 8,08 мМЕ/мл,
антимюллеровый гормон (АМГ) менее 1,0 нг/мл, ингибин В менее 45,0 пг/мл),
нормальный овариальный резерв и отказ от оперативного лечения, персистенция
кисты после 2-цикловой терапии КОК. Критерии включения во 2-ю группу:
репродуктивный возраст, эндометриоз-ассоциированное бесплодие, первичная и
рецидивирующая ЭКЯ более 3 см, нормальный овариальный резерв. Критерии
исключения из исследования — отсутствие эндометриоза яичников, наличие
сочетанных факторов бесплодия (трубно-перитонельный, маточный, мужской), отказ
пациентки от участия в исследовании.
Комплексное обследования включало результаты оценки клинических и
анамнестических данных; ультразвукового исследования органов малого таза (на 5–7
день от начала менструации), выполненного в режимах 3D и 4D с использованием
аппаратов «Voluson E-8» (США), «Hitachi-Aloka ProSound SSD-3500 SX» (Япония),
относящихся к системе контактного сканирования, с использованием
трансабдоминального и трансвагинального датчиков с частотой 3,5 и 5,0 МГц;
исследования базального уровня гипофизарных и яичниковых гормонов — ФСГ, АМГ,
ингибин В — в сыворотке крови (на 3-й день менструального цикла) методом
иммуноферментного анализа (ELISA) до хирургического лечения. Для определения
уровня АМГ использовалась тест-система «AMH Gen II ELISA» (США); для определения
уровня ингибина В — тест-система «Inhibin B Gen II ELISA» (США); уровня ФСГ —
тест-система «ARCHITECT FSH» (Abbott Ireland Diagnostics Division, Ирландия).
Полученные результаты сопоставлялись с референсными значениями гормонов для
женщин репродуктивного возраста в фолликулярную фазу менструального цикла: АМГ —
1,00–10,60 нг/мл (независимо от возраста); ингибин В для женщин старше 18 лет —
45–255 пг/мл; ФСГ — 3,03–8,08 мМЕ/мл. Проводилось исследование концентрации
онкомаркеров СА 125, тест-система «ARCHITEСT СА 125» (Abbott Laboratories
Diagnostics Division, США), полученные данные сопоставлялись с референсными
значениями СА 125–0,0–35,0 Е/мл.
Биометрический анализ осуществлялся с использованием пакета Statistica 6,
возможностей программы Microsoft Excel. Во всех процедурах статистического
анализа критический уровень значимости р принимался равным 0,05.
Результаты и обсуждение
Анализ клинических особенностей эндометриоза яичников у инфертильных
пациенток, средний возраст которых на момент исследования составил 30,53 ± 0,59
года (M ± SE), свидетельствовал о доминировании первичного бесплодия (71,8%)
независимо от распространенности эндометриоза (р = 0,05). Общая длительность
бесплодия у пациенток с ЭКЯ колебалась от 1 до 13 лет, средний стаж составил 2,0
(1,0; 5,0) года (Р50 (Р25; Р75)). По результатам корреляционного анализа
установлены корреляционные связи между бесплодием и распространенностью
эндометриоза яичников (rs = –0,52; p = 0,000), наличием эндометриомы
и длительностью бесплодия (rs = +0,15; p = 0,041).
У 24,6% (15/61) пациенток в прошлом выполнено хирургическое лечение в объеме
цистэктомии по поводу ЭКЯ. Рецидивирующая форма эндометриоза яичников
встречалась в 2,5 раза чаще у пациенток 1-й группы (6/46,2%) в сравнении со 2-й
группой (9/18,8%) (χ2 = 4,14; р = 0,042). В зависимости от
распространенности эндометриоза яичников и размера ЭКЯ частота рецидивирования
эндометриоза не имела статистически значимых различий (р > 0,05). Длительность
периода между оперативным лечением в анамнезе и рецидивом ЭКЯ на этапе включения
в исследование колебалась от 1 года до 18 лет. В соответствии с этим средняя
длительность эндометриоза яичников составила 2,5 (1,0; 6,0) года (Р50 (Р25;
Р75)), не имея различий в зависимости от распространенности эндометриоза и
размера кисты (р > 0,05).
По результатам эхографического исследования органов малого таза у
неоперированных инфертильных пациенток диагностированы эндометриомы размером от
10 до 120 мм преимущественно с односторонней локализацией (80,3%) и одинаковой
частотой эндометриом размерами менее 3 см и более 3 см. Средний диаметр кист у
пациенток 1-й группы составил 20,0 (17,0; 28,5) мм (Р50 (Р25; Р75)), 2-й группы
— 50,0 (40,0; 70,0) мм.
Учитывая наличие опухолевидного образования в яичниках пациенток группы
исследования, проводилось исследование концентрации онкомаркера СА 125, который
является наиболее доступным в настоящее время среди метаболических опухолевых
маркеров для диагностики опухолей женских половых органов, хотя отсутствует его
корреляция со степенью распространенности генитального эндометриоза, а также его
концентрация в сыворотке крови может повышаться при рецидивирующей форме
эндометриоза, при наличии воспалительных заболеваний органов малого таза без
признаков онкологической патологии [18]. Медиана и интерквартильный размах
уровня СА 125 у пациенток в 1-й и 2-й группах составили 30,50 (25,50; 34,25)
Е/мл и 29,50 (16,73; 37,93) Е/мл соответственно и были сопоставимы с референсным
значением уровня СА 125 (0,0–35,0 Е/мл).
Поскольку при выполнении цистэктомии (по данным литературы) отмечается
высокая частота редукции овариального резерва, некоторые исследователи полагают,
что не все женщины с эндометриоз-ассоциированным бесплодием должны быть
подвержены хирургическому лечению [14, 19–21].
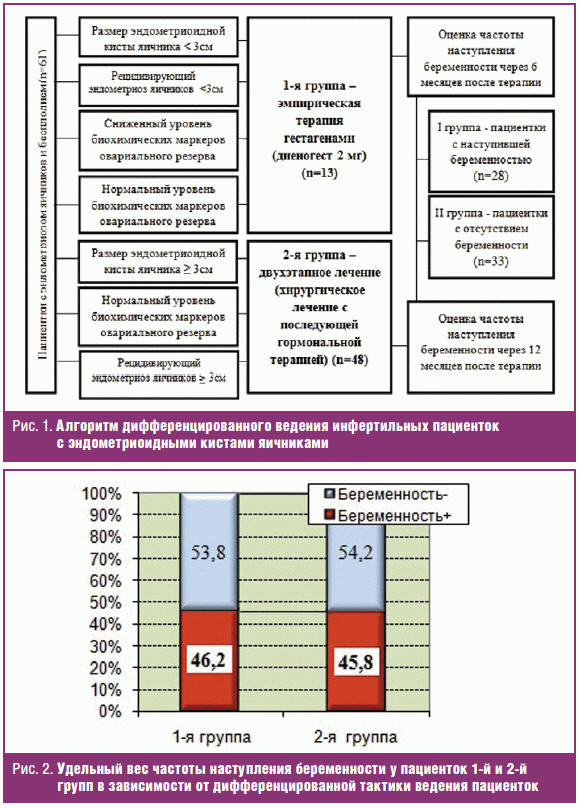
В нашем исследовании дифференцированная лечебная тактика ведения пациенток с
бесплодием определялась размером ЭКЯ, наличием рецидивирующей формы эндометриоза,
исходным уровнем гормонов ФСГ, ингибина В и АМГ (рис. 1).
Удельный вес эмпирической терапии у пациенток с односторонними ЭКЯ составил
22,4% (11/49), с двусторонними — 16,7% (2/12) (χ2 = 0,19; р = 0,661).
Среди пациенток с ЭКЯ менее 3 см удельный вес больных, проводивших эмпирическую
терапию (11/30), не имел статистически значимых различий в сравнении с
комбинированным двухэтапным лечением (19/30) (χ2 = 0,43; р = 0,510).
Эффективность лечения в группах оценивалась по частоте наступления
беременности в течение 6 месяцев после завершения эмпирической терапии (интервал
был продиктован необходимостью более активной тактики ведения с учетом снижения
овариального резерва и возраста женщин), в течение 12 месяцев после окончания
комбинированного лечения. Выполнен многосторонний анализ частоты наступления
беременности (ЧНБ) у инфертильных пациенток с ЭКЯ в зависимости от
дифференцированной тактики ведения данного контингента больных,
распространенности эндометриоза, размера ЭКЯ, а также от исходов лечения.
Кумулятивная ЧНБ в течение 6 месяцев после консервативного лечения составила
46,2% (6/13) случаев (рис. 2): спонтанная беременность наступила у 4 пациенток и
2 пациенток, сохраняющих инфертильность в течение 6 месяцев после
консервативного лечения, диагностирована беременность после проведения одного
цикла экстракорпорального оплодотворения (ЭКО).
Двухэтапное лечение (хирургическое лечение с последующей гормональной
терапией) проводилось пациенткам 2-й группы. Хирургическое лечение с
гистологической верификацией диагноза выполнено в объеме односторонней и
двусторонней цистэктомии, деструкции поверхностных очагов эндометриоза на
контрлатеральном яичнике и очагов эндометриоза на тазовой брюшине. В
соответствии с рекомендациями ведения больных с бесплодием оценивалось состояние
полости матки и эндометрия при проведении гистероскопии с биопсией эндометрия,
для уточнения проходимости маточных труб выполнялась хромогидротубация.
Послеоперационная гормональная терапия, в соответствии с позицией
международного общества по эндометриозу (World Endometriosis Society, WES,
2013), целесообразна для профилактики рецидивов эндометриоза, не имея
преимуществ в лечении бесплодия.
Кумулятивная ЧНБ у прооперированных пациенток через 12 месяцев после
комбинированного лечения составила 45,8% (22/48) случаев (рис. 2): спонтанная
беременность наступила у 14 пациенток и у 8 из 21 пациентки, направленных на
проведение ЭКО, что не имело различий с 1-й группой (χ2 = 0,36; р =
0,549).
Полученные результаты, относительно частоты наступления беременности в
зависимости от тактики ведения, согласуются с данными некоторых исследователей,
согласно которым кумулятивная ЧНБ (включая вспомогательные репродуктивные
технологии) в течение 1 года после оперативного лечения ЭКЯ и у больных с
эндометриомами до 2 см без оперативных вмешательств на яичниках в анамнезе
составила 58,5% и 40% соответственно [22].
В работах некоторых исследователей восстановление фертильности при
эндометриозе яичников зависит от тяжести эндометриоза [1], согласно данным
других исследований такая зависимость не прослеживается [23, 24]. По результатам
наших данных, в зависимости от распространенности эндометриоза кумулятивная ЧНБ
не имела существенных различий: среди пациенток с односторонними эндометриомами
(n = 49) она составила 23/46,9% случаев, у пациенток с двусторонними ЭКЯ (n =
12) — 5/41,7% случаев (χ2 = 0,30; р = 0,585). Не исключено, что
отсутствие различий объясняется доминированием числа больных с односторонними
эндометриомами.
В зависимости от размеров односторонней ЭКЯ кумулятивная ЧНБ у пациенток с
эндометриомами менее 3 см (n = 30) в сравнении с эндометриомами более 3 см (n =
19) не имела различий, составив 14/46,7% и 9/47,4% случаев соответственно (χ2
= 0,00; р = 0,962). ЧНБ среди пациенток с эндометриомами менее 3 см после
завершения эмпирической терапии уступала эффективности комбинированного лечения,
составив 6/14 и 8/14 случаев соответственно (χ2 = 1,29; р = 0,256).
Не исключено влияние сниженного овариального резерва и преобладания
рецидивирующей формы ЭКЯ на показатель ЧНБ при назначении эмпирической терапии (р
< 0,05). Сравнительный анализ ЧНБ у прооперированных пациенток в зависимости от
размера эндометриомы (19/30 пациенток с ЭКЯ менее 3 см и 19 пациенток с ЭКЯ
более 3 см) не имел статистически значимых различий: 42% (8/19) и 47,4% (9/19)
соответственно (χ2 = 0,11; р = 0,744). Отсутствие различий по ЧНБ в
зависимости от размеров эндометриомы вытекает из ранее опубликованных нами
данных [25]. Было доказано, что биохимические параметры овариального резерва (ФСГ,
АМГ, ингибин В, активин А) инфертильных больных с первичными односторонними
эндометриомами яичников, обследованных до хирургического лечения, не имеют
статистически значимых различий в зависимости от размера эндометриомы в
сравнении со здоровыми женщинами.
Применяемые на современном этапе методы лечения эндометриоза яичников
позволяют осуществить репродуктивную функцию в 20–58,5% случаев [6, 7, 10]. По
результатам нашего исследования у пациенток с ЭКЯ и бесплодием (1-я и 2-я
группы), 80,3% (49/61) из которых имели односторонний процесс, кумулятивная ЧНБ
составила 45,9% (28/61) случаев: спонтанная беременность — 64,3%/18 случаев, ЧНБ
после экстракорпорального оплодотворения (ЭКО) — 35,7%/10 случаев (рис. 3).

В зависимости от исходов восстановления фертильности после завершения терапии
проведен анализ факторов (возраст, наличие рецидивирующей формы эндометриоза
яичников, длительность бесплодия, уровень биохимических маркеров овариального
резерва, размер ЭКЯ и распространенность эндометриоза), сопровождающих течение
эндометриоза яичников, у пациенток с отсутствием беременности (табл.).
При отсутствии беременности у пациенток с эндометриозом яичников после
лечения установлено преобладание женщин в возрасте старше 30 лет (в 2,8 раза), с
рецидивирующей формой эндометриоза яичников (в 3,4 раза) (р < 0,05), в меньшей
мере — при снижении овариального резерва (в 1,4 раза) и длительностью бесплодия
более 5 лет (в 1,3 раза) (р > 0,05) в сравнении с пациентками с благоприятным
исходом лечения. При сравнительном анализе исходов лечения в зависимости от
распространенности эндометриоза отмечалось доминирование односторонних ЭКЯ в 1-й
и 2-й группах: 82,1% и 75,6% случаев соответственно (χ2 = 0,37; р =
0,544). В зависимости от размера ЭКЯ у пациенток 1-й и 2-й групп исследования
удельный вес эндометриомы размером менее 3 см составил 50% случаев и 48,5%
случаев соответственно (χ2 = 0,01; р = 0,906).
В нашем исследовании проведена оценка отдаленных результатов лечения
прооперированных пациенток (2-я группа) в отношении выявления рецидива
эндометриоза после завершения терапии. По данным литературы, частота
рецидивирования эндометриоидных кист яичников в течение 1–5 лет после
хирургического лечения варьирует от 8% до 30% [26–29]. Частота возникновения
рецидива у пациенток данной группы составила 6/12,5% случаев в течение 15
месяцев после завершения двухэтапной комбинированной терапии. Полученные
результаты согласуются с данными ряда исследователей, в которых частота рецидива
ЭКЯ колебалась от 11,5% до 12,7% в течение 12–18 месяцев наблюдения [28–30].
В некоторых исследованиях возникновение рецидива наблюдалось с одинаковой
частотой как на ранее оперированном яичнике по поводу первичного эндометриоза,
так и на интактном яичнике [23] и может зависеть от размера (увеличения)
эндометриомы [30]. По нашим данным не установлено зависимости частоты
возникновения рецидива от распространенности эндометриоза, размера эндометриомы,
а также вовлечения в процесс интактного или ранее оперированного яичника по
поводу первичного эндометриоза (р > 0,05), что требует дальнейшего наблюдения.
Выводы
- У пациенток с бесплодием, имеющим эндометриоидные кисты яичников размерами
до 3 см, вариантом лечения является эмпирическая терапия с учетом
рецидивирования эндометриоза и/или снижения маркеров овариального резерва с
целью профилактики его редукции. - Эффективность восстановления фертильности у пациенток с эндометриозом
яичников после завершения эмпирической терапии диеногестом не уступает
двухэтапной схеме лечения, частота наступления беременности составила 46,2% и
45,8% случаев соответственно. - Эффективность восстановления репродуктивной функции у пациенток с
эндометриоидными кистами яичников и бесплодием зависит от возраста женщин и
наличия рецидивирующей формы эндометриоза яичников (р < 0,05).
Литература
-
Краснопольская К. В., Попов А. А., Киракосян К. Э., Михайлова Ю. М.
Эффективность лечения бесплодия, ассоциированного с перитонеальным и
яичниковым эндометриозом // Акушерство и гинекология. 2012. № 8 (1). С. 46–50. -
Синчихин С. П., Мамиев О. Б., Степанян Л. В. Консервативная
монотерапия пациенток с миомой матки // Акушерство и гинекология. 2014. № 3.
С. 79–83. -
Клинышкова Т. В., Фролова Н. Б., Мозговой С. И. Клиническое
значение комплексной оценки рецепторного статуса эндометрия при
эндометриальных полипах // Акушерство и гинекология. 2011. № 3. С. 37–41. -
Kennedy S., Bergqvist A., Chapron C. et al. ESHRE guideline for
the diagnosis and treatment of endometriosis // Hum Reprod. 2005. Vol. 20. Р.
2698–2704. -
Кулаков В. И. Бесплодный брак. Современные подходы к диагностике
и лечению. М.: ГЭОТАР-Медиа, 2006. 616 с. -
Гаспаров А. С., Дубинская Е. Д. Эндометриоз и бесплодие:
инновационные решения. М.: МИА. 2013. 128 с. -
Gandhi A. R., Carvalho L. F., Nutter B., Falcone T. Determining
the fertility benefit of controlled ovarian hyperstimulation with intrauterine
insemination after operative laparoscopy in patient with endometriosis // J
Minim Invasive Gynecol. 2014. Vol. 21. № 1. Р. 101–108. -
Dechanet C., Rihaoui S., Reyftmann L. et al. Endometriosis and
fertility: Results after surgery and Assisted Reproductive Technology (ART) //
Gynecol Obstet Fertil. 2011. Vol. 39. № 1. Р. 3–7. -
Горский С. Л. Реализация репродуктивной функции при синдроме
поликистозных яичников и перитонеальном эндометриозе с использованием
оперативной лапароскопии и экстракорпорального оплодотворения. Автореф. дис. …
д-ра мед. наук. М., 2010. 40 с. -
Hou Z., Mao Y. D., Liu G. Y. Study on the factors associated with
clinical pregnancy rate of in-vitro fertilization in endometriosis related
infertility // Zhonghua Fu Chan Ke Za Zhi. 2013. Vol. 48. № 1. P. 6–10. -
Littman E., Giudice L., Lathi R. et al. Role of laparoscopic
treatment of endometriosis in patients with failed in vitro fertilization
cycles // Fertil. Steril. 2005. Vol. 84. Р. 1574–1578. -
Koch J., Rowan K., Rombauts L. et al. Endometriosis and
Infertility — a consensus statement from ACCEPT (Australasian CREI Consensus
Expert Panel on Trial evidence) // Aust. N Z J Obstet. Gynaecol. 2012. Vol.
52. № 6. P. 513–522. -
Ruiz-Flores F. J., Garcia-Velasco J. A. Is there a benefit for
surgery in endometrioma-associated infertility? // Curr Opin Obstet Gynecol.
2012. Vol. 24. № 3. Р. 136–140. -
Psaroudakis D., Hirsch M., Davis C. Review of the management of
ovarian endometriosis: paradigm shift towards conservative approaches // Curr
Opin Obstet Gynecol. 2014. Vol. 26. № 4. Р. 266–274. -
Андреева Е. Н., Яроцкая Е. Л., Адамян Л. В. Клинический профиль
российских пациенток с диагнозом «генитальный эндометриоз», получающих лечение
агонистом гонадотропного релизинг-гормона. Результаты российского открытого
многоцентрового наблюдательного исследования // Проблемы репродукции. 2011. №
2. С. 50–62. -
Сухих Г. Т., Адамян Л. В. Новые технологии в диагностике и
лечении гинекологических заболеваний // Материалы XXVI Международного
конгресса с курсом эндоскопии. М., 2013. С. 3–9. -
Гаспаров А. С., Дубинская Е. Д., Титов Д. С., Лаптева Н. В.
Клиническое значение овариального резерва в реализации репродуктивной функции
// Акушерство и гинекология. 2014. № 4. С. 11–16. - Эндометриоз: диагностика, лечение и реабилитация. Клинические
рекомендации. М., 2013. 86 с. -
Almog B., Sheizaf B., Shalom-Paz E. et al. Effects of excision of
ovarian endometrioma on the antral follicle count and collected oocytes for in
vitro fertilization // Fertil Steril. 2010. Vol. 94. Р. 2340–2342. -
Garcia-Velasco J. A., Somigliana E. Management of endometriomas
in women requiring IVF: to touch or not to touch // Hum Reprod. 2009. Vol. 24.
№ 3. Р. 496–501. -
Benadlia L., Pasin R., Somigliana E. et al. Unoperated ovarian
endometriomas and responsiveness to hyperstimulation // Hum Reprod. 2011. Vol.
26. Р. 1356–1361. -
Гаспаров А. С., Дубинская Е. Д., Дмитриева Н. В., Яковенко С. А.
Отдаленные результаты лечения бесплодия с использованием вспомогательных
репродуктивных технологий у пациенток с эндометриоидными кистами яичников.
Тезисы VI Общероссийского научно-практического семинара «Репродуктивный
потенциал России: версии и контрверсии» М.: Изд-во журнала Status Praesens.
2013. 248 с. -
Lee H. J., Lee J. E., Ku S. Y. et al. Natural conception rate
following laparoscopic surgery in infertile women with endometiosis // Clin
Exp Reprod Med. 2013. Vol. 40. № 1. Р. 29–32. -
De Ziegler D., Borghese B., Chapron C. Endometriosis and
infertility: pathophysiology and management // Lancet. 2010. Vol. 376. № 9742.
Р. 730–738. -
Клинышкова Т. В., Перфильева О. Н., Гордиенко Н. Г., Тодоренко В. Н.
Влияние размера эндометриомы яичника на состояние овариального резерва
пациенток с бесплодием // Российский вестник акушера-гинеколога. 2015. Т. 15.
№ 1. С. 47–51. -
Busacca M., Chiaffarino F., Candiani M. et al. Determinants of
long-term clinically detected recurrence rates of deep, ovarian, and pelvic
endometriosis // Am. J. Obstet. Gynecol. 2006. Vol. 195. № 2. Р. 426–432. -
Kim M. L., Kim J. M., Seong S. J. et al. Recurrence of ovarian
endometrioma after second-line, conservative, laparoscopic cyst enucleation //
Am. J. Obstet. Gynecol. 2014. Vol. 210. № 3. P. 216. -
Yuan M., Wang W. W., Li Y. et al. Risk factors for recurrence of
ovarian endometriomas after surgical excision // J. Huazhong. Univ. Sci.
Technolog. Med. Sci. 2014. Vol. 34. № 2. P. 213–219. -
Yang X. H., Ji F., AiLi A. et al. Effect of laparoscopic ovarian
endometriosis cystectomy combined with postoperative GnRH-a therapy on ovarian
reserve, pregnancy, and outcome recurrence // Clin. Exp. Obstet. Gynecol.
2014. Vol. 41. № 3. P. 272–275. -
Moini A., Arabipoor A., Ashrafinia N. Risk factors for recurrence
rate of ovarian endometriomas following a laparoscopic cystectomy // Minerva.
Med. 2014. Vol. 105. № 4. P. 295–301.
Статья опубликована в журнале
Лечащий Врач
материал MedLinks.ru







