Введение
Хронические заболевания вен (ХЗВ) остаются распространенной медицинской и социально-экономической проблемой. Так, по данным программы Vein Consult — крупнейшего эпидемиологического исследования распространенности ХЗВ, те или иные симптомы заболевания по классификации CEAP обнаруживались у 83,6% из 91 545 человек, обратившихся за помощью и обследованных в рамках исследования [1]. По данным ряда авторов, частота выявления ХЗВ среди взрослых составляет в среднем 25%, при этом разброс распространенности варикозной болезни вен нижних конечностей как наиболее частого примера ХЗВ варьирует от 2% до 56% среди мужчин и от 1% до 60% среди женщин [2]. В России в исследовании у работников промышленного предприятия признаки ХЗВ обнаруживались у 67,5% женщин и 50,4% мужчин, варикозное расширение вен в целом — у 20% [3]. Общая распространенность ХЗВ среди жителей сельской местности в России составила 62,4% [4]. Несмотря на некоторые методологические недостатки приведенных работ, их результаты показывают высокую распространенность ХЗВ.
Актуальной остается проблема высокой коморбидности подобных патологий с другими сердечно-сосудистыми заболеваниями. Так, наличие симптоматики ХЗВ часто ассоциировано с эмфиземой легких / хронической обструктивной болезнью легких, сахарным диабетом (СД), артериальной гипертензией (АГ), хронической сердечной недостаточностью (ХСН), заболеваниями периферических артерий и др. [5–8], причем сопутствующие патологии могут взаимно отягощать друг друга [7]. Патогенетически нарушения непосредственно в сосудистом русле сочетаются с изменениями в сосудистой стенке. Взаимосвязь и взаимозависимость этих изменений обусловливают усиление патологического процесса с развитием тяжелых осложнений.
Одной из важных проблем современной ангионеврологии является поражение венозной системы головного мозга, которое может проявляться острыми, в виде церебральных венозных тромбозов (ЦВТ), и хроническими формами церебральной венозной недостаточности (ХЦВН). В литературе недостаточно данных о распространенности именно ХЦВН, хотя, по мнению ряда авторов [9], ХЦВН встречаются значимо чаще, чем диагностируются, что, возможно, связано с полиморфизмом, неспецифичностью клинических проявлений и жалоб, предъявляемых пациентами на ранних стадиях ХЦВН. Основными патогенетическими механизмами развития ХЦВН являются повышение гидростатического давления в проксимальных венах и капиллярах, повышение внутричерепного давления, цитотоксический и вазогенный отеки головного мозга с развитием стазов, а в тяжелых случаях (при ЦВТ) — формирование диапедезных кровоизлияний и ишемических очагов [10].
С учетом того, что артериальная и венозная системы головного мозга взаимосвязаны, и при этом венозная часть сосудистого русла рассматривается как рефлексогенная зона, ответственная за развитие компенсаторных реакций, влияющих на постоянство мозгового кровотока, применение препаратов, обладающих венотоническим, антиагрегантным, противотромботическим, ангиопротективным эффектами, является общепризнанным в лечении цереброваскулярной патологии.
Известно, что объединяющим элементом сосудистой системы, состоящей из артерий, вен и капилляров, являются клетки эндотелия, выстилающие внутреннюю поверхность абсолютно всех сосудов организма. В нормальных физиологических условиях эндотелиальные клетки играют критическую роль в поддержании сосудистого гомеостаза, регулируя вязкость крови и фибринолиз, сосудистый тонус, ангиогенез, адгезию лейкоцитов и агрегацию тромбоцитов [11]. Дисфункция эндотелия характеризуется дисбалансом факторов вазодилатации и вазоконстрикции, повышением уровня активных форм кислорода и провоспалительных медиаторов, а также снижением биодоступности оксида азота — главного фактора регуляции тонуса сосудов. Возникновение эндотелиальной дисфункции ведет к нарушению проницаемости эндотелиального барьера, стимулирует формирование воспалительного и протромботического фенотипа, что в той или иной степени является частью патогенеза сосудистых заболеваний, таких как атеросклероз, АГ, СД, ХЗВ [12–14].
В контексте эндотелиопатии как фактора сосудистых нарушений не менее актуальной остается проблема пандемии COVID-19. Поражение сердечно-сосудистой системы на фоне COVID-19 формируется на уровне эндотелиального слоя, выстилающего все сосудистое русло. Развитие системного сосудистого воспаления обусловливает увеличение риска других осложнений, особенно у коморбидных пациентов (c АГ, СД, атеросклерозом, ишемической болезнью сердца (ИБС), ХСН, ХЗВ, хронической венозной недостаточностью (ХВН), ангиопатией и др.) [15, 16]. COVID-19 вызывает формирование воспалительного фенотипа сосудов, характеризующегося развитием эндотелиальной дисфункции, формированием коагуло- и тромбопатий [17].
Таким образом, объединенные сходством патогенетических механизмов и факторов риска сердечно-сосудистые поражения требуют использования средств, обеспечивающих многостороннее влияние на состояния, сопровождающиеся сосудистыми нарушениями и патологией системы гемостаза. Одно из важнейших мест в патогенетической терапии подобных заболеваний занимает ангиопротективная, венотонизирующая, антиагрегантная, противотромботическая терапия. В связи с этим особый интерес вызывают препараты, обладающие комплексным действием на различные звенья сосудистых нарушений. К числу таких средств относится лекарственный препарат АнгиоНорм®, разработанный ФПК «ФармВИЛАР» на базе ВНИИ лекарственных и ароматических растений (ВИЛАР).
Содержание статьи
Компоненты препарата
АнгиоНорм® представляет собой сухой экстракт, получаемый из смеси лекарственного растительного сырья — семян каштана конского, корней солодки, плодов боярышника и плодов шиповника в соотношении 30:15:20:35 соответственно.
Содержание плодов каштана конского обеспечивает антиоксидантные, противовоспалительные, венотонизирующие, противоотечные свойства препарата. Экстракт содержит флавоноиды (кверцетин, кемпферол), проантоцианидин A2 (антиоксидант) и кумарины (эскулин и фраксин) [18], но главным действующим веществом является тритерпеновый сапонин — эсцин [19]. Он способен значимо повышать толерантность эндотелия вен к гипоксии [20]. Воздействуя на клетки эндотелия венозных сосудов на молекулярном уровне, эсцин предотвращает появление двух главных пусковых факторов острого воспаления венозной стенки: падения содержания аденозинтрифосфата (АТФ) и активизации фосфолипазы А2, ответственной за синтез медиаторов воспаления. Блокируя развитие острого повреждения эндотелия, эсцин препятствует деградации мукополисахаридов и поддерживает тонус мышечных элементов венозной стенки, предотвращает адгезию нейтрофилов и тромбоцитов к интиме сосудов [20, 21]. Эсцин снижает проницаемость сосудистой стенки посредством увеличения чувствительности кальциевых каналов, что в итоге приводит к повышению венозного и артериального тонуса [22]. Противовоспалительный эффект эсцина обусловлен подавлением активации и адгезии нейтрофилов. Также ингибируется связанное с этим высвобождение медиаторов воспаления. Проантоцианидин A2, антиоксидант, содержащийся в составе экстракта, участвует в подавлении окислительного стресса и санации свободных радикалов, которые являются важным фактором патогенеза сосудистой недостаточности [23].
Корни солодки содержат сапонин глицирризин (от 8% до 24%), флавоноиды различных типов (ликвиритин, ликвиритозид, изоликвиритин — 3–4%) [24]. Глицирризин ингибирует миграцию нейтрофилов в месте развития воспаления, обладает подавляющей тромбин активностью [25]. Глицирризин подавляет прилипание нейтрофилов к эндотелию сосудов в начальной фазе формирования тромба без снижения способности к свертыванию крови [26, 27]. Состав активных действующих веществ экстракта корней солодки обеспечивает антиагрегационный и противовоспалительный эффекты препаратов с содержанием солодки [28].
Плоды боярышника содержат флавоноиды (гиперозид, кверцетин, изокверцетин, рутин и др.), кофейную и хлорогеновую кислоты, тритерпеновые соединения (урсоловая, олеаноловая кислоты) [24]. Имеются данные о положительном влиянии препаратов боярышника на энергетический обмен в тканях сердца, сосудорасширяющем действии, способности уменьшать возбудимость нервной системы, нормализовать сон, снижать артериальное давление и проницаемость капилляров, оказывать кардиотонический, антисклеротический, антиаритмический, седативный, десенсибилизирующий и антиоксидантный эффекты [29, 30].
Плоды шиповника содержат аскорбиновую кислоту, каротиноиды, витамины K1, B2 и P, флавоноиды (кверцетин, изокверцетин, рутин, гиперозид) [24]. Аскорбиновая кислота как антиоксидант снижает деградацию оксида азота перекисными радикалами, способствуя восстановлению эндотелия сосудов, тормозит утолщение интимы сосудов, нормализует структуру сосудистой стенки [31, 32]. Помимо аскорбиновой кислоты антиоксидантную активность обеспечивает полифенольная фракция. За счет подавления простагландина E2 способствует противовоспалительной активности экстракта [33]. Препараты шиповника оказывают капилляроукрепляющее, адаптогенное, поливитаминное действие.
Особенности комбинированного состава экстракта АнгиоНорм® обусловливают широкий спектр его фармакологической активности. Фармакологические свойства Ангио-Норм®, определяемые количественным и качественным составом экстракта, нашли свое подтверждение в экспериментальных доклинических и клинических исследованиях.
Доклинические исследования
Доклинические исследования фармакологической активности, токсикологических свойств и безопасности препарата АнгиоНорм® были проведены в отделе медицины ВИЛАР. Изучалось его возможное влияние на свертывающую систему крови. Препарат обладал выраженной антиагрегационной и антиатромбоцитарной активностью и эффективно воздействовал на клеточное звено гемостаза. В условиях in vitro показано, что исследуемый препарат достоверно и дозозависимо ингибировал агрегацию тромбоцитов человека при использовании в качестве проагреганта как АДФ, так и коллагена. Полное ингибирование коллаген-индуцированной агрегации тромбоцитов отмечалось при концентрации препарата 5,0 мг/мл.
У кроликов пероральное введение исследуемого препарата в дозе 100 мг/кг резко подавляло коллаген-индуцированную агрегацию тромбоцитов ex vivo: агрегация тромбоцитов снижалась в 3,2, 2,8 и 1,75 раза в зависимости от продолжительности введения препарата (1, 7 и 14 сут соответственно), причем эффект сохранялся на протяжении 14 сут введения препарата, показатель возвращался к исходным значениям через 1 нед. после отмены препарата. Препарат не оказывал существенного влияния на агрегацию тромбоцитов, индуцированную АДФ. Оценка состояния плазменного гемостаза показала, что исследуемый препарат не увеличивал тромбопластиновое время, но укорачивал активированное частичное тромбопластиновое время (АЧТВ), что указывало на некоторую активацию гемостатических реакций по внутреннему пути. Таким образом, результаты опытов свидетельствовали, что препарат оказывает значимое влияние на клеточное звено гемостаза — выраженное антиагрегационное действие in vitro и ex vivo.
В эксперименте у крыс пероральное применение препарата АнгиоНорм® в дозах 20 и 100 мг/кг вызывало снижение проницаемости капилляров кожи на 66,2% и 94,4% соответственно. По капилляропротективному свойству он существенно превосходил комбинацию экстракта семян конского каштана обыкновенного и тиамина гидрохлорида. Применение исследуемого препарата в дозе 100 мг/кг уменьшало воспалительный отек конечностей у мышей на модели формалинового артрита на 27% (p<0,05), гистаминового отека — на 41,2%, уменьшало объем воспалительного экссудата на модели перитонита на 53,9%. По противовоспалительному действию на модели гистаминового отека и перитонита АнгиоНорм® существенно превосходил комбинацию экстракта семян конского каштана обыкновенного и тиамина гидрохлорида. Сочетание капилляропротективной и противовоспалительной активности может способствовать проявлению венотонизирующего действия.
В экспериментальных моделях у крыс применение препарата АнгиоНорм® в дозах 20 и 100 мг/кг увеличивало почечный диурез на 24% и 50% соответственно, что усиливает общее противоотечное действие препарата. В условиях экспериментальных моделей язв желудка у крыс применение этого препарата демонстрировало выраженное протективное действие на слизистую, усиливая ее репаративные свойства. Данный факт может косвенно подтверждать противовоспалительное действие препарата.
В доклинических исследованиях показаны анальгетический и стресс-протективный эффекты препарата АнгиоНорм® [34, 35].
В исследованиях безопасности и переносимости было показано, что АнгиоНорм® не обладает общетоксическим действием и относится к малотоксичным веществам.
Клинические исследования
Эффективность и безопасность препарата АнгиоНорм® у пациентов были оценены в ходе ряда клинических исследований (см. таблицу). Так, исходя из фармакологических свойств, АнгиоНорм® способствует улучшению трофики тканей. В исследовании В.Ф. Корсун и соавт. [35] было показано, что применение этого препарата способствовало разрешению симптомов лимфостаза в группе пациенток (n=12) после мастэктомии. У всех пациенток на фоне приема исследуемого препарата в течение 1 мес. в стандартной дозировке заметно уменьшались застойные явления в плечевой области: исчезали боли, нормализовалась упругость ткани. У большинства пациенток отмечалось улучшение показателей гемореологии: прием исследуемого препарата приводил к снижению агрегационной активности тромбоцитов на 71,4% (p<0,05), к увеличению содержания тромбоцитов на 5,2%, удлинению тромбопластинового времени на 2,3% за счет ингибирования внутреннего механизма свертывания крови, удлинению протромбинового и тромбинового времени, снижению уровня фибриногена в плазме крови на 4,4% и к стабилизации значений международного нормализованного отношения. Положительное действие препарата на трофику тканей авторы объяснили эффектом укрепления стенки сосудов, что приводило к повышению тонуса венозных и лимфатических сосудов и устранению застойных явлений в этих системах [35, 36].
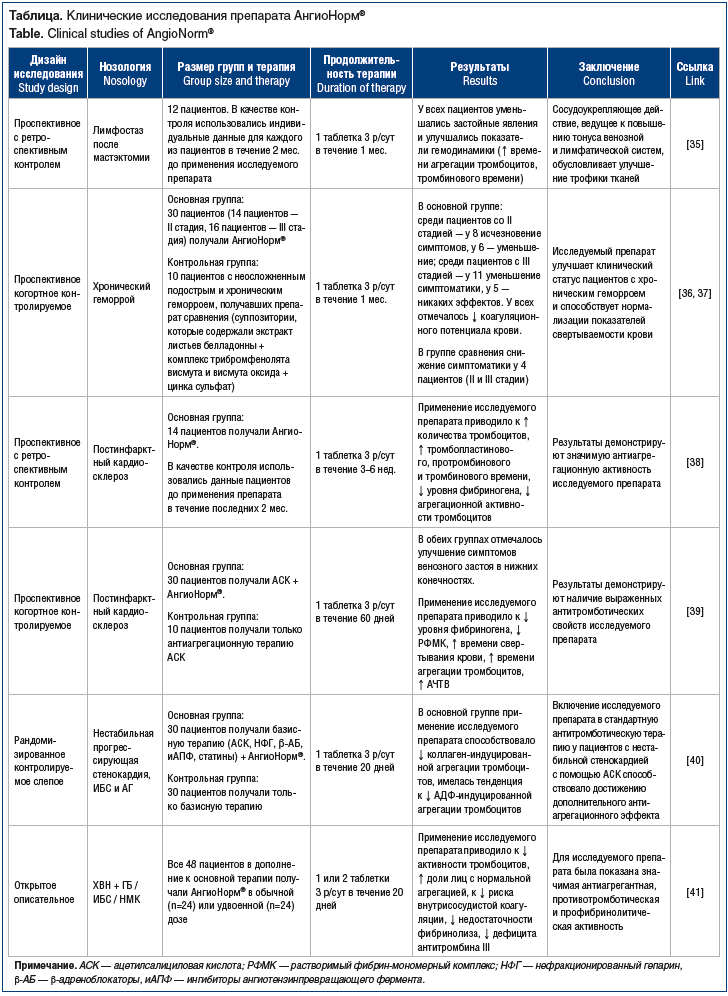
Возможность использования препарата АнгиоНорм® в составе базовой терапии геморроя была исследована в работе И.В. Воскобойниковой и соавт. [37]. Исследование включало наблюдение за 30 пациентами в возрасте от 29 до 74 лет с подострым и хроническим течением геморроя (у 14 пациентов — хронический геморрой II стадии, у 16 пациентов — III стадии), исследуемый препарат принимали в стандартной дозе 300 мг/сут в течение 1 мес. В группу сравнения было включено 10 пациентов с неосложненным подострым и хроническим геморроем, применявших в качестве компонента базовой терапии ректальные суппозитории, которые содержали экстракт листьев белладонны + комплекс трибромфенолята висмута и висмута оксида + цинка сульфат. В основной группе у 8 пациентов со II стадией отмечалось исчезновение субъективной симптоматики (боль, анальный зуд, кровянистые выделения, тенезмы), у 6 — уменьшение симптоматики. У 11 пациентов с III стадией наблюдалось уменьшение субъективной симптоматики, тогда как у 5 не было никакого эффекта. Вместе с тем все пациенты, применявшие препарат исследования, отметили более выраженное улучшение общего самочувствия, отсутствие побочных явлений. В группе сравнения положительный эффект в виде уменьшения симптоматики был выражен у 2 пациентов со II стадией хронического геморроя и у 2 пациентов с III стадией. В основной группе применение исследуемого препарата способствовало уменьшению коагуляционного потенциала крови, которое проявлялось снижением уровня фибриногена с 5,06±0,16 до 4,5±0,16 г/л (p<0,05), снижением уровня растворимого фибрин-мономерного комплекса (РФМК) с 8,35±0,21 до 5,32±0,9 мг / 100 мл (p<0,05), увеличением времени агрегации тромбоцитов с 11,3±0,07 до 15,1±1,21 с (p<0,05), увеличением времени свертывания крови и АЧТВ. В целом было показано, что исследуемый препарат улучшал клинический статус пациентов с хроническим геморроем и способствовал нормализации показателей свертываемости крови, что могло быть актуально у пациентов с хроническими венозными нарушениями [36, 37].
В работе Т.В. Чуйко и соавт. [38] оценивалась эффективность применения препарата АнгиоНорм® в комплексной терапии пациентов с сосудистыми нарушениями. В исследовании приняло участие 14 пациентов, у которых анализировалась динамика неспецифических симптомов постинфарктного кардиосклероза. Курс терапии исследуемым препаратом составлял 3–6 нед. по 3 таблетки в сутки через 40 мин после еды. В качестве контроля использовались данные пациентов до применения препаратов в течение последних 2 мес. Применение исследуемого препарата приводило к увеличению количества тромбоцитов, удлинению показателя тромбопластинового времени, протромбинового и тромбинового времени, снижению уровня фибриногена в плазме крови, агрегационной активности тромбоцитов. У 93,3% пациентов уменьшались боли в икроножных мышцах, у 81,8% — одышка при физической нагрузке. У 6 из 14 больных отмечалась необходимость в снижении дозы ацетилсалициловых антиагрегантов. Результаты исследования ярко демонстрируют антиагрегационную активность исследуемого препарата, в связи с чем авторы предполагают, что в определенных случаях препарат может быть использован как средство выбора вместо химически синтезированных антиагрегантов.
В другом исследовании у пациентов с постинфарктным кардиосклерозом сравнивалась эффективность базовой антиагрегантной терапии ацетилсалициловой кислотой (АСК) в дозе 75–125 мг в сочетании с препаратом АнгиоНорм® (n=30) и без него (n=10). Исследуемый препарат применялся в рекомендуемой дозировке на протяжении 60 дней. Улучшение симптомов венозного застоя в нижних конечностях (отечность, боли и судороги в икроножных мышцах) регистрировалось как в основной, так и в контрольной группе. Применение исследуемого препарата в основной группе привело к уменьшению уровня фибриногена, достоверному уменьшению уровня РФМК, увеличению времени свертывания крови, достоверному увеличению времени агрегации тромбоцитов, увеличению АЧТВ. Вследствие выраженных антитромботических свойств авторы рекомендовали использование исследуемого препарата в комплексной терапии постинфарктного кардиосклероза [39].
Антитромботические свойства препарата АнгиоНорм® были изучены в рандомизированном слепом клиническом исследовании у пациентов с нестабильной (прогрессирующей) стенокардией. В исследование было включено 60 пациентов с верифицированным диагнозом ИБС, который у 100% ассоциировался с АГ. Все пациенты получали базисную терапию, включавшую АСК, нефракционированный гепарин (который отменялся до назначения исследуемого препарата), β-адреноблокаторы (метопролол или бисопролол), ингибиторы АПФ (эналаприл или периндоприл), статины. Дозы базисных препаратов зависели от клинических проявлений основной патологии и показателей гемодинамики. Было сформировано 2 группы: основная (n=30), в которой пациенты получали АнгиоНорм® дополнительно к стандартной терапии, и контрольная (n=30). Продолжительность курса лечения исследуемым препаратом составила 20 дней, препарат принимался согласно инструкции в стандартной дозировке 300 мг/сут. По результатам 3-недельной терапии в обеих группах регистрировалась положительная динамика достижения целевых уровней артериального давления, что свидетельствовало о хорошей сочетаемости исследуемого препарата с антигипертензивными и антиангинальными препаратами. На 20-й день в основной группе отмечалось значимое снижение количества лейкоцитов периферической крови (р=0,03) и СОЭ (р=0,04) по сравнению с исходными показателями. Помимо этого, в группе активного лечения применение исследуемого препарата способствовало снижению коллаген-индуцированной агрегации тромбоцитов (р=0,04) по сравнению с контрольной группой, имелась тенденция к снижению показателей АДФ-индуцированной агрегации тромбоцитов (р=0,05), тогда как параметры адреналин-индуцированной (р=0,63) и спонтанной (р=0,58) агрегации тромбоцитов в обеих группах были сопоставимы. Включение исследуемого препарата в стандартную антитромботическую терапию у пациентов с нестабильной стенокардией с помощью АСК способствовало достижению дополнительного антиагрегационного эффекта, что может находить применение в широкой клинической практике врачей-кардиологов [40].
Венотонизирующая активность препарата АнгиоНорм® была изучена в открытом обсервационном исследовании у пациентов (n=48), страдающих ХВН нижних конечностей в фазе декомпенсации, а также у пациентов с заболеваниями, сопровождающимися артериальными сосудистыми нарушениями (АГ, ИБС, нарушения мозгового кровообращения). В дополнение к основной терапии все пациенты получали исследуемый препарат по 1 таблетке 3 р/сут (n=24) или 2 таблетки 3 р/сут (n=24), продолжительность приема составляла 20 дней. У большинства пациентов отмечалась высокая эффективность исследуемого препарата в отношении субъективных (боли, тяжесть в ногах, судороги, парестезии, утомляемость икроножных мышц и отеки) и объективных (варикозы, отеки, трофические нарушения) симптомов ХВН. Только у 2 пациентов с ХВН IV–V стадии по СЕАР терапия исследуемым препаратом не оказала какого-либо положительного действия. Анализ показателей гемостаза показал, что на фоне приема исследуемого препарата у пациентов с ХВН снижалась активность тромбоцитов по типу гиперагрегации (p<0,05), а доля лиц с нормальной функцией тромбоцитов возросла до 91,6%. В группе пациентов с артериальными нарушениями доля лиц с нормоагрегацией достигала 100%. АнгиоНорм® способствовал снижению числа лиц с повышенным уровнем РФМК — молекулярного маркера внутрисосудистого свертывания, следствием чего являлось снижение подобного риска. На фоне приема исследуемого препарата снижалась недостаточность фибринолиза более чем в 4 раза у пациентов с ХВН (p=0,03) и более чем в 2 раза у пациентов с артериальными сосудистыми нарушениями (p=0,04). В обеих группах значимо снижался дефицит антитромбина III (p<0,05). Таким образом, для исследуемого препарата была показана антиагрегантная, противотромботическая и профибринолитическая активность, эффективность в отношении сосудистых нарушений венозного (ХВН) и артериального русла (АГ, ИБС, нарушения мозгового кровообращения) [41].
Заключение
Препарат АнгиоНорм® сочетает антиагрегационные, ангиопротекторные, венотонизирующие и противовоспалительные свойства, обладает улучшающим микроциркуляцию действием. Широкий спектр действия препарата обусловлен сочетанием компонентов, входящих в его состав. Доклинические (экспериментальные) и клинические исследования позволили подтвердить наличие у препарата данных фармакологических свойств. Клинические исследования продемонстрировали хорошую эффективность, безопасность и переносимость терапии у пациентов с различными нарушениями сосудистого и микроциркуляторного русла (ХВН, АГ, ИБС, нарушения мозгового кровообращения, геморрой, трофические язвы на фоне варикозно-расширенных вен, постинфарктные состояния, лимфостаз верхней конечности после оперативного удаления опухоли молочной железы). Результаты свидетельствуют о возможности длительного и безопасного использования данного препарата в комплексной терапии сосудистых поражений различного происхождения в амбулаторных и стационарных условиях.
Сведения об авторах:
Соловьева Элла Юрьевна — д.м.н., доцент, заведующая кафедрой неврологии ФДПО РНИМУ им. Н.И. Пирогова Минздрава России; 117437, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0003-1256-2695.
Абдуллаев Шерзод Пардабоевич — к.б.н., научный сотрудник НИИ молекулярной и персонализированной медицины ФГБОУ ДПО РМАНПО Минздрава России; 125993,
Россия, г. Москва, ул. Баррикадная, д. 2/1; ORCID iD 0000-0001-9001-1499.
Контактная информация: Абдуллаев Шерзод Пардабоевич, e-mail: sherzodx5@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 19.04.2022.
Поступила после рецензирования 18.05.2022.
Принята в печать 10.06.2022.
About the authors:
Ella Yu. Solovieva — Dr. Sc. (Med.), Associate Professor, Head of the Department of Neurology, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0003-1256-2695.
Sherzod P. Abdullaev — C. Sc. (Bio.), Researcher at the Research Institute of Molecular and Personalized Medicine, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0001-9001-1499.
Contact information: Sherzod P. Abdullaev, e-mail: sherzodx5@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 19.04.2022.
Revised 18.05.2022.
Accepted 10.06.2022.
Информация с rmj.ru





