Введение
Рациональная антибактериальная терапия стала одной из приоритетных задач для мировой и отечественной медицины. Растущая антибиотикорезистентность, более высокая скорость появления новых патогенов в сравнении со скоростью синтеза новых молекул с антимикробной активностью, развитие в ряде случаев побочных эффектов антибактериальных препаратов диктуют необходимость, с одной стороны, строгого соблюдения показаний к назначению антибактериальных средств с определенной клиническими рекомендациями продолжительностью и курсовой дозой, а с другой — учета и минимизации рисков, ассоциированных с применением антибиотиков [1, 2].
В реальной клинической практике наиболее частым побочным эффектом антимикробной терапии следует признать антибиотик-ассоциированную диарею (ААД), которая развивается с частотой до 25% от всех случаев применения антибиотиков [1]. Формирование данного осложнения, помимо дополнительных рисков возникновения электролитных нарушений и снижения качества жизни пациентов, также способствует формированию резистентных штаммов бактерий [1, 3].
Настоящий обзор подготовлен с целью систематизации данных о механизмах развития ААД, подходов к ее профилактике, диагностике и терапии.
АДД: механизмы развития, диагностика, лечение и профилактика
Антибиотик-ассоциированная диарея, являющаяся одним из наиболее распространенных осложнений антибиотикотерапии, характеризуется наличием жидкого стула не менее 3 раз в сутки на фоне проведения антибактериальной терапии или в течение 2 мес. после ее окончания. Таким образом, ААД — это диарея, хронологически связанная с применением антибактериальных средств при отсутствии других этиологических факторов [1, 2].
Механизмы формирования ААД гетерогенны, что определяет дифференцированный подход к профилактике заболевания и ведению больных.
Прежде всего, возможно формирование ААД в связи с непосредственным влиянием антибактериального лекарственного средства на стенку кишки. Так, применение амоксициллина в комбинации с ингибиторами β-лактамаз усиливает моторную активность тонкой кишки за счет активации III фазы мигрирующего моторного комплекса, которая характеризуется интенсивными ритмическими сокращениями стенки кишки, обеспечивающими в норме транзит в толстую кишку до половины общего объема содержимого тонкой кишки [4]. Механизмы, способствующие непосредственному усилению моторики тонкой кишки при приеме амоксициллина в комбинации с клавулановой кислотой, изучены недостаточно. Предполагается, что амоксициллин в комбинации с клавулановой кислотой имеет сродство к рецепторам в стенке тонкой кишки либо оказывает паракринное влияние, о чем свидетельствует усиление двигательной активности тонкой кишки у большинства больных ААД уже в первые 10 мин после приема препарата [4]. Все 14-членные макролиды, среди которых влияние на моторную функцию пищеварительного тракта наиболее изучено у эритромицина, являются агонистами рецептора мотилина. Эритромицин стимулирует двигательную активность антрального отдела желудка и двенадцатиперстной кишки за счет активации III фазы мигрирующего моторного комплекса, вместе с тем снижая тонус пилорического сфинктера, что приводит к возникновению диареи [5]. Кроме того, по данным отдельных исследований, эритромицин может повышать концентрацию мотилина в плазме крови [6]. Неомицин и тетрациклин обладают энтеротоксическим эффектом. Изменения слизистой оболочки кишечника на ультраструктурном уровне у здоровых людей отмечаются уже через неделю после начала приема антибиотика в виде: укорочения кишечных ворсинок; инфильтрации собственной оболочки кишечника плазматическими клетками, эозинофилами и макрофагами; интенсификации процессов митоза энтероцитов, которые ассоциируются с развитием диарейного синдрома и регрессируют после окончания приема антибиотика [7]. Введение цефтриаксона и цефоперазона может приводить к развитию билиарной недостаточности вследствие нарушения процессов дегидроксилирования желчных кислот и формирования цефтриаксон-кальциевого комплекса, выпадающего в осадок в желчных путях у детей с формированием цефтриаксон-ассоциированного холелитиаза [8]. Билиарная недостаточность создает условия для нарушения процессов эмульгирования жиров и активации ферментов поджелудочной железы, развития синдрома мальдигестии и усиления кишечной перистальтики [6].
При ААД, связанной с непосредственным влиянием антибактериального лекарственного средства на стенку кишки, не происходит увеличения объема каловых масс, не возникает электролитных нарушений, а синдром диареи купируется самостоятельно после прекращения приема антибактериальных средств.
Другой тип ААД связан с модуляцией состава микробиоценоза кишечника и протекает в двух вариантах. Первый вариант, так называемая идиопатическая ААД, протекает без проявлений интоксикации и встречается в 70–80% всех случаев ААД. Лечение антибиотиками оказывает выраженное негативное влияние на количественный и качественный состав как полостной, так и пристеночной микробиоты кишечника, проявляющееся уже через несколько дней от начала терапии. Вместе с тем наблюдается значительное распространение штаммов бактерий, содержащих гены резистентности [9]. Деструктивное действие антибактериальных препаратов связано не только с прямым бактерицидным и бактериостатическим действием на определенные штаммы, входящие в антимикробный спектр препарата. Сложные патогенетические взаимодействия между бактериальными видами могут быть нарушены вследствие прерывания цепочек утилизации и синтеза веществ отдельными штаммами, попавшими в спектр действия антибиотика [10]. Дисбиоз наиболее часто проявляется в виде снижения количества представителей Firmicutes и Bacteroidetes и избыточного роста представителей Enterobacteriaceae, что снижает устойчивость к колонизации патогенными бактериями и увеличивает возможность развития энтеропатогенных бактерий, антибиотикорезистентных штаммов, таких как ванкомицин-резистентный энтерококк [11, 12]. Кроме того, измененный состав кишечной микробиоты ассоциирован с нарушением целостности эпителиального кишечного барьера и повышением кишечной проницаемости. Так, снижение представительства Bifidobacteriaceae приводит к падению выработки короткоцепочечных жирных кислот (КЦЖК), участвующих в модуляции воспалительных процессов, поддержании целостности эпителиального барьера и регуляции моторной активности кишки, что, помимо ААД, создает риски развития воспалительных заболеваний кишечника и функциональных заболеваний толстой кишки [13–15]. Стоит отметить, что влияние различных групп антибиотиков на кишечную микробиоту существенно различается. Так, лечение фторхинолонами подавляет аэробную грамотрицательную флору, создавая тем самым условия для роста грамположительных палочек и дрожжей [16]. Ванкомицин подавляет рост представителей Enterococcus, Clostridioides, Bifidobacteria и Bacteroides, что способствует росту резистентных энтерококков, некоторых видов Lactobacillaceae и условно-патогенных Enterobacteriaceae [11]. Цефалоспорины III поколения в высоких концентрациях выделяются с калом и оказывают негативное воздействие на Enterobacteriaceae, в то же время позволяя развиваться представителям Enterococcus и Candida, а также инфекции C. difficile [17]. Терапия метронидазолом, несмотря на эффективность в отношении анаэробов, ассоциирована с незначительными изменениями состава кишечной микрофлоры и увеличением представительства лактобацилл. Однако использование метронидазола в комбинации с кларитромицином при эрадикационной терапии Helicobacter pylori способствует росту Enterococcus и макролидорезистентных грамотрицательных штаммов, подавляя при этом представителей Escherichia, Bifidobacteria и Bacteroides [9]. Изменения в составе кишечной микробиоты могут сохраняться до 4 лет после завершения курса антибиотикотерапии [18].
В общем анализе крови больного не выявляется лейкоцитоза и увеличения скорости оседания эритроцитов, а при проведении эндоскопии не выявляется макроскопических изменений слизистой оболочки кишки при отсутствии других органических заболеваний [19].
Другим вариантом этого типа является ААД, связанная с инфекцией C. difficile — анаэробной спорообразующей грамположительной палочкой, передающейся фекально-оральным путем. Споры бактерии устойчивы к воздействию тепла, кислоты и антибиотиков, что способствует ее распространению в медицинских учреждениях и создает условия для рецидива заболевания даже после эрадикации вегетативных форм инфекции. Псевдомембранозный колит впервые был описан в 1883 г. C. difficile была обнаружена впервые в 1935 г. исследователями Hall и O’Toole в кале новорожденных и названа Bacillus difficilis из-за сложностей с выделением и культивированием [20, 21]. Сегодня инфекция C. difficile остается актуальной проблемой мирового здравоохранения, что связано с ростом заболеваемости, смертности и расходов на ее лечение. Так, ежегодно в США регистрируется около полумиллиона случаев заболевания C. difficile, из которых 20 тыс. случаев заканчиваются смертью пациента. В Европе частота заболевания составляет примерно 7 случаев на 10 000 койко-дней [22, 23]. Прием антибактериальных препаратов способствует нарушению состава микробиоты толстой кишки, снижая колонизационную резистентность и формируя нишу для распространения C. difficile. Основными факторами вирулентности C. difficile являются белковые токсины А и В, которые вызывают инактивацию Rho ГТФазы эпителиоцитов, нарушают формирование актинового цитоскелета клеток с их последующим апоптозом или некрозом. C. difficile вызывает повреждение эпителиального барьера слизистой оболочки толстой кишки с активацией воспалительных процессов в стенке кишки и выбросом провоспалительных цитокинов в системный кровоток [24]. Применение антибиотиков является главным фактором риска развития клостридиальной инфекции, наиболее часто развитие заболевания наблюдается при лечении цефалоспоринами, фторхинолонами, клиндамицином и некоторыми пенициллинами. В связи со значительным разнообразием клинических проявлений принято классифицировать C. difficile-ассоциированную инфекцию в зависимости от тяжести заболевания. Легкой степенью считают наличие диареи в сочетании с абдоминальной болью. Тяжелое течение заболевания характеризуется водянистой диареей с кровью и гипоальбуминемией в сочетании с лейкоцитозом более 15×109/л или болезненностью при пальпации живота. Осложненным течением заболевания считают случаи водянистой диареи с кровью в сочетании с одним или более признаками из следующих: лихорадка выше 38,5 °C, илеус, изменение сознания, повышение уровня лейкоцитов более 25×109/л или снижение менее 2×109/л, а также тяжелая органная недостаточность [25].
Диагностика инфекции, вызванной C. difficile, помимо наличия характерной клинической картины, включает в себя выявление токсинов C. difficile в фекалиях пациентов с диареей [25]. В клинической практике наиболее часто применяют иммуноферментный анализ для определения токсинов А и В в кале. Чувствительность теста составляет 75–95%, специфичность — 83–98% [26]. Исследование глутаматдегидрогеназы позволяет выявить C. difficile у пациента, однако тест не дает возможности дифференцировать токсигенные и нетоксигенные штаммы C. difficile, поскольку фермент глутаматдегидрогеназа синтезируется всеми штаммами. Высокой чувствительностью и специфичностью обладает тест амплификации нуклеиновых кислот для токсигенного штамма C. difficile, однако применение его в клинической практике весьма ограничено [25]. Эндоскопическая картина псевдомембранозного колита характеризуется наличием бляшек диаметром до 1–2 см желто-зеленого цвета, плотно спаянных с подлежащей слизистой оболочкой. Между наложениями виднеются участки гиперемированной слизистой оболочки кишки. При попытке удаления пленки слизистая кишки кровоточит. В более тяжелых случаях наложения могут полностью покрывать слизистую оболочку толстой кишки с формированием очагов некроза и язв [27]. Гистологическое исследование биопсийного материала не является рутинным исследованием при установлении инфекции C. difficile, однако может иметь большое значение для дифференциальной диагностики. При легком течении заболевания во время гистологического исследования можно обнаружить скопления фибрина, муцина и нейтрофилов на участках между криптами. Тяжелое течение заболевания характеризуется также включением в бляшки поверхностной части крипт и расширением просвета крипт. В финальной стадии заболевания слизистая оболочка и подслизистый слой некротизированы, замещены массами фибрина со скоплениями нейтрофилов, в слизистой оболочке выявляется большое количество кровоизлияний [25, 28].
В условиях планируемой антибактериальной терапии крайне важно выделение факторов риска развития ААД: возраст старше 65 лет, иммунодефицитные состояния, длительный прием ингибиторов протонной помпы, глюкокортикостероидов, проведение химиотерапии, длительная госпитализация, повторный прием антибактериальных средств. Именно в этой когорте лиц необходимо проводить профилактику, направленную на поддержание микробиома в условиях антибактериальной терапии.
Состав микробиоты является одним из важных факторов, определяющих двигательную активность желудочно-кишечного тракта (ЖКТ) (рис. 1).
![Рис. 1. Механизмы влияния микробиоты на моторику кишечника. Адаптировано по [31] Fig. 1. Mechanisms of the effect of microbiota of intestinal motility (adapted from [31]) Рис. 1. Механизмы влияния микробиоты на моторику кишечника. Адаптировано по [31] Fig. 1. Mechanisms of the effect of microbiota of intestinal motility (adapted from [31])](https://medblog.su/wp-content/uploads/2022/07/antibiotik-assotsiirovannaya-diareya-v-praktike-klinitsista-podhody-k-profilaktike-i-terapii-livzan-m-a-fedorin-m-m.png)
Так, продукты жизнедеятельности микроорганизмов взаимодействуют с толл-подобными рецепторами и дендритными клетками. Система толл-подобных рецепторов оказывает влияние на функцию энтеральной нервной системы и нервно-мышечную передачу, определяя моторную активность кишки. Синтезируемые КЦЖК регулируют выделение цитокинов Т-хелперами и генерацию регуляторных Т-клеток, ингибируя воспалительные процессы путем снижения экспрессии гистоновой деацетилазы [29]. Микробиота ЖКТ регулирует выработку серотонина путем повышения его синтеза энтерохромаффинными клетками через высвобождение метаболитов, таких как дезоксихолат, который активирует трансмембранные рецепторы, сопряженные с G-белком, экспрессируемые энтерохромаффинными клетками. Серотонин также высвобождается из энтерохромаффинных клеток в ответ на выработку кишечной микробиотой КЦЖК и стимулирует рецепторы афферентных волокон, что приводит к сократительной активности гладкой мускулатуры кишки [30]. Кроме того, ряд микроорганизмов способен к самостоятельной выработке серотонина. Кальцитонин-ген родственный пептид модулирует функцию дендритных клеток и участвует в передаче информации о составе кишечной микробиоты в центральную нервную систему [31]. Хотя опубликованы некоторые данные о влиянии газов, выделяющихся в процессе жизнедеятельности микробиоты ЖКТ (метан, водород), на моторику кишечника через энтеральную нервную систему, однако механизмы эти пока малоизучены [32].
Таким образом, модуляция кишечной микробиоты позволяет нормализовать моторную активность кишечника. Среди препаратов, оказывающих положительное влияние на состав кишечной микробиоты, выделяют: пробиотики, содержащие живые штаммы микроорганизмов; пребиотики, стабилизирующие среду обитания и стимулирующие рост нормальной микрофлоры; симбиотики, сочетающие в себе свойства пре- и пробиотиков [33, 34]. Механизмы действия пробиотиков представлены на рисунке 2.
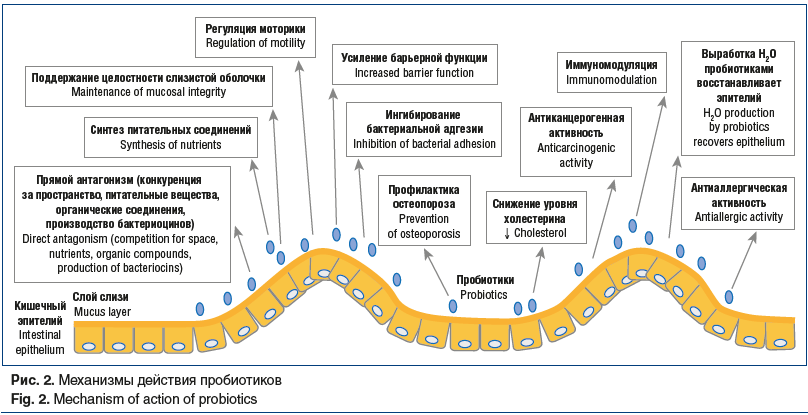
Восстановление нормальной микрофлоры кишки в результате приема про-, пре- и симбиотиков способствует ограничению пространства для патогенной флоры в просвете кишки. Пробиотические организмы вступают в конкуренцию с патогенными бактериями за питательные вещества в полости кишки, способствуют поддержанию концентрации питательных веществ для симбионтных микроорганизмов и нормального уровня pH в полости кишки [34, 35]. Кроме того, ряд пробиотических штаммов способен к самостоятельной выработке бактерицидных веществ [36]. Выработка провоспалительных цитокинов и инициация фагоцитоза макрофагами в условиях приема пробиотиков осуществляется путем стимуляции толл-подобных рецепторов продуктами жизнедеятельности симбиотических микроорганизмов, что позволяет снизить уровень воспаления в стенке кишки. Ряд пробиотических штаммов участвует в регуляции активности Т-лимфоцитов и способствует повышению секреции IgA в слизистой оболочке. Прием пробиотиков позволяет уменьшить концентрацию воспалительных цитокинов, снижая выраженность воспалительных процессов [37]. Отдельные штаммы оказывают положительное влияние на обмен холестерина за счет деконъюгации желчных кислот или связывания эндогенного или экзогенного холестерина и свободных желчных кислот с микробной клеткой [38].
С целью профилактики ААД пробиотики должны быть рекомендованы пациентам из группы риска с выбором пробиотических культур, продемонстрировавших свою эффективность и безопасность по данным клинических исследований и метаанализов.
В 2017 г. опубликован систематический обзор и метаанализ, включивший 17 рандомизированных клинических исследований с 3631 пациентом, которые продемонстрировали эффективность применения пробиотиков для снижения риска развития ААД (8,0% в группе приема пробиотиков против 17,7% в контрольной группе, ОР 0,49, 95% ДИ 0,36–0,66). Наибольшая эффективность была продемонстрирована для штаммов Lactobacillus rhamnosus GG (LGG) и Saccharomyces boulardii (Энтерол®) [39]. Установлено, что эффективность пробиотиков наиболее высока при начале приема в течение 24 ч после введения первой дозы антибиотика. Пробиотические штаммы следует назначать во время лечения антибиотиками, а затем продолжать прием в течение не менее 2 нед. после завершения курса антибиотикотерапии. Большинство метаанализов продемонстрировали наибольшую эффективность пробиотиков при суточной дозе не менее 109–1010 микроорганизмов [40].
Особо актуальным вопрос выбора пробиотического штамма стал в эпоху пандемии COVID-19. Так, до 95% госпитализированных пациентов с COVID-19 получают антибактериальные препараты для предотвращения вторичных бактериальных инфекций. Кроме того, опубликованы предположения исследователей о возможной модуляции иммунного ответа на инфекцию COVID-19 при приеме пробиотиков, что позволило бы снизить вероятность избыточного иммунного ответа с развитием «цитокинового шторма» [40].
Систематический обзор, включивший 249 рандомизированных контролируемых исследований, в которых оценивались 22 наиболее распространенных пробиотиков, позволил установить наибольшую эффективность в профилактике и лечении ААД препаратов, содержащих штаммы: S. boulardii, смесь трех штаммов Lactobacillus (L. acidophilus, L. casei, L. rhamnosus) и L. casei [41].
Эффективность профилактики развития инфекции C. difficile при приеме антибиотиков была оценена в метаанализе, включившем 23 рандомизированных клинических исследования. Наибольшую эффективность продемонстрировали четыре пробиотика: S. boulardii CNCM I-745, L. casei DN114001, трехштаммовая смесь L. acidophilus CL1285, L. casei LBC80R и L. rhamnosus CLR2 и двухштаммовая смесь L. acidophilus и Bifidobacterium bifidum [42]. В руководстве Американской гастроэнтерологической ассоциации по профилактике инфекции C. difficile подчеркнута важность специфичности штаммов пробиотиков. Рекомендовано четыре типа пробиотиков для первичной профилактики C. difficile: S. boulardii CNCM I-745, смесь L. acidophilus CL1285, L. casei LBC80R и L. rhamnosus CLR2 «Bio-K+» и две смеси L. acidophilus, B. bifidum, Lactobacillus delbrueckii subsp. bulgaricus (с включением или без включения Streptococcus salivarius subsp. thermophilus) [43].
Сахаромицеты S. boulardii CNCM I-745 (Энтерол®) представляют собой пробиотические грибы из шкурки плодов личи. Впервые S. boulardii были выделены исследователем H. Boulard в 1923 г. в Индокитае. Систематический обзор, включивший 27 рандомизированных плацебо-контролируемых исследований с участием 5029 пациентов, продемонстрировал эффективность и безопасность S. boulardii в 84% случаев. Метаанализ выявил значительную терапевтическую эффективность S. boulardii в профилактике ААД (ОР 0,47, 95% ДИ 0,35–0,63, p<0,001) [44]. Прием препарата Энтерол® позволяет снизить риск развития ААД в 2 раза, а вероятность возникновения ААД, связанной с C. difficile, в 3 раза [45]
Штамм S. boulardii CNCM I-745 рекомендован для профилактики и лечения ААД у пациентов с COVID-19 с обязательным дальнейшим врачебным контролем динамики тяжести состояния пациента [46]. При приеме S. boulardii CNCM I-745 (Энтерол®) увеличивается синтез КЦЖК, в частности ацетата, бутирата и пропионата, что способствует более быстрой регенерации кишечного эпителия и росту собственной облигатной микрофлоры. S. boulardii CNCM I-745 оказывает антимикробное действие, обусловленное антагонистическим эффектом в отношении патогенных и условно-патогенных микроорганизмов, в том числе C. difficile, Candida albicans, Escherichia coli [47]. Препарат расщепляет бактериальные цито- и энтеротоксины, способствует повышению ферментативной функции кишечника, а также обладает естественной устойчивостью к антибиотикам, благодаря чему может эффективно применяться уже во время проведения курса антибактериальной терапии. Лиофилизированные S. boulardii синтезируют гормоноподобные субстанции спермин и спермидин, стимулирующие восстановление эпителиального кишечного барьера, что сопровождается повышением ферментативной активности кишечника за счет стимуляции выработки ферментов лактазы, сахаразо-изомальтазы и мальтазы [24]. Активация работы транспортного канала SGLT-1 усиливает всасывание питательных веществ, натрия и глюкозы [48]. S. boulardii также оказывают стимулирующее действие на иммунную систему кишечника, повышая секрецию IgA [48]. S. boulardii проходят через пищеварительный тракт в неизменном виде без колонизации и полностью выводятся из организма в течение 2–5 дней после прекращения приема.
Заключение
Таким образом, несмотря на высокую распространенность ААД, сегодня существуют эффективные средства профилактики и лечения этого заболевания, среди которых ведущее место занимают пробиотики. Одним из наиболее эффективных препаратов для профилактики и лечения ААД является пробиотическая культура S. boulardii, которая может успешно применяться для профилактики идиопатической и связанной с инфекцией C. difficile ААД, а также в качестве монотерапии для коррекции идиопатической ААД и в составе комбинированной терапии для лечения инфекции C. difficile.
Сведения об авторах:
Ливзан Мария Анатольевна — д.м.н., профессор, член-корр. РАН, заведующая кафедрой факультетской терапии и гастроэнтерологии, ректор ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-6581-7017.
Федорин Максим Михайлович — ординатор кафедры факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-0238-4664.
Контактная информация: Федорин Максим Михайлович, e-mail: maxim.f@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 04.04.2022.
Поступила после рецензирования 27.04.2022.
Принята в печать 26.05.2022
About the authors:
Maria A. Livzan — Dr. Sc. (Med.), Professor, Corresponding Member of the RAS, Head of the Department of Faculty Therapy and Gastroenterology, Chancellor Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-6581-7017.
Maxim M. Fedorin — Resident of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation;
ORCID iD 0000-0002-0238-466. Contact information: Maxim M. Fedorin, e-mail: maxim.f@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 04.04.2022.
Revised 27.04.2022.
Accepted 26.05.2022
.
Информация с rmj.ru






