Введение
Инсектная аллергия (ИА) представляет собой иммуноопосредованные реакции, возникающие при ужалениях, укусах насекомыми, при соприкосновении с ними, вдыхании частиц тел насекомых и/или продуктов их жизнедеятельности. Аллергические реакции на ужаление пчелой, осой, шершнем — насекомыми, относящимися к отряду перепончатокрылых (Hymenoptera), характеризуются тяжестью симптомов, бурным течением и возможностью летального исхода [1].
Распространенность ИА к яду перепончатокрылых в России составляет 0,4–8% [2]. Среди взрослого населения Европы сенсибилизацию к жалящим насекомым (ЖН) выявляют в 9,2–28,7% случаев, а статистическое наблюдение системных реакций колеблется от 0,3% до 7,5% [3, 4]. В России системные реакции к яду ЖН отмечены у 5,3% обследованных пациентов [5]. Смертность от анафилактических реакций на яд ЖН составляет 0,03–0,48% на 1 млн населения ежегодно [6].
Согласно данным WHO/IUIS субкомитета по номенклатуре аллергенов в составе яда медоносных пчел вида Apis mellifera содержится 12 аллергенов: Api m1 — фосфолипаза А2, Api m2 — гиалуронидаза, Api m3 — кислая фосфатаза, Api m4 — мелиттин, Api m5 — дипептидилпептидаза IV (аллерген С), Api m6 — ингибитор протеазы, Api m7 — протеаза, Api m8 — карбоксилэстераза, Api m9 — карбоксипептидаза, Api m10 — икарапин (богатый углеводами протеин), Api m11.0101, Api m11.0201 — главные протеины молочка для питания матки (маточного молочка) 8 и 9, Api m 12 — вителлогенин [6]. Известно, что наивысшую аллергенную активность проявляют фосфолипаза А2 (Api m1), гиалуронидаза (Api m2), кислая фосфатаза (Api m3). Аллергенную активность проявляет и мелиттин (Api m4) [1], который является основным компонентом яда пчелиного (ЯП). Это щелочной пептид, состоящий из 26 аминокислот (молекулярная масса 2840 Да) [7–10], составляет 35–50% общей массы сухого яда. Мелиттин образует в растворе нити, которые могут создать впечатление о большей молекулярной массе. Он способен находиться в растворе в равновесном состоянии в виде мономера или агрегата (димер-тетрамер) [8, 11]. Особенность строения мелиттина определяет не только его поверхностную активность как детергента, но и исключительную мембранную токсичность на клеточном и субклеточном уровнях. Повреждение мембран клеток происходит, главным образом, посредством увеличения проницаемости. Это приводит к усиленному выходу ионов калия и в последующем — к цитолизу. Токсическое действие мелиттина усиливается при взаимодействии с органеллами клеток, что вызывает высвобождение ферментов из лизосом или медиаторов (гистамин, брадикинин) из гранул тучных клеток, базофилов крови [12] и тромбоцитов. Мелиттин реагирует также и со связанными с мембранами ферментными системами. Например, он повреждает катион-активированную аденозинтрифосфатазу и ацетил-холинэстеразу и прерывает окислительное фосфорилирование в митохондриях [13]. Эти эффекты свидетельствуют о высокой токсичности
мелиттина.
Во множестве зарубежных исследований сообщалось, что мелиттин может индуцировать апоптоз и проявлять антипролиферативные свойства. Мелиттин мог бы стать идеальным средством против рака, однако его применение ограничено литическими свойствами [14].
Мелиттин обладает потенциалом для использования в адъювантной иммунотерапии. Ответ иммунной системы на различные раздражители зависит от секреции различных метаболитов из макрофагов. Одним из мощных стимулов является липополисахарид (ЛПС) — компонент, выделенный из грамотрицательных бактерий, который индуцирует секрецию провоспалительных цитокинов в культурах клеток макрофагов. Эта секреция усиливается, когда ЛПС сочетается с мелиттином. Способность мелиттина повышать высвобождение фактора некроза опухоли α, интерлейкинов (ИЛ-1β, -6, -10), цитокинов из макрофагов была исследована на клеточной линии ТНР-1. Реакции на мелиттин и ЛПС, применяемые отдельно или в комбинации, характеризовались метаболическим профилированием, а результаты метаболизма использовались для оценки потенциала мелиттина в качестве иммунной адъювантной терапии. Добавление мелиттина усиливало выделение воспалительных цитокинов, индуцированных ЛПС. Уровни полярных и неполярных метаболитов были значительно изменены (p<0,05) после активации клеток комбинацией ЛПС и мелиттина по сравнению с необработанными контрольными клетками. В целом результаты этого исследования показали, что мелиттин может иметь потенциальное применение в качестве адъюванта вакцины [15].
Неоднократно были предприняты попытки создания лекарственных форм аллергенов для лечения ИА у больных с аллергией к яду пчел. В патенте RU 2279888 С1 [16] указана следующая информация: аллергоид для аллерген-специфической иммунотерапии больных с аллергическими реакциями на ужаления пчелами, характеризующийся тем, что он содержит аллергенные фракции с молекулярной массой 3–12, 16–31, 38–46, а также 20 и 60 кДа и полученный путем полимеризации суммарно аллергенной фракции формальдегидом и стабилизации NaBH4. Данный патент предусматривает использование мелиттина (3 кДа) в противоаллергическом препарате. В другом патенте, RU 2010 130 532 A [17], указано, что созданный препарат был получен путем диализа нативного пчелиного яда с использованием мембраны с границей пропускания 10 кДа. Первичные аминогруппы белковых частей мелиттин-истощенного пчелиного яда подвергали карбамилированию или тиокарбамилированию либо образованию групп гуанидинового типа для получения мономерного аллергоида. Данный патент в отличие от предыдущего патента не предусматривал использование мелиттина в противоаллергическом препарате.
Таким образом, существует необходимость в проведении исследований, позволяющих подтвердить или опровергнуть возможность использования мелиттина в противоаллергических препаратах.
Как правило, для работы используют мелиттин из пчелиного яда фирмы Sigma (США), отличающегося высокой стоимостью. Интерес представляет изучение токсических и аллергенных свойств мелиттина из отечественного яда пчелиного сырца (ЯПС).
Цель настоящей работы — изучение токсических и аллергенных свойств мелиттина пчелиного яда отечественного производителя.
Материал и методы
Работа выполнена на базе лаборатории молекулярных механизмов аллергии ФГБУ «ГНЦ Институт иммунологии» ФМБА России.
Исследуемые вещества: мелиттин из пчелиного яда фирмы Sigma (США) — белый порошок без запаха, а также мелиттин, полученный из ЯПС ООО «Апис», — белый порошок без запаха. Контрольное вещество — фосфатно-солевой буферный раствор, рН от 7,2 до 7,4, фирмы Sigma.
Для изучения токсических свойств мелиттина использованы лабораторные животные (самцы, каждый вид — по 90 голов): беспородные мыши массой 20–22 г, мыши линии Balb/c массой 20–22 г, крысы линии Wistar массой 180–200 г, морские свинки массой 250–300 г.
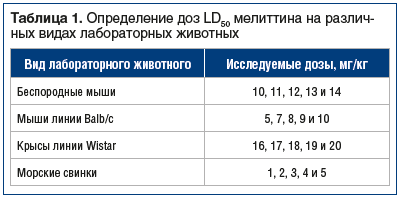
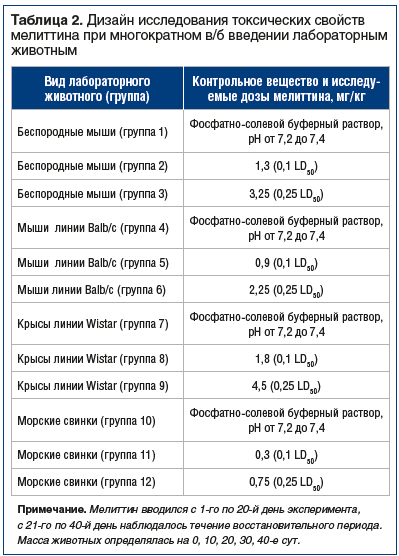
Дизайн исследования токсических свойств мелиттина при однократном внутрибрюшинном (в/б) введении лабораторным животным представлен в таблицах 1, 2. Количество животных на каждую дозу мелиттина составляло 10 голов [18]. При определении токсичности учитывался показатель опасности ядовитых и умеренно-токсичных веществ, а именно LD50 — средняя доза вещества, вызывающая гибель половины животных исследуемой группы.
Аллергенные свойства мелиттина изучались с применением исследуемого пептида, полученного из ЯПС ООО «Апис». В качестве контроля использовались: адъювант гидроксид алюминия (Sigma, США), в качестве сравнения — очищенный ЯПС ООО «Апис» (Россия), белый кристаллический порошок без запаха [43].
Лабораторные животные: мыши самцы линии Balb/c
массой 20–22 г (90 голов), морские свинки самцы массой 250–300 г (90 голов).
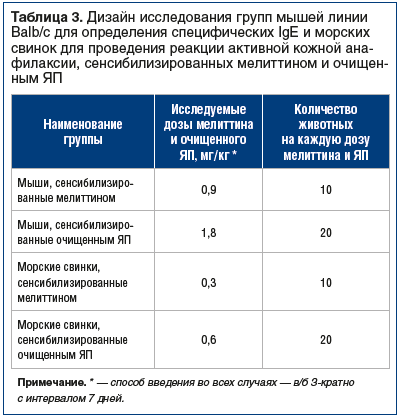
Дизайн исследования аллергенных свойств мелиттина при 3-кратном введении исследуемого вещества лабораторным животным представлен в таблице 3.
Статистический анализ данных проводился с использованием программы Statistica (version 8.0, StaSoft Inc., США). Все данные были выражены как среднее значение ± ошибка среднего. Статистическая значимость была оценена при помощи t-критерия Стьюдента, различия считались значимыми при p≤0,05.
Результаты исследования
Изучение токсических свойств мелиттина
Проведено исследование токсических свойств мелиттина при однократном в/б введении беспородным мышам самцам и мышам самцам линии Balb/c. LD50 для беспородных мышей составила 13 мг/кг, для мышей линии Balb/c — 9 мг/кг при введении как мелиттина зарубежного производства, так и мелиттина из ЯПС. Полученные данные демонстрируют тождественность токсического эффекта мелиттина отечественного и зарубежного производства. Поэтому дальнейшие исследования токсических свойств мелиттина проводили, не используя дорогостоящий мелиттин производства США.
При проведении исследования токсических свойств мелиттина из ЯПС ООО «Апис» при однократном в/б введении крысам линии Wistar и морским свинкам отмечено, что LD50 составила 18 мг/кг и 3 мг/кг соответственно.
Также было проведено исследование токсических свойств мелиттина из ЯПС при многократном в/б введении беспородным мышам в следующих дозах: 1,3 мг/кг (0,1 LD50) и 3,25 мг/кг (0,25 LD50), по 10 мышей на каждую дозу, и мышам линии Balb/c 0,9 мг/кг (0,1 LD50) и 2,25 мг/кг (0,25 LD50), по 10 мышей на каждую дозу. Продолжительность введения составила 20 дней с последующим 20-дневным периодом наблюдения.
Во время курса введения мелиттина и восстановительного периода проводили определение массы животных на 0, 10, 20, 30, 40-й день. Масса тела (г) мышей в контрольной группе (группа 1): до введения растворителя — 21,4±1,6; 10-й день курса введения — 23,6±1,8; 20-й день курса введения — 25,8±1,5; 30-й день после курса введения — 27,2±1,4; 40-й день после курса введения — 29,5±1,7. Масса тела (г) мышей в экспериментальной группе (группа 2): до введения мелиттина в дозе 1,3 мг/кг — 21,2±1,5; 10-й день курса введения — 23,3±1,1; 20-й день курса введения — 24,5±1,6; 30-й день после курса введения — 25,8±1,3; 40-й день после курса введения — 26,9±1,5. Масса тела (г) мышей в экспериментальной группе (группа 3): до введения мелиттина в дозе 3,25 мг/кг — 20,6±1,7; 10-й день курса введения — 21,9±1,2; 20-й день курса введения — 21,8±1,5; 30-й день после курса введения — 23,7±1,3; 40-й день после курса введения — 24,8±1,4.
Результатами дальнейшего исследования было определение массы тела у мышей линии Balb/c в период курса введения мелиттина и в восстановительном периоде. Масса тела (г) мышей в контрольной группе (группа 4): до введения растворителя — 21,3±1,4; 10-й день курса введения — 23,4±1,7; 20-й день курса введения — 25,2±1,5; 30-й день после курса введения — 27,1±1,3; 40-й день после курса введения — 29,3±1,6. Масса тела (г) мышей в экспериментальной группе (группа 5): до введения мелиттина в дозе 0,9 мг/кг — 20,8±1,3; 10-й день курса введения — 23,1±1,5; 20-й день курса введения — 24,7±1,6; 30-й день после курса введения — 25,6±1,7; 40-й день после курса введения — 26,7±1,4. Масса тела (г) мышей в экспериментальной группе (группа 6): до введения мелиттина в дозе 2,25 мг/кг — 21,5±1,2; 10-й день курса введения — 22,7±1,8; 20-й день курса введения — 21,4±1,3; 30-й день после курса введения — 22,6±1,3; 40-й день после курса введения — 23,5±1,1. Полученные результаты представлены на рисунке 1.
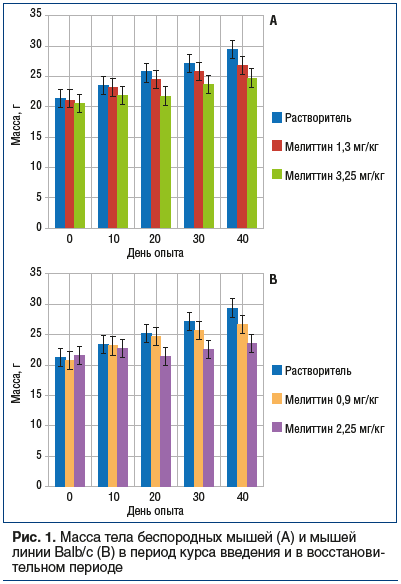
Проведено также исследование токсических свойств мелиттина при многократном в/б введении крысам линии Wistar в следующих дозах: 1,8 мг/кг (0,1 LD50) и 4,5 мг/кг (0,25 LD50), по 10 крыс на каждую дозу, и морским свинкам в следующих дозах: 0,3 мг/кг (0,1 LD50) и 0,75 мг/кг (0,25 LD50), по 10 морских свинок на каждую дозу. Продолжительность введения также составила 20 дней с последующим 20-дневным периодом наблюдения. Определение массы животных осуществлялось на 0, 10, 20, 30, 40-й день эксперимента. Масса тела (г) крыс в контрольной группе (группа 7): до введения растворителя — 192,5±7,6; 10-й день курса введения — 205,2±9,2; 20-й день курса введения — 219,8±9,7; 30-й день после курса введения — 232,8±10,6; 40-й день после курса введения — 246,2±11,3. Масса тела (г) крыс в экспериментальной группе (группа 8): до введения мелиттина в дозе 1,8 мг/кг —195,7±8,4; 10-й день курса введения — 207,1±7,9; 20-й день курса введения — 217,6±8,9; 30-й день после курса введения — 229,4±10,3; 40-й день после курса введения — 242,3±10,7. Масса тела (г) крыс в экспериментальной группе (группа 9): до введения мелиттина в дозе 4,5 мг/кг — 193,4± 8,3; 10-й день курса введения — 202,8±7,5; 20-й день курса введения — 211,5±8,6; 30-й день после курса введения — 223,9±9,4; 40-й день после курса введения — 235,6±10,3.
Масса тела (г) морских свинок в контрольной группе (группа 10): до введения растворителя — 273,4±10,2; 10-й день курса введения — 287,5±11,6; 20-й день курса введения — 302,7±10,8; 30-й день после курса введения — 317,4±11,9; 40-й день после курса введения — 329,8±12,3. Масса тела (г) морских свинок в экспериментальной группе (группа 11): до введения мелиттина в дозе 0,3 мг/кг — 276,3±10,7; 10-й день курса введения — 284,8±11,2; 20-й день курса введения — 294,5±11,2; 30-й день после курса введения — 305,3±11,7; 40-й день после курса введения — 315,6±12,6. Масса тела (г) морских свинок в экспериментальной группе (группа 12): до введения мелиттина в дозе 0,75 мг/кг — 269,8±10,5; 10-й день курса введения — 282,1±10,3; 20-й день курса введения — 288,1±11,2; 30-й день после курса введения — 295,5±11,6; 40-й день после курса введения — 305,4±11,4. Полученные результаты представлены на рисунке 2.
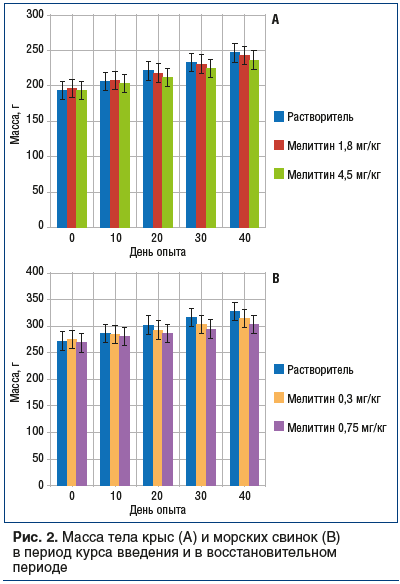
Таким образом, полученные результаты свидетельствуют, что наиболее стойкими к действию мелиттина являются крысы — доза LD50 мелиттина составила 18 мг/кг,
а наиболее чувствительными — мыши линии Balb/c — 9 мг/кг и морские свинки — 3 мг/кг. Отмечено также, что динамика увеличения массы тела в восстановительном
периоде (21–40-й дни опыта) у крыс идет с бо′льшим приростом массы, чем у морских свинок, а также то, что мелиттин в дозе 0,25 LD50 оказывает в 2 раза большее токсическое действие, чем в дозе 0,1 LD50.
Таким образом, найдена модель экспериментальных животных, наиболее чувствительных к токсическим свойствам мелиттина, а показанная в работе тождественность токсической активности мелиттина из ЯПС и яда зарубежного производства позволила в дальнейшей работе по изучению аллергенных свойств мелиттина использовать изучаемый пептид из ЯП отечественного производителя.
Изучение аллергенных свойств мелиттина
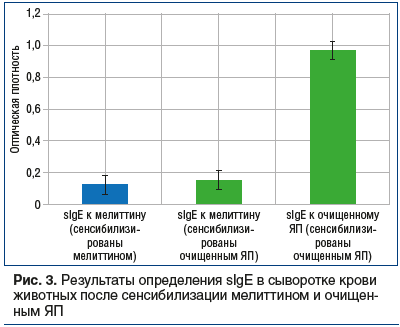
Определение специфических IgE (sIgE) в сыворотке крови животных после сенсибилизации мелиттином и очищенным ЯП. Проведено исследование аллергенных свойств мелиттина из ЯП при 3-кратном в/б введении мышам линии Balb/с с адъювантом (гидроксидом алюминия) в дозе 0,9 мг/кг на 1 животное и очищенного ЯП с адъювантом в дозе 1,8 мг/кг на 1 животное, 3-кратно с интервалом 7 дней. На 21-й день от начала сенсибилизации проводили методом иммуноферментного анализа определение уровней sIgE в сыворотке крови животных с использованием набора Mouse IgE ELISA Set (Becton Dickinson, США) по уровню оптической плотности (optical density — OD): уровень sIgE к мелиттину у мышей, сенсибилизированных мелиттином, составил 0,118±0,016 OD; уровень sIgE к мелиттину у мышей, сенсибилизированных ЯП, — 0,146±0,014 OD (р<0,05); уровень sIgE к ЯП у мышей, сенсибилизированных ЯП, — 0,963±0,047 OD.
Результаты представлены на рисунке 3. Уровень sIgE к мелиттину был незначительно выше у мышей после сенсибилизации ЯП в сравнении с уровнем sIgE у мышей, сенсибилизированных одним мелиттином. Для сравнения проведенной сенсибилизации к ЯП определяли уровень sIgE к очищенному ЯП.
Проведено исследование аллергенных свойств мелиттина при в/б введении морским свинкам с адъювантом (гидроксидом алюминия) в дозе 0,3 мг/кг на 1 животное и очищенного ЯП с адъювантом в дозе 0,6 мг/кг на 1 животное, 3-кратно с интервалом 7 дней. На 21-й день от начала сенсибилизации проводили постановку реакции активной кожной анафилаксии (АКА). Результаты исследования по определению уровней гомоцитотропных специфических антител, определяемых по вычислению среднего диаметра окрашенных красителем синим Эванса пятен (см × см) после в/к введения различных доз мелиттина, представлены в таблице 4.

Значения средних диаметров окрашенных пятен у морских свинок, сенсибилизированных мелиттином, после в/к введения мелиттина были незначительно меньше, чем у морских свинок, сенсибилизированных ЯП, после разрешения реакции АКА мелиттином.
Проведено также исследование сыворотки крови 16 пациентов с аллергией к ЯП по определению уровней sIgE к ЯП и мелиттину, определяемых по оптической плотности, с использованием набора фирмы Dr. Fooke (Германия). Получены следующие результаты: у 5 пациентов уровень sIgE к ЯП составил 0,765±0,058 OD (3 класс), уровень sIgE к мелиттину — 0,169±0,037 OD (1 класс), уровни sIgE к ПЯ и мелиттину в сыворотке крови 11 пациентов составили 0,236±0,043 OD (2 класс) и 0,078±0,026 OD (0 класс) соответственно. Результаты представлены на рисунке 4.
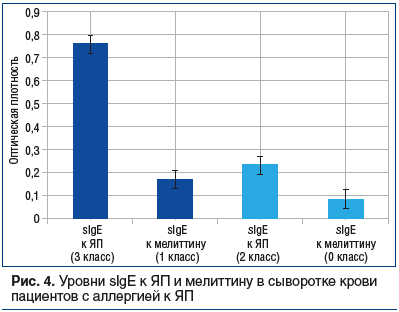
Проведенные исследования свидетельствуют о слабых аллергенных свойствах мелиттина по сравнению с ЯП.
Заключение
Таким образом, изученные показатели динамики увеличения массы тела различных животных в восстановительном периоде при воздействии различных доз мелиттина, выраженное токсическое воздействие 0,25 LD50 в сравнении с дозой 0,1 LD50, а также низкий уровень содержания специфических IgE в крови животных, сенсибилизированных мелиттином, в сравнении с уровнем исследуемых антител при сенсибилизации ЯП, небольшие значения средних диаметров окрашенных пятен у морских свинок, сенсибилизированных мелиттином, после в/к введения указанного белка, наличие низкого уровня специфических IgE в крови пациентов с инсектной аллергией к яду пчел свидетельствуют о наличии у мелиттина выраженных токсических свойств, но слабых аллергенных, что указывает на нецелесообразность использования исследуемого пептида в составе противоаллергических препаратов. Наличие доказанного токсического эффекта мелиттина позволяет сделать вывод о целесообразности применения исследуемого белка с выраженными цитотоксическими свойствами в составе препаратов для лечения онкопатологии, заболеваний опорно-двигательного аппарата, а также препаратов с антибактериальной направленностью.
.
Информация с rmj.ru