Содержание статьи
Введение
Акромегалия — тяжелое нейроэндокринное заболевание, обусловленное гиперпродукцией гормона роста — соматотропного гормона (СТГ) у лиц с законченным физиологическим ростом и характеризующееся патологическим диспропорциональным периостальным ростом костей, хрящей, мягких тканей, внутренних органов, а также нарушением функционального состояния сердечно-сосудистой, легочной системы, периферических эндокринных желез, различных видов метаболизма [1–4].
Точные данные о распространенности акромегалии установить сложно, т. к. от момента проявления первых признаков заболевания до установки точного диагноза в среднем проходит 5–15 лет. Средний возраст на момент диагностики акромегалии составляет 40–50 лет.
На 1 млн населения приходится от 50 до 70 случаев заболевания акромегалией. Ежегодно фиксируется 3–4 повторных случая [3, 9].
В 95% случаев первичная избыточная секреция гормона роста обусловлена аденомой гипофиза. Очень редко (~2%) гиперфункция гормона роста может быть вызвана СТГ-секретирующей опухолью внегипофизарной локализации. Менее чем в 3% всех случаев акромегалия возникает вследствие повышенной секреции соматолиберина, которая приводит к гиперплазии соматотрофов и формированию аденомы гипофиза. Причина развития СТГ-продуцирующих аденом гипофиза пока не известна.
Диагностика
Диагностика акромегалии на первый взгляд не очень сложна, учитывая характерные изменения внешности больного, но вследствие медленного развития физикальных изменений заболевание в течение многих лет остается нераспознанным.
Увеличение конечностей и головные боли являются самыми распространенными жалобами, которые позволяют поставить диагноз. С учетом многоликости клинической картины диагноз может быть заподозрен различными специалистами: эндокринологами, терапевтами, неврологами, гинекологами, травматологами и т. д.
Гормональное исследование
Для диагностики акромегалии исследуются уровни СТГ и инсулиноподобного ростового фактора 1 (ИРФ-1). Более надежным показателем по сравнению с СТГ является ИРФ-1, т. к. он в меньшей степени подвергается циркадным изменениям благодаря более длительному периоду полужизни [5, 6]. Исследование ИРФ-1 можно проводить в любое время суток (натощак — необязательно). ИРФ-1 является надежным маркером для диагностики, мониторинга и скрининга акромегалии [3–5].
Ложное повышение уровня ИРФ-1 возможно при беременности, системных заболеваниях, состояниях, сопровождающихся повышенным катаболизмом (ВИЧ-инфекция, СПИД, обширные хирургические вмешательства), печеночной и почечной недостаточности, голодании, сахарном диабете. Кроме того, применение оральных эстрогенов подавляет секрецию СТГ и может вызвать снижение уровня ИРФ-1 у пациентов с акромегалией при исходно незначительном его повышении [3, 8].
Для исследования гормональных показателей в динамике рекомендуется пользоваться одной и той же лабораторной методикой, т. к. возможны расхождения показателей между различными лабораториями.
При подтвержденном высоком уровне ИРФ-1 и характерной клинической картине с целью диагностики акромегалии дополнительное исследование СТГ в ходе орального глюкозотолерантного теста (ОГТТ) не проводится. В случаях, когда отмечается незначительное повышение уровня ИРФ-1 и клиническая картина заболевания не ярко выражена, проводится дополнительное исследование уровня СТГ в ходе ОГТТ: 75 г сухой взвеси глюкозы на 200 мл воды per os с последующим исследованием уровня СТГ каждые 30 мин в течение 2 ч. Диагноз акромегалии исключается при СТГ надир в ходе ОГТТ <1 нг/мл либо при использовании высокочувствительных наборов <0,4 нг/мл в любой из 5 точек, кроме базальной [3–6].
При наличии у пациента сахарного диабета возможно исследование среднего уровня СТГ за сутки (норма <2,5 нг/мл) [3–5].
При верификации у пациента акромегалии и опухоли гипофиза необходимо проведение ряда дополнительных лабораторных исследований: 1) исследование пролактина (ПРЛ) (для выявления возможно смешанной СТГ/ПРЛ секретирующей аденомы гипофиза); 2) исследование других тропных гормонов гипофиза для исключения гипопитуитаризма при наличии макроаденомы гипофиза [3–5].
Инструментальное обследование
С целью визуализации аденомы гипофиза необходимо проведение магнитно-резонансной томографии (МРТ) головного мозга (при необходимости с контрастным усилением), при противопоказаниях к проведению МРТ (наличие кардиостимулятора, металлических имплантатов) возможно проведение компьютерной томографии головного мозга.
При наличии макроаденомы гипофиза с супраселлярным ростом и симптоматики компрессии хиазмы необходимо проведение периметрии.
Лечение
Цели лечения акромегалии [3, 5–7]:
Нормализация гормональных показателей (базальный уровень СТГ ≤2,5 нг/мл — при терапии аналогами соматостатина длительного действия, минимальный уровень СТГ в ходе ОГТТ <1 нг/мл — после хирургического лечения и нормализация ИРФ-1 соответственно возрасту и полу).
Уменьшение объема опухоли.
Контроль за развившимися осложнениями и устранение обратимых симптомов заболевания.
Снижение риска преждевременной смертности.
Методы лечения
Транссфеноидальная аденомэктомия — первая линия терапии при интраселлярных микроаденомах и неинвазивных макроаденомах, а также в случае компрессии хиазмы зрительных нервов.
При наличии у пациента макроаденомы гипофиза с экстраселлярным ростом возможно проведение аденомэктомии с целью уменьшения объема опухоли для возможного улучшения ответа на медикаментозную или лучевую терапию.
Медикаментозная терапия включает несколько классов препаратов.
Аналоги соматостатина длительного действия — препараты первой линии в качестве медикаментозной терапии акромегалии [1–6]. Наиболее часто аналоги соматостатина назначаются в качестве дополнительной терапии при отсутствии биохимического контроля над акромегалией после хирургического лечения. Также возможно назначение данных препаратов в качестве первичной терапии пациентам с макроаденомой гипофиза и заведомо низкой вероятностью радикальной аденомэктомии либо при наличии противопоказаний к проведению хирургического вмешательства [3–7].
Еще одним показанием к назначению аналогов соматостатина является период до наступления максимального эффекта после проведения лучевой терапии [3–7].
Из побочных эффектов возможны симптомы со стороны желудочно-кишечного тракта (метеоризм, диарея, реже запоры), образование взвеси/камней желчного пузыря, выпадение волос; симптомы, как правило, выражены незначительно и не требуют отмены препарата.
Антагонисты рецепторов СТГ. К данной группе препаратов относится пэгвисомант — генно-инженерный аналог эндогенного гормона роста с 9 мутациями, антагонист рецепторов гормона роста. Применяется в дозе 10–30 мг. Для оценки эффективности используют только определение уровня ИРФ-1. Одним из важных эффектов пэгвисоманта является его способность к коррекции различных метаболических нарушений, которые становятся основной причиной инвалидизации и повышенной смертности у данных больных.
Агонисты дофамина представлены двумя препаратами: каберголином и бромокриптином. Каберголин — селективный агонист D2-дофаминовых рецепторов, более эффективен, чем бромокриптин. Возможно назначение каберголина в качестве вспомогательной терапии при неэффективности аналогов соматостатина. Четкая взаимосвязь эффективности агонистов дофамина при акромегалии с наличием либо отсутствием сопутствующей гиперпролактинемии отсутствует [3–7].
Лучевая терапия в настоящее время представлена стереотаксической радиохирургией (гамма-нож, кибернож). Сроки наступления ремиссии при применении стереотаксической радиохирургии — от 2 до 7 лет. Главное отличие стереотаксической хирургии от других методов лучевой терапии — возможность направить однократно очень большую дозу узким фокусированным пучком на четко ограниченную зону, что значительно уменьшает число осложнений и повышает эффективность данного вида облучения [3].
Лучевая терапия в качестве первичного метода может применяться в случае невозможности проведения аденомэктомии и медикаментозной терапии. Как дополнительный метод терапии может применяться при нерадикально проведенной аденомэктомии (особенно в сочетании с неблагоприятной гистологической картиной: большим количеством митозов, высоким индексом Ki-67, клеточной атипией). Противопоказанием к проведению лучевой терапии является близкое расположение аденомы гипофиза (менее 5 мм) к хиазме зрительных нервов, т. к. после терапии развивается отек, способный привести к сдавлению перекреста зрительных нервов.
Выбор тактики лечения каждого конкретного пациента зависит от множества факторов. Чаще всего цели лечения можно достичь лишь при комбинации всех вышеперечисленных методов терапии, особенно при наличии у пациента макроаденомы гипофиза с распространением ее за пределы турецкого седла, а также клинически значимых осложнений и сопутствующих заболеваний.
Клиническое наблюдение
Пациентка К., 78 лет, обратилась в клинику с жалобами на общую слабость, выраженную утомляемость, отсутствие аппетита, тошноту по утрам, сухость во рту, жажду, учащенное мочеиспускание, наличие «мешков» под глазами, снижение массы тела на 12 кг за 3 мес.
Анамнез заболевания: изменение внешности по акромегалоидному типу в виде укрупнения черт лица, увеличения кистей рук, стоп впервые отметила в 1975 г. В поликлинику по месту жительства впервые обратилась в 1994 г. Из доступных на тот момент методов диагностики ей была проведена краниография, выявлено значительное увеличение размеров турецкого седла, остеопороз спинки и двухконтурность дна турецкого седла. Была направлена на обследование к эндокринологу, но обратилась к нему по ряду причин к только в 1997 г. Проведено обследование: СТГ базальный — 9,5 нг/мл (норма — до 2,5), уровень ИРФ-1 не исследовался. МРТ гипофиза: эндо-супраселлярная аденома 12×12×12 мм, V=0,8 см3. Эндокринологом был назначен бромокриптин 2,5 мг по 1 таблетке 3 р/сут, принимала нерегулярно, на контрольное обследование не пришла.
Объективно: в 2012 г. обратилась в консультативно-диагностический отдел ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, где ей было проведено обследование: ИРФ-1–437 нг/мл (норма — 118–314 нг/мл), СТГ в ходе ОГТТ — 9,6–9,9–10,5–10,1–9,9 нг/мл, пролактин — 127 мЕд/л (норма — 90–540 мЕд/л), адренокортикотропный гормон — 2,5 пмоль/л (норма — 1,5–11 пмоль/л), кортизол крови — 155 нмоль/л (норма — 190–650), тиреотропный гормон — 0,1 мкЕд/мл (норма — 0,2–4,0 мкЕд/мл), свободный Т4–5,5 пмоль/л (норма — 11–22 пмоль/л), лютеинизирующий гормон — 4,3 Ед/л (норма — <20 Ед/л), фолликулостимулирующий гормон — 3,7 Ед/л (норма — >20 Ед/л), кортизол свободный суточной мочи исследовался дважды: 100 нмоль/л, 80 нмоль/л (норма — 120–400 нмоль/л).
Также была выполнена МРТ гипофиза, выявлена отрицательная динамика по сравнению с 1997 г., размеры опухоли увеличились до 18×24×14 мм, V=2,9 см3 (рис. 1).
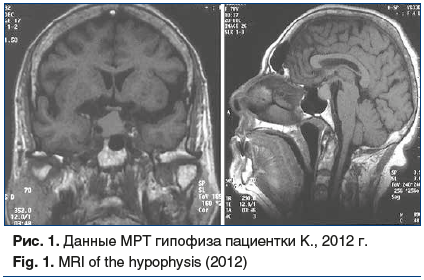
Проведены дополнительные обследования для выявления возможных осложнений:
Периметрия: нарушения полей зрения нет.
УЗИ щитовидной железы: патологии не выявлено.
ЭКГ: ритм синусовый, частота сердечных сокращений — 88/мин, горизонтальное положение электрической оси сердца, недостаточность кровоснабжения миокарда — верхушечно-боковой области на фоне диффузных изменений миокарда.
ЭХО-кардиография: фракция выброса — 62%, гипертрофия миокарда левого желудочка, диастолическая дисфункция по I типу.
УЗИ молочных желез: киста левой молочной железы малых размеров.
Денситометрия: в поясничном отделе позвоночника — остеопения, в шейке левой бедренной кости — норма.
Консультирована кардиологом. Заключение: Гипертоническая болезнь 2-й степени, очень высокого риска. Ишемическая болезнь сердца. Стенокардия напряжения
II функционального класса (ФК). Хроническая сердечная недостаточность II–III ФК по NYHA. Распространенный атеросклероз с преимущественным поражением аорты, коронарных сосудов и сосудов головного мозга. Хирургическое лечение является нежелательным методом терапии ввиду высоких рисков.
На основании проведенных обследований установлен окончательный диагноз: Акромегалия, активная фаза. Эндо-супра-параселлярная макроаденома гипофиза (соматотропинома). Пангипопитуитаризм: вторичная надпочечниковая недостаточность, вторичный гипотиреоз, вторичный гипогонадизм. Гипертоническая болезнь 2-й степени, очень высокого риска. Ишемическая болезнь сердца. Стенокардия напряжения II ФК. Хроническая сердечная недостаточность II–III ФК по NYHA. Распространенный атеросклероз с преимущественным поражением аорты, коронарных сосудов и сосудов головного мозга.
Лечение. С учетом возраста больной и наличия у нее сердечно-сосудистой патологии, из-за чего хирургическое лечение было бы сопряжено с высокими рисками осложнений, пациентке был назначен аналог соматостатина длительного действия Октреотид-депо в максимальной дозировке 40 мг 1 раз в 28 дней, с последующим мониторингом уровня СТГ и ИРФ-1 каждые 3 мес. на фоне терапии. Через 3 мес. на фоне терапии Октреотидом-депо отмечалась нормализация уровня СТГ и ИРФ-1 соответственно возрасту и полу, в дальнейшем эффективность сохранялась на протяжении 12 мес. лечения. Также была назначена заместительная терапия вторичного гипотиреоза (левотироксин натрия 25 мкг утром натощак 10 дней, с последующей коррекцией дозы до 50 мкг) и вторичной надпочечниковой недостаточности (гидрокортизон 10 мг утром, 10 мг днем, 5 мг вечером, с контролем общего самочувствия).
Через 12 мес. терапии Октреотидом-депо проведена контрольная МРТ гипофиза, отмечалась выраженная положительная динамика размеров опухоли: 8×11×10 мм, V=0,4 см3 (рис. 2).
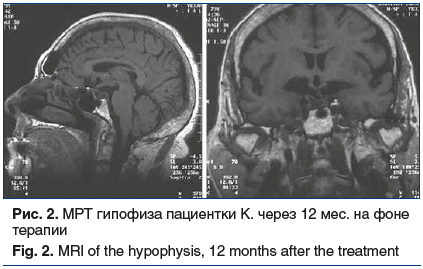
В дальнейшем пациентка продолжила терапию Октреотидом-депо в дозе 40 мг 1 раз в 28 дней, на протяжении всего времени терапии у нее сохранялась полная клинико-биохимическая ремиссия и контроль над опухолью. От предложенного ей радиохирургического лечения пациентка воздержалась, что также обусловлено ее возрастом.
Заключение
Целью лечения акромегалии являются устранение гиперпродукции СТГ опухолью гипофиза, нормализация уровня ИРФ-1 в крови и отсутствие отрицательной динамики со стороны аденомы гипофиза, а в идеале — уменьшение ее размеров. Несмотря на то, что первой линией терапии акромегалии в настоящий момент остается хирургическое лечение, существенно изменившаяся за последние годы консервативная терапия позволяет успешно достигать цели лечения у пациентов, которым по той или иной причине противопоказано хирургическое вмешательство. Например, у пожилых пациентов, лиц с наличием сопутствующей патологии применение Октреотида-депо поддерживает уровни СТГ и ИРФ-1 в пределах целевых значений соответственно возрасту и полу, что в свою очередь позволяет контролировать прогрессирование осложнений, связанных с акромегалией, а также достигнуть редукции опухоли.
Благодарность
Редакция благодарит компанию ООО «Фарм-Синтез» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgement
Editorial Board is grateful to LLC «Pharm-Sintez» for the assistance in technical edition of this publication.
Сведения об авторе:
Покрамович Юлия Геннадьевна — научный сотрудник отделения терапевтической эндокринологии отдела терапии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского; 129110, Россия, г. Москва, ул. Щепкина, д. 61/2; ORCID iD 0000-0001-5289-8973.
Контактная информация: Покрамович Юлия Геннадьевна, e-mail: pokramovich_81@mail.ru. Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 05.08.2020, поступила после рецензирования 18.08.2020, принята в печать 13.09.2020.
About the author:
Yuliya G. Pokramovich — researcher of the Department of Therapeutic Endocrinology od the Division of Therapy, M.F. Vladimirskiy Moscow Regional Research and Clinical Institute, 61/2, Shchepkin str., Moscow, 129110, Russian Federation; ORCID iD 0000-0001-5289-8973.
Contact information: Yuliya G. Pokramovich, e-mail: pokramovich_81@mail.ru. Financial Disclosure: author has no a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 05.08.2020, revised 18.08.2020, accepted 13.09.2020.
.
Информация с rmj.ru





