Дигидрокверцетин в комплексном лечении ожирения у детей
Т. В. Строкова, доктор медицинских наук
Е. В. Павловская, кандидат медицинских наук
А. Г. Сурков, кандидат медицинских наук
Е. Н. Кутырева
А. В. Будаковская
Г. Ю. Мальцев, кандидат медицинских наук
ФГБУ НИИ питания РАМН, Москва
Интерес к биологическому действию дигидрокверцетина (ДКВ) и созданию препаратов на его основе обусловлен широким спектром его фармакологического действия и доказанной безопасностью при длительном применении. Впервые ДКВ был выделен в 1948 году [1]. В качестве сырьевого источника используют измельченную древесину лиственницы сибирской, содержащей до 3,5% флавоноидов. В экспериментальных исследованиях in vitro и in vivo подтверждены антиоксидантное, противовоспалительное, гепатопротекторное, ангиопротекторное, антиагрегантное, гиполипидемическое, антиаритмическое, гипотензивное, противоишемическое действия ДКВ [1–3]. Разработана и с 2000 года зарегистрирована на российском фармацевтическом рынке биологически активная добавка (БАД) к пище Капилар (10 мг дигидрокверцетина в 1 таблетке).
К настоящему времени эффективность ДКВ также подтверждена в ряде клинических исследований, в которых БАД Капилар или препарат Диквертин включали в схему стандартной терапии больных со стенокардией напряжения [2, 4, 5], в раннем постинфарктном периоде [6], больных с постинфарктным кардиосклерозом [7], больных, перенесших реконструктивные операции на коронарных сосудах [8], больных гипертонической болезнью и нейроциркуляторной дистонией гипертонического типа [9, 10], больных хроническими облитерирующими заболеваниями артерий нижних конечностей [11], больных хронической обструктивной болезнью легких [12], острой пневмонией [13], больных сахарным диабетом 2-го типа [14, 15].
Показано, что включение ДКВ в схемы стандартной терапии различных заболеваний приводило к достоверному улучшению показателей функций внешнего дыхания, центральной и периферической гемодинамики, оксигенации крови, улучшению микроциркуляции, к повышению толерантности к физической нагрузке, улучшению психоэмоционального состояния больных и повышению терапевтического и реабилитационного эффектов лечения, улучшению отдаленных результатов. Позитивное влияние ДКВ на микроциркуляцию выражалось в улучшении реологических свойств крови и усилении активных вазомоторных механизмов регуляции микроциркуляции. Также отмечалось положительное влияние препарата на неврологическое состояние пациентов, что проявлялось в достоверном уменьшении частоты возникновения головной боли, симптома «шума в голове» и частоты случаев нарушений координации движений.
В нашем исследовании мы использовали ДКВ при лечении ожирения. Во всех странах мира отмечается рост числа детей и подростков, страдающих ожирением [16]. Увеличение распространенности данного заболевания сопровождается изменением структуры заболеваемости в детском возрасте и нарастанием числа подростков с метаболическим синдромом, артериальной гипертензией, неалкогольной жировой болезнью печени и сахарным диабетом 2-го типа, что в дальнейшем приводит к повышению заболеваемости и риска смерти у молодых взрослых [17, 18].
В развитии вышеперечисленных осложнений ожирения важную роль играет окислительный стресс [19, 20]. Этот процесс сопровождается увеличением уровня свободных радикалов, активацией перекисного окисления липидов, нарушением обмена белков и нуклеиновых кислот, подавлением гликолиза, ингибированием активности ряда ферментов (глюкозо-6-фосфатазы, аденилатциклазы и др.), что приводит к нарушению функции многих тканей [21]. Повышение образования свободных радикалов сопровождается нарушениями работы антиоксидантных ферментов организма, таких как глутатион, супероксиддисмутаза, каталаза, глутатионпероксидаза.
Основной целью лечения детей с ожирением является постепенное снижение массы тела, приводящее к снижению риска развития сахарного диабета и кардиоваскулярных заболеваний [22]. Для профилактики осложнений, наряду с редукцией массы тела, существенное значение придается терапии ассоциированных расстройств, таких как нарушение толерантности к углеводам, дислипидемия, инсулинорезистентность, артериальная гипертензия и др. Для снижения риска метаболических осложнений необходимо также проведение комплекса терапевтических мероприятий, направленных на коррекцию окислительного стресса у этого контингента больных. Одним из диетологических подходов к повышению антиоксидантной защиты организма является включение в стандартную диетотерапию источников биологически активных веществ растительного происхождения, обладающих антиоксидантным действием (флавоноидов) [23].
Нами проведено исследование эффективности назначения БАД Капилар в комплексной терапии у детей с ожирением. Под нашим наблюдением находились 50 пациентов с ожирением в возрасте от 10 до 17 лет 11 мес (в среднем 13,03 ± 0,3 года), из них: мальчиков — 17, девочек — 33. По принципу случайной выборки все пациенты были разделены на две группы. Основную группу составили 35 пациентов в возрасте 13,2 ± 0,4 года, из них мальчиков — 12 (34,3%), девочек — 23 (65,7%). В контрольную группу вошло 15 детей в возрасте 12,6 ± 0,5 года (10 девочек — 66,7% и 5 мальчиков — 33,3%). Группы достоверно не отличались по основным клинико-лабораторным показателям (табл. 1).
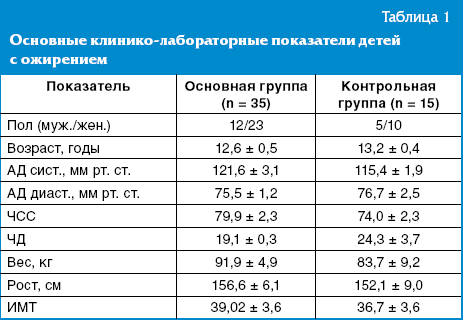
В течение 21 дня наблюдения дети обеих групп жалоб не предъявляли. Все дети получали низкокалорийную диету, пациенты основной группы получали БАД Капилар. Динамика массы тела за период госпитализации была сопоставима в обеих группах: наблюдалось снижение веса на 6,7 ± 0,4 и 6,1 ± 0,7 кг соответственно в основной и контрольной группах, что было сопоставимо потере 7,3 ± 0,2% и 7,4 ± 0,4% изначальной массы тела. Индекс массы тела (ИМТ) в 1-й группе в начале наблюдения составил 39,02 ± 3,6 (97,9 ± 0,2 перцентиля), через 21 день — 36,7 ± 3,6 (96,9 ± 0,4 перцентиля). В контрольной группе аналогичный показатель составил 31,4 ± 2,8 (96,7 ± 0,5 перцентиля) до лечения и 29,4 ± 2,9 (94,1 ± 0,8 перцентиля, р < 0,05) на момент завершения исследования. При этом отмечалось уменьшение окружности талии (с 100,8 ± 3,2 до 94,3 ± 2,8 см) и бедер (с 110,6 ± 2,2 до 104,7 ± 2,09 см) в основной группе. В контрольной также наблюдалась положительная динамика антропометрических показателей (уменьшение окружности талии с 95,1 ± 5,6 до 89,8 ± 5,7 см, окружности бедер с 103,9 ± 3,7 до 98,8 ± 3,3 см).
Все средние показатели общего и биохимического анализа крови, определяемые в начале госпитализации и через 21 день от начала терапии, оставались в пределах нормальных значений.
Проведение стандартного глюкозотолерантного теста выявило нарушение толерантности к глюкозе (НТГ) у 11 пациентов (31,4%) 1-й группы и 3 (20%) пациентов 2-й группы (табл. 2). Повторное проведение теста через 21 день показало, что нарушение толерантности к глюкозе сохранялось лишь у 6 (17,1%) пациентов 1-й группы и ни у одного ребенка 2-й группы.
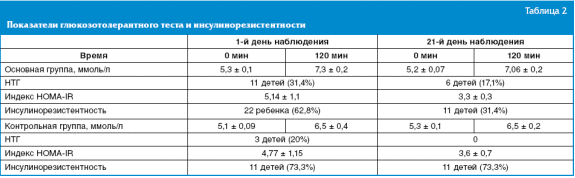
Средний показатель индекса HOMA-IR (Homeostasis Model Assessment of Insulin Resistance) до начала лечения составлял 5,14 ± 1,1 (при норме до 2,85) в основной группе и 4,77 ± 1,15 — в контрольной. При этом инсулинорезистентность была выявлена у 22 (62,8%) детей первой группы и 11 (73,3%) — второй. Через 3 недели лечения индекс HOMA-IR составил 3,3 ± 0,3 и 3,6 ± 0,7 в основной и контрольных группах соответственно. Инсулинорезистентность сохранялась у 11 (31,4%) пациентов основной группы и у всех детей второй группы.
При исследовании содержания продуктов перекисного окисления липидов — диеновых конъюгатов и малонового диальдегида в плазме крови и основных антиоксидантных ферментов эритроцитов — глутатионпероксидазы и супероксиддимутазы — единственным достоверным (р < 0,05) различием следует считать увеличение активности супероксиддисмутазы эритроцитов у больных основной группы. То же касается и вспомогательного индекса ферментной антиоксидантной защиты (АОИ ферм.) (р < 0,05). Этот эффект проявляется и на уровне общего антиоксидантного индекса (АОИ общ.) (р < 0,01). В целом в основной группе доказано достоверное антиоксидантное действие препарата, направленное на снижение окислительного стресса по индексу АОИ общ. (значения изменялись с –1,33 до –1,07 при норме = 0, р < 0,01), в то время как в группе сравнения динамики показателя не отмечалось (–0,97 и –1,00). Эти изменения были вызваны, в основном, гемопоэтической составляющей, связанной с появлением новых эритроцитов с повышенным содержанием супероксиддисмутазы (или усилением ее активности).
Исходно показатели микроциркуляции между пациентами разных групп существенно не различались. В среднем, линейная скорость кровотока (Vas) равнялась 2,73 см/с, объемная скорость кровотока (Qas) — 1,29 мл/с, индекс пульсации (Pi) составил 3,09, а индекс резистентности (Ri) — 0,39.
Уже через 7 дней приема препарата Капилар было зарегистрировано улучшение показателей микроциркуляции у большинства пациентов: скорость линейного кровотока возрастала в 1,2 раза по отношению к исходным показателям, объемная скорость кровотока — в 1,2 раза, индекс пульсации — в 1,3 раза, а индекс резистентности — в 1,2 раза. Показатели микрогемодинамики достигли своего пика на 21-й день исследования (рис. 1).
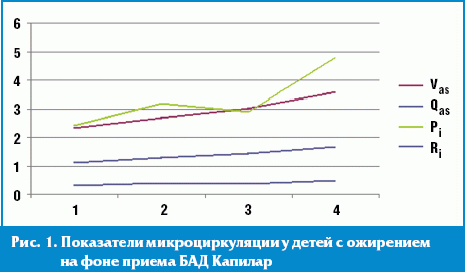
В контрольной группе, напротив, отмечалась тенденция к замедлению кровотока и снижению упруго-эластических свойств сосудов к 8-му дню исследования, которая сохранялась на протяжении всего периода наблюдения, что может быть связано с активным снижением массы тела, особенно в первые дни диетотерапии, уменьшением количества общей жидкости в организме пациентов и снижением объема циркулирующей крови (рис. 2).
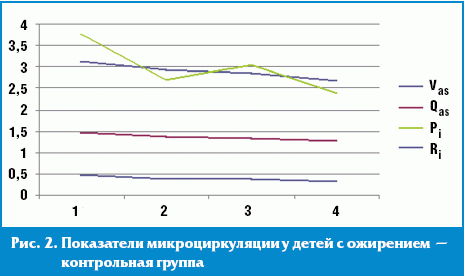
Таким образом, после приема курса дигидрокверцетина к концу исследования линейная скорость кровотока у пациентов основной группы была в 1,34 раза выше тех же параметров, зафиксированных в контрольной группе, объемная скорость кровотока — в 1,32 раза, индекс пульсации — в 2 раза, индекс резистентности — в 1,58 раза.
Обобщая полученные данные, можно утверждать, что регулярный прием БАД Капилар способствует быстрой и полной ответной реакции микроциркуляторного русла, выражающейся в увеличении скоростных и объемных показателей кровотока, а также улучшении упруго-эластических свойств сосудов микроциркуляторного русла, что сохраняется на всем протяжении исследования (21 день).
Результаты проведенного исследования показали хорошую переносимость и отсутствие побочных эффектов БАД Капилар у детей с ожирением. Ни у одного пациента не отмечено нежелательных явлений на фоне применения препарата. БАД Капилар не оказывает отрицательного влияния на показатели функционального состояния печени и желчевыделительной системы у детей с ожирением.
Таким образом, у детей с ожирением употребление в течение 21 дня БАД Капилар сопровождалось редукцией массы тела, уменьшением процентного содержания жировой ткани и антропометрических показателей (окружностей живота и бедер), сопоставимыми с показателями контрольной группы. Основные различия в группах были связаны с показателями микроциркуляции и антиоксидантного статуса. Включение БАД Капилар в состав стандартной гипокалорийной диеты приводит к нормализации антиоксидантного статуса пациентов, связано со снижением окислительного стресса, что сопровождается улучшением микроциркуляции и показателей углеводного обмена: увеличением скоростных и объемных показателей кровотока, улучшением упруго-эластических свойств сосудов микроциркуляторного русла и, в конечном итоге, уменьшением количества пациентов с нарушением толерантности к глюкозе и инсулинорезистентностью. Учитывая постоянное нарастание и пиковые значения микрогемодинамики к 21-му дню в основной группе исследования, можно заключить, что эффективность препарата прямо пропорциональна длительности приема.
Все вышеперечисленное является важным в профилактике развития таких осложнений ожирения, как артериальная гипертензия, нарушенная толерантность к глюкозе, сахарный диабет 2-го типа, метаболический синдром.
Результаты проведенного исследования, а также отсутствие побочных эффектов позволяют рекомендовать включение таблетированной формы БАД Капилар в комплексную терапию детей с ожирением в возрасте старше 10 лет.
Литература
- Плотников М. Б., Тюкавкина Н. А., Плотникова Т. М. Лекарственные препараты на основе диквертина. Издательство Томского университета. 2005. 222 с.
- Белая О. Л., Байдер Л. М., Куроптева З. В., Артамошина Н. Е. Антиоксидантные свойства биофлавоноида диквертина. Сборник материалов конгресса XVI Российский национальный конгресс «Человек и лекарство». Москва, 6–10.04.2009 г. Тезисы докладов. С. 37.
- Кубатиев А. А., Ядигарова З. Т., Рудько И. А. и др. Диквертин — эффективный ингибитор агрегации тромбоцитов // Вопр. биол., мед. и фармацевтич. химии. 1999. № 3. С. 47–50.
- Schegolkov A. M., Dergacheva L. I. The Efficiency of Biologically Active Substance CAPILAR Used in Medical Rehabilitation of Cardiosurgical Patients // International journal of immunorehabilitation. 2007. Vol. 9. № 2. P. 92–93.
- Белая О. Л., Фомина И. Г., Байдер Л. М., Куроптева З. В., Тюкавкина Н. А. Влияние биофлавоноида диквертина на антиоксидантную систему церулоплазмин/трансферритин и перекисное окисление липидов у больных стабильными формами ишемической болезни сердца с дислипидемией // Клиническая медицина. 2006. № 7. С. 46–50.
- Шакула А. В., Щегольков А. М., Климко В. В., Ярошенко В. П., Некрасов В. И., Дергачева Л. И. Применение дигидрокверцетина в комплексной медицинской реабилитации больных ишемической болезнью сердца на госпитальном и амбулаторно-поликлиническом этапах // Consilium medicum. 2008. Т. 10. № 12. С. 44–48.
- Schegolkov A. M., Dergacheva L. I. The Efficiency of Biologically Active Substance CAPILAR Used in Medical Rehabilitation of Cardiosurgical Patients // International journal of immunorehabilitation. 2007. Vol. 9. № 2. P. 92–93.
- Щегольков А. М., Белякин С. А., Шакула А. В., Климко В. В., Ярошенко В. П., Дергачева Л. И. Медицинская реабилитация больных ишемической болезнью сердца после операции аортокоронарного шунтирования с применением дигидрокверцетина // Вестник восстановительной медицины. 2007. № 3 (21). С. 93–96.
- Шакула А. В., Некрасов В. И., Щегольков А. М., Климко В. В., Ярошенко В. П., Дергачева Л. И. Применение дигидрокверцетина в комплексном лечении больных гипертонической болезнью // Врач. 2008. № 4. С. 42–46.
- Скедина М. А., Белозерова И. Н., Дергачева Л. И. Комплексное исследование динамики состояния сердечно-сосудистой системы при использовании препаратов дигидрокверцетина у больных с гипертонией // Вестник восстановительной медицины. 2008. № 6 (28). С. 32–35.
- Шакула А. В., Щегольков А. М., Климко В. В., Ярошенко В. П., Некрасов В. И., Дергачева Л. И. Комплексное лечение больных ишемической болезнью сердца в поликлинических условиях: применение дигидрокверцетина // Справочник поликлинического врача 2008. № 3. С. 36–39.
- Шакула А. В., Щегольков А. М., Будко А. А., Ярошенко В. П., Марочкина Е. И., Дергачева Л. И. Комплексная медицинская реабилитация больных хронической обструктивной болезнью легких // Врач. 2008. № 11. С. 67–71
- Теселкин Ю. О., Бабенкова И. В., Новоженов В. Г. и др. Использование нового антиоксидантного средства диквертина при лечении больных острой пневмонией // Вопр. биол., мед. и фармацевт. химии. 1999. № 1. С. 36–40.
- Балаболкин М. И., Никишова М. С., Волкова А. К. и др. Применение антиоксидантов из группы флавоноидов в лечении диабетической ретинопатии при сахарном диабете 2 типа // Проблемы эндокринологии. 2003. № 3. Т. 49. С. 3–6.
- Недосугова Л. В., Никишова М. С., Волковой А. К., Балаболкин М. И., Рудько И. А., Кубатиев А. А., Дергачева Л. И. Коррекция процессов свободно-радикального окисления на фоне применения биофлавоноида дигидрокверцетина при сахарном диабете типа 2 // Вестник восстановительной медицины. 2006. № 4 (18). С. 51–54.
- Проблема ожирения в Европейском регионе ВОЗ и стратегии ее решения. Европейская министерская конференция ВОЗ по борьбе с ожирением «Питание и физическая активность в интересах здоровья». Стамбул, Турция, 15–17 ноября 2006 г. Всемирная Организация Здравоохранения. Европейское региональное бюро.
- Ebbeling C. B., Pawlak D. B., Ludwig D. S. Childhood obesity: public-health crisis, common sense cure // Lancet. 2002, 360: 473–482.
- Nathan B. M., Moran A. Metabolic complications of obesity in childhood and adolescence: more than just diabetes // Curr Opin Endocrinol Diabetes Obes. 2008, Feb; 15 (1): 21–29.
- A Clinical Guide to Pediatric Weight Management and Obesity. Hassink S. G. Lippincott Williams&Wilkins, 2007, pp. 114–129.
- Non-alcoholic steatohepatitis (NASH). U. Leuscher. 5 th edition. 2006. Dr. Falk Pharma GmbH.
- Дедов И. И., Балаболкин М. И., Мамаева Г. Г. и др. Сахарный диабет: ангиопатии и окислительный стресс. Пособие для врачей. М.: МЗ РФ, ГУ ЭНЦ РАМН, 2003. 85 с.
- Egger B. Helping patients lose weight — what works? // Aust Fam Physician. 2008, Jan-Feb; 37 (1–2): 20–23.
- Мальцев Г. Ю., Васильев А. В. Антиоксидантный индекс эритроцитов в мониторинге лечебного питания // Вопросы питания. 1999. № 2. С. 41–43.
Статья опубликована в журнале Лечащий Врач
материал MedLinks.ru






