Эффективность негормональной терапии атрофического вагинита у женщин в постменопаузе
Содержание статьи
Введение
С учетом увеличения продолжительности жизни женщин остаются актуальными проблемы эстроген-дефицитного состояния, влияющего на все системы организма [1]. У большинства женщин в пери- и постменопаузальном периоде имеются атрофические изменения в тканях вульвы и влагалища. Симптомы атрофического вагинита (АВ) появляются примерно у половины женщин в постменопаузе, оказывая потенциально негативное влияние на качество жизни [2–4].
В 2014 г. был предложен новый термин — «генитоуринарный менопаузальный синдром». Изменение терминологии было вызвано необходимостью (1) признать вовлечение в процесс атрофии нижних отделов мочевыделительной системы, (2) определить менопаузу как этиологический фактор и (3) избегнуть отрицательных коннотаций, связанных с термином «атрофия» [5].
АВ в основном встречается после менопаузы, но может наблюдаться и у женщин репродуктивного возраста, особенно у онкологических больных, получающих химио- или лучевую терапию. АВ негативно влияет на качество жизни, сексуальное желание, уверенность в себе [6]. Зачастую женщины рассматривают свои симптомы как вариант нормы и не предъявляют активных жалоб, поэтому частота диагноза занижена, а лечение в таких случаях отсутствует [7, 8].
Принимая во внимание патогенез заболевания, терапия эстрогенами признается «золотым стандартом» [9]. При этом системная гормональная терапия устраняет симптомы АВ лишь в трети случаев. Применение же локальной (вагинальной) эстрогенотерапии приводит к регрессу симптомов [10]. Преимущества локальной терапии очевидны: отсутствие первичного метаболизма в печени, минимальное влияние на эндометрий, низкая гормональная нагрузка, минимальные побочные эффекты, не требуется дополнительный прием прогестагенов, отсутствует системное действие [11]. Женщинам, имеющим противопоказания или непереносимость гормонов, а также желающим избежать гормональной терапии, показаны негормональные препараты для облегчения местной симптоматики. Негормональные средства обеспечивают временное купирование симптомов АВ, не имеют долгосрочных терапевтических эффектов, при этом безопасны, эффективны и легки в применении [12].
Цель исследования — оценить эффективность негормональной терапии АВ у женщин в постменопаузе.
Материал и методы
Выполнено пилотное сравнительное исследование с участием 36 пациенток постменопаузального возраста.
Критерии включения: наличие жалоб, характерных для АВ (47% пациенток, n=17); объективные признаки АВ при отсутствии жалоб (53% пациенток, n=19; АВ у таких пациенток был выявлен на основании индекса вагинального здоровья (ИВЗ)).
Критерии исключения: тяжелая соматическая патология; воспалительные заболевания органов малого таза; злокачественная и предраковая патология матки, шейки матки, придатков матки; инфекции, передаваемые половым путем; применение системной или местной менопаузальной гормональной терапии (МГТ) в течение 3 мес. до текущего исследования; противопоказания к МГТ.
Все пациентки с АВ были разделены на 3 группы: I группа получала интравагинальный крем, содержащий эстриол 0,5 мг; II группа получала негормональный многокомпонентный растительный препарат per vaginam, обладающий регенеративными, антимикробными, противогрибковыми, противовирусными, иммуномодулирующими, противовоспалительными и анальгезирующими свойствами (отказ от гормонотерапии был мотивирован гормонофобией); III группа (контрольная) лечения не получала (отказ от лечения был мотивирован нежеланием получать какую-либо терапию, в т. ч. использовать препараты per vaginam) (табл. 1).
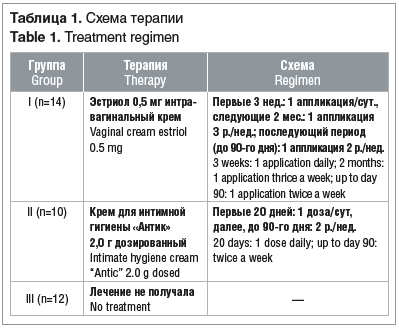
Возраст больных составил: 52,36±0,58 года в I группе, 51,3±0,86 — во II и 50,67±0,51 — в III (р>0,05). Длительность постменопаузы варьировала от 1 до 3 лет. Больные всех 3 групп были сопоставимы по возрасту, продолжительности постменопаузы, длительности заболевания, сопутствующей патологии (р>0,05).
Проводился сбор анамнеза, оценивались субъективные и объективные критерии АВ. Для субъективной оценки выраженности атрофических процессов применялась анкета, включающая вопросы о частоте симптомов, таких как эмоциональная неустойчивость, нарушения сна, быстрая утомляемость, сухость, жжение, неприятный запах в области наружных половых органов, диспареуния.
Для объективной оценки атрофических процессов применяли ИВЗ, основанный на определении рН и визуальной оценке состояния влагалища [13]. Определение рН проводилось с помощью индикаторных полосок (Кольпо-тест рН, ООО «Биосенсор», Россия). Во время гинекологического осмотра наносили влагалищную жидкость на сенсорный элемент тест-полоски так, чтобы полностью смочить всю поверхность сенсорного элемента. Через 1–2 секунды удаляли избыток жидкости на сенсорном элементе легким прикосновением ребра полоски к чистой бумажной салфетке на 2–3 секунды. Через 15 секунд с момента нанесения влагалищной жидкости сравнивали окраску сенсорного элемента с эталонной цветовой шкалой на этикетке комплекта при хорошем освещении. У здоровой женщины рН обычно в пределах 3,5–5,5. Значение рН у нелеченных женщин в постменопаузе составляет 5,5–7,0 в зависимости от возраста и сексуальной активности.
Количество условно-патогенных микроорганизмов определяли культуральным методом и методом полимеразной цепной реакции в режиме реального времени.
Длительность наблюдения составила 90 дней с промежуточной оценкой эффективности через 20 дней от начала лечения. Эффективность терапии оценивали по уменьшению или устранению симптомов АВ, повышению качества жизни, повышению ИВЗ и нормализации рН.
Для анализа полученных данных применяли методы описательной статистики с вычислением средней арифметической и ее стандартной ошибки. Для оценки межгрупповых различий использовали непараметрический критерий U Манна — Уитни для двух независимых выборок. Различия считались достоверными при р<0,05.
Результаты исследования
Динамика симптомов у обследованных пациенток
В данном клиническом обследовании были получены результаты, свидетельствующие об АВ и подтверждающие первоначальный диагноз. При опросе были выявлены как жалобы, характерные для АВ, так и нейровегетативные симптомы климактерического синдрома (табл. 2). Необходимо отметить, что в 21–40% случаев женщины связывали наличие нейровегетативной симптоматики именно с неприятными ощущениями, дискомфортом в области влагалища.
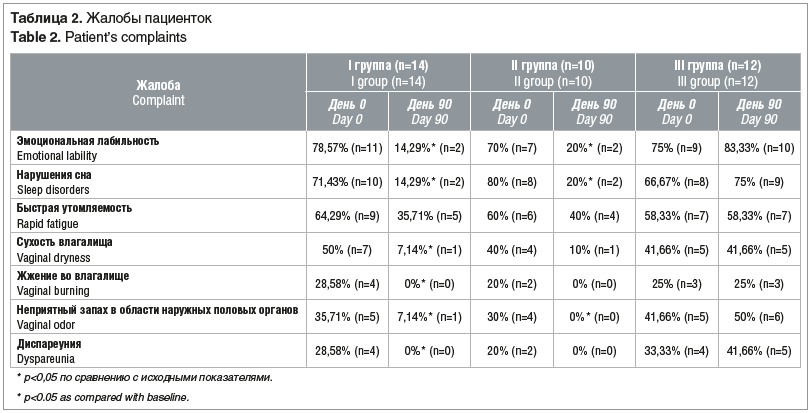
Достоверных различий в частоте и выраженности симптомов между группами пациенток на этапе включения в исследование не было (р>0,05).
В нашем исследовании пациентки не предъявляли жалоб на другие составляющие генитоуринарного менопаузального синдрома. Возможно, это связано с тем, что в нижних отделах мочевыделительной системы и вульве меньше рецепторов к эстрогенам, чем во влагалище [14], и у исследуемых групп пациенток (с длительностью постменопаузы 1–3 года) еще не развились атрофические изменения вульвы, мочевого пузыря и уретры.
При микробиологическом исследовании неспецифический вагинит и бактериальный вагиноз были выявлены у 57% (n=8), 60% (n=6) и 67% (n=8) пациенток I, II и III групп соответственно (р>0,05).
Значение рН влагалищного содержимого составило 6,14±0,08 в I группе, 6,02±0,11 — во II и 6,19±0,06 — в III (р>0,05). Показатель ИВЗ — 13,21±0,44, 12,0±0,79 и 12,75±0,39 в I, II и III группах соответственно (р>0,05).
Жалобы на дискомфорт при половом акте, неприятный запах в области половых органов являются закономерным результатом сокращения объема лубриканта, гликогена, полезной лактофлоры. В результате рН влагалища смещается в щелочную сторону, на фоне чего активизируется условно-патогенная микрофлора и провоцируется воспалительная реакция [15].
Все пациентки, получавшие лечение, хорошо переносили терапию и завершили трехмесячный курс лечения. На фоне проведенной терапии были зафиксированы изменения субъективных и объективных критериев степени тяжести атрофических процессов во влагалище.
Психоэмоциональные нарушения
По сравнению с исходным уровнем через 20 дней от начала лечения при анкетировании было выявлено, что частота психоэмоциональных нарушений была выше в III группе в 3,57 раза, чем в I группе (р<0,05), и в 1,9 раза — чем во II группе (р>0,05). Через 90 дней частота встречаемости психоэмоциональных нарушений у пациенток I и II групп достоверно снизилась по сравнению с исходными показателями, а также была достоверно ниже, чем в III группе по результатам лечения (р<0,05) (рис. 1).
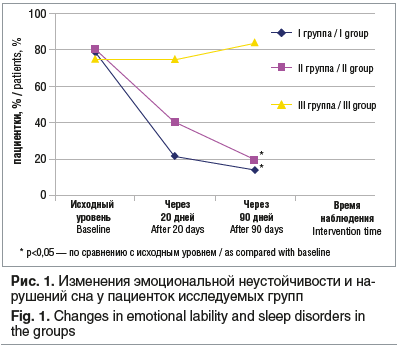
Безусловно, местное применение МГТ и негормональных препаратов не оказывает непосредственного влияния на общее состояние. Однако, учитывая объективное улучшение состояния влагалища у пациенток I и II групп, можно предположить, что устранение атрофических и воспалительных процессов во влагалище привело к улучшению общего состояния пациенток.
Кроме того, к моменту завершения наблюдения (через 90 дней от начала лечения) у 78,57% пациенток I группы и 100% пациенток II группы отсутствовали жалобы на неприятный запах в области наружных половых органов (изменение по сравнению с частотой встречаемости на исходном уровне было достоверным, р<0,05), что положительно влияло на общее состояние пациенток.
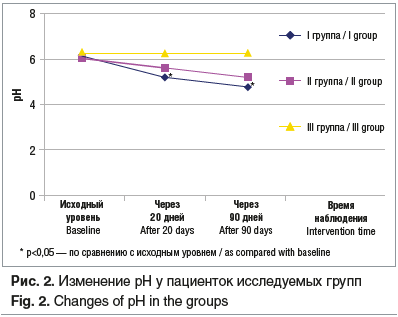
Динамика значений pH
Анализ рН (рис. 2) на фоне терапии показал статистически значимое снижение pH в I группе через 20 и 90 дней как по сравнению с исходным уровнем, так и по сравнению с данным показателем у пациенток III группы. Во II группе (крем для интимной гигиены «Антик» дозированный) снижение pH показало достоверные различия при сравнении с аналогичным показателем у пациенток III группы через 20 и 90 дней (р<0,05), однако снижение pH относительно исходного уровня было менее выраженным (р>0,05). Достоверных различий в динамике снижения pH между I и II группами не выявлено (р>0,05).
Динамика ИВЗ
До начала лечения стенка влагалища у пациенток имела низкую эластичность, низкий уровень транссудата, поверхность слизистой оболочки стенки была воспалена, легко кровоточила при контакте, имелись множественные петехии, эпителий был тонким и рыхлым. ИВЗ до лечения варьировал от 9 до 15.
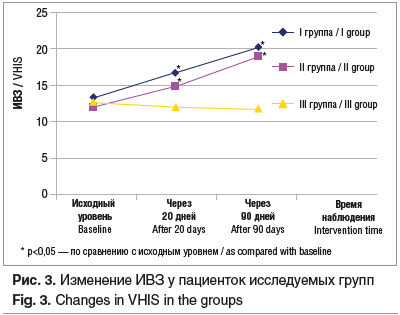
На фоне терапии у пациенток I и II групп при снижении рН влагалищного содержимого закономерно был повышен ИВЗ. Через 20 дней у пациенток I группы ИВЗ увеличился на 25,97% (р<0,05), у пациенток II группы — на 23,3% по сравнению с исходным уровнем (р<0,05). Через 90 дней увеличение по сравнению с исходным уровнем составило 54,13% (р<0,05) и 57,5% (р<0,05) в I и II группах соответственно. Достоверных различий между I и II группами не было.
ИВЗ в I группе через 20 дней был выше на 39,6% (р<0,05), через 90 дней — на 75,82% (р<0,05), чем ИВЗ в III группе в аналогичные сроки. ИВЗ через 20 дней у пациенток II группы был выше, чем у пациенток III группы, на 24,16% (р<0,05), через 90 дней — на 63,21% (р<0,05) (рис. 3).
Результаты бактериологического исследования после окончания терапии показали отсутствие диагностически значимого количества условно-патогенных микроорганизмов у 78% (n=11) и 40% (n=4) пациенток I и II групп соответственно.
Более выраженное снижение рН у пациенток I группы (местная терапия эстрогенами) было обусловлено как эстриолом, входящим в состав МГТ, так и молочной кислотой. Биологический эффект эстрогенов при урогенитальных расстройствах, вне зависимости от способа применения, включает в себя пролиферацию влагалищного эпителия с увеличением пролиферации и дифференцировки эпителиоцитов, что приводит к снижению рН, увеличению пула лактобацилл и повышению ИВЗ [16]. Перечисленные изменения сопровождаются снижением рН влагалища и почти двукратным увеличением индекса созревания эпителия влагалища.
У пациенток II группы, получавших «Антик», ИВЗ в большей степени увеличился за счет такого показателя, как «целостность эпителия», благодаря регенерирующему действию масла какао, кровоостанавливающему действию экстрактов туи, красной щетки, боровой матки и тысячелистника. Кроме того, положительные изменения в эпителии влагалища у пациенток II группы связаны с наличием в креме экстракта ряда растений, реализующих иммуномодулирующий и противовоспалительный эффект, экстракта Витекса священного, обладающего эстрогеноподобным действием, а также наличием дигидрокверцетина, инициирующего синтез коллагена, эластина, гликозаминогликанов.
Заключение
Женщины зачастую рассматривают симптомы АВ как вариант нормы, несмотря на то что это состояние отрицательно влияет на качество жизни, сексуальную функцию и т. д. Поэтому при работе с такой категорией пациенток важно активно использовать методы, выявляющие атрофические процессы. Существует несколько эффективных методов терапии АВ, при этом стандартом лечения является местная терапия эстриолом. Однако для пациенток, которым гормонотерапия противопоказана, а также в случае нежелания применять гормональные препараты, альтернативой может служить применение негормональных средств, таких как растительный многокомпонентный крем для интимной гигиены «Антик» дозированный, что позволит сохранить здоровье женщин постменопаузального возраста и улучшить их качество жизни.
Сведения об авторах:
Нариманова Метанат Рафиговна — к.м.н., ассистент кафедры акушерства и гинекологии лечебного факультета, ORCID iD 0000-0003-0677-2952;
Сапрыкина Людмила Витальевна — к.м.н., ассистент кафедры акушерства и гинекологии лечебного факультета, ORCID iD 0000-0002-2931-0956.
ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. 117997, Россия, г. Москва, ул. Островитянова, д. 1.
Контактная информация: Сапрыкина Людмила Витальевна, e-mail: lioudsap@yandex.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 04.07.2019.
About the authors:
Metanat R. Narimanova – MD, PhD, Аssistant of the Department of Obstetrics and Gynecology, ORCID iD 0000-0003-0677-2952;
Lyudmila V. Saprykina – MD, PhD, Аssistant of the Department of Obstetrics and Gynecology, ORCID iD 0000-0002-2931-0956.
N.I. Pirogov Russian National Research Medical University. 1, Ostrovityanov str., Moscow, 117437, Russian Federation.
Contact information: Lyudmila V. Saprykina, e-mail: lioudsap@yandex.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 04.07.2019.
Информация с rmj.ru