Структура заболеваемости и современные подходы к терапии ОРВИ у детей
Содержание статьи
- 1 Введение
- 2 Виды ОРВИ
- 3 Общий подход к лечению ОРВИ
- 4 1. Этиотропные
- 5 1.1. Инактивирующие вирусы
- 6 1.2. Осуществляющие помощь иммунокомпетентным структурам в инактивации возбудителей
- 7 1.3. Направленные на возбудителя микоплазменной или бактериальной инфекции
- 8 2. Посиндромная патогенетическая терапия
- 9 Заключение
Введение
Бесспорно, острые респираторные инфекции (ОРИ) неизменно занимают ведущее место в структуре инфекционной патологии, особенно среди детей. В России ежегодно регистрируется примерно 70–80 тыс. заболеваний на 100 тыс. населения данного возраста (в 3,3 раза выше, чем у взрослых) без тенденции к снижению, при этом частота встречаемости гриппа во время сезонного подъема заболеваемости наблюдается не всегда чаще, а иногда и реже, чем ОРИ другой этиологии в сумме [1].
ОРИ не являются легкой «простудой», о чем мы постоянно слышим с экрана телевизора и читаем в Интернете, — это острые инфекции с разной степенью тяжести течения, обусловленные преимущественно вирусами, принадлежащими как минимум к 7 семействам (Orthomyxoviridae, Paramyxoviridae, Picornaviridae, Соronaviridae, Reoviridae, Рarvoviridaе, Adenoviridae) [2]. При этом следует заметить, что возбудителей «простуды» не существует вовсе, и это понятие не имеет никакого отношения к медицине.
Спектр возбудителей может быть разным, но, как правило, он обусловлен сезоном и возрастом наблюдаемых. Так, в роддомах и палатах новорожденных чаще циркулируют респираторно-синцитиальный (РС) и риновирусы, гемофильная палочка, в детских дошкольных коллективах — адено-, РС и парагриппозный вирусы, среди школьников — аденовирусы, микоплазма пневмонии. Вирус гриппа доминирует у пациентов любого возраста во время эпидемического подъема гриппа. Примерно в 25–30% случаев, особенно во вновь созданных коллективах (группа детского дошкольного учреждения, первый класс школы, палата стационара, казарма), имеет место одновременное участие в инфекционном процессе нескольких возбудителей, обусловленное эффектом «перемешивания».
Несмотря на общие входные ворота при ОРВИ любой этиологии (слизистая оболочка носовых ходов и носоглотки) с обязательным развитием локального воспаления (ринит, фарингит), эти инфекции отличаются значительным полиморфизмом клинической симптоматики и отсутствием, кроме вирусов гриппа, чувствительности к современным противогриппозным препаратам (ингибиторам нейраминидазы), широко используемым в настоящее время при лечении гриппа (табл. 1). Доказано, что выраженность и быстрота развития клинических проявлений, а также тяжесть течения ОРВИ и частота развития осложнений обусловлены как патогенностью возбудителя, так и активностью факторов защиты пациента.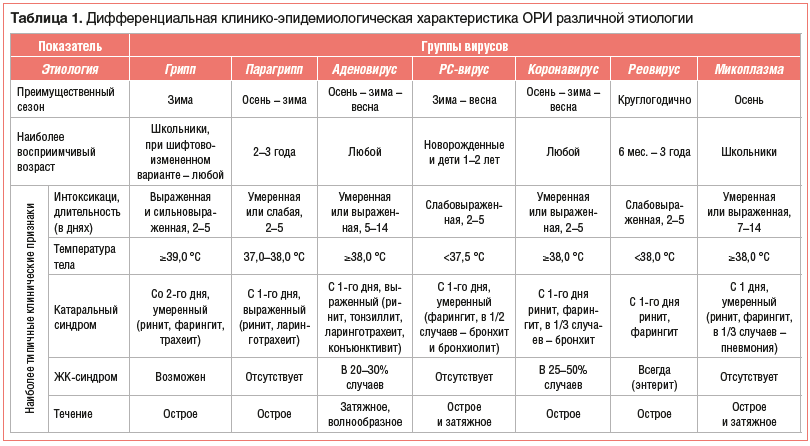
Виды ОРВИ
Грипп — это тоже ОРВИ, наиболее распространенная и тяжелая. Вызывается РНК-содержащими вирусами, которые относятся к семейству Orthomyxoviridae (род Influenzaе), включающему вирусы гриппа типов A, B и C. Способность вирусов к антигенной изменчивости определяет высокую восприимчивость населения и вовлечение в эпидемический процесс всех возрастных групп взрослых и детей. Отмечено, что если ранее эпидемические подтипы вирусов сменяли друг друга, то в последние десятилетия наблюдается одновременная циркуляция вирусов гриппа А (H1N1), A (H3N2) и В [3]. Заболевание начинается на фоне полного здоровья, реже после кратковременного недомогания. Основные проявления: общеинтоксикационный синдром и симптомы поражения респираторного тракта с преобладанием первого над вторыми. Легкие формы возможны только у привитых. При тяжелых формах гриппа процесс бурно прогрессирует с развитием проявлений системной воспалительной реакции и геморрагического синдрома с возможным кровоизлиянием в жизненно важные органы: легкие, надпочечники, мозг, кишечник и др. [4–7]. Возможно развитие инфекционно-токсического шока, одним из проявлений которого вследствие тканевой гипоксии и ацидоза является поражение прежде всего ЦНС в виде нейротоксического синдрома (токсической энцефалопатии) с отеком мозговой ткани и нарушением церебральной гемодинамики. Возможно развитие токсического геморрагического отека легких или острого респираторного дистресс-синдрома, в основе которого лежит повреждение альвеоло-капиллярной мембраны и увеличение капиллярной проницаемости для больших молекул. Выраженные нарушения микроциркуляции вследствие значительного содержания сосудов нередко возникают и в проксимальных отделах желудочно-кишечного тракта (ЖКТ).
Парагрипп вызывается РНК-содержащими вирусами, относящимися к семейству Paramyxoviridae (роды Respirovirus (1 и 3 типы). Основное место локализации вирусов — слизистая гортани. Описанные выше микроциркуляторные нарушения для парагриппа не характерны. Обычно имеет место развитие катарального ларинготрахеита (бронхита) с наиболее выраженными изменениями в гортани [8]. Тяжелые формы парагриппа обычно связаны с развитием острого стенозирующего ларинготрахеита (ОСЛТ), причиной чего могут быть рефлекторный спазм мускулатуры гортани и трахеи, отек и инфильтрация слизистой и подскладочного пространства гортани; обтурация дыхательных путей слизисто-гнойным содержимым. Изменения в легких обычно выражены слабее. Но возможно, особенно у детей раннего возраста, появление патологических процессов в альвеолярных структурах (округление, слущивание, появление включений, нейтрофилов, серозной жидкости, гиалиновых мембран), гипертрофия реснитчатых и других эпителиальных клеток мелких бронхов. Описано развитие отека митохондрий, вакуолизации и некроза клеток, а в некоторых случаях — образование многоядерных клеток и синтициальных пластов с длительно сохраняющейся гиперплазией эпителия. Нередко в просвете бронхиол обнаруживаются пробки из рыхлой соединительной ткани. Подобные изменения при парагриппе наблюдаются в печени, почках, поджелудочной железе, ЦНС и других органах (при генерализации процесса) [9].
Респираторно-синцитиальная вирусная (РСВ) инфекция вызывается вирусом, относящимся также к семейству Paramyxoviridae (род Pneumovirus 2 подтипа А и В). Возбудитель имеет выраженную тропность к эпителию слизистой нижних дыхательных путей. Поражает людей всех возрастных групп, вызывая как спорадические случаи, так и вспышки, преимущественно среди детей раннего возраста (в роддомах, домах ребенка, детских стационарах) и пожилых людей (в домах престарелых), а также у лиц с системными и хроническими заболеваниями или после трансплантации органов. В этиологии бронхитов и бронхиолитов у детей младшего возраста на долю РСВ приходится до 70%. Риск инфицирования у детей первого года жизни составляет 63%, 1–2 лет — 37%, в старшем возрасте — 17% [10]. При этом первые практически всегда переносят клинически выраженное заболевание. В первый день заболевание проявляется умеренно выраженными интоксикацией и катаральными симптомами в носоглотке (ринофарингит) на фоне нормальной или субфебрильной температуры тела с последующим подъемом ее в ряде случаев на 2–3-й день и развитием типичной симптоматики поражения бронхов. Маленький калибр бронхов и бронхиол делает детей особенно уязвимыми в отношении развития острой бронхиальной обструкции. Принадлежность ребенка к группе риска развития тяжелой формы РСВ-инфекции: недоношенность, масса тела при рождении
Коронавирусная (КВ) инфекция вызывается РНК-содержащим вирусом, относящимся к семейству Coronaviridae (род Coronavirus, 5 групп вирусов). Вирус поражает в основном эпителий респираторного тракта (в т. ч. бронхов и легких) и ЖКТ, что сопровождается соответствующей симптоматикой поражения этих систем [11]. Возможно развитие и тяжелых форм инфекции с началом, подобным гриппу: фебрильной температурой тела и интоксикацией. Доказано, что для КВ характерен широкий тканевой тропизм, в т. ч. способность поражать печень, мозг, органы зрения, железистую, нервную и лимфоидную ткани [12]. Известно, что КВ явился возбудителем вспышки тяжелого острого респираторного синдрома (ТОРС) в Китае в 2002 г. и ближневосточного респираторного синдрома (БВРС), регистрируемого в странах Ближнего Востока в течение последних 6 лет [13]. Одним из опасных свойств КВ является способность поражать макрофаги, что приводит к блокаде иммунного ответа.
Аденовирусная инфекция вызывается ДНК-содержащими вирусами, принадлежащими к семейству Adenoviridae (род Mastadenovir, более 50 серотипов в составе 7 групп А, B1, B2, C, D, E, F, имеющих общий комплементсвязывающий антиген, но различающихся по тканевому тропизму). Основная локализация аденовирусов — слизистая оболочка и лимфатическое кольцо носоглотки, конъюнктива глаза, а также слизистая оболочка и мезентериальные лимфоузлы кишечника, реже — эндотелий сосудов, что обусловливает развитие воспаления экссудативного типа и появление некротических изменений с образованием фибрина (экссудативный фарингит, пленчатые тонзиллит, конъюнктивит, вульвовагинит). Заболевание начинается с выраженных симптомов в носоглотке (затрудненного носового дыхания из-за отечности слизистой носа и небных миндалин, затем обильного серозно-слизистого ринита и тонзиллита) на фоне фебрильной, субфебрильной или даже нормальной температуры тела и интоксикации, максимальная выраженность которых достигается в последующие дни и длительно (до 2 нед.) сохраняется. Почти всегда отмечается одутловатость лица, век, отечность миндалин, задней стенки глотки с гиперплазией фолликулов. Возможно появление на поверхности миндалин, конъюнктив, голосовых связок пленчатых серовато-белесоватых блестящих налетов. Регистрируется последовательно развивающаяся полиорганность поражений: респираторный тракт, бронхи, легкие, конъюнктива и роговица глаза, все группы лимфоузлов, кишечник, соответственно, имеет место многообразие последовательно появляющихся симптомов. Поражение гортани, в т. ч. с ОСЛТ, наблюдается у каждого пятого ребенка. Стеноз формируется не в 1-й день, протекает тяжело и более продолжительно по сравнению с другими ОРВИ. Возможно развитие бронхита с длительно сохраняющейся в 25% случаев острой бронхиальной обструкцией. Нередко наблюдается увеличение печени и селезенки, а также всех групп лимфоузлов, в т. ч. мезентериальных с развитием мезаденита, проявляющегося приступообразными болями в животе, иногда с симптомами раздражения брюшины, симулирующими картину «острого живота» [15]. Возможно внутриутробное инфицирование, а также заражение новорожденных во время родов с развитием вышеописанной симптоматики.
Общий подход к лечению ОРВИ
Пациенты с легкими и среднетяжелыми формами ОРВИ лечатся в основном амбулаторно. Госпитализации подлежат больные с тяжелыми и осложненными формами заболевания, новорожденные и дети первых лет жизни со среднетяжелыми формами болезни, но с осложненным течением, обострением сопутствующих заболеваний, а также пациенты из закрытых учебных заведений или проживающие в неблагоприятных бытовых условиях. При подозрении на ТОРС или БРВС, если пациент прибыл из стран Ближнего Востока, независимо от тяжести процесса, он должен быть госпитализирован в бокс [15].
Диета должна соответствовать возрасту и состоянию больного, быть полноценной, богатой витаминами, содержать достаточное количество жидкости (минеральная вода, чай с лимоном, соки, отвары липы, мать-и-мачехи, мяты, подорожника, календулы; плодов и ягод: шиповника, малины, черной смородины, земляники, клюквы, брусники). Желательно, чтобы кормление больного было ненасильственным, а пища — легкоусвояемой.
Лечение должно быть патогенетически обусловленным, по возможности этиотропным и зависящим от выраженности клинической симптоматики, тяжести заболевания, наличия осложнений и сопутствующей коморбидной патологии.
Основные группы препаратов для лечения ОРИ
Этиотропные
1.1. Инактивирующие вирусы — возбудителей заболевания, препятствуют проникновению их в клетки-мишени и их репродукции.
1.2. Осуществляющие помощь иммунокомпетентным структурам в инактивации возбудителей (препараты интерферона (IFN) и индукторы IFN).
1.3. Направленные на возбудителя микоплазменной или бактериальной инфекции.
Посиндромные, патогенетически обусловленные, направленные на ликвидацию того или иного симптома заболевания
1. Этиотропные
Препараты этиотропной терапии. Основное условие достижения эффекта этиотропной терапии — ее своевременность. Лечение необходимо начинать при появлении первых симптомов заболевания.
1.1. Инактивирующие вирусы
Препаратов, обладающих специфической противовирусной активностью по отношению к возбудителям ОРВИ, немного. Это блокаторы ионных каналов: римантадин и его полимерное производное — римантадин + альгинат натрия; ингибиторы нейраминидазы — осельтамивир и занамивир, ингибитор слияния — умифеновир, аналоги нуклеозидов широкого спектра действия (рибавирин и инозин пранобекс (Изопринозин)).
В настоящее время регистрируется резистентность вирусов к римантадину, отсутствующая в случае применения комбинации римантадин + альгинат натрия. Включение на ранних сроках заболевания в комплексную терапию ОРВИ любой этиологии этого препарата статистически значимо сокращает сроки выздоровления детей [16].
Доказано, что прием оcельтамивира способствует достоверному сокращению продолжительности всех основных симптомов гриппа при условии применения в первые 48 ч заболевания. Неэффективен в случае ОРВИ другой этиологии. Назначается детям в возрасте старше 1 года (табл. 2).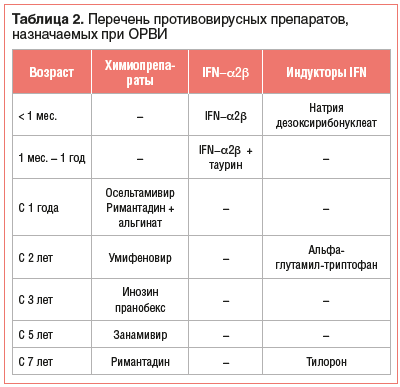
Занамивир применяется в виде ингаляции через дискхалер, эффективен только при гриппе. Препарат противопоказан лицам с бронхиальной астмой и при наличии бронхообструкции, т. к. у лиц с осложненным преморбидным фоном может сам провоцировать ее развитие. Разрешен для лечения детей с 5 лет.
Умифеновир эффективен при лечении взрослых и детей в возрасте от 2 лет, заболевших как гриппом, так и ОРВИ другой этиологии, в т. ч. с кишечным синдромом, способствуя достоверному сокращению продолжительности лихорадочного периода, интоксикации, катаральных симптомов в носоглотке, острого стенозирующего ларинготрахеита, диарейного синдрома и всего заболевания в целом [17]. Успешно использовался для профилактики тяжелых осложнений при гриппе A(H1N1)pdm09 у беременных [18].
ВОЗ включила умифеновир в перечень препаратов с прямой противовирусной активностью.
Наиболее актуален поиск препаратов, объединяющих в себе противовирусную и иммуномодулирующую активность с понятным и безопасным метаболизмом. Таким препаратом является Изопринозин (инозин пранобекс, код АТХ-J05 АХ05), синтетический аналог инозина, наиболее известного представителя пуринов. Изменяя стереохимическую структуру рибосом, препарат подавляет синтез вирусных белков, тормозит репликацию вирусов и блокирует их репродукцию, а также восстанавливает и повышает функциональную активность клеток иммунной системы (макрофагов, нейтрофилов, лимфоцитов и NK-клеток), модулируя иммунный ответ по клеточному типу, стимулирует продукцию антител и образование цитокинов. На клеточных культурах обнаружено наличие у препарата умеренной противовирусной активности в отношении вирусов гриппа, в т. ч. типа A(H1N1)pdm09, В и типа А/H5N2 птиц, РС-, адено- и парагриппозного вирусов [19]. Препарат зарегистрирован более чем в 70 странах мира под различными торговыми названиями в 2 лекарственных формах (сироп и таблетки). Запатентован в 1972 г., используется в США как иммуномодулятор с противовирусной активностью с 1973 г., в странах Евросоюза — с 1978 г. В РФ разрешен для применения у взрослых и детей с 3-летнего возраста (РИ П № 15167/01 от 29.04.2011, выданное Федеральной службой по надзору в сфере здравоохранения). Клиническими наблюдениями над 2503 детьми в возрасте 3 лет и старше с ОРВИ в 13 городах России силами 121 врача доказано, что препарат обладает статистически значимой лечебно-профилактической эффективностью, в т. ч. при наличии у пациентов осложненного преморбидного фона (у часто болеющих, с наличием аллергозов, хронических инфекций ЛОР-органов и респираторного тракта и т. д.). Использование инозина пранобекса при лечении ОРВИ у пациентов всех возрастных групп (в т. ч. у лиц с бронхитом) способствовало значимому сокращению продолжительности как симптомов интоксикации, так и катарального воспаления в носоглотке, гортани и бронхах, а также всего заболевания в целом [20].
1.2. Осуществляющие помощь иммунокомпетентным структурам в инактивации возбудителей
Интерфероны и их индукторы. Ведущая роль в противовирусной защите на первых этапах заболевания принадлежит системе интерферонов (IFN) — естественных цитокинов, обладающих универсальным антивирусным свойством — подавлением репликации множества РНК- и ДНК-содержащих вирусов благодаря ингибированию процессов транскрипции и трансляции вирусных матриц. Кроме того, IFN, как и другие цитокины, оказывают влияние на функциональную активность практически всех органов и систем организма, участвующих в регуляции гомеостаза. Они обладают гормоноподобными свойствами, регулируют процессы перекисного окисления липидов на клеточных мембранах и оказывают иммуномодулирующее действие. Любой дисбаланс в продукции IFN может привести к нарушению иммунонейроэндокринных взаимодействий [21]. Наиболее детально изучены IFN-α, -γ и -β, из которых в состав препаратов, используемых для лечения ОРВИ, чаще других входит рекомбинантный IFN-α2β (моно или с добавлением антиоксидантов). Их эффективность увеличивается при условии применения с момента появления первых симптомов заболевания.
Рекомбинантный IFN-α2β в виде капель и назального спрея разрешен для применения у взрослых (в т. ч. беременных и кормящих матерей) и детей любого возраста. Лечебный эффект препарата начинался уже на 2-е сут лечения — ликвидировались практически все симптомы заболевания [22]. В целом продолжительность заболевания на фоне приема препарата у пациентов сокращалась на 2 дня. Назначение IFN-α2β беременным женщинам способствовало предотвращению развития у них пневмонии [18]. Введение препарата сразу после рождения недоношенным детям, родившимся с очень низкой и экстремально низкой массой тела, перенесшим критическое состояние и переведенным из отделения реанимации, показало, что ОРВИ у получавших рекомбинантный IFN-α2β развивались реже, протекали легче, с более редким развитием осложнений, были статистически значимо менее продолжительными [23].
IFN-α2β человеческий рекомбинантный в виде мази, геля, суппозиториев может использоваться как для сезонной профилактики у пациентов любого возраста, в т. ч. у новорожденных, беременных женщин и кормящих матерей, так и для экстренной профилактики в очагах заболевания, в т. ч. и в детских стационарах. Использование препарата (оптимально в виде геля) способствует статистически значимому уменьшению частоты развития внутрибольничных инфекций. Доказана также эффективность препарата при раннем лечении ОРВИ и острых тонзиллитов бактериальной или сочетанной этиологии, причем наиболее эффективным было одновременное применение препарата в виде свечей и геля [24]. Использование данного комплекса способствовало также сокращению продолжительности выделения возбудителей заболевания (вирусных и бактериальных), что предотвращало повторное и перекрестное инфицирование пациентов и развитие внутрибольничных инфекций.
В терапии ОРВИ используются и различные индукторы интерферона. Следует иметь в виду, что если препараты IFN-α2b в качестве заместительной терапии рекомендовано применять при ОРВИ любой этиологии у лиц любого возраста, в т. ч. часто болеющих детей) с низким уровнем циркулирующего IFN-α в сыворотке крови, а также у лиц с недостаточной IFN-продуцирующей активностью иммунокомпетентных клеток, то применение только индукторов IFN у этих пациентов не окажет воздействия. Желательно сочетать введение индукторов IFN и этиотропных препаратов.
Натрия дезоксирибонуклеат — низкомолекулярный иммуномодулятор природного происхождения, обладающий способностью восстанавливать дисбаланс иммунного ответа. Препарат оптимизирует специфические реакции против грибковой, вирусной и бактериальной инфекций. При его включении в комплексную терапию ОРВИ у детей (в т. ч. новорожденных и с сопутствующей аллергической патологией) имело место сокращение продолжительности основных симптомов заболевания и, соответственно, более быстрое выздоровление больного ребенка, независимо от преморбидного фона [25].
Тилорон восстанавливает дисбаланс Т-клеточного звена иммунитета, активизирует синтез IFN и усиливает антителообразование. Применяется у взрослых и детей с 7 лет.
При рациональном выборе противовирусной терапии учитывается эпидемиологическая ситуация, предполагаемая этиология ОРВИ, клиническая симптоматика заболевания, возраст пациента и его преморбидный фон, а также активность и фармакокинетика препарата с учетом побочных эффектов. Для предупреждения полипрагмазии желательно назначать препараты с комплексной активностью (например, Изопринозин).
1.3. Направленные на возбудителя микоплазменной или бактериальной инфекции
Антибактериальная терапия. Антибактериальные препараты не обладают противовирусной активностью и не предупреждают развития бактериальных осложнений, а их прием способствует лишь развитию побочных реакций, в т. ч. аллергических, поэтому при лечении неосложненных форм ОРВИ нет необходимости их назначать. Нерациональное применение антибиотиков является одной из основных причин нарушения саногенеза, что создает предпосылки для гибели нормальной кишечной, накожной и респираторной микрофлоры, селекции антибиотикоустойчивых микроорганизмов, росту грибов, особенно представителей рода Candida, подавлению местной резистентности и, что нередко наблюдается, формированию вторичного иммунодефицита, способствующего образованию хронических очагов инфекции и прогрессированию уже имеющихся. Назначение этих препаратов показано только в том случае, если участие бактериальной инфекции невозможно исключить, что чаще всего бывает у лиц младшего возраста при тяжелой форме заболевания, а также при гриппе, обусловленном новым вариантом возбудителя.
2. Посиндромная патогенетическая терапия
Применение препаратов направлено на нормализацию нарушенных функций организма с учетом знания патогенеза заболевания и зависит от тяжести течения инфекционного процесса и выраженности клинической симптоматики: на борьбу с проявлениями токсикоза, ликвидацию лихорадки и респираторного синдрома, а также других симптомокомплексов и осложнений, развившихся в течение заболевания [26–30].
Заключение
Таким образом, в настоящем обзоре представлены доказательства того, что ОРВИ, доминирующие в структуре инфекционной патологии, особенно среди детей, не являются легкой «простудой». Это острые инфекции, отличающиеся полиморфизмом симптоматики разной степени тяжести течения, преимущественно обусловленные вирусами, принадлежащими как минимум к 7 семействам. Многими клиническими исследованиями доказана эффективность использования при лечении пациентов с ОРВИ общепринятых противовирусных препаратов (этиотропных, интерферонов, индукторов IFN) с ограничением применения антибиотиков.
Информация с rmj.ru