Материал и методы: в открытое одноцентровое исследование эффективности и безопасности 4-недельной терапии кандесартаном были включены 54 пациента (медиана возраста 55 лет, 37% мужчин) с неосложненной ранее нелеченой или неконтролируемой на фоне монотерапии АГ I–II степени, обратившиеся за амбулаторной помощью. Всем пациентам до и после исследования измерялись клиническое артериальное давление (АД) и частота сердечных сокращений, выполнялись биохимический анализ крови, суточное мониторирование АД (СМАД), аппланационная тонометрия, эхокардиография.
Результаты исследования: период наблюдения составил 4 нед. Наблюдалось снижение медианы систолического/диастолического АД с 153/95 до 138/89 мм рт. ст. (р
Заключение: 4-недельная монотерапия российским препаратом кандесартана (Ангиаканд) в дозе 16 мг/сут у пациентов среднего возраста с неосложненной неконтролируемой АГ I–II степени сопровождается значимым снижением как периферического, так и центрального систолического и диастолического АД и пульсового давления и отличается высоким профилем безопасности.
Ключевые слова: сердечно-сосудистые заболевания, артериальная гипертония, артериальная жесткость, ренин-ангиотензин-альдостероновая система, РААС, блокаторы РААС, Ангиаканд.
Для цитирования: Кобалава Ж.Д., Шаварова Е.К., Хромова И.А. Антигипертензивная эффективность монотерапии кандесартаном у пациентов с неосложненной артериальной гипертонией // РМЖ. 2018. №11(I). С. 2-6
Zh.D. Kobalava, E.K. Shavarova, I.A. Khromova
RUDN University, Moscow
Aim: to evaluate the antihypertensive effect and safety of the drug Angiakand (“Canonpharma Production”, Russia) in patients with uncomplicated uncontrolled arterial hypertension (AH).
Patients and Methods: 54 patients (median of age 55 years, 37% of men) with uncomplicated previously untreated or uncontrolled monotherapy AH of 1–2 st., who applied for ambulatory care were included in an open, single-center study of the efficacy and safety of a 4-week candesartan therapy. All patients before and after the study had their clinical blood pressure (BP) and heart rate measured, also biochemical blood test, ambulatory BP monitoring (ABPM), applanation tonometry, echocardiography were made.
Results: the observation period was 4 weeks. There was a decrease in the median of systolic/diastolic blood pressure from 153/95 to 138/89 mm Hg. (p<0.001) according to the clinical measurement and from 134/79 to 125/74 mm Hg. (p<0.001) according to the ABPM data. Target values of clinical BP were achieved in 33 (61%), and daily mean BP in 36 (68%) patients. Central systolic blood pressure decreased from 141 to 129 (p<0.001), central diastolic blood pressure — from 92 to 84 (p<0.001), central pulse BP — from 48 to 41 mm Hg. (p<0.05). Accurate changes in pulse wave velocity, indices of left ventricular diastolic function, functional state of the kidneys, electrolyte level were not established. 1 (2%) patient had a transient headache, which was not the reason for drug withdrawal. No other adverse reactions were reported.
Conclusion: a four-week monotherapy with the Russian medication called candesartan (Angiakand) at a dose of 16 mg/day in middle-aged patients with uncomplicated uncontrolled AH of 1–2 st. is accompanied by a significant decrease in both peripheral and central systolic and diastolic blood pressure and pulse pressure, differing in the high safety profile.
Key words: cardiovascular diseases, arterial hypertension, arterial stiffness, renin-angiotensin-aldosterone system, RAАS, RAAS blockers, Angiakand.
For citation: Kobalava Zh.D., Shavarova E.K., Khromova I.A. The antihypertensive efficacy of candesartan monotherapy in patients with uncomplicated arterial hypertension // RMJ. 2018. № 11(I). P. 2–6.
В статье представлены результаты оригинального исследования, посвященного антигипертензивной эффективности монотерапии кандесартаном у пациентов с неосложненной артериальной гипертонией. Показано, что 4-недельная монотерапия кандесартаном в дозе 16 мг/сут сопровождается значимым снижением АД и отличается высоким профилем безопасности.
Содержание статьи
Введение
Артериальная гипертония (АГ) остается основным модифицируемым фактором риска ряда сердечно-сосудистых заболеваний (ССЗ) и смерти от всех причин во всем мире [1–3]. Несмотря на очевидные успехи в диагностике и лечении АГ в течение последних трех десятилетий, связанное с АГ количество утраченных лет жизни с поправкой на длительность инвалидизации (индекс DALY) увеличилось с 1990 г. на 40% [4].
Один из ключевых механизмов развития АГ заключается в активации ренин-ангиотензин-альдостероновой системы (РААС), регулирующей водно-электролитный обмен [5]. Блокаторы рецепторов ангиотензина-II (БРА) наряду с ингибиторами ангиотензин-превращающего фермента (АПФ) являются наиболее широко используемыми антигипертензивными средствами [6, 7]. В сравнении с другими классами антигипертензивных препаратов при сопоставимой эффективности в предотвращении сердечно-сосудистых исходов и смерти [8, 9] терапия БРА ассоциируется с меньшей частотой прекращения лечения вследствие побочных реакций [10].
Многие антигипертензивные препараты доступны на фармацевтическом рынке в виде генериков. Одобрение к использованию генерические препараты получают, как правило, на основании результатов одного-двух фармакокинетических исследований биоэквивалентности с оригинальным антигипертензивным препаратом в группах практически здоровых добровольцев. Однако абсорбция и биодоступность лекарственных средств у лиц с АГ, относящихся к более старшей возрастной категории, может отличаться от таковых у здоровых добровольцев, что ставит правомочный вопрос о терапевтической эквивалентности генерического препарата [11, 12].
Целью нашего исследования явилась оценка антигипертензивного эффекта и безопасности препарата Ангиаканд («Канонфарма продакшн», Россия) у пациентов с неосложненной неконтролируемой АГ.
Материал и методы
В открытое одноцентровое исследование эффективности и безопасности 4-недельной терапии кандесартаном были включены 54 пациента с неосложненной ранее не леченной или неконтролируемой на фоне монотерапии блокатором РААС АГ I–II степени, обратившиеся за амбулаторной помощью. Критериями исключения являлись вторичная АГ, инфаркт миокарда, инсульт, сердечная недостаточность II–IV функционального класса (по классификации NYHA), декомпенсированный сахарный диабет, скорость клубочковой фильтрации (СКФ) 2, рассчитанная по формуле CKD-EPI; тяжелая печеночная недостаточность, противопоказания к назначению исследуемого препарата.
Средний возраст обследованных составил 55 лет, клинико-демографическая характеристика группы представлена в табл. 1.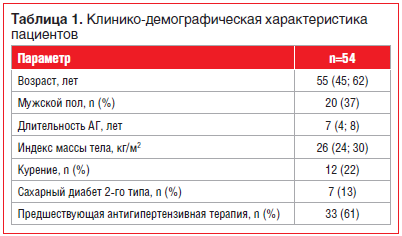
Спектр предшествующих антигипертензивных препаратов в обследованной группе был представлен следующими группами препаратов: β-адреноблокаторы — 3 (6%), антагонисты кальция дигидропиридинового ряда — 6 (11%), тиазидные диуретики — 7 (13%), блокаторы РААС — 17 (31%) пациентов. Из сопутствующей терапии допускалось применение гиполипидемических препаратов. Все пациенты с сахарным диабетом в качестве перорального сахароснижающего препарата получали метформин.
Для измерения клинического артериального давления (АД) и частоты сердечных сокращений (ЧСС) использовался валидированный полностью автоматический осциллометрический прибор для измерения АД на плече «OMRON 705CP-II» (Япония). АД измерялось троекратно в утренние часы до приема антигипертензивных препаратов после 10-минутного отдыха в положении сидя на доминантной руке, за уровень АД на данном визите принималось среднее трех измерений.
Всем выполнялся биохимический анализ крови (калий, натрий, хлор, магний, креатинин, мочевая кислота). Для контроля среднего суточного, дневного и ночного уровня АД проводилось суточное мониторирование АД (СМАД) в амбулаторных условиях (Bplab, ООО «Петр Телегин», Нижний Новгород, Россия). Использовали стандартную методику, при которой автоматическая регистрация АД осуществлялась с интервалом 15 мин днем (с 7 до 23 часов) и 30 мин ночью (с 23 до 7 часов). Структурно-функциональные параметры миокарда оценивались при двухмерной эхокардиографии (ЭХО-КГ) с допплеровским режимом и одновременной регистрацией ЭКГ (аппарат «VIVID 7», GE, США).
Измерение центрального давления и скорости каротидно-бедренной пульсовой волны осуществлялось методом аппланационной тонометрии с помощью системы «SphygmoCor» (Atcor, Австралия) в утренние часы до приема антигипертензивных препаратов после 10-минутного отдыха в положении лежа. Датчиком Millar регистрировали пульсовую волну на лучевой артерии, которая с использованием трансформирующей функции программного обеспечения прибора преобразовывалась в кривую центрального давления в аорте. Скорость пульсовой волны (СПВ) измерялась путем последовательной регистрации пульсовой волны на сонной и бедренной артериях параллельно с записью ЭКГ в 3-х отведениях. На каждом визите проводилось не менее двух измерений, в последующем полученные данные усреднялись.
Все лабораторно-инструментальные исследования выполнялись до начала исследования и через месяц после лечения. Дополнительно через неделю проводился контроль клинического АД и ЧСС.
Антигипертензивная монотерапия, которую исходно получали 24 (60%) пациента, отменялась, как минимум, за 2 нед. до начала исследования. Условием включения было наличие АГ II степени у лиц, не получающих лечения, или I–II степени у пациентов, находящихся на терапии. Всем пациентам на первом визите назначалась стартовая терапия кандесартаном (препарат Ангиаканд, «Канонфарма продакшн», Россия) в дозе 16 мг/сут. Исследуемый препарат рекомендовался к приему 1 р./день утром. В случае если через неделю приема Ангиаканда на визите фиксировалось АД выше 180/110 мм рт. ст., пациент исключался из исследования с последующей коррекцией антигипертензивной терапии.
Приверженность терапии оценивлась путем прямого вопроса о приеме исследуемого препарата и подсчета таблеток.
Доля пациентов, достигших целевого среднесуточного АД через 4 нед. терапии, являлась основным критерием эффективности терапии. Безопасность терапии оценивали по количеству нежелательных явлений, возникших после приема первой дозы препарата и приведших к прекращению приема препарата, и по количеству клинически значимых нежелательных явлений.
Исследование было одобрено этическим комитетом Медицинского института ФГАОУ ВО «Российский университет дружбы народов».
Статистическую обработку данных проводили с использованием пакета прикладных программ Statistica, версия 8.0, с применением стандартных алгоритмов статистики. Данные представлены в виде медианы (Me) и межквартильного интервала (IQR). В связи с ненормальным распределением данных при сравнении средних значений использовали непараметрический критерий Манна — Уитни, для сравнения зависимых переменных использовали критерий Вилкоксона. Качественные переменные описаны абсолютными (n) и относительными (%) значениями. Для сравнения частот признаков и качественных переменных пользовались критерием Пирсона хи-квадрат (χ2). Различия средних величин и корреляционные связи считали достоверными при р
Результаты исследования
Исследуемая группа пациентов характеризовалась преобладанием женщин, принадлежностью к средней возрастной категории, 33 (61%) пациента имели анамнез предшествующей антигипертензивной терапии, индекс массы тела (ИМТ) >25 кг/м2 был у 32 (59%) больных (см. табл. 1).
Динамика периферического артериального давления
Исходно медиана клинического систолического АД (САД) составила 153 мм рт. ст., диастолического АД (ДАД) — 95 мм рт. ст. Через неделю наблюдался отчетливый клинический эффект (медиана САД/ДАД 145 (133; 150) / 91 (86; 95) мм рт. ст.). У одного пациента через неделю на визите САД превышало 180 мм рт. ст., в связи с чем он был исключен из исследования.
Через 4 нед. антигипертензивной терапии наблюдалось достоверное снижение медианы САД/ДАД до 138/88 мм рт. ст. (р
При анализе среднесуточного индекса АД отмечалось снижение доли нон-дипперов после 4-х недель терапии — с 14 (26%) до 8 (15%) пациентов (р>0,05).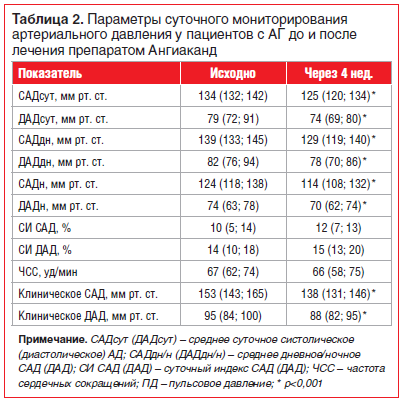
Оценка центральных гемодинамических эффектов
На фоне 4-недельной терапии кандесартаном отмечалось значимое снижение центрального САД (цСАД), ДАД (цДАД) и центрального пульсового давления (цПД). Исходное значение цСАД было 141, ДАД — 92, ПД — 48 мм рт. ст. Динамика САД, ДАД, ПД в аорте представлена в таблице 3.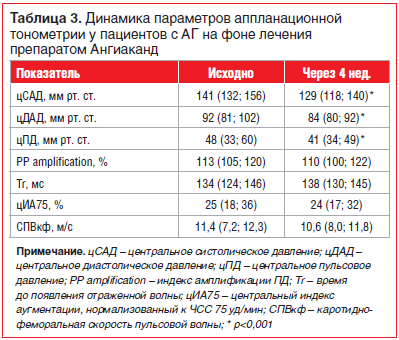
Достоверной динамики параметров, характеризующих отраженную волну, не было выявлено, так же как и индекса амплификации ПД и скорости каротидно-феморальной пульсовой волны.
Хотя 4-недельная терапия кандесартаном не оказала значимого влияния на показатели ЭХО-КГ (табл. 4), тем не менее у 2 (4%) пациентов исчезли признаки диастолической дисфункции ЛЖ.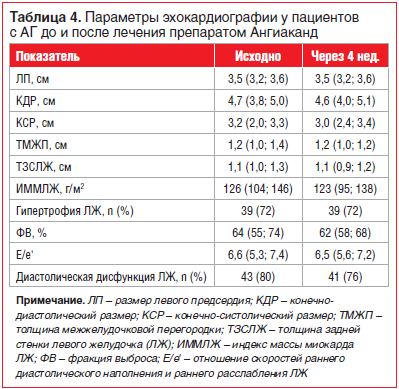
Оценка безопасности и приверженности терапии с использованием кандесартана
Динамика лабораторных параметров представлена в таблице 5. Назначение кандесартана не оказало существенного влияния на функциональное состояние почек и уровень электролитов.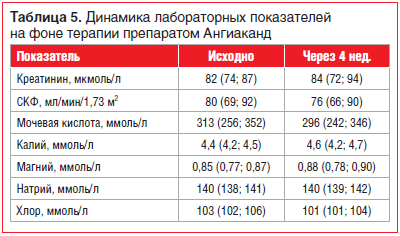
Из побочных реакций у 1 (2%) пациента в течение первой недели терапии отмечалась преходящая неинтенсивная головная боль, которая не послужила поводом для отмены препарата. Приверженность терапии составила 94 (90; 96)%.
Обсуждение
Демонстрация биоэквивалентности генерических препаратов предполагает их терапевтическую эффективность. С точки зрения эффективности антигипертензивной терапии всегда рассматриваются степень снижения АД и уменьшение частоты неблагоприятных сердечно-сосудистых исходов. Хотя подавляющее большинство рандомизированных клинических исследований (РКИ) было выполнено с использованием оригинальных, а не генерических лекарственных препаратов, все же в некоторых РКИ применялись и те и другие. А. Kesselheim et al. выполнили большой систематический метаанализ, включавший 47 исследований (из которых 38 (81%) были РКИ), с целью сравнения конечных точек клинической эффективности и безопасности оригинальных и генерических препаратов для лечения ССЗ [13]. Анализ результатов РКИ не установил преимуществ оригинальных лекарственных препаратов над генерическими. Следует подчеркнуть, что метаанализ включал такие классы препаратов, как β-адреноблокаторы, антагонисты кальция, диуретики, блокаторы РААС, дезагреганты, статины, α-адреноблокаторы и даже варфарин, имеющий узкое терапевтическое окно. Исследователи сделали вывод, что клиницистам и пациентам следует рассматривать утвержденные FDA (Food and Drug Administration — Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (США)) критерии биоэквивалентности генерических препаратов как охватывающие и их терапевтическую эквивалентность.
M. Paz et al., используя ресурс центрального Кокрейновского регистра контролируемых исследований, выполнили метаанализ, включавший 94 305 пациентов из 208 двойных слепых РКИ как минимум с 8-недельным периодом наблюдения. Целью метаанализа являлась оценка антигипертензивного эффекта как монотерапии, так и комбинированного лечения [14]. Средний возраст больных с АГ составил 54,5 года, из них 55% были мужчины, среднее САД/ДАД — 155/99 мм рт. ст., сахарный диабет выявлен у 11%. Согласно полученным данным монотерапия сопровождалась в среднем снижением клинического САД на 10–15 мм рт. ст., ДАД — на 8–10 мм рт. ст. Монотерапия кандесартаном, назначавшимся в средней дозе 16,3 мг/сут, приводила к снижению САД на 13,8 (15,4; 12,3), а ДАД — на 8,9 (18,8; 3,5) мм рт. ст. При этом женский пол и ИМТ >25 кг/м2 ассоциировались с более выраженным снижением как САД, так и ДАД.
В нашем исследовании, где женщин было больше,
в т. ч. с избыточной массой тела, величина снижения клинического АД составила 15 мм рт. ст. для САД и 7 мм рт.ст. для ДАД, что соотносится с данными метаанализа
Paz M. et al.
В последних рекомендациях по лечению АГ (2018) представлена новая концепция более широкого использования СМАД наряду с домашним мониторированием АД с целью не только диагностики, но и контроля АГ [15]. СМАД обладает более высокой предсказательной ценностью в отношении поражения органов-мишеней, чем клиническое (офисное) измерение АД [16], является более чувствительным, чем офисное АД, и результаты измерения АД, полученные при суточном мониторировании, считаются лучшим предиктором коронарных событий, инсульта и фатальных исходов [17–21].
По данным Ирландского исследования, при обращении за амбулаторной первичной медицинской помощью лишь 12% пациентов достигали целевого АД по данным офисного измерения АД и более 1/3 больных по данным СМАД [22]. Анализ Испанской медицинской базы данных, включавшей 700 000 пациентов с АГ пожилого возраста, продемонстрировал, что среди леченых пациентов доля достигших целевого АД, также возрастала с 37% по данным офисного измерения АД до 54% по данным СМАД [23]. В нашем исследовании, особенностью которого было превалирование больных среднего возраста, 36 (68%) пациентов достигли целевого АД по данным СМАД, что на 7% выше, чем по данным клинического АД через 4 нед. терапии кандесартаном, при этом различия между двумя методиками были статистически недостоверны.
В ряде исследований и метаанализах было показано, что у пациентов с АГ центральное АД более тесно взаимосвязано с сердечно-сосудистыми событиями, чем периферическое АД, а степень влияния различных классов антигипертензивных препаратов на центральное АД варьирует [24]. В нашей работе лечение кандесартаном сопровождалось достоверным снижением цСАД, цДАД и цПД на 12, 8 и 7 мм рт. ст. соответственно. При этом мы не обнаружили значимой динамики параметров отраженной волны и СПВ, так же как и показателей
ЭХО-КГ. В исследовании Spratt J. et al. у пациентов с АГ (n=35), получавших в течение 24 нед. терапию кандесартаном в качестве монотерапии или в комбинации с гидрохлортиазидом, наряду со снижением центрального АД отмечалось также снижение центрального индекса аугментации на 9% (р
Короткая длительность наблюдения (4 нед.) является существенным ограничением нашего исследования, которая, возможно, не позволила развиться терапевтическим эффектам кандесартана в отношении прямых и косвенных параметров артериальной ригидности, показателей диастолической функции ЛЖ, гипертрофии ЛЖ.
При высокой приверженности терапии кандесартаном (94%) в нашем исследовании побочная реакция в виде головной боли развилась лишь у 1 (2%) пациента. В исследовании X–CELLENT, сравнивавшем эффективность и безопасность 12-недельной терапии индапамидом (1,5 мг/сут), кандесартаном (8 мг/сут) и амлодипином (5 мг/сут) у пациентов с систоло-диастолической и изолированной систолической АГ (n=1758), частота нежелательных эффектов при назначении кандесартана (n=435) не превышала 5,1%, при этом головная боль была наиболее частой побочной реакцией — у 1,6% пациентов [26]. В этом исследовании в качестве вторичного критерия эффективности оценивался комбинированный антигипертензивный ответ на терапию, определявшийся как достижение целевого клинического АД
Заключение
Четырехнедельная монотерапия российским препаратом кандесартана Ангиаканд в дозе 16 мг/сут у пациентов среднего возраста с неосложненной неконтролируемой АГ I–II степени приводит к значимому снижению как периферического, так и центрального САД, ДАД и ПД и отличается высоким профилем безопасности.
Литература
1. Chow C. K., Teo K. K., Rangarajan S. et al. PURE Study Investigators. Prevalence, awareness, treatment, and control of hypertension in rural and urban communities in high-, middle-, and low-income countries // JAMA 2013. Vol. 310. P.959–968.
2. Falaschetti E., Mindell J., Knott C., Poulter N. Hypertension management in England: a serial cross-sectional study from 1994 to 2011. Lancet // 2014. Vol. 383. P.1912–1919.
3. Tocci G., Rosei E. A., Ambrosioni E. et al. Blood pressure control in Italy: analysis of clinical data from 2005–2011 surveys on hypertension // J Hypertens 2012. Vol. 30. P.1065–1074.
4. Forouzanfar M. H., Liu P., Roth G. A. et al. Global burden of hypertension and systolic blood pressure of at least 110 to 115 mm Hg, 1990–2015 // JAMA 2017. Vol. 317. P.165–182.
5. Atlas S. A. The renin-angiotensin aldosterone system: pathophysiological role and pharmacologic inhibition // J Manag Care Pharm. 2007. Vol. 13. P.9–20.
6. Кобалава Ж. Д., Шаварова Е. К. Место антагонистов рецепторов к ангиотензину II в современных рекомендациях // РМЖ. 2008. № 16 (11). C.1609–1616 [Kobalava Zh.D., Shavarova E. K. Mesto antagonistov receptorov k angiotenzinu II v sovremennyh rekomendaciyah // RMJ. 2008. № 16 (11). C.1609–1616 (in Russian)].
7. Кобалава Ж. Д., Шаварова Е. К. Антагонисты рецепторов ангиотензина II в кардиологической клинике: современный взгляд на проблему // Журнал «Сердце» 2008. № 7 (4). С. 34–39 [Kobalava Zh.D., SHavarova E. K. Antagonisty receptorov angiotenzina II v kardiologicheskoj klinike: sovremennyj vzglyad na problemu // Zhurnal «Serdce» 2008. № 7 (4). S.34–39 (in Russian)].
8. Thomopoulos C., Parati G,. Zanchetti A. Effects of blood pressure-lowering on outcome incidence in hypertension: 5. Head-to-head comparisons of various classes of antihypertensive drugs — overview and meta-analyses // J Hypertens 2015. Vol. 33. P.1321–1341.
9. Ettehad D., Emdin C. A., Kiran A. et al. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis // Lancet 2016. Vol. 387. P.957–967.
10. Kronish I. M., Woodward M., Sergie Z. et al. Meta-analysis: impact of drug class on adherence to antihypertensives // Circulation. 2011. Vol. 123. P.1611–1621.
11. Carter B. L. Equivalence of generic and brand-name drugs for cardiovascular disease (Letter) // JAMA. 2009. Vol. 301. P.1654.
12. Meredith P. A. Potential concerns about generic substitution: Bioequivalence versus therapeutic equivalence of different amlodipine salt forms // Curr Med Res Opin. 2009. Vol. 25. P.2179–2189.
13. Kesselheim A. S., Misono A. S., Lee J. L. et al. Clinical equivalence of generic and brand-name drugs used in cardiovascular disease: a systematic review and meta-analysis // JAMA. 2008. Vol. 300. P.2514–2526.
14. Paz M. A., de-La-Sierra A., Saez M. et al. Treatment efficacy of anti-hypertensive drugs in monotherapy or combination: ATOM systematic review and meta-analysis of randomized clinical trials according to PRISMA statement // Medicine (Baltimore). 2016. Vol. 95 (30). e4071.
15. Williams B., Mancia G., Spiering W. et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension // Eur Heart J. 2018. Vol. 39 (33). P.3021–3104.
16. Gaborieau V., Delarche N., Gosse P. Ambulatory blood pressure monitoring versus self-measurement of blood pressure at home: correlation with target organ damage // J Hypertens. 2008. Vol. 26. P.1919–1927.
17. Banegas J. R., Ruilope L. M., de la Sierra A. et al. Relationship between clinic and ambulatory blood-pressure measurements and mortality // N Engl J Med 2018. Vol. 378. P.1509–1520.
18. Investigators A. B.C.–H., Roush G. C. et al. Prognostic impact from clinic, daytime, and night-time systolic blood pressure in nine cohorts of 13,844 patients with hypertension // J Hypertens. 2014. Vol. 32. P.2332–2340; discussion 2340.
19. Fagard R. H., Celis H., Thijs L. et al. Daytime and nighttime blood pressure as predictors of death and cause-specific cardiovascular events in hypertension // Hypertension. 2008. Vol. 51. P.55–61.
20. Parati G., Ochoa J. E., Bilo G. et al. European Renal and Cardiovascular Medicine Working Group of the European Renal Association-European Dialysis and Transplant Association. Hypertension in chronic kidney disease part 2: role of ambulatory and home blood pressure monitoring for assessing alterations in blood pressure variability and blood pressure profiles // Hypertension 2016. Vol. 67. P.1102–1110.
21. Piper M. A., Evans C. V., Burda B. U. et al. Diagnostic and predictive accuracy of blood pressure screening methods with consideration of rescreening intervals: a systematic review for the U. S. Preventive Services Task Force // Ann Intern Med. 2015. Vol. 162. P.192–204.
22. Uallachain G. N., Murphy G., Avalos G. The RAMBLER study: the role of ambulatory blood pressure measurement in routine clinical practice: a cross-sectional study // Ir Med J. 2006. Vol. 99. P.276–279.
23. Banegas J. R., De La Cruz J. D., Graciani S. et al. Impact of ambulatory blood pressure monitoring on reclassification of hypertension prevalence and control in older people in Spain // J Clin Hyperten. 2015. Vol. 17. P.453–461.
24. Williams B., Lacy P. S., Thom S. M. et al. CAFE Investigators, Anglo-Scandinavian Cardiac Outcomes Trial Investigators, CAFE Steering Committee and Writing Committee. Differential impact of blood pressure-lowering drugs on central aortic pressure and clinical outcomes: principal results of the Conduit Artery Function Evaluation (CAFE) study // Circulation. 2006. Vol. 113. P.1213–1225.
25. Spratt J. C.S., Webb D. J., Shiels A., Williams B. Effects of candesartan on cardiac and arterial structure and function in hypertensive subjects // JRAAS. 2001. Vol. 2. P.227–232.
26. London G., Schmieder R., Calvo C., Asmar R. Indapamide SR Versus Candesartan and Amlodipine in Hypertension: The X–CELLENT Study // Am J Hypertens. 2006. Vol. 19. P.113–121.
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
Информация с rmj.ru




