Содержание статьи
Введение
Сахарный диабет (СД) — это группа метаболических заболеваний, проявляющихся хронической гипергликемией, возникающей в результате инсулинорезистентности (ИР) или относительной инсулиновой недостаточности [1].
Наиболее распространенными формами являются СД 1 типа и 2 типа. СД 1 типа характеризуется абсолютной недостаточностью инсулина, в связи с чем основным лечением данного заболевания является заместительная инсулинотерапия. СД 2 типа — это многофакторное заболевание. К основным звеньям его патогенеза относят развитие ИР, дисфункцию α- и β-клеток поджелудочной железы (ПЖ), нарушение инкретинового ответа, парадоксальную реабсорбцию глюкозы в почках и др. Лечение СД 2 типа осуществляется преимущественно пероральными сахароснижающими препаратами (ПССП), действие которых основано на коррекции основных звеньев патогенеза данного заболевания [1].
Существуют формы диабета, обладающие признаками как 1 типа, так и 2 типа. К таким формам относят латентный аутоиммунный диабет взрослых (latent autoimmune diabetes mellitus in adults, LADA), диабет взрослого типа у молодых (Maturity-onset diabetes of the young, MODY) и некоторые другие [2]. В отличие от LADA, имеющего собственные критерии постановки диагноза, MODY представляет собой гетерогенную группу заболеваний, объединенных общими признаками. К ним относят аутосомно-доминантный тип наследования, начало в молодом возрасте (до 25–30 лет), отсутствие аутоантител — маркеров СД 1 типа, сохранную эндогенную секрецию инсулина на протяжении длительного времени (отсутствие кетоацидоза (КА) в дебюте заболевания, стабильный уровень С-пептида в течение многих лет) [1, 3]. Однако низкий процент подтверждения случаев MODY (около 2–3%) свидетельствует о том, что вышеописанные признаки не являются критериями для постановки диагноза [4]. Более того, эти признаки не являются специфичными для MODY, т. к., по данным Chambers et al., пациентам с MODY в 76% случаев выставляется диагноз «СД 1 типа» и в 15% случаев — «СД 2 типа», несмотря на наличие у пациентов комплекса характеристик, свойственных MODY [5]. Таким образом, единственно достоверным методом диагностики MODY является молекулярно-генетическое тестирование [6, 7].
Для принятия решения о необходимости генетического тестирования следует уметь выделять нетипичные признаки течения СД, помогающие провести дифференциальную диагностику между редкими формами диабета и заподозрить у пациента MODY [7]. Дифференциально-диагностический поиск MODY представлен в данном клиническом наблюдении.
Клиническое наблюдение
Пациент К., 30 лет, родом из Нигерии, поступил в эндокринологическое отделение ГБУЗ «ГКБ им. В.П. Демихова ДЗМ» с жалобами на повышение уровня глюкозы в крови до 18 ммоль/л, общую слабость, повышенную утомляемость, сухость во рту, жажду, учащенное мочеиспускание, снижение остроты зрения в течение нескольких последних месяцев.
Анамнез заболевания
Несмотря на то, что пациент отмечал учащение мочеиспускания с детского возраста, диагноз «СД 2 типа» был поставлен только около 7 лет назад. Тогда уровень гликемии натощак составлял 13 ммоль/л. С целью коррекции уровня глюкозы в крови эндокринологом по месту жительства был рекомендован прием метформина 1000 мг утром и вечером. Однако пациент принимал препарат нерегулярно: при учащении мочеиспускания, появлении сухости во рту. Около 5 лет назад в связи с повышением уровня глюкозы до 18 ммоль/л натощак проводилось лечение препаратом сульфонилмочевины (ПСМ), название и дозу препарата не помнит. После приема ПСМ возникали симптомы гипогликемии: внутренняя дрожь, слабость, чувство голода, в связи с чем в период с 2016 по 2019 г. пациент принимал ПССП эпизодически — при появлении учащенного мочеиспускания и сухости во рту.
Ухудшение состояния — с сентября 2019 г., отмечались подъемы уровня глюкозы до 20–22 ммоль/л. Из-за выраженного повышения уровня глюкозы в крови и появления жалоб на сухость во рту, жажду, частое мочеиспускание пациент ежедневно принимал метформин в дозе 1000 мг дважды в день. На этом фоне отмечались колебания гликемии от 10 до 18 ммоль/л.
Уровень глюкозы в крови контролирует по глюкометру 1 раз в 3–4 дня в разное время. Симптомы гипогликемии возникали при снижении уровня глюкозы в крови менее 3,5 ммоль/л через 1–3 ч после приема ПСМ и метформина (при развитии гипергликемии принимал от 3 до 8 таблеток препаратов, их дозу назвать не может). Диету с исключением потребления легкоусваиваемых углеводов и ограничением потребления медленных углеводов не соблюдает. Со слов, наследственность отягощена по материнской линии: у бабушки СД выявлен в возрасте 30–32 лет, у матери — с 27 лет. Тип диабета неизвестен. Мать постоянно принимает гликлазид с модифицированным высвобождением и метформин (дозы препаратов выяснить не удалось). На этом фоне гликемия от 7 до 16 ммоль/л.
Со слов пациента, с 2017 г. у него хронический панкреатит. В 2017 и 2018 гг. отмечались два эпизода обострения хронического панкреатита на фоне алкогольной интоксикации, которые проявлялись тошнотой, рвотой, болями в животе, повышением температуры тела до 38,5 °C, по поводу чего пациент госпитализировался в хирургическое отделение по месту жительства, где проводилось лечение: диетотерапия и медикаментозная терапия (название препаратов не помнит).
Поступил в эндокринологическое отделение ГБУЗ «ГКБ им. В.П. Демихова ДЗМ» самотеком в связи с декомпенсацией углеводного обмена.
Результаты обследования
Физикальное обследование. Общее состояние удовлетворительное. Конституция нормостеническая. Рост — 174 см, вес — 75 кг, индекс массы тела (ИМТ) — 24,8 кг/м2 (норма). Кожные покровы чистые, умеренно влажные. Подкожная жировая клетчатка развита удовлетворительно, распределена равномерно. В легких дыхание везикулярное, хрипов нет. Тоны сердца ясные, ритмичные. АД — 120/76 мм рт. ст., ЧСС — 70 уд/мин. Живот при пальпации мягкий, безболезненный. Печень пальпируется по краю реберной дуги, безболезненна. Стул — регулярный, оформленный. Мочеиспускание — свободное, симптом поколачивания — отрицательный с обеих сторон.
По данным лабораторных исследований от 02.02.2020: холестерин общий — 7,7 ммоль/л, триглицериды — 1,04 ммоль/л, что указывает на наличие дислипидемии. Уровень гликированного гемоглобина (HbA1c) — 8,8%, что свидетельствует о декомпенсации углеводного обмена. Антитела (АТ) к β-клеткам ПЖ — титр менее 1:4 (результат отрицательный). Инсулин — 3,1 мкЕД/мл (норма — 2,7–10,4 мкЕД/мл), С-пептид — 1,2 нг/мл (норма — 1,1–4,4 нг/мл). В общем анализе мочи от 02.02.2020: глюкозурия — 58 ммоль/л, кетоновые тела не обнаружены.
Дифференциально-диагностический поиск типа диабета
С учетом нетипичного течения СД и анамнестических данных (двукратное обострение хронического панкреатита на фоне алкогольной интоксикации) проводилась дифференциальная диагностика между основными типами СД (1 типа и 2 типа) и редкими формами (LADA, MODY, панкреатогенный СД).
Постепенное бессимптомное развитие заболевания, отягощенный семейный анамнез по материнской линии, наличие дислипидемии, отрицательный титр АТ к β-клеткам ПЖ (аутоантитела к транспортеру цинка, тирозинфосфатазе 2, инсулину, глутаматдекарбоксилазе не исследовались) позволяют заподозрить наличие СД 2 типа. Однако этот тип СД характеризуется выраженной ИР на фоне избыточной массы тела, а также гиперинсулинемией [2]. В связи с тем, что, по данным лабораторных исследований, отмечаются низконормальные значения инсулина (3,1 мкЕД/мл) и С-пептида (1,2 нг/мл) в крови на фоне нормального ИМТ (24,8 кг/м2), диагноз «СД 2 типа» маловероятен.
В отличие от пациентов с традиционным СД 2 типа, пациенты с панкреатогенным СД, как правило, худощавого телосложения. У них отмечается легкое течение заболевания, что объясняется низкой потребностью в инсулине из-за имеющегося синдрома мальабсорбции на фоне недостаточности внешнесекреторной функции ПЖ. Склонность к гипогликемическим состояниям у данной когорты пациентов обусловлена дисфункцией α-клеток ПЖ и снижением секреции глюкагона [2, 8]. Таким образом, при панкреатогенном СД гипергликемические эпизоды сменяются относительной гиперинсулинемией, что клинически проявляется развитием гипогликемических событий. При этом гипогликемии развиваются преимущественно натощак [8].
У данного пациента имеются эпизоды обострений хронического панкреатита в анамнезе и возникают гипогликемические эпизоды на фоне проводимой сахароснижающей терапии, поэтому клиника заболевания напоминает течение панкреатогенного СД. Однако данный диагноз маловероятен из-за отсутствия обострений хронического панкреатита на фоне несоблюдения диетического дробного питания в течение последних 2 лет. Единичные эпизоды гипогликемий объясняются передозировкой ПСМ.
Классическими признаками проявления СД 1 типа являются острое начало заболевания, развитие КА и симптомов метаболической декомпенсации, которые молниеносно прогрессируют при отсутствии лечения и быстро исчезают при инициировании заместительной инсулинотерапии [2]. Прием ПССП на фоне абсолютной инсулиновой недостаточности ассоциирован с развитием и прогрессированием кетоацидотического состояния. Наиболее достоверным критерием подтверждения СД 1 типа является выявление в крови АТ к β-клеткам ПЖ, глутаматдекарбоксилазе, тирозинфосфатазе 2, инсулину, транспортеру цинка. Именно образование указанных АТ определяет развитие данного заболевания [1]. Отсутствие АТ к β-клеткам ПЖ у пациента К. не исключает диагноз «СД 1 типа» [3, 9] в связи с тем, что другие типы АТ, подтверждающие диагноз, не исследовались. Однако в данном клиническом случае диагноз «СД 1 типа» носит маловероятный характер в связи с постепенным развитием и медленным прогрессированием заболевания, отсутствием развития КА на фоне приема ПССП, наличием низконормальных значений инсулина (3,1 мкЕД/мл) и С-пептида (1,2 нг/мл) в крови через 7 лет после дебюта заболевания.
Патогенетически схожим с СД 1 типа заболеванием является LADA. Также в диагностический поиск включен LADA в связи с наличием комплекса признаков, соответствующих критериям данного патологического состояния: нормальной массы тела, отсутствия КА в дебюте заболевания, длительного малосимптомного течения. Однако для LADA характерно постепенное, очень медленное развитие абсолютного дефицита инсулина, что лабораторно проявляется прогрессивным снижением уровней С-пептида и инсулина в крови [10]. При анализе клинико-лабораторные данных пациента обращает на себя внимание наличие низконормальных показателей инсулина и С-пептида в крови на фоне длительного течения заболевания, что ставит под сомнение диагноз LADA. Более того, у пациента имеются родственники первой линии родства, имеющие СД. Отягощенная наследственность нетипична для LADA (так же как и для СД 1 типа), ее наличие скорее указывает на СД 2 типа или MODY [10].
Роль наследственности при MODY подтверждается в исследовании Heuvel-Borsboom et al., по данным которого отягощенный семейный анамнез по MODY-3 увеличивает вероятность развития заболевания на 50% [11]. По данным Misra et al., наиболее часто MODY встречается в африканско-карибских, британских и южноазиатских этнических группах [12]. Таким образом, с учетом африканского происхождения (Нигерия), негроидной расы, анамнестических данных (отягощенный семейный анамнез по материнской линии), дебюта СД в молодом возрасте, отсутствия избыточной массы тела, отсутствия развития КА в дебюте заболевания и на фоне терапии ПССП, низконормальных показателей С-пептида и инсулина в крови на фоне длительного течения заболевания у пациента заподозрено наличие MODY. Более того, с учетом выраженной глюкозурии по данным общего анализа мочи, анамнестических данных (наличие учащенного мочеиспускания в течение длительного времени до постановки диагноза СД и назначения ПССП) у пациента заподозрен подтип 3 MODY. Для подтверждения данного диагноза пациент направлен на молекулярно-генетическое исследование (секвенирование панели AS 468 «Сахарный диабет-гиперинсулинизм» 27 генов) в ФГБУ «НМИЦ эндокринологии» Минздрава России.
Клинический диагноз. Основное заболевание: E11.8 Инсулинонезависимый сахарный диабет с неуточненными осложнениями. Сопутствующие заболевания: Дислипидемия. Хронический панкреатит вне обострения.
Проводимое лечение
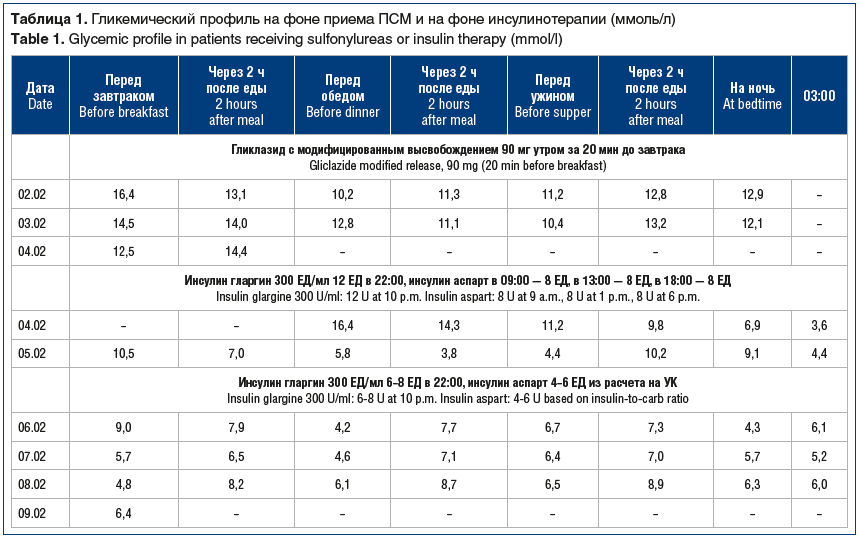
С целью коррекции показателей гликемии проводилась пробная терапия ПСМ на фоне исключения потребления легкоусваиваемых углеводов и ограничения потребления медленных углеводов. Несмотря на то, что при лечении пациентов с 3-им подтипом MODY отдается предпочтение терапии ПСМ [1, 13], на фоне приема гликлазида с модифицированным высвобождением 90 мг/сут у пациента К. достижения целевых показателей гликемии не отмечалось (табл. 1). Было принято решение о переводе пациента на базис-болюсную инсулинотерапию. Из расчета суточной потребности базального инсулина на основании массы тела пациенту был назначен инсулин гларгин 300 ЕД/мл в дозе 18 ЕД в 22:00. Также был назначен инсулин аспарт (углеводный коэффициент (УК) = 1 хлебная единица (ХЕ)): 2 ЕД перед завтраком, 1 ХЕ: 1,5 ЕД перед обедом и 1 ХЕ: 1 ЕД перед ужином (см. табл. 1).
В связи с развитием эпизодов гипогликемий на фоне проводимой инсулинотерапии в отделении проводилась коррекция терапии: доза инсулина гларгин 300 ЕД/мл была снижена до 6 ЕД в 22:00; также были подобраны УК: 1 ХЕ: 0,7 ЕД перед завтраком, 1 ХЕ: 0,5 ЕД перед обедом и ужином. На фоне коррекции инсулинотерапии отмечалось достижение околоцелевых показателей гликемии (см. табл. 1).
Заключение
Описанное клиническое наблюдение призывает обращать пристальное внимание на клинико-лабораторные проявления СД, особенно в тех случаях, когда отсутствует должная компенсация углеводного обмена на фоне проводимой сахароснижающей терапии. При выявлении у пациента нетипичных клинических и лабораторных проявлений заболевания целесообразно проанализировать возможность наличия у него редких форм диабета, в т. ч. MODY. При подозрении на наличие MODY с целью подтверждения диагноза необходимо проведение генетического тестирования — с помощью секвенирования панели AS 468 «Сахарный диабет-гиперинсулинизм» 27 генов. Верификация диагноза MODY на основании результатов, полученных при помощи молекулярно-генетического исследования, позволяет персонализированно подбирать сахароснижающую терапию, избегать необоснованного назначения инсулинотерапии и достигать лучшего гликемического контроля у таких
пациентов.
Сведения об авторах:
Лобанова Кристина Геннадьевна — ассистент кафедры эндокринологии лечебного факультета ФГАОУ ВО РНИМУ
им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-3656-0312.
Титова Виктория Викторовна — ассистент кафедры эндокринологии лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-8684-6095.
Долгова Кристина Сергеевна — клинический ординатор кафедры эндокринологии лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0001-8859-6790.
Контактная информация: Лобанова Кристина Геннадьевна, e-mail: miss.sapog@mail.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 21.07.2020, поступила после рецензирования 09.08.2020, принята в печать 17.08.2020.
About the authors:
Kristina G. Lobanova — Assistant of the Department of Endocrinology of the Medical Faculty, Pirogov Russian National Research Medical University, 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-3656-0312.
Viktoria V. Titova — Assistant of the Department of Endocrinology of the Medical Faculty, Pirogov Russian National Research Medical University, 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-8684-6095.
Kristina S. Dolgova — clinical resident of the Department of Endocrinology of the Medical Faculty, Pirogov Russian National Research Medical University, 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0001-8859-6790.
Contact information: Kristina G. Lobanova, e-mail: miss.sapog@mail.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 21.07.2020, revised 09.08.2020, accepted 17.08.2020.
.
Информация с rmj.ru





