Введение
По данным Федеральной службы государственной статистики, в 2018 г. от болезней системы кровообращения умерли 856 100 человек [1]. Одно из ведущих мест среди причин внезапных смертей от болезней системы кровообращения занимают венозные тромбоэмболические осложнения (ВТЭО), к которым относятся тромбоз глубоких вен (ТГВ), тромбоз подкожных вен и тромбоэмболия легочных артерий (ТЭЛА) [2, 3]. В РФ ежегодно регистрируется около 80 000 новых случаев ВТЭО [4]. ТЭЛА — распространенная форма ВТЭО, которая потенциально может привести к летальному исходу [2, 3]. По данным статистических отчетов Министерства здравоохранения РФ, частота развития ТЭЛА составляет 35–40 случаев на 100 000 человек [4]. Летальность при нераспознанной острой ТЭЛА — около 30% и, несмотря на совершенствование методов диагностики, сохраняется на высоком уровне [5]. В течение месяца после выявления ТГВ от легочной эмболии умирают 6% пациентов [4]. В отдаленном периоде ТГВ развивается посттромботическая болезнь нижней конечности, после перенесенной ТЭЛА формируется хроническая постэмболическая легочная гипертензия [4].
Риск возникновения ВТЭО существенно увеличивается с возрастом, а у лиц старше 75 лет — удваивается, что связано с возрастными изменениями системы гемостаза [6]. Правильная оценка рисков, использование более информативных методов диагностики, эффективная и своевременная антитромботическая терапия, адекватное следование клиническим рекомендациям в большинстве случаев позволяют предотвратить ВТЭО [7, 8].
Назначение нефракционированного или низкомолекулярного гепаринов, с последующим переводом на непрямые антикоагулянты, представляет собой базовую терапию венозных тромбоэмболических осложнений [9, 10]. Однако использование подобной схемы терапии сопряжено с трудоемким подбором дозы препарата, высоким риском нежелательных фармакокинетических и фармакодинамических лекарственных взаимодействий, а также взаимодействий с пищевыми продуктами и требует высокой комплаентности [11]. Появление прямых пероральных антикоагулянтов (ПОАК) существенно упростило антитромботическую терапию. По эффективности и безопасности они сопоставимы с варфарином [12].
Отдельного внимания заслуживают пациенты с синдромом старческой астении, или «хрупкости», поскольку применение антикоагулянтов у пациентов данной категории сопряжено с высоким риском геморрагических осложнений. Как указывают Н.М. Воробьева и соавт. [6, 13], синдром старческой астении увеличивает риск развития как тромбоза, так и кровотечения, что требует еще более взвешенного подхода при выборе препарата и его дозы. «Хрупкие» пациенты имеют сниженную массу тела, нарушение функции почек [14], что приводит к изменению фармакокинетики и фармакодинамики лекарственных средств. Пожилой и старческий возраст характеризуется полиморбидностью, что влечет за собой прием большого количества медикаментов по сравнению с пациентами среднего возраста. В свою очередь, полифармакотерапия влияет на эффективность и безопасность антитромботической терапии. Назначенная терапия не должна оставаться неизменной. Антикоагулянтную терапию необходимо регулярно пересматривать и корректировать для своевременного выявления и коррекции модифицируемых факторов риска геморрагических осложнений [14–16].
Несмотря на активное внедрение в клиническую практику ПОАК, современных исследований, посвященных прямому сравнению эффективности и безопасности данных препаратов, довольно мало. Проведение прямого сравнения ПОАК при использовании у пациентов пожилого и старческого возраста позволит выработать эффективный алгоритм выбора антикоагулянта с учетом возраста и сопутствующих заболеваний, имеющихся у пациентов.
Цель исследования: оценка частоты геморрагических осложнений у пациентов старческого возраста с перенесенным тромбозом глубоких вен, принимающих ПОАК.
Материал и методы
В исследовании приняли участие 370 пациентов старческого возраста, у которых был выявлен тромбоз в системе нижней полой вены. В зависимости от назначенных ПОАК все пациенты были рандомизированы методом последовательных номеров в 3 группы: в 1-й группе пациенты принимали апиксабан в дозе 5 мг 2 р/сут; во 2-й группе — ривароксабан в дозе 20 мг 1 р/сут; в 3-й группе — дабигатран по 150 мг 2 р/сут. Группы были сопоставимы по полу, возрасту, сопутствующей патологии, риску геморрагических осложнений. Критериями включения в исследование были: возраст старше 75 лет; клиренс креатинина не менее 50 мл/мин. Критерий исключения — наличие ограничения в общении вследствие когнитивных нарушений.
Срок наблюдения за пациентами составил 3 мес. или 6 мес. с момента начала терапии ПОАК, в зависимости от формы тромбоза (дистальная, проксимальная) и сроков назначения антикоагулянтов. Набор пациентов осуществлялся на протяжении 3 лет. С пациентами регулярно проводилось телефонное интервьюирование для оценки возникновения геморрагических осложнений и выявления случаев госпитализации пациентов. Риск кровотечений оценивали по шкале HAS-BLED (Hypertension, Abnormal renal-liver function, Stroke, Bleeding history or predisposition, Labile international normalized ratio, Elderly [65 years], Drugs or alcohol concomitantly) от 0 до 9 баллов (риск кровотечения считается высоким при оценке 3 балла и выше) [17]. Выявленные геморрагические осложнения классифицировали по методу, предложенному S. Fihn et al. [18]. Геморрагические осложнения относили к категории больших в случае возникновения забрюшинных или внутричерепных кровотечений, если возникала необходимость трансфузии компонентов крови, а также когда требовалось оперативное вмешательство. Во всех остальных случаях кровотечение относили к категории малых.
Анализ полученных результатов осуществлялся с помощью программы Microsoft Office Exсel (2011) и общедоступных статистических онлайн-калькуляторов. Клинические характеристики в группах представлены с помощью методов описательной статистики. Для оценки достоверности различий использовали U-критерий
Манна — Уитни. Различия признавали статистически значимыми при p<0,05.
Результаты и обсуждение
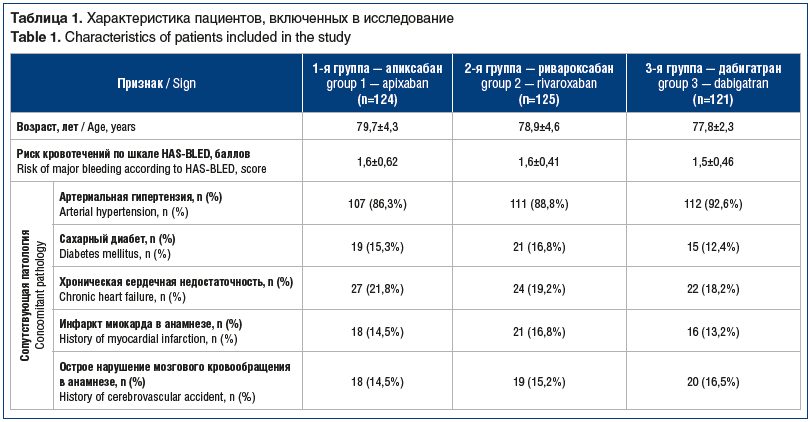
Сравнительная характеристика трех групп пациентов представлена в таблице 1. За время проведения исследования 4 пациента выбыли из исследования по причине летального исхода, не связанного с приемом антикоагулянтов. Частота осложнений в исследуемых группах за время наблюдения представлена в таблице 2.
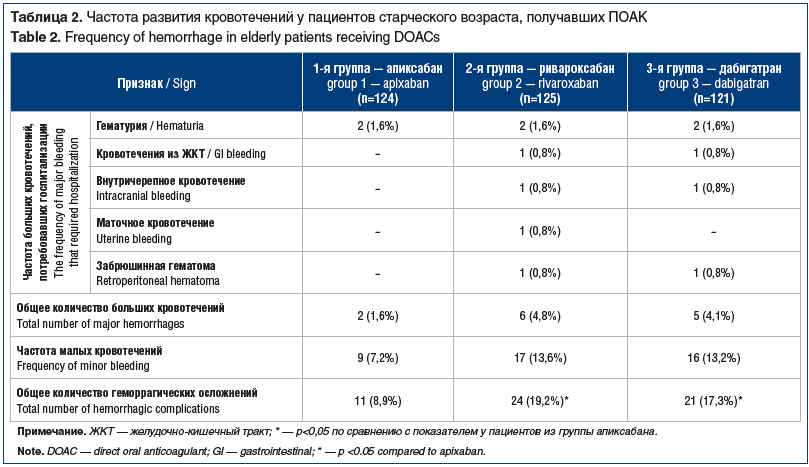
Таким образом, в группе пациентов, принимавших апиксабан, было зарегистрировано статистически значимо меньшее общее количество геморрагических осложнений в сравнении с группами, принимавшими два других ПОАК. В группе апиксабана их было на 10,3% меньше, чем в группе ривароксабана (p=0,029), и на 8,4% меньше, чем в группе дабигатрана (p=0,049). При сравнении частоты геморрагических осложнений у пациентов из групп ривароксабана и дабигатрана статистически значимых различий выявлено не было.
Полученные результаты в целом согласуются с данными по безопасности ПОАК, представленными в литературе. При непрямом сравнении безопасности ПОАК, основанном на результатах 6 исследований III фазы (RE-COVER I, RE-COVER II, EINSTEIN-DVT, EINSTEIN-PE, AMPLIFY и Hokusai-VTE), было показано, что применение апиксабана для лечения острых ВТЭО связано с более низким риском кровотечений по сравнению с применением дабигатрана, ривароксабана и эдоксабана [19]. Ранее G. Alotaibi et al. [20] установили, что при использовании апиксабана, дабигатрана или ривароксабана для профилактики рецидивов ВТЭО частота развития больших кровотечений существенно не различалась, однако апиксабан в дозе 2,5 мг 2 р/сут был связан с меньшей частотой клинически значимых малых кровотечений, чем ривароксабан (20 мг/сут) или дабигатран 150 мг 2 р/сут.
Метаанализ, выполненный с целью сравнения безопасности применения ПОАК при ВТЭО показал, что частота больших или клинически значимых кровотечений при использовании дабигатрана и ривароксабана была существенно выше, чем при использовании плацебо, тогда как при использовании апиксабана или плацебо частота больших или клинически значимых кровотечений существенно не различалась [21].
Заключение
В современном мире лечащий врач имеет в своем распоряжении богатый выбор ПОАК. Их назначение регламентировано инструкциями, а эффективность подтверждена данными рандомизированных исследований. Назначая антикоагулянты пациенту пожилого и старческого возраста, лечащий врач должен взвешивать все риски, прогнозировать и оценивать все возможные осложнения, которые могут возникнуть у пациента. Понимая особенности применения каждого препарата у пациентов разных возрастных групп, врач имеет возможность персонализировать терапию и сделать ее эффективной и безопасной. В ходе проведенного исследования апиксабан продемонстрировал более благоприятный профиль безопасности в отношении общей частоты развития геморрагических осложнений при лечении тромбоза в системе нижней полой вены в сравнении с другими ПОАК у пациентов старческого возраста. Однако необходимо отметить, что возможности использования ПОАК у «хрупких» пациентов с ВТЭО требуют дальнейшего изучения.
Сведения об авторах:
Хруслов Максим Владимирович — д.м.н., заместитель главного врача по медицинской части, начальник регионального сосудистого центра БМУ КОКБ; 305007, Россия, г. Курск, ул. Сумская, д. 45а; ORCID iD 0000-0001-9856-1284.
Пономарева Ирина Владимировна — ассистент кафедры хирургических болезней № 1 ФГБОУ ВО КГМУ Минздрава России; 305041, Россия, г. Курск, ул. Карла Маркса, д. 3; ORCID iD 0000-0003-1850-6491.
Сафронова Людмила Владимировна — заведующая хирургическим отделением ОБУЗ «Курская городская поликлиника № 7»; 305047, Россия, г. Курск, ул. Заводская, д. 25.
Сорокина Анна Сергеевна — врач-кардиолог БМУ КОКБ; 305007, Россия, г. Курск, ул. Сумская, д. 45а; ORCID iD 0000-0003-4112-3093.
Контактная информация: Хруслов Максим Владимирович, e-mail: khruslov@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 09.07.2021.
Поступила после рецензирования 03.08.2021.
Принята в печать 26.08.2021.
About the authors:
Maxim V. Khruslov — Dr. Sc. (Med.), Deputy Chief Medical Officer, Head of the Regional Vascular Center, Kursk Regional Clinical Hospital; 45A, Sumskaya str., Kursk, 305007, Russian Federation; ORCID iD 0000-0001-9856-1284.
Irina V. Ponomareva — Assistant Professor of the Department of Surgical Diseases No. 1, Kusrk State Medical University; 3, Karl Marx str., Kursk, 305041, Russian Federation; ORCID iD 0000-0003-1850-6491.
Lyudmila V. Safronova — Head of the Department of Surgery, Kursk City Outpatient Clinic No. 7; 25, Zavodskaya str., Kursk, 305047, Russian Federation.
Anna S. Sorokina — cardiologist, Kursk Regional Clinical Hospital; 45A, Sumskaya str., Kursk, 305007, Russian Federation; ORCID iD 0000-0003-4112-3093.
Contact information: Maxim V. Khruslov, e-mail: khruslov@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 09.07.2021.
Revised 03.08.2021.
Accepted 26.08.2021.
.
Информация с rmj.ru





