Оптимизация антихеликобактерной терапии в современной клинической практике
А.Н. Казюлин1, Е.В. Парцваниа-Виноградова1, Д.Т. Дичева1, Е.Г. Лебедева1, Н.Л. Головкина2
1 ГБОУ ВПО Московский государственный медико-стоматологический университет им. А.И. Евдокимова Минздрава России. 127473, Россия, Москва, ул. Делегатская, д. 20, стр. 1;
2 ФКУЗ Главный клинический госпиталь МВД России. 123060, Россия, Москва, ул. Народного Ополчения, д. 35
В обзоре указаны пути оптимизации антихеликобактерной терапии. Показатель эффективности эрадикационной терапии (ЭТ) коррелирует с распространенностью антибиотикорезистентности штамма в популяции. Фактором, влияющим на эффективность ЭТ, является полиморфизм генов (CYP2C19, MDR1), определяющий особенность метаболизма препаратов. Удвоение стандартной дозировки ингибитора протонной помпы обеспечивает более выраженный антисекреторный эффект в течение более длительного времени, что повышает эффективность ЭТ. В силу необходимости достижения внутрижелудочного рН>4 на протяжении 90% времени обосновано применение ингибитора протонной помпы нового поколения. Введение препаратов висмута в основные схемы ЭТ демонстрирует положительное влияние на уровень эрадикации и регламентируется современными российскими рекомендациями.
Ключевые слова: эрадикационная терапия, антибиотикорезистентность, продолжительность курса, ингибитор протонной помпы, препараты висмута.
alexander.kazyulin(а)yandex.ru
Для цитирования: Казюлин А.Н., Парцваниа-Виноградова Е.В., Дичева Д.Т. и др. Оптимизация антихеликобактерной терапии в современной клинической практике. Consilium Medicum. 2016; 18 (8): 32-36.
Введение
Несмотря на разработку стандартных схем антихеликобактерной терапии эффективность эрадикации колеблется от 70 до 80%, что заставляет исследователей искать пути оптимизации уже существующих режимов эрадикационной терапии (ЭТ). Большинство авторов сходятся во мнении, что показатель эффективности ЭТ коррелирует с распространенностью антибиотикорезистентности штамма Helicobacter pylori в популяции. Фактором, влияющим на эффективность ЭТ, является полиморфизм генов (CYP2C19, MDR1), определяющий особенность метаболизма препаратов. В случае неуспеха ЭТ сохраняется высокий риск рецидивирования Н. pylori-ассоциированных заболеваний. Помимо этого, значительно увеличивается риск возникновения рака желудка ввиду того, что Н.pylori рассматривается в качестве канцерогена 1-го типа (Международное агентство по изучению рака). Все перечисленное иллюстрирует необходимость поиска путей повышения эффективности ЭТ.
Региональные особенности
Нарастание уровня резистентности к антибактериальным препаратам в последние годы привело к необходимости модернизации нынешних схем ЭТ инфекции Н. pylori [1-5]. В соответствии с положениями Киотского консенсуса 2015 г., назначая схему эрадикации, нужно руководствоваться данными об успешности конкретных схем в конкретном регионе [6, 7]. Показатель эффективности ЭТ коррелирует с распространенностью антибиотикорезистентности штамма в популяции [8,9].
Согласно данным Российской группы по изучению Н. pylori, продолжается рост количества резистентных к антибиотикам штаммов Н. pylori в Москве. Резистентность к амоксициллину выявляется крайне редко. Этот феномен может возникнуть у пациентов, длительно или многократно применявших амоксициллин, как правило, по назначению врачей других профилей. При изучении механизмов формирования резистентности к амоксициллину исследователями была продемонстрирована значимость точечных мутаций в пенициллинсвязывающем белке (РВР-1А).
В России, согласно наблюдениям последних лет, уровень резистентности к кларитромицину колеблется от 8 до 19,3%, что позволяет активно применять его в схемах ЭТ [10, 11]. Из макролидных антибиотиков кларитромицин обладает наибольшей активностью в отношении Н.pylori. Поэтому во всех международных рекомендациях и рекомендациях Российской гастроэнтерологической ассоциации именно кларитромицин является обязательным компонентом стандартной эрадикационной терапии 1-й линии. К тому же, учитывая собственное противовоспалительное действие, минимальное влияние на микрофлору, а также способность разрушать бактериальные биопленки, кларитромицин повышает эффективность ЭТ и комплаенс пациентов. Отечественными учеными неоднократно изучалась эффективность кларитромицина (препарат Фромилид®, КРКА) [12]. Препарат продемонстрировал высокую эффективность. В исследовании особенно подчеркивалось оптимальное соотношение показателя эффективности, цены, качества, что немаловажно в настоящих экономических условиях. Приведенные выше данные позволяют рекомендовать Фромилид® в качестве надежного компонента ЭТ.
При оценке уровня резистентности к метронидазолу получены следующие результаты: в середине 1990-х отмечалось устойчивое повышение среднеевропейского уровня резистентности. Исходные данные, характерные для России, где продолжается рост числа штаммов Н. pylori, устойчивых к производным нитроимидазола, к 1998 г. достигли 56,6% [10, 11] (см. рисунок). Причиной такого высокого уровня резистентности является широкое применение препарата для лечения урогенитальных и других инфекций, а также нерациональное использование их в схемах ЭТ в предшествующие годы. Однако обращают на себя внимание данные о возможности восстановления чувствительности к метронидазолу у прежде резистентного штамма Н. pylori в анаэробных условиях. Исследователи объясняют этот феномен тем, что, находясь в полости желудка, H. pylori периодически попадает в анаэробные условия, в связи с чем у ряда больных с резистентными штаммами ЭТ с включением метронидазола достигает успеха. Приведенные данные иллюстрирует диаграмма динамики роста резистентности Н. pylori антибиотикам в Москве.
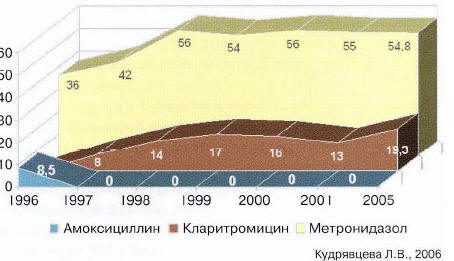
Рис. Динамика резистентности Н. pylori в Москве в 1996-2005 гг.
Как было отмечено выше, немаловажным фактором, влияющим на эффективность ЭТ, также является полиморфизм генов (CYP2C19, MDR1), так как последний определяет особенность метаболизма препаратов [1, 2, 9, 13]. Согласно последним публикациям привилегированны схемы эрадикации с эффективностью более 90%, что делает актуальными исследования для определения схем в конкретном регионе, стремящихся к наивысшему уровню эрадикации [14-16].
На сегодняшний день существует несколько путей корригирования схем ЭТ [8, 12, 17, 18]:
- продление курса ЭТ;
- удвоение дозировки ингибитора протонной помпы (ИПП);
- дополнение схемы ЭТ препаратами висмута;
- назначение пробиотиков.
Рассмотрим каждый из предлагаемых подходов отдельно.
Продление курса ЭТ
Наиболее известной и часто применяемой мерой оптимизации ЭТ является увеличение длительности курса назначаемого лечения. Если в рекомендациях I и II Маастрихтского консенсуса обсуждалось назначение 7-дневной антихеликобактерной терапии, то в дальнейшем представления о необходимой длительности ЭТ были пересмотрены. По данным III Маастрихтского консенсуса (2005 г.), увеличение продолжительности ЭТ до 10-14 дней приводило к повышению показателя эффективности на 9-12%. Однако, в силу неуклонного роста антибиотикорезистентности к используемым препаратам на сегодняшний день этот показатель эффективности терапии при увеличении ее длительности не превышает 4-6%. По данным четырех мета-анализов 10-дневная схема лечения увеличивает частоту эрадикации на 4%, 14-дневная — на 5-6% по сравнению с 7-дневной схемой лечения. Различий по частоте побочных эффектов выявлено не было [19, 20]. В то же время увеличение продолжительности терапии неизбежно приводит к повышению стоимости курсового лечения, что бывает чрезвычайно важным для целого ряда пациентов Российской популяции [21, 22].
Удвоение стандартной дозировки ИПП
Другим способом усовершенствования ЭТ представляется удвоение стандартной дозировки ИПП, что обеспечивает более выраженный антисекреторный эффект в течение более длительного времени [23-25]. По результатам исследований зарубежных авторов эффективность антихеликобактерной терапии при этом повышается на 6-10% [20, 26, 27]. По данным исследований, для достижения успешной эрадикации крайне важна выраженность активности назначаемого антисекреторного препарата. Так, уровень рН в желудке выше 4 Ед в течение 90% времени за сутки приводит к 100% эрадикации, несмотря на наличие устойчивых к кларитромицину штаммов Н. pylori, что, вероятнее всего, связано с повышением устойчивости кларитромицина и амоксициллина в слабокислой среде желудка [28-30]. Учитывая сказанное, использование удвоенных стандартных доз ИПП закономерно для любых схем ЭТ [19, 23, 31, 32]. В силу необходимости достижения внутрижелудочного рН>4 на протяжении 90% времени обосновано применение ИПП последних поколений — моноизомеров (эзомепразол), демонстрирующих более выраженную антисекреторную активность за счет фармакокинетических особенностей [33]. Большое количество исследований было посвящено S-энантиомеру классической молекулы омепразола (эзомепразолу, препарат Эманера®, КРКА). Так, российскими исследователями был изучен антисекреторный потенциал препарата Эманера® путем длительного (48-часового) мониторирования внутрижелудочного рН у пациентов с язвенной болезнью и эрозивным гастродуоденитом. В исследовании сравнивали стандартные показатели рН в 1-й день исследования (без ИПП) и 2-й день (после приема 40 мг препарата Эманера®). Длительное (48-часовое) мониторирование внутрижелудочного рН показало высокий антисекреторный ответ препарата Эманера® в дозе 40 мг уже при 1-м применении: время поддержания рН>4 составило 18,5 ч, медиана среднесуточного рН оказалась впечатляющей — 6,25, медиана площади под кривой распределения значений рН от 1 до 10 после приема 40 мг препарата Эманера® увеличилась на 46,4%, наиболее наглядно демонстрируя антисекреторную эффективность препарата [34].
Обоснованность концепции о необходимости более мощной антисекреторной терапии для повышения уровня эрадикации была проиллюстрирована последним мета-анализом A. McNicholl и соавт. (2012 г.), обобщившим результаты 35 исследований (5998 пациентов). Данная работа продемонстрировала более длительную и выраженную антисекреторную активность эзомепразола и рабепразола относительно ИПП первых поколений в схемах ЭТ на 4,7% (отношение шансов 1,32, 95% доверительный интервал 1,01-1,73) и 4,1% (отношение шансов 1,21, 95% доверительный интервал 1,02-1,42) соответственно [33]. Прямые доказательства повышения эффективности ЭТ путем удвоения дозы ИПП получены из метаанализа, который продемонстрировал увеличение частоты излечения на 6-10% по сравнению со стандартными дозами. Наиболее эффективны при этом ИПП второго поколения (эзомепразол 40 мг два раза в день) [20].
Препараты висмута
В современной клинической практике активно применяются различные препараты висмута (висмута субцитрат, висмута субсалицилат, висмута трикалия дицитрат — ВТД). Особенностью данной группы препаратов является то, что резистентности к ним вплоть до настоящего времени зарегистрировано не было [2, 31]. Препараты обсуждаемой группы практически не всасываются в кровь и выделяются кишечником, что объясняет редкость побочных явлений при их применении и дает им несомненные клинические преимущества. Нужно отметить, что характерной особенностью препаратов висмута является окрашивание стула в темный цвет вследствие их преобразования в просвете кишечника в сульфид висмута. Поэтому, назначая данные препараты, необходимо предупредить пациента об этой особенности, так как в ряде случаев окрашенный стул напоминает мелену Учитывая слабую эрадикационную активность препарата, использование его в качестве монотерапии инфекции Н.pylori нерационально, однако именно включение его в основные схемы ЭТ дает обнадеживающий результат.
Среди всех препаратов данной группы ВТД зарекомендовал себя как наиболее эффективное средство повышения эффективности ЭТ. В России доступным препаратом ВТД является Улькавис® (КРКА, Словения), хорошо зарекомендовавший себя в клинической практике. Фармакокинетические механизмы данного препарата многогранны, что обосновывает его включение в схемы ЭТ. Он оказывает не только бактерицидный, но и цитопротективный эффект, который реализуется благодаря связыванию с гликопротеинами эпителиоцитов в краях и дне язвы, где ВТД образует на слизистой оболочке желудка аналог прикрепленного слизистого геля, защищающего эпителиоциты от воздействия кислотно-пептического фактора. Такая протекция потенцирует репаративные процессы в зоне эрозивно-язвенных дефектов [31, 35]. Помимо этого, ВТД обладает свойствами опосредованной цитопротекции за счет стимуляции синтеза простагландинов группы Е, повышения выделения НСО3-мукоцитом в желудочную слизь, а также связывания пепсина [31].
Чрезвычайно важным представляется и антиоксидантное действие рассматриваемого препарата. Так, ВТД защищает молекулу ДНК от воздействия реактивных форм кислорода, что оказывает протективный эффект по отношению к молекулам ДНК, предотвращая мутации, приводящих к неопластической трансформации ткани слизистой оболочки желудка [36].
Активно обсуждается влияние препарата висмута на резистентность Н. pylori к антибиотикам [37]. По данным исследования Q.Sun и соавт. (2010 г.), включение в схему эрадикации препарата висмута приводило к повышению эффективности лечения на 15,4% и к снижению резистентности Н.pylori к кларитромицину при пролонгации стандартной тройной ЭТ до 14 дней (висмутсодержащая квадротерапия) [38]. Сказанное подтверждается также данными исследований российских авторов. Режим висмутсодержащей 4-компонентной терапии достоверно повышает уровень эрадикации до 93,7%. В случае инфицирования резистентными к кларитромицину штаммами Н.pylori успешной эрадикации удавалось достичь у 84,6% пациентов [39].
Таким образом, применение ВТД актуально не только в схемах классической квадротерапии, но также в качестве 4-го компонента в схемах стандартной тройной ЭТ 1-й линии в целях оптимизации антихеликобактерной терапии. Эта позиция поддерживается современными российскими рекомендациями [40], базисом которых являются результаты исследований, демонстрирующих дополнительный прирост эффективности эрадикации на 15-20% при включении ВТД 4-м компонентом в схему стандартной тройной ЭТ. Помимо этого, недавний клинический опыт зарубежных коллег демонстрирует нам целесообразность включения ВТД в схемы последовательной терапии [41].
Основным принципом лечения заболеваний, ассоциированных с Н.pylori, является принцип эрадикации Н.pylori, подразумевающий полное уничтожение вегетативных и кокковых форм бактерии в слизистой оболочке желудка и двенадцатиперстной кишки. К сегодняшнему дню предложено значительное количество различающихся по составу и длительности лечения схем ЭТ, обязательным компонентом которых являются антибиотики и ИПП. В то же время активно продолжаются исследования по поиску путей оптимизации схем антихеликобактерной терапии. В силу широкого распространения Н. pylori-ассоциированных заболеваний в РФ для каждого практикующего врача чрезвычайно важным являются мониторирование и практическое применение в своей лечебной деятельности предлагаемых современных подходов оптимизации схем ЭТ, что, несомненно, приведет к существенному снижению уровня инфицированности и поражения Н.pylori-ассоциированными заболеваниями, а также сыграет важную роль в профилактике рака желудка — второй по смертности онкологической патологии в мире.
Литература/References
- Маев И.В., Самсонов А.А., Андреев Д.Н. Инфекция Helicobacter pylori. M, 2016. / Maev I.V., Samsonov A.A., Andreev D.N. Infektsiia Helicobacter pylori. M., 2016. [in Russian]
- Маев И.В., Кучерявый Ю.А., Андреев Д.Н. Актуальные возможности оптимизации антихеликобактерной терапии. Лечащий врач. 2014; 4: 73-9. / Maev I.V., Kucheriavyi Iu.A, Andreev D.N. Aktual’nye vozmozhnosti optimizatsii antikhelikobakternoi terapii. Lechashchii vrach. 2014; 4:73-9. [in Russian]
- Megraud F, Coenen S, Versporten A et al. Helicobacter pylori resistance to antibiotics in Europe and its relationship to antibiotic consumption. Gut 2013; 62 (1): 34-42.
- Liou JM, Chang CY, Chen MJ et al. The Primary Resistance of Helicobacter pylori in Taiwan after the National Policy to Restrict Antibiotic Consumption and Its Relation to Virulence Factors-A Nationwide Study. PLoS One 2015; 10 (5): e0124199.
- Маев И.В., Самсонов А.А., Андреев Д.Н. и др. Клиническое значение инфекции Helicobacter pylori. Клин, медицина. 2013; 91 (8): 4-12. / Maev I.V., Samsonov A.A., Andreev D.N. i dr. Klinicheskoe znachenie infektsii Helicobacter pylori. Klin, meditsina. 2013; 91 (8): 4-12. [in Russian]
- Sugano K, Tack J, Kuipers EJ et al; faculty members of Kyoto Global Consensus Conference. Kyoto global consensus report on Helicobacter pylori gastritis. Gut 2015; 64 (9); 1353-67.
- Маев И.В., Андреев Д.Н., Самсонов А.А. и др. Эволюция представлений о дефиниции, классификации, диагностике и лечении гастрита, ассоциированного с инфекцией Helicobacter pylori (по материалам Киотского консенсуса, 2015). Фарматека. 2016; 6 (319): 24-33. / Maev I.V., Andreev D.N., Samsonov A.A. i dr. Evoliutsiia predstavlenii о definitsii, klassifikatsii, diagnostike i lechenii gastrita, assotsiirovannogo s infektsiei Helicobacter pylori (po materialam Kiotskogo konsensusa, 2015). Farmateka. 2016; 6 (319): 24-33. [In Russian]
- Маев И.В., Кучерявый Ю.А., Андреев Д.Н. Причины неэффективности антигеликобактерной терапии. Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. 2013; 23 (6): 62-72. / Maev I.V., Kucheriavyi Iu.A., Andreev D.N. Prichiny neeffektivnosti antigelikobakternoi terapii. Ros. zhum. gastroenterologii, gepatologii, koloproktologii. 2013; 23 (6): 62-72. [in Russian]
- Маев И.В., Самсонов A.A., Андреев Д.Н. Болезни желудка. М., 2015. / Maev I.V, Samsonov A.A., Andreev D.N. Bolezni zheludka. M, 2015. [in Russian]
- Кудрявцева Л.В. Биологические свойства Helicobacter pylori. Альманах клин, медицины. 2006; XIV: 39-46. / Kudriavtseva L.V. Biologicheskie svoistva Helicobacter pylori. Al’manakh klin. meditsiny 2006; XIV 39-46. [in Russian]
- Кудрявцева Л.В. Динамика резистентности штаммов к амоксициллину, кларитромицину и метронидазолу в России в 1996-2001 гг. Consilium Medicum. Педиатрия (Прил.). 2002; 2:63-4. / Kudriavtseva L.V. Dinamika rezistentnosti shtammov k amoksitsillinu, klaritromitsinu i metronidazolu v Roscii v 1996-2001 gg. Consilium Medicum. Pediatrics (Suppl). 2002; 2:63-4. [in Russian]
- Подгорбунских Е.И., Маев И.В., Исаков В.А. Фромилид — обязательный компонент терапии первой линии кислотозависимых заболеваний, ассоциированных с Helicobacter pylori // Рос. журн. гастроэнтерол. гепатол. колопроктол. -2002.-Т. 12,№5.-С.87-92.
- Maev I.V., Andreev D.N., Kucheryavyi Yu.A., Dicheva D.T. Host factors influencing the eradication rate of helicobacter pylori. World AppI Sci J 2014; 30 (30): 134-40.
- Андреев Д.Н., Кучерявый Ю.А. Факторы микро- и макроорганизма, влияющие на эффективность антихеликобактерной терапии. Consilium Medicum. 2013; 15 (8): 5-10. / Andreev D.N., Kucheriavyi Iu.A. Faktory mikro- i makroorganizma, vliiaiushchie na effektivnost’ antikhelikobakternoi terapii. Consilium Medicum. 2013; 15 (8): 5-10. [in Russian]
- Маев И.В., Кучерявый Ю.А., Андреев Д.Н., Баркалова Е.В. Эрадикационная терапия инфекции Helicobacter pylori: обзор мировых тенденций. Терапевт, арх. 2014; 86 (3): 94-9. / Maev I.V., Kucheriavyi Iu.A., Andreev D.N., Barkalova E.V. Eradikatsionnaia terapiia infektsii Helicobacter pylori: obzor mirovykh tendentsii. Terapevt. arkh. 2014; 86 (3): 94-9. [in Russian]
- Graham DY, Lee YC, Wu MS. Rational Helicobacter pylori therapy: evidence-based medicine rather than medicine-based evidence. Clin Gastroenterol Hepatol 2014; 12: 177-86.
- Wu JY, Hsu PI, Wu DC et al. Feasibility of shortening 14-day hybrid therapy while maintaining an excellent Helicobacter pylori eradication rate. Helicobacter 2014; 19 (3): 207-13.
- Tepes B, O’Connor A, Gisbert J, O’Morain С. Treatment of Helicobacter pylori infection 2012. Helicobacter 2012; 17 (Suppl. 1): 36-42.
- Malfertheiner P, Megraud F, O’Morain С et al. Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report. Gut 2007; 56: 772-81.
- Malfertheiner P, Megraud F, O’Morain С et al. Management of Helicobacter Pylori infection — Maastricht IV. Florence Consensus Report Gut 2012; 61:646-64.
- O’Connor JR Taneike I, O’Morain С Improving compliance with helicobacter pylori eradication therapy: when and how? Therap Adv Gastroenterol 2009; 2 (5): 273-9.
- Маев И.В., Андреев Д.Н., Кучерявый Ю.А. Инфекция Helicobacter pylori и экстрагастродуоденальные заболевания. Терапевт, арх. 2015; 87 (8): 103-10. / Maev I.V., Andreev D.N., Kucheriavyi Iu.A. Infektsiia Helicobacter pylori i ekstragastroduodenal’nye zabolevaniia. Terapevt. arkh. 2015; 87 (8): 103-10. [in Russian]
- Кучерявый Ю.А., Баркалова Е.В. Двойные дозы ингибиторов протонной помпы — путь повышения эффективности тройной антихеликобактерной терапии первой линии. Лечебное дело. 2012; 1: 36-42. / Kucheriavyi Iu.A., Barkalova E.V. Dvoinye dozy ingibitorov protonnoi pompy — put’ povysheniia effektivnosti troinoi antikhelikobakternoi terapii pervoi linii. Lechebnoe delo. 2012; 1: 36-42. [in Russian]
- Маев И.В., Андреев Д.Н., Дичева Д.Т., Гончаренко А.Ю. Фармакотерапевтические аспекты применения ингибиторов протонной помпы. Мед. вести. МВД. 2013; 3: 9-14. / Maev I.V., Andreev D.N., Dicheva D.T., Goncharenko A.Ju. Farmakoterapevticheskie aspekty primeneniia ingibitorov protonnoi pompy. Med. vestn. MVD. 2013; 3: 9-14. [in Russian]
- Маев И.В., Андреев Д.Н., Гончаренко А.Ю., Дичева Д.Т. Ингибиторы протонной помпы как основа лечения кислотозависимых заболеваний. Справочник поликлинического врача. 2013; 7-8:42-4. / Maev I.V., Andreev D.N., Goncharenko AJu, Dicheva D.T. Ingibitory protonnoi pompy kak osnova lecheniia kislotozavisimykh zabolevanii. Spravochnik poliklinicheskogo vracha. 2013; 7-8:42-4. [in Russian]
- Vallve M, Vergara M, Gisbert JP, Calvet X. Single vs. double dose of a proton pump inhibitor in triple therapy for Helicobacter pylori eradication: a meta-analysis. Aliment Pharmacol Ther 2002; 16 (6): 1149-56.
- Villoria A, Garcia P, Calvet X et al. Meta-analysis: high-dose proton pump inhibitors vs. standard dose in triple therapy for Helicobacter pylori eradication. Aliment Pharmacol Ther 2008; 28 (7): 868-77.
- Sugimoto M, Furuta T, Shirai N et al. Evidence that the degree and duration of acid suppression are related to Helicobacter pylori eradication by triple therapy. Helicobacter 2007; 12 (4): 317-23.
- Андреев Д.Н., Маев И.В., Кучерявый Ю.А., Дичева Д.Т. Оценка влияния сопутствующих анамнестических и клинических факторов на эффективность и безопасность антихеликобактерной терапии. Арх. внутр. медицины. 2016; 6 (1): 29-33. / Andreev D.N., Maev I.V., Kucheriavyi Iu.A., Dicheva D.T. Otsenka vliianiia soputstvuiushchikh anamnesticheskikh i klinicheskikh faktorov na effektivnost’ i bezopasnost’ antikhelikobakternoi terapii. Arkh. vnutr. meditsiny, 2016; 6 (1): 29-33. [in Russian]
- Кучерявый Ю.А., Баркалова Е.В. Выраженность кислотосупрессивного действия ингибиторов протонной помпы и эффективность современных эрадиационных схем. Фарматека. 2013; 10: 11-7. / Kucheriavyi Iu.A., Barkalova E.V. Vyrazhennost’ kislotosupressivnogo deistviia ingibitorov protonnoi pompy i effektivnost’ sovremennykh eradiatsionnykh skhem. Farmateka. 2013; 10:11-7. [in Russian]
- Peura DA, Crowe SE. Helicobacter pylori. In: Feldman M, Friedman LS, Brandt LJ eds. Sleisenger & Fordtran’s Gastrointestinal and Liver Disease. 9th ed. Philadelphia, Pa: Saunders Elsevier; 2010; chap 50.
- Gasparetto M, Pescarin M, Guariso G. Helicobacter pylori Eradication Therapy: Current Availabilities. ISRN Gastroenterol 2012; 2012:186734.
- McNicholI AG, Linares PM, Nyssen OP et al. Meta-analysis: esomeprazole or rabeprazole vs. first-generation pump inhibitors in the treatment of Helicobacter pylori infection. Aliment Pharmacol Ther 2012; 36 (5): 414-25.
- Курилович С., Чекалина Е., Белковец А., Щербакова Л. Антисекреторная активность эзомепразола (Эманера®) у пациентов с кислотозависимыми заболеваниями. Врач. 2015; 8: 35-40. / Kurilovich S, Chekalina E, Belkovets A, Shcherbakova L Antisekretornaia aktivnost’ ezomeprazola (Emanera®) u patsientov s kislotozavisimymi zabolevaniiami. Vrach. 2015; 8: 35-40. [in Russian]
- Bland MV, Ismail S, Heinemann JA, Keenan JI. The action of bismuth against Helicobacter pylori mimics but is not caused by intracellular iron deprivation. Antimicrob Agents Chemother 2004; 48 (6): 1983-8.
- Grisham MB, Jourd’heuil D, Wink DA. Review article: chronic inflammation and reactive oxygen and nitrogen metabolism — implications in DNA damage and mutagenesis. Aliment Pharmacol Ther 2000; 14 (Suppl. 1): 3-9.
- Williamson R, Pipkin GA. Does bismuth prevent antimicrobial resistance of Helicobacter pylori? In: Helicobacter Pylori. Basic Mechanisms to Clinical Cure 1998. Ed. by R.H.Hunt, G.N.J.Tytgat. Dordrecht; Boston; London: Kluwer Acad. Publ, 1998; p. 416-25.
- Sun Q, Liang X, Zheng Q et al. High efficacy of 14-day triple therapy-based, bismuth-containing quadruple therapy for initial Helicobacter pylori eradication. Helicobacter 2010; 15 (3): 233-8.
- Маев И.В., Самсонов А.А., Коровина Т.Н. и др. Висмута трикалия дицитрат повышает эффективность антихеликобактерной терапии первой линии. Эксперимент. и клин, гастроэнтерология. 2012; 8:92-7. / Maev IV, Samsonov A.A, Коrovina XL i dr. Vismuta trikaliia ditsitrat povyshaet effektivnost’ antikhelikobakternoi terapii pervoi linii. Eksperiment. i klin. gastroenterologiia. 2012; 8: 92-7. [in Russian]
- Ивашкин В.Т., Маев И.В., Лапина Т.Л. и др. Рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых. Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. 2012; 1:87-9. / Ivashkin V.T., Maev I.V., Lapina T.L. i dr. Rekomendatsii Rossiiskoi gastroenterologicheskoi assotsiatsii po diagnostike i lecheniiu infektsii Helicobacter pylori u vzroslykh. Ros. zhurn. gastroenterologii, gepatologii, koloproktologii. 2012; 1: 87-9. [in Russian]
- Uygun A, Ozel AM, Sivri В et al. Efficacy of a modified sequential therapy including bismuth subcitrate as first-line therapy to eradicate Helicobacter pylori in a Turkish population. Helicobacter 2012; 17 (6): 486-90.
Статья опубликована на сайте http://www.gastroscan.ru
материал MedLinks.ru





