Содержание статьи
Низкий уровень активируемого тромбином ингибитора фибринолиза увеличивает риск кровотечений в период длительной терапии варфарином
Н. М. Воробьева*, доктор медицинских наук
А. Б. Добровольский*, доктор биологических наук, профессор
Е. В. Титаева*, кандидат биологических наук
З. Б. Хасанова*
А. Ю. Постнов*, доктор медицинских наук
А. И. Кириенко**, доктор медицинских наук, профессор, академик РАМН
Е. П. Панченко*, доктор медицинских наук, профессор
* ФГБУ РКНПК МЗ РФ, Москва
** ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Антагонисты витамина К (АВК) высокоэффективны для первичной и/или вторичной профилактики тромбоэмболических осложнений у больных с фибрилляцией предсердий, протезированными клапанами сердца, венозными тромбоэмболическими осложнениями (ВТЭО) и после инфаркта миокарда. Среди препаратов этого класса наиболее изученным и широко применяемым является варфарин, эффективность и безопасность которого были подтверждены в многочисленных исследованиях с участием десятков тысяч пациентов.
Кровотечения — наиболее частое и серьезное осложнение терапии АВК, ограничивающее их применение. По данным S. Schulman и соавт. [1], ежегодная частота АВК-ассоциированных больших кровотечений составляет 1–3%. В настоящее время факторы риска АВК-ассоциированных кровотечений хорошо известны и подробно изучены. К ним относят интенсивность антикоагуляции (чрезмерная гипокоагуляция — повышение значений международного нормализованного отношения (МНО) более 3,0); характеристики пациентов (пожилой возраст, кровотечения в анамнезе, злокачественные новообразования, ишемический инсульт, артериальная гипертензия, цереброваскулярные заболевания, сахарный диабет, злоупотребление алкоголем, почечная недостаточность, заболевания печени); фармакогенетические факторы (полиморфизмы генов CYP2C9 и VKORC1); одновременный с АВК прием антитромботических препаратов, парацетамола, нестероидных противовоспалительных средств; лекарственные взаимодействия АВК (антибиотики, амиодарон и др.); продолжительность терапии АВК [1].
В последние годы некоторые исследователи высказывают предположения о том, что, кроме вышеперечисленных факторов, на риск кровотечений могут оказывать влияние и компоненты фибринолитической системы крови, в частности активируемый тромбином ингибитор фибринолиза (АТИФ), участвующий в регуляции баланса между процессами коагуляции и фибринолиза. Активируемый тромбином ингибитор фибринолиза — это профермент, наиболее мощным активатором которого является комплекс тромбин/тромбомодулин. Поскольку активация АТИФ зависит от генерации тромбина, логично предположить, что АТИФ может быть одним из факторов, влияющих как на эффективность, так и на безопасность антикоагулянтной терапии.
Целью нашего исследования являлось изучение значимости нового коагуляционного показателя — активируемого тромбином ингибитора фибринолиза — для оценки безопасности длительной терапии варфарином у больных ВТЭО.
Материал и методы исследования
В исследование включили 98 больных (70 мужчин, 28 женщин) в возрасте 18–76 лет, перенесших эпизод тромбоза глубоких вен (ТГВ) и/или тромбоэмболии легочной артерии (ТЭЛА) и не имевших противопоказаний для антикоагулянтной терапии. Больных с известной непереносимостью или аллергическими реакциями на антикоагулянты, с геморрагическими осложнениями в анамнезе, наличием заболеваний или состояний, потенциально опасных развитием кровотечений, а также при невозможности адекватного контроля над терапией в исследование не включали.
Лечение эпизода ВТЭО начинали с введения парентеральных антикоагулянтов. Все пациенты получили нефракционированный или низкомолекулярный гепарин в течение не менее 5 дней с последующим переходом на прием варфарина (Варфарин Никомед, «Никомед», Дания). Подбор дозы варфарина осуществляли при помощи алгоритмов [2]. В соответствии с текущими рекомендациями [3–4] нагрузочную дозу варфарина 5,0–7,5 мг назначали до окончания курса гепаринотерапии. МНО определяли на 3-й день терапии варфарином. Далее дозу варфарина подбирали с учетом уровня МНО (контроль каждые 2–3 дня) до достижения целевых показателей (2,0–3,0). Дозу гепарина уменьшали вдвое при достижении уровня МНО 1,8–2,0 и отменяли при значениях МНО ≥ 2,0. После получения двух последовательных близких значений МНО в пределах терапевтического диапазона (2,0–3,0) дозу варфарина считали подобранной, следующий контроль МНО осуществляли через 1 месяц. Всем пациентам впоследствии было выполнено фармакогенетическое тестирование, однако подбор дозы варфарина во всех случаях проводили эмпирическим путем.
Минимальная длительность терапии варфарином составляла 3 месяца. Далее продолжительность его приема определяли индивидуально для каждого пациента с учетом клинического статуса, наличия или отсутствия факторов риска ВТЭО и других показаний для лечения антикоагулянтами. Большинство пациентов имели показания для неопределенно долгого приема антикоагулянтов. Антикоагулянтная терапия была расценена как «достаточная» и прекращена через 3, 6 или 12 месяцев от начала лечения у 26 человек. Еще у 2 больных варфарин был отменен через 3 и 6 месяцев из-за высокого риска внутричерепного кровоизлияния, превышавшего потенциальную пользу антикоагулянтной терапии. Таким образом, продолжительность приема варфарина составила 3 месяца у 3 больных, 6 месяцев — у 4, 12 месяцев — у 21, неопределенно долго — у 70 человек. Медиана длительности терапии варфарином была 18 месяцев.
Длительность проспективного наблюдения за больными составила 18 месяцев. Конечной точкой исследования были геморрагические осложнения, которые разделяли на большие и малые кровотечения в соответствии с классификацией, предложенной S. D. Fihn и соавт. [5]. К большим геморрагиям относили фатальное, жизнеугрожающее и серьезное кровотечение. Малыми считали любые другие геморрагические эпизоды, не требовавшие госпитализации, проведения дополнительного обследования и лечения.
Выделяли следующие виды больших и малых кровотечений: спровоцированные, спонтанные (беспричинные) и кровотечения в терапевтическом диапазоне значений МНО (2,0–3,0). Геморрагический эпизод считали спровоцированным, если его появлению предшествовало воздействие известного провоцирующего фактора (травма, лихорадочное состояние, одновременное с варфарином употребление алкоголя, биологически активных добавок или лекарств, повышающих уровень МНО), а значения МНО при его возникновении в большинстве случаев превышали 3,0. Кровотечение расценивали как спонтанное, если оно случалось без видимой причины (в отсутствие известных провоцирующих факторов) на фоне терапевтических значений МНО или при уровне МНО менее 2,0. Кровотечения в терапевтическом диапазоне значений МНО могли быть как спровоцированными, так и спонтанными.
Уровень АТИФ определяли фотометрическим методом с использованием наборов реактивов «STA®–STACHROM® TAFI» (Diagnostica Stago, Германия). В соответствии с рекомендациями производителя реактивов референсные значения уровня АТИФ у здоровых добровольцев составляют 108 ± 25%. У всех больных уровень АТИФ был измерен однократно при включении в исследование (в течение первого месяца приема варфарина).
Ретроспективно всем пациентам выполнили фармакогенетическое тестирование. Исследовали 2 полиморфизма в гене CYP2C9 (430С/T и 1075А/С) и полиморфизм 3673G/A гена VKORC1. Для генотипирования полиморфизмов CYP2C9 использовали метод ПЦР-пиросеквенирования, для полиморфизма VKORC1 — метод ПЦР-ПДРФ (полимеразная цепная реакция — полиморфизм длин рестрикционных фрагментов).
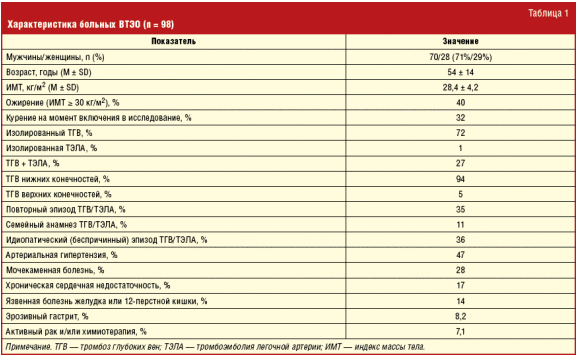
Клиническая характеристика больных ВТЭО представлена в табл. 1. Среди обследованных преобладали мужчины. Возраст больных составил в среднем 54 года. У большинства пациентов был изолированный ТГВ, у 2 человек — изолированная ТЭЛА. В 27% случаев ТГВ осложнился развитием тромбоэмболии в систему легочной артерии. Суммарная частота ТЭЛА составила 28%. У трети больных настоящий эпизод ВТЭО был повторным, у 36% — идиопатическим (беспричинным). Среди сопутствующих заболеваний, являющихся факторами риска и/или потенциальными источниками кровотечений, отмечена довольно высокая частота встречаемости артериальной гипертензии, язвенной болезни желудка или 12-перстной кишки, мочекаменной болезни, а также злокачественных новообразований в активной стадии.
Статистическая обработка данных выполнена с использованием программы SPSS 17.0 for Windows (SPSS Inc., США). Вид распределения количественных признаков анализировали при помощи теста Колмогорова–Смирнова. При параметрическом распределении признака вычисляли среднее (M) и стандартное отклонение (SD); результаты представлены как M ± SD. Для количественных признаков, вид распределения которых не соответствовал параметрическому, определяли медиану (Me) и интерквартильный размах (25-й процентиль; 75-й процентиль); результаты представлены как Ме (25%; 75%). Для сравнения групп применяли U-критерий Манна–Уитни и двусторонний точный тест Фишера. Для определения риска кровотечений использовали однофакторный анализ (модель пропорциональных рисков Кокса) с поправкой на возраст и пол. Статистически значимыми считали различия при двустороннем p < 0,05.
Результаты
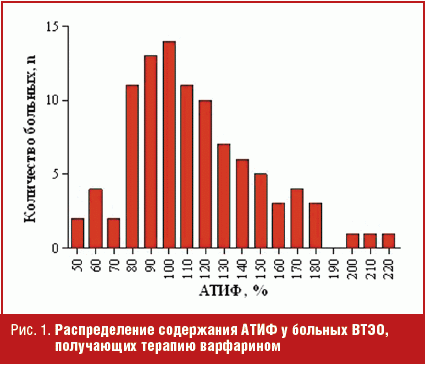
Уровень АТИФ у больных ВТЭО, получающих терапию варфарином, варьировал от 50% до 217% (медиана — 106, интерквартильный размах — 90–133). Распределение содержания АТИФ было непараметрическим (рис. 1), поэтому использовали квартильный анализ. Значения АТИФ менее 90% (ниже 25-го процентиля) были расценены как «низкие», а равные или превышающие 90% (выше 25-го процентиля) считали «высокими». Это деление весьма условно, поскольку уровень АТИФ у больных венозными тромбозами изучен мало.
Частота геморрагических осложнений в течение 18 месяцев терапии варфарином у всех больных составила 25% и была практически одинаковой у лиц с «низким» и «высоким» уровнем АТИФ (21% и 26% соответственно, р = 0,79). Поскольку различий по уровню АТИФ между пациентами с наличием и отсутствием кровотечений также не обнаружили (112% (92; 146) и 106% (89; 132) соответственно, р = 0,39), то для уточнения взаимосвязи АТИФ с риском геморрагических осложнений были проанализированы только больные с наличием кровотечений (n = 24), при этом у 5 из них содержание АТИФ было «низким».
Частота больших кровотечений составила 8,3% (по одному эпизоду у больных «низким» и «высоким» содержанием АТИФ). Оба эпизода больших кровотечений оказались фатальными. Пациент с «низким» уровнем АТИФ (73%) умер от внутричерепного кровоизлияния, с «высоким» АТИФ (91%) — от геморрагического шока, причиной которого послужили обширные подкожные гематомы и постгеморрагическая анемия. Все остальные случаи кровотечений были расценены как малые.
У половины больных (50%) геморрагические осложнения возникли при терапевтических значениях МНО (2,0–3,0). Частота спонтанных кровотечений составила 62%, спровоцированных — 38%. У трети пациентов (33%) спонтанные кровотечения случились на фоне целевых показателей МНО.
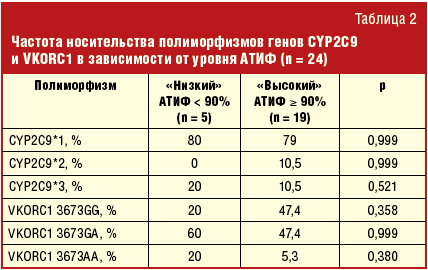
По частоте носительства полиморфизмов генов, определяющих гиперчувствительность к варфарину, различий между пациентами с «низким» и «высоким» уровнем АТИФ выявлено не было (табл. 2).
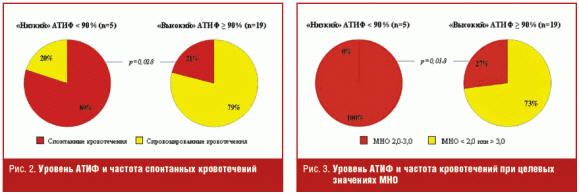
У больных с «низким» уровнем АТИФ частота спонтанных кровотечений оказалась существенно выше, чем у пациентов с «высоким» его содержанием (рис. 2). По данным однофакторного анализа уровень АТИФ менее 90% был ассоциирован с 4-кратным увеличением риска спонтанных кровотечений (относительный риск (ОР) 4,16; 95% доверительный интервал (ДИ) 1,04–16,65; р = 0,044).
Важно отметить, что у больных с «низким» уровнем АТИФ абсолютно все кровотечения произошли на фоне целевых значений МНО (рис. 3). По данным однофакторного анализа уровень АТИФ менее 90% был ассоциирован с 6-кратным увеличением риска кровотечений при целевых значениях МНО (ОР 6,06; 95% ДИ 1,35–27,24; р = 0,019).
Обсуждение
Наше пилотное исследование посвящено изучению значимости нового коагуляционного показателя — АТИФ — для оценки безопасности длительной терапии варфарином. АТИФ — это компонент фибринолитической системы крови, представляющий собой плазменный белок, специфически отщепляющий С-концевые остатки аминокислоты лизина, экспонирующиеся на начальных этапах лизиса фибрина [6]. Это устраняет эффект ускорения лизиса, наблюдающийся в результате появления новых участков связывания тканевого активатора плазминогена и плазминогена после частичного расщепления фибрина.
История открытия этого компонента системы фибринолиза довольно интересна. Впервые о присутствии в плазме крови лабильной карбоксипептидазной активности сообщили D. Hendriks и соавт. в 1989 году [7]. Поскольку новый фермент оказался нестабильным при 37 °С, он получил название карбоксипептидаза U. В том же году W. Campbell и H. Okada [8] обнаружили увеличение карбоксипептидазной активности аргинина, индуцированной каскадом коагуляции, и назвали вновь открытый фермент «карбоксипептидаза R». Через 2 года D. L. Eaton и соавт. [9] обнаружили новый профермент как примесь в реакциях превращения α2-антиплазмина и дали ему название «плазменная карбоксипептидаза В», поскольку он обладал схожей активностью с панкреатической карбоксипептидазой В. Наконец, в 1995 г. при исследовании профибринолитического эффекта протеина С L. Bajzar и соавт. [10] идентифицировали профермент, реализующий свой антифибринолитический эффект после активации тромбином. Этот профермент был назван АТИФ. Оказалось, что вновь открытый профермент идентичен ранее описанным прокарбоксипептидазам U, R и B.
Биохимические исследования показали, что АТИФ может быть активирован различными протеазами, такими как плазмин, трипсин и тромбин. Тромбин — это ключевой фермент системы гемостаза, который катализирует превращение фибриногена в фибрин, а также стимулирует свое собственное образование и является самым мощным из известных активаторов тромбоцитов. Как ни парадоксально, но тромбин может ингибировать активацию свертывания крови. Связываясь с тромбомодулином на поверхности интактного эндотелия, он теряет свои прокоагулянтные свойства, но становится мощным активатором протеина C. Активированный протеин C может прерывать образование тромбина, инактивируя факторы свертывания Vа и VIIIа, и, как было показано в экспериментах in vitro, может стимулировать фибринолиз. Свободный тромбин активирует АТИФ с низкой скоростью. Напротив, связывание тромбина с тромбомодулином приводит не только к активации протеина С, но и к 1000-кратному увеличению скорости активации АТИФ комплексом тромбин/тромбомодулин [11], что, в свою очередь, замедляет фибринолиз и повышает риск тромбоза.
Антикоагулянтный эффект АВК реализуется за счет ингибирования эпоксидредуктазы витамина К и, возможно, редуктазы витамина К, что приводит к снижению образования в печени витамин К-зависимых факторов свертывания крови (II, VII, IX и X) и к уменьшению таким образом генерации тромбина. Поскольку активация АТИФ напрямую зависит от генерации тромбина, следовательно, уменьшение образования тромбина снижает активацию АТИФ, а низкое содержание АТИФ увеличивает активность эндогенного фибринолиза, что в итоге способствует более быстрому лизису тромбов и повышению риска кровотечений. Наоборот, увеличение генерации тромбина способствует активации АТИФ и снижению фибринолитической активности крови, что приводит к усилению тромбообразования и замедлению лизиса тромбов. В единичных клинических исследованиях [12–13] было показано, что высокий уровень АТИФ ассоциируется с повышением риска как первого эпизода ТГВ, так и его рецидива. Влияние АТИФ на риск кровотечений на фоне терапии АВК практически не изучено.
Тем не менее, имеются данные, что АТИФ может влиять на риск кровотечений и в отсутствие приема антикоагулянтов. Так, в недавно опубликованной работе J. H. Foley и соавт. [14] была продемонстрирована возможность количественного определения активации АТИФ в цельной крови у больных гемофилией А, а также выявлена ассоциация между активацией АТИФ и частотой кровотечений. В частности, у больных тяжелой формой гемофилии А с содержанием в крови фактора VIII < 1% была обнаружена обратная взаимосвязь между уровнем АТИФ и гемартрозом (r = –0,77; p = 0,03), а также между уровнем АТИФ и всеми кровотечениями (r = –0,75; p = 0,03).
Наша работа впервые показала, что у больных ВТЭО с наличием геморрагических осложнений на фоне терапии варфарином «низкий» уровень АТИФ ассоциируется со значительным увеличением риска спонтанных кровотечений и кровотечений на фоне терапевтических значений МНО. Данная находка имеет большое практическое значение, поскольку именно такие кровотечения наиболее опасны для пациентов и вызывают сложности у врачей, тем более что тактика ведения больных в этих ситуациях окончательно не определена. При возникновении спонтанного кровотечения, особенно на фоне целевых значений МНО и при отсутствии потенциального источника кровотечения, у врача возникает вопрос о целесообразности продолжения антикоагулянтной терапии и повышении ее безопасности. Мы предполагаем, что в таких случаях определение уровня АТИФ может помочь в принятии решения, поскольку «низкий» уровень АТИФ может быть одной из причин на первый взгляд «беспричинных» кровотечений. Можно также предположить, что если кровотечение возникает на фоне избыточного фибринолиза за счет «низкого» содержания АТИФ, то теоретически «антидотом» варфарина в таком случае может быть лекарственная форма ингибитора фибринолиза, например, аминокапроновая или транексамовая кислота, которые широко применяются в клинической практике. Это особенно важно, учитывая, что пероральная форма витамина К1, являющегося антидотом варфарина, не зарегистрирована в нашей стране и пока отсутствует на отечественном фармацевтическом рынке.
Наше исследование имеет ряд ограничений, обусловленных как небольшим количеством пациентов, так и тем, что уровень АТИФ был измерен лишь однократно при включении в исследование. Кроме того, поскольку взятие крови для определения АТИФ проводили на фоне приема варфарина, нельзя исключить его влияние на содержание АТИФ, хотя нам не удалось обнаружить в доступной литературе каких-либо данных, указывающих на это. Поэтому вопрос о влиянии антикоагулянтов на содержание в крови АТИФ в настоящее время остается открытым.
Таким образом, результаты нашего пилотного исследования свидетельствуют в пользу того, что у больных ВТЭО, получающих терапию варфарином, уровень АТИФ может быть одним из факторов, влияющих на безопасность длительного лечения. Полученные нами данные, безусловно, нуждаются в подтверждении в крупных проспективных исследованиях, поэтому дальнейшие исследования в этом направлении представляются перспективными и актуальными.
Выводы
- У больных ВТЭО с наличием геморрагических осложнений в течение 18 месяцев терапии варфарином уровень АТИФ менее 90% ассоциируется с 4–6-кратным увеличением риска спонтанных (беспричинных) кровотечений и кровотечений на фоне терапевтических значений МНО (2,0–3,0).
- Наше пилотное исследование продемонстрировало необходимость дальнейших проспективных исследований в этом направлении.
Литература
- Schulman S., Beyth R. J., Kearon C. et al. Hemorrhagic complication of anticoagulant and thrombolytic treatment. American College of Chest Physicians evidence-based clinical practice guidelines (8 th edition) // Chest. 2008; 133: 257 S-298 S.
- Панченко Е. П., Кропачева Е. С. Профилактика тромбоэмболий у больных мерцательной аритмией // М.: МИА, 2007: 140 с.
- Kearon C., Akl E. A., Comerota A. J. et al. Antithrombotic therapy for VTE disease: Antithrombotic Therapy and Prevention of Thrombosis, 9 th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines // Chest. 2012; 141 (Suppl): e419S-e494S.
- Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений // Флебология. 2010; 4 (1): 4–37.
- Fihn S. D., McDonell M., Martin D. et al. Risk factors for complications of chronic anticoagulation. A multicenter study // Ann Intern Med. 1993; 118: 511–520.
- Bajzar L., Nesheim M. E., Tracy P. B. The profibrinolytic effect of activated protein C in clots formed from plasma is TAFI-dependent // Blood. 1996; 88: 2093–2100.
- Hendriks D., Scharpe S., van Sande M., Lommaert M. P. Characterisation of a carboxypeptidase in human serum distinct from carboxypeptidase N // J Clin Chem Clin Biochem. 1989; 27: 277–285.
- Campbell W., Okada H. An arginine specific carboxypeptidase generated in blood during coagulation or inflammation which is unrelated to carboxypeptidase N or its subunits // Biochem Biophys Res Commun. 1989; 162: 933–939.
- Eaton D. L., Malloy B. E., Tsai S. R. et al. Isolation, molecular-cloning, and partial characterization of a novel carboxypeptidase-B from human plasma // J Biol Chem. 1991; 266: 21833–21838.
- Bajzar L., Manuel R., Nesheim M. E. Purification and characterization of TAFI, a thrombin-activable fibrinolysis inhibitor // J Biol Chem. 1995; 270: 14477–14484.
- Crawley J. T. B., Zanardelli S., Chion C. K. N. K., Lane D. A. The central role of thrombin in hemostasis // J Thromb Haemost. 2007; 5 (suppl. 1): 95–101.
- van Tilburg N. H., Rosendaal F. R., Bertina R. M. Thrombin activatable fibrinolysis inhibitor and the risk for deep vein thrombosis // Blood. 2000; 95: 2855–2859.
- Eichinger S., Schonauer V., Weltermann A. et al. Thrombin-activatable fibrinolysis inhibitor and the risk for recurrent venous thromboembolism // Blood. 2004; 103: 3773–3776.
- Foley J. H., Nesheim M. E., Rivard G. E., Brummel-Ziedins K. E. Thrombin activatable fibrinolysis inhibitor activation and bleeding in haemophilia A // Haemophilia. 2012; 18 (3): e316–e322.
Статья опубликована в журнале Лечащий Врач
материал MedLinks.ru