Содержание статьи
Введение
Накопленные к настоящему времени научные данные и клинические протоколы свидетельствуют о значимой роли инфекционных факторов в развитии ряда гестационных осложнений второй половины беременности и реализации послеродовых гнойно-септических заболеваний [1]. Восходящий путь проникновения микроорганизмов в плодные оболочки и амниотическую полость из нижних отделов генитального тракта рассматривается как один из факторов, способствующих преждевременному разрыву плодных оболочек и запуску преждевременных родов [2]. Преждевременные роды являются полиэтиологичным событием. Инфекционные причины, такие как бактериальный вагиноз (БВ), вульвовагинальный кандидоз (ВВК), гонорея, хламидиоз, трихомониаз, а также инфекции, вызываемые стрептококком группы B, очень значимы в патогенезе развития, хотя и относятся к потенциально модифицируемым факторам риска с возможностью их своевременной диагностики, медикаментозного воздействия на данный этиологический фактор с целью улучшения перинатальных исходов [3].
«Золотым стандартом» диагностики заболеваний, сопровождающихся патологическими выделениями из половых путей у женщин репродуктивного возраста, являются: микроскопическое исследование нативных и/или окрашенных по Граму биологических материалов, полученных из верхней трети боковых сводов влагалища, рН-метрия влагалищного отделяемого, а также использование полимеразной цепной реакции в режиме реального времени [4]. Однако ввиду частого бессимптомного или малосимптомного течения инфекций нижнего отдела генитального тракта возможность своевременного выявления заболевания ограничена. Чаще всего инфекционные агенты обнаруживаются при появлении клинических симптомов либо при обращении пациентки к акушеру-гинекологу с жалобами на патологические выделения из половых путей. Алгоритм обследования при беременности подразумевает рутинное микроскопическое исследование влагалищных мазков в I и III триместрах при нормально протекающей беременности и внепланово при наличии клинической симптоматики [5].
Особенность ведения беременных с нарушением влагалищного биотопа на современном этапе подразумевает, что чаще встречаются заболевания, имеющие смешанную этиологию, вызванные одновременным наличием у пациентки сочетания двух и более групп микроорганизмов в виде микст- и коинфекций, ассоциированных с условно-
патогенными бактериями (Mycoplasma hominis, Ureaplasma urealyticum, транзиторная флора), грибами рода Candida, инфекциями, передаваемыми половым путем (ИППП), вирусами, причем их сочетание может быть разнообразным, создавая определенные трудности в диагностике и выборе адекватной терапии инфекции [6]. К наиболее распространенным заболеваниям урогенитального тракта во время беременности относят различные сочетания неспецифических микст-инфекций: БВ, ВВК и аэробного вульвовагинита [2, 4, 7]. Показаниями к лечению ВВК и БВ являются наличие клинических проявлений при лабораторно подтвержденном диагнозе, а также бессимптомное носительство у женщин во время беременности, подтвержденное обнаружением возбудителей в ходе лабораторных исследований [4]. В настоящее время отдают предпочтение использованию топических форм препаратов для лечения неосложненной смешанной генитальной инфекции во время беременности, что обеспечивает возможность создания высоких концентраций лекарственного препарата на поверхности слизистой оболочки при низкой системной токсичности [1, 4]. Выбор препарата для лечения таких пациенток должен быть обусловлен не только возможностью воздействия на все этиологически значимые микроорганизмы с учетом лабораторного подтверждения возбудителя, но и определением соотношения польза/риск для пациентки/плода [8, 9].
С учетом вышеизложенного наше внимание привлек комбинированный препарат, сочетающий в своем составе основные компоненты (10 мг метронидазола и 20 мг клотримазола в 1 г препарата), взаимно дополняющие друг друга [10, 11]. Интравагинальный путь введения обеспечивает низкие концентрацию в сыворотке крови и риск системных побочных эффектов [12] при локальном попадании препарата в очаг инфекционного процесса; это становится возможным благодаря двухразовой аппликации, что создает и поддерживает стабильную концентрацию клотримазола в вагинальном секрете в течение 48–72 ч. Препарат имеет гелевую форму, что обеспечивает стабильность в процессе хранения и однородность лекарственной формы, а текучесть и пластическая вязкость определяют скорость высвобождения действующих веществ из лекарственной формы, повышая биоадгезивные свойства: лучшее перемешивание с влагалищным секретом и равномерное распределение по слизистой оболочке влагалища [13]. Данные литературы свидетельствуют о том, что относительная биодоступность вагинального геля в 2 раза выше биодоступности одноразовой дозы влагалищных таблеток метронидазола (500 мг), чем обусловлен высокий терапевтический эффект при применении низких концентраций лекарственного препарата [14].
Цель исследования: изучить клинико-лабораторную эффективность использования комбинированного препарата (метронидазол 10 мг + клотримазол 20 мг в 1 г геля) при лечении неспецифических вульвовагинитов смешанной этиологии у беременных в III триместре.
Материал и методы
Проведено проспективное неконтролируемое открытое сравнительное исследование в параллельных группах. Под наблюдением было 105 беременных, находившихся на этапе дородовой госпитализации в акушерском отделении патологии беременности родильного дома КГБУЗ «КМКБ № 20 им. И.С. Берзона». Из них случайным распределением в основную группу вошли 53 пациентки, в группу сравнения — 52 беременные. Набор пациенток осуществлялся с августа 2020 г. по апрель 2021 г.
Критерии включения: срок гестации — III триместр беременности (от 370–6 до 390–2 недель на момент начала лечения); наличие/отсутствие клинических проявлений при лабораторно подтвержденном диагнозе БВ или ВВК; отсутствие тяжелых экстрагенитальных заболеваний или гестационных осложнений, требующих экстренного родоразрешения; информированное добровольное согласие пациентки на проведение лечебных мероприятий с соблюдением четкого приема препарата (согласно инструкции к лекарственному средству).
Критерии невключения: I и II триместры беременности, повышенная чувствительность к любому из компонентов препарата, использование системной или топической антибиотикотерапии в течение 1 мес. перед исследованием, выявленные ИППП, острый воспалительный процесс другой локализации в момент в течение 30 дней до проводимого исследования.
Пациентки основной группы (n=53) получали лечение препаратом Метрогил®Плюс, содержащим 10 мг метронидазола и 20 мг клотримазола в 1 г геля (М+К) в течение
5 дней. Лекарственное средство беременные вводили интравагинально, самостоятельно с помощью индивидуальных одноразовых аппликаторов, согласно инструкции к использованию лекарственного препарата (рекомендуемая доза составила 5 г (1 полный аппликатор) 2 р/сут — утром и вечером). Пациенткам группы сравнения (n=52) проведен курс лечения с использованием интравагинальных суппозиториев (500 мг метронидазола и 100 мг миконазола нитрата) по 1 суппозиторию 2 р/сут — утром и вечером в течение 7 дней. Для восстановления состояния нормоценоза влагалища все беременные получали перорально пробиотические штаммы лиофилизированных лактобактерий Lactobacillus rhamnosus GR-1® и Lactobacillus reuteri RC-14® по 1 капсуле утром и вечером в течение 7 дней.
У всех пациенток проводили оценку антропометрических данных, акушерско-гинекологического и экстрагенитального анамнеза. Диагноз БВ и ВВК подтверждали наличием жалоб (обильные патологические выделения из половых путей, зуд и жжение в области наружных половых органов, дискомфорт, дизурические расстройства, неприятный запах), данными объективного осмотра реr speculum (гиперемия, отек слизистой влагалища, патологические выделения (бели)), рН-метрии вагинальной жидкости, микроскопического исследования влагалищных мазков (увеличение 1000) и после лечения. Для дифференциально-диагностической окраски микроорганизмов отделяемого влагалища и шейки матки по Граму использовали «Диахим-набор», НПФ «Арбис +». Указанные исследования проводили до и после лечения.
Первичными критериями оценки эффективности проведенной терапии были: динамика жалоб, данных объективного осмотра реr speculum, рН-метрии вагинальной жидкости, микроскопического исследования влагалищных мазков, наличие побочных эффектов (локальный дискомфорт / боль при введении, кровянистые выделения из половых путей) на протяжении всего периода наблюдения и удовлетворенность при использовании препаратов. Вторичными критериями явились: характер начала родовой деятельности, общая продолжительность и особенности течения родов (влагалищные/оперативные), развитие признаков хориоамнионита и внутриамниотической инфекции плода, родового травматизма (разрыв шейки матки, влагалища), состояние новорожденного на 1-й и 5-й минуте после рождения по шкале Апгар, особенности течения послеродового периода.
Статистическая обработка данных проведена с использованием пакета прикладных программ Statistica 6.0. При анализе количественных признаков проводили проверку на нормальность распределения, вычисляли среднее арифметическое (М) и стандартное отклонение (SD). Статистическую значимость различий между двумя средними показателями оценивали с помощью t-критерия Стьюдента. Для условно количественных (порядковых) признаков вычисляли медиану (Ме) и интерквартильный размах (Q1; Q3). При оценке качественных показателей вычисляли фактические и относительные частоты наблюдений (абс., %). Изучение взаимосвязи между парами качественных признаков проводили путем анализа парных таблиц сопряженности с вычислением критерия χ2 Пирсона, точного критерия Фишера. Различия считали статистически значимыми при p≤0,05.
Результаты исследования
Средний возраст беременных основной группы составил 29,5±5,5 года, группы сравнения — 30,4±5,6 года (р=0,81), срок беременности пациенток при включении в исследование — 37,7±0,6 нед. и 38,1±0,5 нед. (р=0,52) соответственно.
Статистически значимых различий в группах сравнения по возрасту, образованию, социальному статусу, семейному положению, акушерско-гинекологическому анамнезу, сопутствующим экстрагенитальным заболеваниям и массо-ростовым показателям не было (табл. 1).
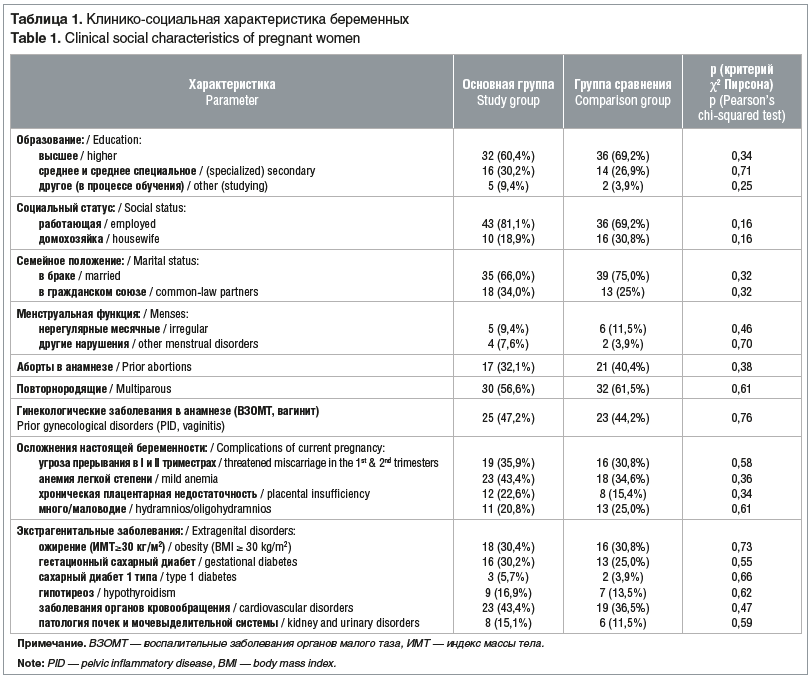
Так, в обеих группах преобладали женщины с предстоящими повторными родами и имеющие в анамнезе прерывание беременности путем проведения артифициального аборта. В структуре экстрагенитальных заболеваний у обследованных с наибольшей частотой наблюдались заболевания органов кровообращения, нарушения углеводного обмена и манифестный или субклинический гипотиреоз, ожирение, а также заболевания почек и мочевыделительной системы (см. табл. 1). Наличие у пациенток обеих групп анамнеза, отягощенного экстрагенитальными заболеваниями, являлось показанием к дородовой госпитализации в акушерский стационар с целью родоразрешения в сроке до 38–39 нед. [1, 15]. Среди осложнений настоящей беременности в группах регистрировали хроническую плацентарную недостаточность, нарушение количества околоплодных вод, угрозу прерывания беременности, анемию легкой степени (см. табл. 1).
Воспалительные заболевания генитального тракта в анамнезе и выявленные в I и II триместрах настоящей беременности имели место у 25 (47,2%) и 23 (43,4%) пациенток основной группы у 23 (44,2%) и 20 (38,5%) женщин группы сравнения. По-видимому, реализация воспалительного процесса в поздние сроки беременности у пациенток обеих групп обусловлена не только физиологическими изменениями в III триместре (гормональный фон и рН среды влагалища), но и склонностью к рецидивированию, что способствует повышению частоты возникновения неспецифических вульвовагинитов смешанной этиологии у беременных.
Диагноз неспецифического вульвовагинита смешанной этиологии был поставлен у всех беременных (критерий формирования выборки). Основными жалобами пациенток основной группы и группы сравнения были: обильные выделения из половых путей — у 44 (83,0%) и 37 (71,2%) пациенток соответственно (p=0,15), неприятный запах —
у 25 (47,2%) и 34 (65,4%) пациенток соответственно (p=0,06), зуд и жжение в области наружных половых органов — в 38 (71,7%) и 28 (53,9%) наблюдениях соответственно (p=0,06). При микроскопическом исследовании вагинальных мазков у пациенток обеих групп до лечения было выявлено повышенное количество лейкоцитов, мелких грамвариабельных и грамотрицательных кокков, наличие ключевых клеток, дрожжевых клеток или псевдомицелия при одновременном выявлении единичных грамположительных палочек (табл. 2).
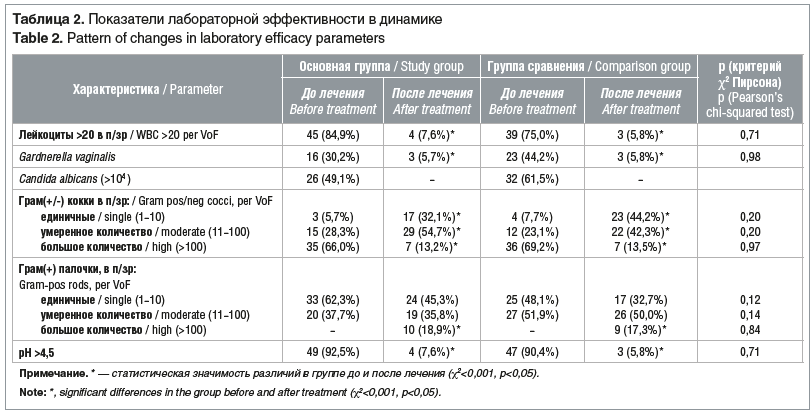
Основным критерием оценки эффективности проведенной терапии являлась частота достижения общего терапевтического эффекта, определяемого по суммарному критерию клинической (субъективное купирование симптомов) и лабораторной (нормализация лабораторных критериев) излеченности у пациенток групп сравнения. Установлено, что после окончания курса терапии пациентки обеих групп отмечали улучшение состояния: уменьшение количества выделений, выраженности локальных проявлений в виде зуда и жжения. Так, отсутствие жалоб было диагностировано у 50 (94,3%) (р<0,05) и 47 (90,4%) (р<0,05) пациенток основной группы и группы сравнения соответственно при отсутствии статистической значимости различий между группами (р=0,45). Патологических симптомов поражения вульвы, шейки и влагалища при исследовании в зеркалах у пациенток исследуемых групп обнаружено не было. Побочные эффекты встречались редко и проявлялись локальным дискомфортом в момент введения препарата у 3 (5,7%) и у 4 (7,7%) пациенток основной группы и группы сравнения соответственно (р=0,68). Случаев болевого синдрома, кровянистых выделений из половых путей в течение всего времени проведения терапии у беременных обеих групп не выявлено. Удовлетворенность от использования препарата и удобство применения в условиях стационара (благодаря наличию одноразовых аппликаторов для введения препарата) отметили 47 (88,7%) беременных основной группы.
Оценка микроскопии (см. табл. 2) после проведенной терапии показала, что количество пациенток с нормальным числом лейкоцитов (лабораторный критерий излеченности) в основной группе стало 49 (92,4%), в группе сравнения — также 49 (94,2%), что было статистически значимо (р<0,05) больше, чем исходно в обеих группах, при отсутствии статистически значимой разницы между группами (р=0,71). У пациенток обеих групп не отмечено случаев диагностирования условных патогенов в клинически значимом титре (Candida albicans (более 104)), присутствие Gardnerella vaginalis констатировали у 3 (5,7%) пациенток основной группы и у 3 (5,8%) — группы сравнения (р=0,98). Использование препарата М+К в течение 5 дней способствовало уменьшению концентрации мелких грамвариабельных и грамотрицательных кокков в сторону преобладания пациенток с единичным (1–10 в п/зр) и умеренным (11–100 п/зр) количеством микроорганизмов при достоверном увеличении количества пациенток с умеренным и большим количеством грамположительных палочек (см. табл. 2), что доказывает отсутствие влияния препарата на лактобациллярную флору. В условиях нормализации показателей влагалищного биотопа pН влагалищной жидкости более 4,5 регистрировали в единичных случаях (см. табл. 2).
Анализ течения родов (табл. 3) показал, что влагалищное родоразрешение имело место у 42 (79,2%) пациенток основной группы и у 43 (82,7%) — группы сравнения, причем в подавляющем большинстве случаев наблюдалось самостоятельное начало родовой деятельности.
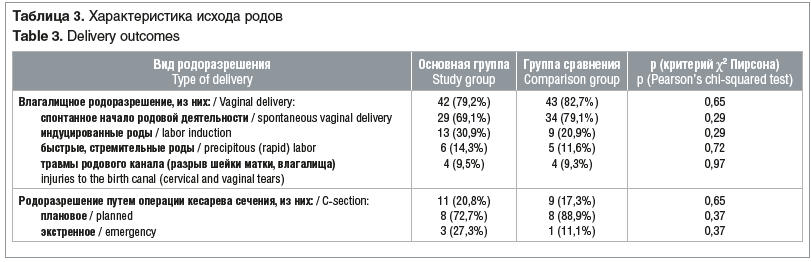
Средняя продолжительность родов в основной группе составила 372,5±120,9 мин, в группе сравнения — 431,3±130,2 мин (р=0,74). Быстрые роды диагностированы у 6 (14,3%) пациенток основной группы и у 5 (11,6%) пациенток группы сравнения (р=0,72). Продолжительность родов более 24 ч не наблюдалась ни в одной группе. Группы были сопоставимы по частоте выполнения операции кесарева сечения, причем в обеих группах оно, как правило, имело плановый характер (см. табл. 3). Масса тела новорожденных у матерей основной группы и группы сравнения была 3390,9±380,9 г и 3557,4±414,4 г соответственно (р=0,77). Оценка по шкале Апгар на 1-й минуте жизни составила 8 (8; 9) баллов, на 5-й минуте — 9 (8; 9) баллов в основной группе и 8 (7; 9) и 9 (8; 9) баллов в группе сравнения соответственно (р=0,93). Рождение детей с признаками реализации внутриамниотической инфекции в исследованных группах не отмечено. Гнойно-септических осложнений в послеродовом периоде не выявлено ни в одной группе.
Обсуждение
Резолюция мультидисциплинарной встречи экспертов на тему «Диагностика и лечение вульвовагинальных инфекций сегодня. Реальная клиническая практика» рекомендует к использованию в работе акушера-гинеколога современных комбинированных топических лекарственных препаратов, имеющих в своем составе препараты из группы имидазолов (метронидазол, обладающий активностью в отношении простейших, факультативных анаэробов) и из группы азолов, с доказанной безопасностью и эффективностью в отношении кандидозной инфекции [16].
Наиболее изученной в настоящее время комбинацией лекарственных препаратов при лечении вульвовагинитов смешанной этиологии у женщин как на прегравидарном этапе, так и во время беременности является сочетание метронидазола и миконазола, обладающее антибактериальным, противопротозойным и противогрибковым действием. Исследования показывают высокую эффективность различных схем дозирования препаратов. Так, оценка эффективности и переносимости лекарственного препарата, содержащего 750 мг метронидазола и 200 мг миконазола, при лечении в течение 7 дней БВ и ВВК у беременных во II триместре выявила высокую терапевтическую эффективность в группе беременных с БВ — 96% (48/51) и в группе с ВВК — 94,2% (65/71) [17]. Аналогичный эффект был получен при использовании 500 мг метронидазола + 100 мг миконазола [18]. Положительный эффект при оценке субъективных и лабораторных показателей у пациенток с БВ на фоне лечения через 14 дней после проведенной терапии был достигнут в виде нормализации клинической и микроскопической картины в 92% в 94,2% случаев соответственно на фоне хорошей переносимости лекарственного препарата. Полученные собственные результаты показывают сопоставимую эффективность проведенной терапии по критерию клинической и лабораторной излеченности в 90,4% и 88,5% случаев соответственно у пациенток группы сравнения, но несколько превышают показатели, полученные ранее E. Ozyurt et al. [19], при которых общий микробиологический уровень излечения смешанных инфекций составил 86% (из них 93% — трихомониаз + БВ и 73% — БВ + ВВК).
Исследования с использованием топических препаратов для лечения вульвовагинальных инфекций смешанной этиологии на гелевой основе с содержанием 10 мг метронидазола и 20 мг клотримазола в 1 г геля показали высокую биодоступность вагинального геля по сравнению с вагинальными таблетками [20]. Имеющиеся в литературе данные свидетельствуют о высокой клинической эффективности препарата М+К in vitro в отношении ключевых микроорганизмов, вызывающих БВ (G. vaginalis и A. vaginae) и ВВК
(C. albicans и C. glabrata) при отсутствии влияния на основные виды лактобацилл — L. iners и L. crispatus [21].
Исследование с включением 200 беременных женщин с вагинальными инфекциями неспецифической этиологии, получивших лечение вагинальным гелем (М+К), в сравнении с пациентками (n=100), которых лечили вагинальными таблетками (метронидазол 100 мг + миконазола нитрат 100 мг), продемонстрировало высокую клинико-лабораторную эффективность двухэтапной терапии неспецифических вагинальных инфекций в сравниваемых группах по окончании курса лечения (100% в обеих группах) и спустя 1 мес. наблюдения (99,0% против 94,0% соответственно, p>0,1), при сохранении высокой клинико-лабораторной эффективности через 2 мес. у беременных основной группы — 98,0% против 90,0% в группе контроля (p<0,05), с более низкой частотой осложнений беременности (8,0% против 20,0%, p<0,05), родов и послеродового периода (18,0% против 37,0%, p<0,01) соответственно [10]. Полученные нами данные выявили сопоставимую эффективность препарата М+К при лечении неспецифических вульвовагинитов смешанной этиологии у беременных в конце III триместра по частоте достижения клинической и лабораторной излеченности у 94,3% и 86,8% пациенток основной группы. Другое пилотное исследование показало высокую эффективность при использовании вагинального геля (М+К) у беременных с ВВК и подтвержденной новой коронавирусной инфекцией COVID-19 во II триместре беременности по критерию терапевтической излеченности у 96,9% (31/32) пациенток с частотой рецидивов в 37–39 нед. 9,4% (3/32) случаев [22].
Заключение
Использование эффективных схем лечения с возможностью воздействия на все этиологические значимые патогены — основной принцип ведения пациенток с воспалительными заболеваниями генитального тракта смешанной этиологии. Выбор препарата для лечения неспецифических вульвовагинитов смешанной этиологии у беременных в III триместре должен быть обусловлен не только включением лекарственного средства в действующие клинические рекомендации и отсутствием противопоказаний, но и высокой эффективностью и низкой токсичностью при ограниченном времени для проведения терапии. Интравагинальный путь введения является предпочтительным, а использование комбинированных форм на гелевой основе поддерживает однородность лекарственной формы и равномерное распределение по слизистой оболочке влагалища, обеспечивая биодоступность и общий терапевтический эффект. Полученные данные показали высокую эффективность проведенной терапии с использованием комбинированного препарата М+К в форме вагинального геля при лечении неспецифических вульвовагинитов смешанной этиологии у беременных в III триместре по частоте достижения клинической и лабораторной излеченности у 94,3% и 86,8% пациенток (р<0,05), при редком выявлении побочных эффектов в виде локального дискомфорта в момент введения препарата у 5,7% и высокой удовлетворенности от использования препарата у 88,7% беременных.
Благодарность
Редакция благодарит компанию «Юник Фармасьютикал Лабораториз» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgment
Editorial Board is grateful to Unique Pharmaceutical Laboratories for the assistance in technical edition of this publication.
ЛСведения об авторах:
Шапошникова Екатерина Викторовна — к.м.н., доцент, доцент кафедры акушерства и гинекологии института последипломного образования ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого Минздрава России; 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; ORCID iD 0000-0001-8068-0699.
Базина Марина Ивановна — д.м.н., доцент, заведующая кафедрой акушерства и гинекологии института последипломного образования ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого Минздрава России; 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; ORCID iD 0000-0002-1971-632X.
Менцик Марина Мубаракзяновна — заместитель главного врача по акушерству и гинекологии КГБУЗ «КМКБ № 20 им. И.С. Берзона»; 660123, Россия, г. Красноярск, ул. Инструментальная, д. 12.
Шагеева Елена Владимировна — заведующая акушерским отделением патологии беременности КГБУЗ «КМКБ № 20 им. И.С. Берзона»; 660123, Россия, г. Красноярск, ул. Инструментальная, д. 12.
Жирова Наталья Владимировна — к.м.н., доцент, доцент кафедры акушерства и гинекологии института последипломного образования ФГБОУ ВО КрасГМУ им. проф.
В.Ф. Войно-Ясенецкого Минздрава России; 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; ORCID iD 0000-0002-9501-8179.
Шагеев Тимур Анварьевич — к.м.н., ассистент кафедры акушерства и гинекологии института последипломного образования ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-
Ясенецкого Минздрава России; 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; ORCID iD 0000-0003-2799-2022.
Контактная информация: Шапошникова Екатерина Викторовна, e-mail: catrinaek@yandex.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 08.07.2021.
Поступила после рецензирования 04.08.2021.
Принята в печать 27.08.2021.
About the authors:
Ekaterina V. Shaposhnikova — C. Sc. (Med.), Associate Professor, associate professor of the Department of Obstetrics & Gynecology of the Institute of Postgraduate Education, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University; 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0001-8068-0699.
Marina I. Bazina — D. Sc. (Med.), Associate Professor, Head of the Department of Obstetrics & Gynecology of the Institute of Postgraduate Education, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University; 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0002-1971-632X.
Marina M. Mentsik — Deputy Head Doctor for Obstetrics & Gynecology, I.S. Berzon Krasnoyarsk Interregional Clinical Hospital; 12, Instrumentalnaya str., Krasnoyarsk, 660123, Russian Federation.
Irina V. Shageeva — Head of the the Obstetrical Department of Pregnancy Diseases, I.S. Berzon Krasnoyarsk Interregional Clinical Hospital; 12, Instrumentalnaya str., Krasnoyarsk, 660123, Russian Federation.
Natalya V. Zhirova — C. Sc. (Med.), Associate Professor, associate professor of the Department of Obstetrics & Gynecology of the Institute of Postgraduate Education, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University; 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0002-9501-8179.
Timur A. Shageev — C. Sc. (Med.), assistant of of the Department of Obstetrics & Gynecology of the Institute of Postgraduate Education, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University; 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0003-2799-2022.
Contact information: Ekaterina V. Shaposhnikova, e-mail: catrinaek@yandex.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 08.07.2021.
Revised 04.08.2021.
Accepted 27.08.2021.
.
Информация с rmj.ru






