Содержание статьи
- 1 Коронавирусы человека (Nidovirales, Coronaviridae): возросший уровень эпидемической опасности
- 1.0.1 Современная таксономия коронавирусов
- 1.0.2 Структура вириона коронавирусов и их физико-химические свойства
- 1.0.3 Структура генома коронавирусов
- 1.0.4 Коронавирусное заболевание верхних дыхательных путей
- 1.0.5 Тяжелый острый респираторный синдром (ТОРС)
- 1.0.6 Ближневосточный респираторный синдром (БВРС)
- 1.0.7 Лечение и профилактика коронавирусных заболеваний человека
М. Ю. Щелканов, доктор биологических наук
Л. В. Колобухина, доктор медицинских наук, профессор
Д. К. Львов, доктор медицинских наук, профессор, академик РАМН
ФГБУ НИИ вирусологии им. Д. И. Ивановского МЗ РФ, Москва
Коронавирус человека был впервые выделен D. Tyrrell и M. Bynoe в 1965 г. от больного острым респираторным заболеванием (ОРВЗ) [1]. В прошлом веке коронавирусы были известны как возбудители острых респираторных заболеваний человека и животных, однако не относились к числу особо опасных вирусных инфекций. Появление сначала тяжелого острого респираторного синдрома (ТОРС) (англ. severe acute respiratory syndrome, SARS) в 2002 г., а затем ближневосточного респираторного синдрома (БВРС) (англ. Middle East respiratory syndrome, MERS) в 2012 г. заставили специалистов существенно повысить уровень эпидемической опасности со стороны коронавирусов. Интенсивное изучение представителей сем. Coronaviridae в начале XXI в. привело к лавинообразному накоплению данных по их молекулярной биологии, таксономии и экологии, за которым не всегда поспевают официальные инструкции, что создает трудности для практических врачей.
С точки зрения современных представлений о таксономии вирусов [2, 3], сем. Coronaviridae входит в состав отряда Nidovirales, который — наряду с Arteriviridae и Roniviridae — содержит оболочечные вирусы с инфекционной односегментной линейной одноцепочечной РНК позитивной полярности, которые имеют ряд общих черт организации генома, его экспрессии и репликации [4].
Семейство Arteriviridae включает вирусы млекопитающих [5]. Прототипный представитель — вирус артериита лошадей (EAV — equine arteritis virus). Значительную опасность для животноводства представляет вирус репродуктивно-респираторного синдрома свиней (PRRSV — porcine reproductive and respiratory syndrome virus). Среди артеривирусов неизвестны патогены человека. Вирус геморрагической лихорадки обезьян (SHFV — simian hemorrhagic fever virus) вызывает опасное заболевание низших приматов.
Семейство Roniviridae включает лишь 2 известных на сегодняшний день представителя: вирус, поражающий жабры креветок (GAV — gill-associated virus) (прототипный), и вирус Нам-Динх (NDiV — Nam Dinh virus), изолированный от кровососущих комаров (Culicinae) в Юго-Восточной Азии [6].
Coronaviridae включает 2 подсемейства: Coronavirinae и Torovirinae. Первое подразделяется на 4 рода: Alphacoronavirus, Betacoronavirus, Gammacoronavirus, Deltacoronavirus. Torovirinae подразделяется на 2 рода: Torovirus (от лат. torus — вздутие, узел — из-за кренделеобразной формы вирионов) и Bafinivirus (от англ. BAcilliform FIsh NIdoviruses — бациллоподобные нидовирусы рыб) (табл. 1). Род Betacoronavirus, в свою очередь, подразделяется на четыре подрода: A, B, C, D (табл. 2).
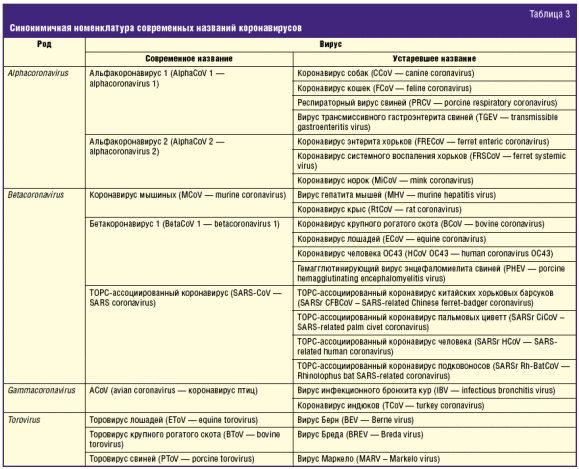
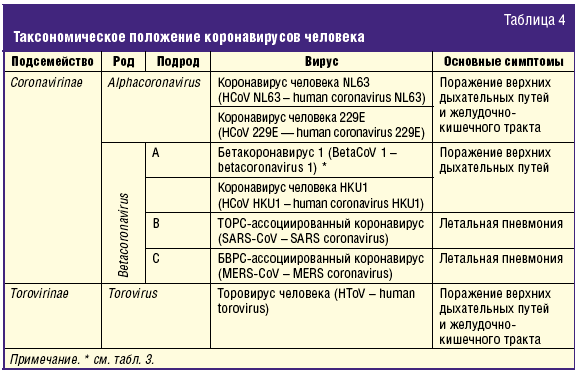
На страницах научных и научно-популярных изданий можно встретить разнообразные интерпретации названий коронавирусов, многие из которых в настоящее время являются устаревшими и сведены в синонимы действующих номенклатурных названий (табл. 3). В частности, широко известный ранее HCoV ОС43 теперь называется BetaCoV 1, а многочисленные ТОРС-подобные вирусы, изолированные от различных хозяев, — синонимичны SARS-CoV [7, 8]. Возбудители инфекционных заболеваний человека содержатся в трех родах коронавирусов (табл. 4). При этом центральное место занимает род Betacoronavirus, в который входят особо опасные возбудители летальных пневмоний — SARS-CoV и MERS-CoV (табл. 4).

Вирион представителей подсем. Coronavirinae имеет сфероидную форму с характерным диаметром 120–160 нм (рис. 1, А–В). Вирусы рода Bafinivirus имеют палочковидную (бациллоподобную) форму 170–200 нм в длину и 75–88 нм в диаметре (рис. 1, Г). Вирусы, входящие в род Torovirus, по форме напоминают крендельки 100–140 × 35–50 нм (рис. 1, Д).
Вирионы всех коронавирусов снабжен липидной оболочкой с отчетливо различимыми на электронно-микроскопических снимках булавовидными пепломерами (рис. 1, А–Ж) длиной 5–10 нм, формируемыми тримерами белка S (180–220 кДа, 1128–1472 а.о). Наличие этих пепломеров, напоминающих зубцы короны, и дало название семейству Coronaviridae.
У представителей Torovirus и Betacoronavirus подрода A имеется дополнительный поверхностный гликопротеин — гемагглютинин-эстераза (НЕ) (65 кДа) — обладающий одновременно гемагглютинирующей и эстеразной активностью. НЕ коронавирусов — также, как и первая субъединица HEF вируса гриппа С (Orthomyxoviridae, Influenza C virus) [13], с которой НЕ высоко гомологична, является ферментом, отщепляющим терминальные остатки О-ацетилированной нейраминовой кислоты от полисахаридных цепочек. Белок М (23–35 кДа) является трансмембранным. Пентамеры белка Е (9–12 кДа, 74–109 а.о.), выявленные в количестве всего нескольких копий на вирион (только у Coronavirinae), способны формировать ионные каналы и представляют собой важный фактор вирулентности. Нуклеокапсид (60–70 нм) имеет спиральную симметрию и формируется фосфорилированным белком N (50–60 кДа, 349–470 а.о.) в комплексе с вирионной РНК [4, 8, 10–12, 14, 15].
Инфицирование коронавирусами вызывает появление высокотитражных сывороток против эпитопов, расположенных на S-, M-, N- и HE-антигенах. S- и HE-белки содержат основные эпитопы для нейтрализующих антител; М- и N-белки содержат менее эффективные нейтрализующие детерминанты, однако наибольший защитный эффект при иммунизации достигается при сочетанном использовании S- и N-белков. Антитела против М-белка выявляются в реакции связывания комплемента. Антигемагглютинирующие антитела связываются с эпитопами S- и HE-белков. Детерминанты клеточного иммунного ответа находятся в составе N-белка [7, 8, 16, 17].
Представители семейства Coronaviridae имеют самые крупные среди известных вирусов РНКовые геномы, размеры которых лежат в пределах 26–32 тыс. н.о. Своеобразным «чемпионом» в этой номинации является коронавирус белух SW1 (BWCoV SW1 — beluga whale coronavirus SW1) из рода Gammacoronavirus — 31 686 н.о.
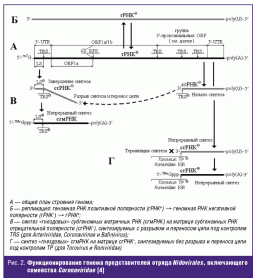
Вирионная РНК коронавирусов, как и у всех представителей отряда Nidovirales. m7G-кэпирована на 5′- и полиаденилирована на 3′-конце. Структура и функционирование генома нидовирусов представлены на рис. 2. Их отличительными особенностями являются экспрессия 3′-проксимальных генов через синтез «гнездовых» субгеномных матричных РНК (сгмРНК) с общими 5′-LS и 3′-концами [4, 18, 19] (от лат. nidus — гнездо — происходит и название отряда), высокий уровень гомологии РНК-зависимых РНК-полимераз (RdRp) и геликаз (Hel) всех представителей отряда [20, 21], а также реплицирование в цитоплазматических везикулах, двухслойные мембраны которых формируются в сети эндоплазматического ретикулума инфицированной клетки [4, 19, 22]. Нетранслируемые 5′-UTR-последовательности длиной 200–600 н.о. (Coronavirinae), 800–900 н.о. (Torovirus) и нетранслируемые 3′-UTR-последовательности длиной 200–500 н.о. (Coronaviridae) содержат регуляторные элементы, способные влиять на биологические свойства (в том числе — вирулентность) вируса. Последовательности, регулирующие транскрипцию (TRS) длиной 5–10 н.о., играют важную роль в синтезе субгеномных РНК отрицательной полярности (сгРНК—), который протекает с разрывом цепи: всякий раз достигая TRS, полимераза может проследовать дальше или же скачкообразно переместиться к 5′-проксимальному TSR с последующим синтезом последовательности, комплементарной лидерной последовательности (LS) — (рис. 2, Б–В). Такие сгРНК— используются затем в качестве матрицы для непрерывного синтеза сгмРНК, все из которых содержат одинаковые 5′-LS и 3′-концы (рис. 2, В). Синтез сгРНК— с переносом цепи на 5′-LS отсутствует у Torovirus, которые используют смешанную стратегию (рис. 2): ORF2, которая содержит на 5′-конце комбинацию DTE и TP, функционально аналогичную TRS, транскрибируется с разрывом цепи (рис. 2, В); остальные сгмРНК синтезируются без разрыва цепи (рис. 2, Г), имея на 5′-концах ORF TP-последовательности, функционально аналогичные IGS ронивирусов [4, 8, 19].
Этиологическими агентами коронавирусного заболевания верхних дыхательных путей являются HCoV NL63, HCoV 229E, BetaCoV 1 (больше известный под названием HCoV ОС43 — табл. 3), HCoV HKU1 и HToV (табл. 4). Вирусы родов Alphacoronavirus (HCoV NL63, HCoV 229E) и Torovirus (HToV) несколько чаще дают осложнения со стороны желудочно-кишечного тракта. Основными клетками-мишенями коронавирусов являются эпителиальные клетки и макрофаги, имеющие на своей поверхности рецепторы, с которыми взаимодействует поверхностный S-белок вируса.
Коронавирусная инфекция распространена повсеместно и регистрируется в течение всего года с пиками заболеваемости зимой и ранней весной, когда эпидемическая значимость ее колеблется от 15,0% до 33,7% [1, 23]. Дети болеют в 5–7 раз чаще, чем взрослые. Инфекция распространяется воздушно-капельным, фекально-оральным и контактным путем. Источником инфекции являются больные с клинически выраженной или стертой формой заболевания [24, 25]. В структуре ОРВИ среди госпитализированных пациентов коронавирусная инфекция в среднем составляет 12,4% (с колебаниями в отдельные годы от 6,8% до 28,6%) [26, 27]. Коронавирусы, как правило, лидируют среди прочих вирусов в этиологии нозокомиальных инфекций. Имеются данные о выделении коронавирусов из мозга больных рассеянным склерозом [28].
При коронавирусном заболевании верхних дыхательных инкубационный период составляет 2–3 сут. Заболевание начинается остро и в большинстве случаев протекает с умеренно выраженной интоксикацией и симптомами поражения верхних отделов респираторного тракта. При этом часто основным симптомом является ринит с обильным серозным отделяемым. Иногда заболевание сопровождается слабостью, недомоганием, больные отмечают першение в горле, сухой кашель. При объективном обследовании отмечается гиперемия и отек слизистой оболочки носа, гиперемия слизистой оболочки задней стенки глотки. Температура тела, как правило, нормальная. Продолжительность болезни 5–7 сут. У части больных (9–24%) наблюдаются лихорадка, симптомы интоксикации, кашель сухой или с мокротой, в легких при аускультации могут выслушиваться хрипы. В ряде случаев (3–8%) коронавирусная инфекция протекает с поражением нижних дыхательных путей и характеризуется развитием пневмонии, которая наиболее тяжело протекает у детей раннего возраста [1, 26, 27, 29].
Описаны нозокомиальные вспышки коронавирусной инфекции, проявляющиеся синдромом острого гастроэнтерита [23, 30].
Иммунитет после перенесенного заболевания непродолжительный и не защищает от реинфекции [1, 8, 16, 17].
Тяжелый острый респираторный синдром (ТОРС)
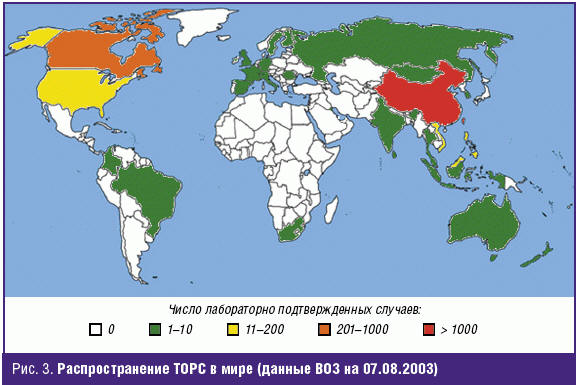
ТОРС, этиологически связанный с SARS-CoV, был впервые зафиксирован в ноябре 2002 г. в провинции Гуандун (КНР) [7, 31, 32]. Отметим попутно, что часто используемое в русскоязычной литературе название «атипичная пневмония» является некорректным и должно быть исключено из научного обихода. К августу 2003 г. ВОЗ сообщила о 8 422 случаях в 30 странах с 916 (10,9%) смертельными исходами [32]. До 60% от всех летальных исходов приходится на медицинских работников. Наибольшее количество заболевших зарегистрировано в Китае, Сингапуре, Канаде. Один завозной случай ТОРС был зарегистрирован и в Российской Федерации, в Благовещенске (рис. 3).
Природным резервуаром SARS-CoV являются летучие мыши (Chiroptera: Microchiroptera). От летучих мышей в природе заражаются виверровые (Viverridae), которых жители Юго-Восточной Азии держат в качестве домашних животных и часто употребляют в пищу. Наиболее вероятен следующий путь проникновения SARS-CoV в человеческую популяцию: летучие мыши → мелкие дикие млекопитающие (гималайские циветты (Paguma larvata), енотовидные собаки (Nyctereutes procyonoides), бирманские хорьковые барсуки (Melogale personata), etc.) → непрожаренное мясо в ресторанах → человек [7, 33, 34].
Инкубационный период в среднем продолжается 2–7 сут, в ряде случаев составляет 10 сут. Начало болезни острое, озноб (97% случаев), температура тела повышается до 38–39 °C (100% случаев). В первые дни преобладают симптомы интоксикации: головная боль (84%), головокружение (61%), слабость (100%), боль в мышцах (81%). Катаральные симптомы в начальном периоде выражены умеренно: может наблюдаться легкий кашель (39%), боль в горле (23%) и ринит (23%) [35]. После 3–7 сут болезни развивается респираторная фаза с выраженными признаками поражения нижних дыхательных путей: усиливается кашель, появляется одышка, чувство нехватки воздуха. При осмотре больных в нижнебоковых и задних отделах грудной клетки определяется притупление перкуторного звука, при аускультации на фоне ослабленного дыхания выслушиваются влажные мелкопузырчатые и крепитирующие хрипы, тахикардия. Нарастает гипоксия и гипоксемия. При рентгенологическом исследовании в легких выявляются мультифокальные инфильтраты с тенденцией к слиянию. У некоторых больных помимо респираторного синдрома наблюдаются признаки поражения желудочно-кишечного тракта: тошнота, повторная рвота, диарея, которая отмечается, по данным различных исследований, до 30% случаев. У подавляющего большинства больных (80–90%) заболевание заканчивается выздоровлением [1, 29, 35].
При прогрессировании болезни у части больных (10–20%) отмечается синдром острого повреждения легких или острый респираторный дистресс-синдром, который чаще всего диагностируется на 3–5 сут пневмонии, однако есть данные о его развитии в первые 2 сут болезни. У больного усиливается сухой кашель, одышка, выявляется тахипноэ, тахикардия. Как правило, температурные значения в этот период очень высокие, артериальное давление снижается. Повышение РаСО2 вызывает угнетение дыхания, алкалоз сменяется ацидозом, нарастает отек легких, экссудат заполняет интерстициальные пространства, развивается общая дыхательная недостаточность.
Рентгенологически в легких определяются одно- и двусторонние плотные инфильтраты. Вирусиндуцированные изменения в нижних дыхательных путях, активация бактериальной флоры вызывают двусторонние сливные долевые пневмонии. В участках некротических изменений в последующем разрастается соединительная ткань, образуются фиброзные рубцы (10%). В периферической крови уже в начале болезни отмечается лимфопения, при развернутом респираторном синдроме наблюдается лейкопения (2,6 × 109 л-1), тромбоцитопения (50–150 × 103). Повышение активности креатинкиназы, печеночных ферментов (аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ)), концентрации С-реактивного белка отмечается у подавляющего числа больных пневмонией. Мультивариантный анализ клинических данных свидетельствует, что тяжелые сопутствующие заболевания и высокий уровень С-реактивного белка в начале болезни являются плохим прогностическим признаком. Летальность, по данным различных исследований, колеблется от 4% до 19,7%, а в группе больных, находящихся на искусственной вентиляции легких, она составила 57,7%. Из осложнений отмечается периферическая полинейропатия, острая печеночная недостаточность, бактериальная и грибковая суперинфекция. Сопутствующие заболевания и пожилой возраст повышают риск тяжелого течения болезни с неблагоприятным исходом [1, 29, 31, 35, 36].
Ближневосточный респираторный синдром (БВРС)
Первые случаи заболевания БВРС, как удалось установить ретроспективно, появились у людей, побывавших в Саудовской Аравии, в апреле 2012 г. [37]. С сентября 2012 г. ВОЗ проводит регулярный мониторинг случаев БВРС в соответствии с Международными медико-санитарными правилами. В мае 2013 г. на специальном заседании группы экспертов Международного комитета по таксономии вирусов возбудитель БВРС получил свое современное название — MERS-CoV и место в таксономической системе царства Virae (табл. 1–2) [9, 38].
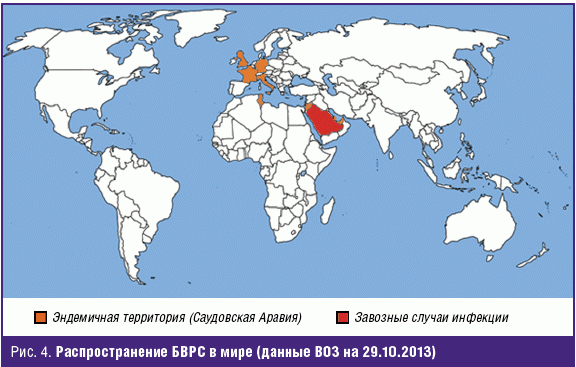
Основная заболеваемость наблюдается в восточной части Саудовской Аравии. Завозные случаи заболевания выявлены в других странах Ближнего Востока (в Иордании, Катаре, ОАЭ), северной Африке (в Тунисе), а в Европе — во Франции, Германии, Великобритании и Италии (рис. 4). На 29.10.2013 лабораторно подтверждены 145 случаев заболевания, из которых 62 (42,8%) оказались летальными [39]. Установлена возможность передачи вируса от человека к человеку при тесном контакте (в том числе — и медицинским работникам) [40].
Природным резервуаром этого коронавируса, как показали результаты молекулярно-генетического изучения, являются летучие мыши [41–43]. Промежуточный хозяин БВРС — источник заражения людей — пока не выявлен. Имеются данные о том, что этим вирусом могут заражаться верблюды [44]. Нельзя исключать возможность прямой передачи инфекции людям через продукты жизнедеятельности летучих мышей, дневки которых могут находиться на чердаках жилых строений. Необходимо помнить, что обитающие у нас виды летучих мышей, подобно птицам, осуществляют сезонные миграции, зимуя на эндемичной по БВРС территории. Таким образом, этот вирус может быть занесен к нам, помимо инфицированных людей, также и летучими мышами.
Клиническая картина БВРС — это ОРВЗ, которое сопровождается лихорадкой, кашлем, одышкой, затрудненным дыханием и в большинстве клинически подтвержденных случаев быстро переходит в тяжелую первичную вирусную пневмонию. У пациентов, страдающих хроническими заболеваниями органов дыхания и сердечно-сосудистой системы, метаболическим синдромом и иммунодефицитными состояниями различного генеза, на первый план в качестве ведущих симптомов могут выдвигаться поражения желудочно-кишечного такта: почечная недостаточность и диарея. ВОЗ рекомендует [45] рассматривать в качестве возможного БВРС, требующего соответствующих лабораторного подтверждения, санитарно-гигиенических мероприятий и госпитального мониторинга, все случаи ОРВЗ, осложненные ОРДС, при наличии эпидемиологических показаний — пребывания на Ближнем Востоке в течение 14 сут до начала заболевания.
Описаны легкие и бессимптомные случаи заболевания, что вызывает беспокойство специалистов в связи с возможностью скрытого распространения заболевания, хотя реальная оценка вероятности такого сценария до сих пор остается неопределенной [46].
Лабораторная диагностика коронавирусной инфекции включает детекцию вирусной геномной РНК методом ОТ-ПЦР в биологическом материале (кровь, моча, назальный секрет). Этот метод особенно важен для ранней диагностики особо опасных ТОРС и БВРС. Изоляция вируса проводится методом биопробы на модели клеточных культурах (например, Vero E6 или MDCK; рекомендуется добавлять трипсин в культуральную среду). Учитывая наличие у вирионов коронавирусов характерных морфологических черт (рис. 1), существенное значение в диагностике коронавирусных заболеваний может иметь электронная микроскопия. Индикация специфических противовирусных антител проводится с помощью твердофазного иммуноферментного анализа (ИФА), реакции связывания комплемента (РСК) и реакции непрямой гемагглютинации (РНГА), позволяющих определить диагностические титры антител уже на 5-е сут после инфицирования (РНГА) [1].
Достоверные данные о клинической эффективности противовирусных препаратов при лечении ТОРС и БВРС, полученные в рамках контролируемых исследований, отсутствуют. Однако можно предполагать эффективность противовирусных средств с широким механизмом действия (например, Рибивирина или Ингавирина). На модели ТОРС были протестированы in vitro 19 антивирусных препаратов: 7 на основе ИФН, 5 аналогов нуклеозида, 3 ингибитора протеаз, 2 ингибитора полимеразы и 2 ингибитора NA. При этом 100-процентное подавление цитопатического действия (ЦПД) было достигнуто при использовании 5000 МЕ/мл Бетаферона, Алферона и Веллферона. Рибавирин имеет ингибирующую активность, но только при высоких концентрациях (0,5–5,0 мг/мл), оказывая цитотоксическое действие на клеточную культуру [27]. Предполагается, что лечение ИФН (Веллферон, Мультиферон, Бетаферон, Алферон) в дозах, используемых для лечения гепатита С, может быть эффективным. Рибавирин может применяться по 8–12 мг/мл каждые 8 ч в течение 7–10 сут при тяжелых формах болезни.
При тяжелых и среднетяжелых формах респираторных заболеваний человека проводится дезинтоксикационная терапия (гемодез, реопиглюкин и т. п.). Объем вводимой жидкости не превышает 400–800 мл/сут.
Наряду с инфузионной терапией необходимо назначение диуретиков из-за угрозы отека легких. Показано введение донорского иммуноглобулина, содержащего антитела к коронавирусам в высоком титре.
При остром респираторном дистресс-синдроме основой патогенетической терапии являются препараты сурфактанта, восстанавливающие поверхностное натяжение в альвеолах. Сурфактант назначается эндотрахеально (150–200 мл). Показано введение глюкокортикоидов (преднизолон, гидрокортизон), в тяжелых случаях рекомендуется в/в введение метилпреднизолона. Для респираторной поддержки показана интубация трахеи и искусственная вентиляция легких с использованием малых дыхательных объемов (VT = 6 мл/кг) [47].
Антибиотики широкого спектра действия назначают при риске активации собственной бактериальной флоры больного.
В настоящее время вакцинопрофилактика против коронавирусных инфекций (включая особо опасные ТОРС и БВРС) не разработана.
Хотя ВОЗ и не рекомендует проводить специальный скрининг в пунктах въезда в связи с эпидемической ситуацией по БВРС и вводить какие-либо ограничения на перемещение людей или товаров, Минздрав Российской Федерации рекомендует воздержаться от поездок в страны Ближнего Востока с высоким риском заражения (рис. 4) без особой необходимости.
Статья опубликована в журнале Лечащий Врач
материал MedLinks.ru