Применение СИ в терапии средней и тяжелой форм акне является эффективным и безопасным и соответствует требованиям к современным принципам лечения. На российском фармацевтическом рынке зарегистрирован новый препарат Верокутан®. Опыт его использования для лечения больных акне продемонстрировал высокую терапевтическую эффективность и низкий риск формирования серьезных нежелательных явлений. Высокие эффективность, безопасность и оптимальный фармакоэкономический индекс повышают комплаентность пациентов.
Ключевые слова: акне, экспосом, синтетические ретиноиды, системная терапия, эффективность, безопасность, изотретиноин, Верокутан®.
Для цитирования: Матушевская Е.В., Антонова Л.А., Матушевская Ю.И., Петрова К.С. Клинический опыт применения системного изотретиноина в лечении тяжелых форм акне // РМЖ. 2018. №82. С. 109-112
E.V. Matushevskaya1, L.A. Antonova2,3, Yu.I. Matushevskaya4, K.S. Petrova5
1 Institution of Advanced Training, Federal Medical and Biological Agency, Moscow
2 Krasnoyarsk Interdistrict Outpatient Department
3 Epilation and Cosmetology Center «Electra» LLC, Krasnoyarsk
4 Lyubertsy Dermatovenerologic Clinic, Moscow Region
5 Volga Research Medical University, Nizhny Novgorod
For the treatment of medium and severe forms of acne, the prescription of systemic drugs as antibiotics, hormonal drugs, synthetic retinoids is indicated. The article presents data on the effectiveness and safety of systemic isotretinoin (SI) in the practice of a dermatologist in the treatment of acne. Issues of the acne pathogenesis, a formation of the phenotypic heterogeneity of the Cutibacterium acnes bacterium are considered, an exposome analysis and its effect on the severity and persistence of acne is carried out. Recommendations are given on the management of patients with acne, depending on the form and severity of the pathological process using SI based on current domestic and foreign recommendations. Data of the clinical use of the drug Verocutane® (based on SI) for the treatment of severe forms of acne are presented.
The SI application in the treatment of medium and severe forms of acne is effective and safe and meets the requirements of modern principles of treatment. A new drug Verocutane® is registered on the Russian pharmaceutical market. The experience of its use in the treatment of patients with acne has demonstrated a high therapeutic efficacy and low risk of serious adverse events. High efficacy, safety, and an optimal pharmacoeconomic index increase patient compliance with acne therapy.
Key words: acne, exposome, synthetic retinoids, systemic therapy, efficacy, safety, isotretinoin, Verocutane®.
For citation: Matushevskaya E.V., Antonova L.A., Matushevskaya Yu.I., Petrova K.S. Clinical experience of using systemic isotretinoin in the treatment of severe forms of acne // RMJ. 2018. № 8(II). P. –112.
В статье представлены данные по изучению эффективности и безопасности системного изотретиноина в практике врача-дерматолога в лечении акне. Даны рекомендации по ведению больных акне в зависимости от формы и тяжести патологического процесса на основании современных отечественных и зарубежных рекомендаций.
Введение
Акне — наиболее распространенное заболевание в практике дерматолога и косметолога, среди всех случаев дерматологических заболеваний составляет 20–30% [1]. По данным различных клинико-эпидемиологических исследований, акне чаще всего начинается в пубертатном периоде и регистрируется у 44,1–94,9% лиц подросткового возраста, у 18,4–50,9% лиц старше 21 года [2, 3]. В 15–30% случаев больные акне нуждаются в медицинской помощи, что обусловлено либо тяжестью заболевания, либо его продолжительностью [4]. Несмотря на активное изучение акне, остается ряд вопросов, требующих дальнейшего решения: совершенствование терапии и разработка новых эффективных методов лечения [5, 6].
Патогенез акне
В настоящее время акне рассматривают как воспалительное заболевание с хроническим рецидивирующим течением, характеризующееся гиперплазией сальных желез, гиперкератозом и образованием комедонов — сально-роговых пробок в протоках сальных желез с частичной или полной их закупоркой. У половины больных акне отмечается наличие генетической предрасположенности. Показано, что патогенез заболевания ассоциирован с полиморфностью многих генов [7–10]. Основные патогенетические факторы развития акне связаны с генетически опосредованными явлениями — увеличенной продукцией кожного сала и дисбалансом липидов секрета сальных желез [7, 11, 12].
Изменение состава липидов крови также может отражаться на изменении дифференцировки кератиноцитов и вызывать фолликулярный гиперкератоз. В свою очередь, липиды играют значительную роль в трансдукции внутриклеточных сигналов и регуляции различных сигнальных путей. Так, липиды сальных желез стимулируют продукцию себоцитами как про-, так и противовоспалительных цитокинов за счет активации ядерных факторов транскрипции.
Большую роль в развитии акне играют бактерии Propionibacterium acnes, которые несут на своей поверхности лиганды Толл-подобных рецепторов (TLR) и вызывают активацию врожденного иммунитета [13]. В обзоре последних обновлений B. Dreno et al. (2018) сообщают о внесении изменений в таксономию бактерий [14]. В современной классификации изменено название Propionibacterium acnes на Cutibacterium acnes в систематике бактерий. C. acnes относится к роду Cutibacterium, который входит в семейство пропионовокислых бактерий Propionibacteriaceae.
Последние данные по изучению C. acnes показали важную роль микробиоты кожи в развитии акне. С применением метагеномных исследований C. acnes у здоровых и больных акне выявлена фенотипическая гетерогенность бактерии, изучены различные филотипы, включая акне-ассоциированный филотип IA. Выявлены специфические факторы, которые определяют различия филотипов C. acnes [15, 16]. Формирование биопленок, высокий воспалительный потенциал и вирулентность отдельных филотипов C. acnes могут усиливать их патогенетическую значимость в развитии акне. Изменение микробиоты кожи вместе с активацией врожденного иммунитета могут привести к хроническому воспалительному состоянию.
Есть много других факторов, которые влияют на степень тяжести, а также на распространенность и персистирование акне, — это факторы окружающей среды, гормоны, отягощенный семейный анамнез, стресс [17]. Экспосом акне определяется как сумма всех факторов окружающей среды, влияющих на возникновение, продолжительность и тяжесть заболевания [18]. Экспосом-факторы, включая питание, медикаменты, загрязняющие вещества, климатические факторы и психосоциальный образ жизни, могут влиять на течение и тяжесть акне путем взаимодействия с эпидермальным барьером, сальными железами, врожденным иммунитетом и микробиотой кожи [19, 20].
Большое значение в развитии или обострении заболевания играют пищевые факторы, такие как инсулиногенная пища, в первую очередь молочные продукты [21, 22].
Однозначно показана связь акне и инсулиноподобного ростового фактора-1 (IGF-1) [23]. Употребление высокогликемичной и молочной пищи вызывает повышение сахара в крови и, соответственно, инсулина и IGF-1. Показано, что повышение IGF-1 ведет к повышению дигидротестостерона в крови. Дигидротестостерон запускает целый каскад явлений, которые приводят к изменению состава липидов кожи, дифференцировке кератиноцитов, что вызывает основной симптом акне — фолликулярный гиперкератоз. В нескольких исследованиях показано, что уровень IGF-1 в крови коррелирует с активностью заболевания.
Таким образом, патофизиология акне представляет собой сложный процесс, в котором учитывается несколько факторов. Микробиом и врожденный иммунитет — одни из центральных патогенетических факторов, которые принимают участие в развитии воспалительной реакции кожи. Два других фактора — это повышенная выработка кожного сала с изменением его состава и гиперкератинизация волосяных фолликулов в результате гиперпролиферации и аномальной дифференциации кератиноцитов верхней части фолликула [24, 25]. Дальнейшее изучение патогенеза акне открывает новые перспективы в лечении этого заболевания.
Лечение акне
Лечение акне представляет собой определенные сложности. Выбор метода терапии зависит от клинической формы и степени тяжести дерматоза: при легком течении заболевания используются только наружные средства, для терапии средних и тяжелых форм показаны препараты системного действия — антибиотики, гормональные препараты, синтетические ретиноиды. Международные рекомендации по лечению акне предлагают рассматривать системный изотретиноин (СИ) — синтетический ретиноид — в качестве первой линии терапии. Согласно последним российским и европейским рекомендациям (European Dermatology Forum, 2016 г.), СИ признан наиболее эффективным средством терапии тяжелых форм акне [26, 27].
Эффективность изотретиноина обусловлена его плейотропным эффектом. СИ воздействует на все основные патогенетические механизмы заболевания, снижает продукцию кожного сала, уменьшает размер сальных желез до 90%, способствует устранению иммунного воспаления в перифолликулярной зоне. Показатели эффективности лечения, частота развития рецидивов и фармакоэкономические расчеты безусловно указывают на превосходство СИ перед другими методами лечения тяжелых форм акне.
В большинстве исследований показано, что для достижения оптимального ответа на лечение и минимизации риска рецидивов больным акне необходимо назначать более высокие дозы СИ и более высокую кумулятивную дозу. Оптимальный режим дозирования при лечении тяжелых форм акне обычно составляет 0,5–1,0 мг/кг/сут. Курсовая доза изотретиноина должна составлять от 120 до 150 мг/кг [28].
При акне средней тяжести возможно применение низких доз СИ. Режим низких доз ассоциирован с меньшей частотой развития нежелательных явлений, что ведет к лучшей переносимости и повышению приверженности пациентов лечению.
Для безопасности терапии СИ следует контролировать лабораторные параметры, главным образом показатели функции печени и липидограмму. Хорошо известны тератогенный эффект СИ и риск эмбриопатии. С целью предотвращения случаев приема СИ во время беременности необходимо соблюдать требования утвержденной FDA (США) программы управления риском iPledge [29].
Собственные наблюдения
Всем больным была проведена монотерапия препаратом Верокутан®, который зарегистрирован в России с 2015 г. (РУ № ЛП-002988 от 07.05.2015). Верокутан® выпускается в форме капсул, содержащих 10,0 или 20,0 мг изотретиноина в качестве активного вещества, является дженериком с доказанной биоэквивалентностью референтному препарату [30]. Стоимость курсовой дозы препарата Верокутан® в 1,5–2 раза ниже, чем у аналогов [31].
Суточная доза препарата Верокутан® зависела от массы тела пациентов, выраженности побочных реакций и формы заболевания. Продолжительность лечения определялась сроками достижения кумулятивной курсовой дозы препарата — 120–150 мг/кг и в среднем составила 22,24±3,47 нед.
У всех больных определялась тяжесть заболевания по дерматологическому индексу акне (ДИА), учитывающему количество комедонов, папул, пустул и узлов по следующим параметрам: единичные — 15 баллов. ДИА
Перед началом терапии, ежемесячно во время терапии и после ее окончания проводилось биохимическое и клиническое исследование венозной крови, выполнялись тесты на беременность для женщин.
Приводим несколько собственных клинических наблюдений применения препарата Верокутан® у больных акне.
Первое наблюдение: пациент А., 18 лет, диагноз: акне (рис. 1).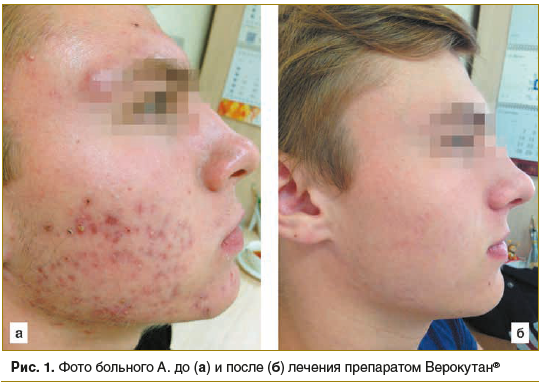
Из анамнеза известно, что впервые высыпания на коже лица появились в 12-летнем возрасте. Лечился амбулаторно у дерматолога по месту жительства (наружными средствами) с временным незначительным положительным эффектом. В течение последних 2 лет появились жалобы на распространение высыпаний и выраженную сальность кожи лица и волосистой части головы.
На момент осмотра сопутствующие заболевания не выявлены, аллергических реакций нет. Локальный статус при поступлении: на коже щек и подбородке отмечались папулезные элементы конической формы величиной до 4 мм, отдельные пустулы, атрофические рубцы. ДИА соответствовал 8 баллам, что можно интерпретировать как акне средней степени тяжести.
Пациенту был назначен Верокутан® в рекомендуемой дозе 0,5 мг/кг, длительность терапии — 24 нед.
Второе наблюдение: пациентка Р., 23 года, диагноз: акне (рис. 2).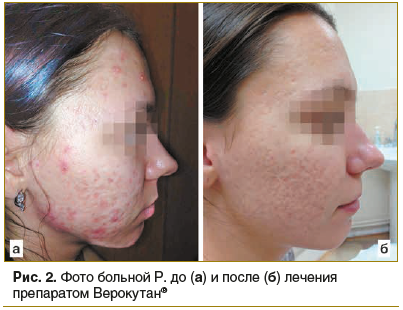
Первые проявления заболевания появились в подростковом возрасте. Из анамнеза жизни следует отметить нерегулярные менструации с 12 лет с длительностью цикла до 40 дней. Сопутствующих заболеваний на момент осмотра не выявлено. Семейный анамнез без особенностей. Вредных привычек не имеет. В плане проведенного лечения можно отметить назначение нескольких курсов системных антибиотиков. Эффект был временный, отмечалось быстрое рецидивирование процесса. Локальный статус при поступлении: при осмотре на фоне жирной кожи лица и эритемы в области лба и щек имеются множественные папулы и пустулы (отдельные элементы размерами до 0,5 см), большое количество атрофических рубцов, множественные открытые и закрытые комедоны. ДИА соответствовал 12 баллам, что было расценено как акне тяжелой степени тяжести.
Пациентке Р. было начато лечение препаратом Верокутан® в стартовой дозе 0,5 мг/кг/сут. Учитывая вес пациентки (56 кг), назначена доза 30 мг/сут. Отмечалась хорошая переносимость препарата. Через месяц доза была увеличена до 1,0 мг/кг/сут. Лечение продолжалось до достижения курсовой дозы 120 мг/кг.
Изменения в биохимическом анализе крови у обоих пациентов не были зарегистрированы. Среди побочных явлений в процессе лечения отмечены транзиторные осложнения: у пациента А. — хейлит, у пациентки Р. — ретиноевый дерматит. Важно отметить, что эти осложнения не являлись серьезными, не требовали коррекции дозировки препарата или прекращения проводимой терапии. С помощью назначения дерматокосметики осложнения были купированы.
У больных в процессе лечения препаратом Верокутан® зарегистрирована выраженная и достоверная положительная динамика ДИА, отражающего тяжесть течения акне и формирование клинической ремиссии, что является важным показателем эффективности терапии акне.
Заключение
Применение СИ в терапии средней и тяжелой форм акне является эффективным и безопасным и соответствует требованиям современных принципов лечения. На российском фармацевтическом рынке зарегистрирован новый препарат Верокутан® (на основе СИ) (АО «Верофарм» — группа Abbott), который производится в соответствии со стандартами общепризнанной в мире надлежащей производственной практики (GMP).
Опыт клинического применения препарата Верокутан® для лечения больных акне продемонстрировал высокую терапевтическую эффективность и низкий риск серьезных нежелательных явлений, что обусловливает целесообразность его активного применения с целью повышения качества оказания медицинской помощи больным акне. Высокая эффективность, безопасность и оптимальный фармакоэкономический индекс повышают комплаентность пациентов.
Литература
1. Nast A., Dreno B., Bettoli V. et al. European evidence-based (S3) guidelines for the treatment of acne // J. Eur. Acad. Dermatol. Venereol. 2012. Vol. 26(Suppl 1). P.1– 29.
2. Cordain L., Linderberg S., Hurtado M. et al. Acne vulgaris: a desease of Western civilization // Arch. Dermatol. 2002. Vol. 119. P.1317–1322.
3. Dreno B., Poli F. Epidemiology of acne // Dermatol. 2003. Vol. 206(1). P.7– 10.
4. Silverberg J.I., Silverberg N.B. Epidemiology and extracutaneous comorbidities of severe acne in adolescence: a U.S. population based study // Br. J. Dermatol. 2014. Vol. 170. P.1136–1142.
5. Lee M.R. Cooper A. Acne vulgaris in monozygotic twins // Australas J. Dermatol. 2006. Vol. 47. P.145.
6. Thiboutot D., Gollnick H., Bettoli V. et al. New insights into the management of acne: an update from the Global Alliance to Improve Outcomes in Acne group // J. Am. Acad. Dermatol. 2009. Vol. 60. P.1–50.
7. Lynn D.D., Umari T., Dunnick C.A., Dellavalle R.P. The epidemiology of acne vulgaris in late adolescence // Adolescent Health Med. Ther. 2016. Vol. 7. P.13–25.
8. Zhang M., Qureshi A.A., Hunter D.J., Han J. A genome-wide association study of severe teenage acne in European Americans // Human genetics. 2014. Vol. 33(3). P.259–264.
9. Hussain S., Faraz A., Iqbal T. The RETN gene rs1862513 polymorphism as a novel predisposing marker for familial Acne vulgaris in a Pakistani population // Iran J. Basic Med. Sci. 2015. Vol. 18(5). P.526–528.
10. Yaykasli K.O., Turan H., Kaya E., Hatipoglu O.F. Polymorphisms in the promoters of MMP-2 and TIMP-2 genes in patients with acne vulgaris // Internat. J. Clin. Experiment Med. 2013. Vol. 6(10). P.967–972.
11. Alestas T., Ganceviciene R., Fimmel S. et al. Enzymes involved in the biosynthesis of leukotriene B4 and prostaglandin E2 are active in sebaceous glands // J. Mol. Med. (Berl.). 2006. Vol. 84. P.75–87.
12. Zouboulis C.C., Jourdan E., Picardo M. Acne is an inflammatory disease andalterations of sebum composition initiate acne lesions // J. Eur. Acad. Dermatol. Venereol. 2014. Vol. 28. P.527–532.
13. Nagy I., Pivarcsi A., Kis K. et al. Propionibacterium acnes and lipopolysaccharide induce the expression of antimicrobial peptides and proinflammatory cytokines/chemokines in human sebocytes // Microbes Infect. 2006. Vol. 8. P.2195–2205.
14. Dreno B., Pecastaings S., Corvec S. et al. Cutibacterium acnes (Propionibacterium acnes) and acne vulgaris: a brief look at the latest updates // J. Eur. Acad. of Dermatol. and Venereol. 2018. Vol. 32(Suppl.2). P.5–14.
15. Omer H., McDowell A., Alexeyev O.A. Understanding the role of Propionibacterium acnes in acne vulgaris: the critical importance of skin sampling methodologies // Clin. Dermatol. 2017. Vol. 35. P.118–129.
16. Kwon H.H., Suh D.H. Recent progress in the research about Propionibacterium acnes strain diversity and acne: pathogen or bystander? // Int. J. Dermatol. 2016. Vol. 55. P.1196–1204.
17. Lynn D.D., Umari T., Dunnick C.A., Dellavalle R.P. The epidemiology of acne vulgaris in late adolescence // Adolesc. Health Med. Ther. 2016. Vol. 7. P.13–25.
18. Dreno B., Bettoli V., Araviiskaia E. et al. The influence of exposome on acne // J. Eur. Acad. of Dermatol. and Venereol. 2018. Vol. 32. P. 812–819.
19. Murillo N., Raoult D. Skin microbiota: overview and role in the skin diseases acne vulgaris and rosacea // Future Microbiol. 2013. Vol. 8. P.209–222.
20. Wolf R., Parish L.C. Effect of soaps and detergents on epidermal barrier Function // Clin. Dermatol. 2012. Vol. 30. P.297–300.
21. Adebamowo C.A., Spiegelman D., Danby F.W. et al. High school dietary dairy intake and teenage acne // J. Am. Acad. Dermatol. 2005. Vol. 52. P.207–214.
22. Smith R.N., Mann N.J., Braue A. et al. The effect of a high-protein, low glycemic-load diet versus a conventional, high glycemic-load diet on biochemical parameters associated with acne vulgaris: a randomized, investigator-masked, controlled trial // J. Am. Acad. Dermatol. 2007. Vol. 57. P.247–256.
23. Hoyt G., Hickey M.S., Cordain L. Dissociation of the glycaemic and insulinaemic responses to whole and skimmed milk // Br. J. Nutr. 2005. Vol. 93. P.175–177.
24. Suh D.H., Kwon H.H. What’s new in the physiopathology of acne? // Br. J. Dermatol. 2015. Vol. 172(Suppl 1). P.13–19.
25. Dreno B. What is new in the pathophysiology of acne, an overview // J. Eur. Acad. Dermatol. Venereol. 2017. Vol. 31(Suppl 5). P.8–12.
26. Болезни кожи. Инфекции, передаваемые половым путем. Федеральные клинические рекомендации. Дерматовенерология 2015. М.: Российское общество Дерматовенерологов и Косметологов. 2016. 768 с. [Bolezni kozhi. Infekcii, peredavaemye polovym putjom. Federal’nye klinicheskie rekomendacii. Dermatovenerologija 2015. M.: Rossijskoe obshhestvo Dermatovenerologov i Kosmetologov. 2016. 768 s. (in Russain)].
27. Nast A., Dreno B., Bettoli V. et al. European Evidence-based (S3). Guideline for the Treatment of Acne. Update 2016 // J. Eur. Acad. Dermatol. Venereol. 2016. Vol. 30(8). P.1261–1268.
28. Nast A., Dréno B., Bettoli V. et al. European Dermatology Forum. European evidence-based (S3) guidelines for the treatment of acne // J. Eur. Acad. Dermatol. Venereol. 2012. Vol. 6(Suppl 1). P.1–29.
29. Howard R., Smith G. The readability of iPledge program patient education materials // J. Am. Acad. Dermatol. 2018. DOI: 10.1016/j.jaad.2018.05.038.
30. Отчет «Открытое рандомизированное, перекрестное исследование сравнительной фармакокинетики и биоэквивалентности препаратов Вероизотретиноин, капсулы, 20 мг (ОАО «Верофарм», Россия) и Роаккутан, капсулы 20 мг («Р.П. Шерер», Германия)» / СПб. 2012. 29 с. [Otchet «Otkrytoe randomizirovannoe, perekrestnoe issledovanie sravnitel’noj farmakokinetiki i biojekvivalentnosti preparatov Veroizotretin oin, kapsuly, 20 mg (OAO «Verofarm», Rossija) i Roakkutan, kapsuly 20 mg (R.P.Sherer, Germanija)». SPb. 2012. 29 s. (in Russian)].
31. Data of Russian pharmaceutical portal. Average retail prices for medicines with INN Izotretinoin (capsules on 8, 10, 16 and 20 mg), 2018. [Электронный ресурс]. URL: https://www.pharmindex.ru/mnn/isotretinoin.html (дата обращения: от 07.10.2018).
32. Кочергин Н.А., Самгин М.А., Монахов С.А., Игнатьев Д. Дерматологический индекс акне // Эстетическая медицина. 2004. №3(1). С.62–65 [Kochergin N.A., Samgin M.A., Monahov S.A., Ignat’ev D. Dermatologicheskij indeks akne // Jesteticheskaja medicina. 2004. №3(1). S.62–65 (in Russain)].
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
Информация с rmj.ru





