ММР-7 и KL-6 играют диагностическую и прогностическую роль: в исследованиях показана обратно пропорциональная зависимость между концентрацией биомаркеров ММР-7 и KL-6 и прогнозом 5-летней выживаемости у больных с ИЛФ. Для прогноза ИЛФ имеет значение уровень содержания интерлейкина-8, который коррелирует с тяжестью данного заболевания. Диагностическая и прогностическая значимость биомаркеров у больных ИЛФ может быть установлена только с учетом клинико-анамнестических, рентгенологических и, в ряде случаев, морфологических методов исследования.
Ключевые слова: идиопатический легочный фиброз, патогенез, биомаркеры.
Для цитирования: Лещенко И.В., Жеребцов А.Д. Идиопатический легочный фиброз: современный взгляд на патогенез и роль биомаркеров // РМЖ. 2018. №10(I). С. 6-10
I.V. Leshchenko1,2, A.D. Zherebtsov1
1 Ural State Medical University, Yekaterinburg
2 Medical Association “Novaya Bolnitsa”, Yekaterinburg
The article is devoted to the pathogenesis of idiopathic pulmonary fibrosis (IPF) and the role of biomarkers in the diagnosis and asssessing of the severity of the disease. IPF is a special form of chronic progressive fibrosing interstitial pneumonia of unknown etiology. It is shown that IPF is a disease of the pulmonary epithelium, which manifests itself as fibrosis, i. e.it is caused by dysfunction of the pulmonary epithelium. The theory of the three-stage development of the IPF is considered. From a diagnostic and differential diagnostic point of view, at suspicion on IPF it is important to determine the level of serum SP-A. The diagnostic role of other biomarkers (evaluated in these studies) is not established. When determining the prognosis, IPF can have the value of IL-8, the level of which correlates with the severity of the disease. Studies have shown that the serum biomarkers SP-A, MMP-7 and KL-6 can play a diagnostic and prognostic role for IPF patients. An inverse relationship was found between the concentration of biomarkers MMP-7 and KL-6 and the prognosis of 5-year survival in patients with IPF. Diagnostic and prognostic significance of biomarkers in IPF patients can be established only taking into account clinico-anamnestic, radiological and, in some cases, morphological methods of investigation.
Key words: idiopathic pulmonary fibrosis, pathogenesis, biomarkers.
For citation: Leshchenko I. V., Zherebtsov A. D. Idiopathic pulmonary fibrosis: modern view of pathogenesis and the role of biomarkers // RMJ. 2018. № 10 (I). P. 6–10.
Статья посвящена вопросам патогенеза идиопатического легочного фиброза и определению роли биомаркеров в диагностике и оценке тяжести заболевания
Содержание статьи
Введение
Интерстициальные заболевания легких (ИЗЛ) в целом, в т. ч. идиопатический легочный фиброз (ИЛФ), – многогранные по своей природе легочные патологии. Считается, что первое описание интерстициального поражения легких сделал G. E. Rindfleisch в 1897 г., назвав заболевание cirrhosis cystica, а годом позже P. von Hansemann в своем наблюдении использовал термин lymphangitis reticularis [1]. С более современных позиций первое описание интерстициального поражения легких представили Хамман и Рич, которые своему случаю дали наименование «фульминантный диффузный интерстициальный фиброз легких» (fulminating diffuse interstitial fibrosis of the lungs), в дальнейшем измененное на «синдром Хаммана — Рича» [2]. Несмотря на то, что в настоящее время это название не применяется, открытие синдрома Хаммана — Рича внесло важный вклад в понимание интерстициальных поражений легких. Во-первых, на основе наблюдений пациентов с данным синдромом был выделен первый гистологический паттерн, ассоциированный с конкретным интерстициальным поражением легких, и, во‑вторых, стало понятно, что некоторые пациенты могут отвечать на терапию кортикостероидами, а у других данная группа препаратов вызывает обострение болезни. В 1948 г. Роббинс первым использовал термин «идиопатический легочный фиброз» для описания пациентов с интерстициальными изменениями на рентгенограммах грудной клетки, которые были похожи на легочный фиброз, но без идентифицированной причины. Одновременно с этим была признана взаимосвязь между фиброзом легких и постинфекционным фиброзом, пневмокониозом, последствиями лучевой терапии, аутоиммунными заболеваниями, такими как ревматоидный артрит или системный склероз.
Согласно современному пониманию ИЛФ определяется как особая форма хронической прогрессирующей фиброзирующей интерстициальной пневмонии неизвестной этиологии, которая возникает преимущественно у людей старшего возраста, поражает только легкие и связана с гистологическим и/или рентгенологическим паттерном обычной интерстициальной пневмонии [3]. Ряд современных исследователей считают, что данное название не отвечает актуальным открытиям в изучении ИЛФ [4]. Накопленные сведения позволяют выделить множество причин развития этого заболевания, что делает термин «идиопатический» уже нецелесообразным.
Современные вопросы патогенеза
Достаточно быстро стало понятно, что в основе ИЛФ лежит разрастание соединительной ткани. Первой концепцией патогенеза ИЛФ была концепция воспаления альвеолярной стенки, ведущего к продукции фиброгенных медиаторов. Однако применение стероидных противовоспалительных препаратов не дало желаемых результатов и приводило только к прогрессированию заболевания. Постепенно концепция повреждения альвеолярного эпителия вылилась в теорию о 3-стадийном развитии ИЛФ (рис. 1) [5].![Рис. 1. Схема трех стадий патогенеза ИЛФ [5] Рис. 1. Схема трех стадий патогенеза ИЛФ [5]](https://medblog.su/wp-content/uploads/2018/12/idiopaticheskij-legochnyj-fibroz-sovremennyj-vzglyad-na-patogenez-i-rol-biomarkerov-leshhenko-i-v-zherebtsov-a-d.png)
Стадия I — предиспозиция (предрасположенность). Суть ее заключается в наличии факторов, обусловливающих повышенную чувствительность альвеолярного эпителия к предполагаемым этиологическим агентам. В качестве этих факторов рассматриваются такие вирусы, как вирус Эпштейна — Барр, цитомегаловирус, вирус гепатита С, influenza, а также табачный дым, древесная пыль, домашний скот, экологические факторы, которые приводят к ускоренному делению альвеолоцитов II типа у генетически предрасположенных лиц, опосредуемому эндоплазматическим ретикулумом (ER-стрессом), активации развернутого белкового ответа (UPR), апоптоза, что в итоге приводит к прогрессирующему истощению (укорочению) теломер. На данном этапе приобретает определенное значение состояние сурфактанта, т. к. с ним контактируют повреждающие факторы. Аномалии белков сурфактанта SP-A и SP-D могут определять силу повреждающего фактора указанных выше антигенов [6].
Стадия II — активация.
Накопленные факторы воздействия окружающей среды у генетически предрасположенных лиц приводят к патологическим изменениям легочного эпителия (бронхоальвеолярного и альвеолярного): перепрограммированию физиологического старения клеток и высвобождению альвеолярным эпителием профибротических медиаторов, таких как трансформирующий ростовой фактор β (TGFβ) и тромбоцитарный фактор роста лиганд α (PDGFα). Эти медиаторы прямо или косвенно через лейкоциты активируют фибробласты, которые начинают вырабатывать патологический межклеточный матрикс (межклеточное вещество) [6, 7].
Стадия III — прогрессирование. Межклеточное вещество способствует дополнительной дифференцировке фибробластов в миофибробласты, которые откладывают еще больше матрикса и дополнительно активируют фибробласты, что приводит к ремоделированию ткани легкого. Ремоделирование легочной ткани изменяет экспрессию ряда веществ межклеточного матрикса, многие из которых способны активировать профибротические сигнальные пути в мезенхимальных клетках. Фибробласты при ИЛФ приобретают деструктивные свойства, что может способствовать хроническому ремоделированию [6, 7].
Роль биомаркеров в диагностике и лечении, оценке прогноза ИЛФ
В исследованиях биомаркеры ИЛФ рассматриваются в качестве необходимого инструмента дифференциальной диагностики, прогнозирования развития заболевания и ответа на лечение.
Общепризнанной классификации биомаркеров легочного фиброза на данный момент не существует. Мы разделили все основные биомаркеры на три большие группы, основанные на их значении:
– для диагностики и дифференциальной диагностики ИЛФ;
– определения прогноза ИЛФ;
– оценки эффективности таргетной антифибротической терапии.
Биомаркеры для диагностики и дифференциальной диагностики ИЛФ
Наибольшее количество исследований проведено в области оценки биомаркеров как метода диагностики ИЛФ и его дифференциальной диагностики с другими заболеваниями легких. Первыми и наиболее изученными являются белки сурфактанта. Уровень SP-A в сыворотке больных ИЛФ был значительно выше, чем у пациентов с другими ИЗЛ [8]. Также уровень SP-A был значительно выше у больных ИЛФ, чем у больных саркоидозом легких и пневмонией [8]. Уровень SP-D в сыворотке больных ИЛФ аналогично SP-A также оказался значительно выше, чем у больных пневмонией, саркоидозом легких и пациентов контрольной группы. В отличие от SP-A, не установлено существенной разницы в содержании SP-D у больных ИЛФ и другими ИЗЛ (включая прогрессирующий системный склероз, легочный альвеолярный протеиноз, идиопатическую неспецифическую интерстициальную пневмонию и саркоидоз).
Матриксные металлопротеиназы (ММР). Представляют собой семейство цинк- и кальцийзависимых эндопептидаз. Они играют важную роль во многих нормальных физиологических процессах, таких как эмбриональное развитие, морфогенез, репродукция и ремоделирование ткани, а также в различных патологических процессах: артритах, злокачественном росте и сердечно-сосудистых заболеваниях. Уровень ММР в здоровой легочной ткани ниже, чем в легком при ИЛФ [9]. По специфичности ММР разделяются на коллагеназы (ММР-1,-8 и -13), желатиназы (ММР-2 и -9) и стромелизины (ММР-3 и -10). Желатиназа A (MMP-2) и желатиназа B (MMP-9), по-видимому, участвуют в легочном фиброзе, но их особая роль в этом процессе остается неясной [10]. В то время как MMP-9 скорее высвобождается воспалительными клетками и может быть связана с воспалительным процессом, вызванным ремоделированием тканей, MMP-2 синтезируется структурными клетками, включая фибробласты, эндотелиальные и эпителиальные клетки, и может быть связана с хронически нарушенным ремоделированием тканей, что приводит к аномальному осаждению коллагена [10].
Нормальные легочные фибробласты не экспрессируют MMP-9 in vitro, тогда как фибробласты из легких, пораженных ИЛФ, напротив, усиленно ее экспрессируют. По-видимому, этот процесс, по меньшей мере частично, связан с секрецией желатиназ MMP-2 и MMP-9. В этом контексте как MMP-2, так и MMP-9 наблюдались в субэпителиально расположенных миофибробластах, а иногда и в зонах обнаженной альвеолярной базальной мембраны, что указывает на то, что эти ММР могут играть роль в миграции миофибробластов в альвеолярные пространства. MMP-7 экспрессируется в нормальных и патологически измененных эпителиальных клетках. MMP-7 синтезируется различными опухолями: молочной железы, толстого кишечника, простаты, желудка, верхних дыхательных путей и пищевода, легких и кожи.
Периостин. Сообщалось, что периостин был повышен у пациентов с ИЛФ, но его источники и механизмы действия остаются неясными [11]. Авторы обнаружили, что уровень периостина в сыворотке повышается у пациентов с ИЛФ, что коррелирует со снижением форсированной жизненной емкости легких (FVC) и диффузионной способности легких (DLсо) [12]. Установлено, что преимущественно периостин существует в олигомерной форме в сыворотке и мономерный периостин представлен как незначительная его фракция [13]. Диагностическое значение придается именно мономерному периостину, уровень которого значительно повышается при ИЛФ по сравнению с другими заболеваниями, также связанными с уровнем периостина (болезнь Альцгеймера, системная склеродермия и бронхиальная астма).
Биомаркеры определения прогноза ИЛФ
На обострение ИЛФ может указывать повышение уровней сурфактантов. В работах отмечалась связь высокого уровня SP-A со значительно более высоким риском смерти больных ИЛФ. Выявлена также аналогичная выраженная связь между высоким уровнем SP-D и повышенным риском смерти [8]. В одном исследовании показано, что мРНК IL-8 и белок IL-8 коррелировали с тяжестью заболевания [12]. Ley et al. рекомендуют использовать в качестве предиктора смерти у пациентов с ИЛФ индекс GAP, включающий пол, возраст и 2 переменные функции легких (FVC и DLco), основанный на простой системе подсчета очков и разработанный в результате исследования 558 больных с ИЛФ [14]. Только индекс GAP, лучевая диагностика и биомаркеры сыворотки крови в комплексе могут повысить точность и чувствительность определения прогноза пациентов с ИЛФ.
В исследовании, проведенном японскими учеными, авторы сравнили диагностическую и прогностическую ценность ряда сывороточных биомаркеров (ММР-7, CCL18, KL-6, SP-A и SP-D) в группе ИЛФ и группах сравнения [15]. В таблице 1 представлена характеристика субъектов, участвующих в исследовании [15].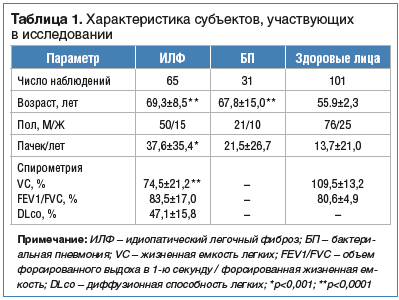
Различия значений пяти биомаркеров (ММР-7, CCL18, KL-6, SP-A и SP-D) методом анализа кривой ROC у пациентов с ИЛФ (n=65), больных с бактериальной пневмонией (n=31) и здоровых лиц (n=101) отражены в таблице 2 [15].![Таблица 2. Различия значений пяти биомаркеров (ММР-7, CCL18, KL-6, SP-A и SP-D) методом анализа кривой ROC у пациентов с ИЛФ (n=65), бактериальной пневмонией (n=31) и здоровых лиц (n=101) [15] Таблица 2. Различия значений пяти биомаркеров (ММР-7, CCL18, KL-6, SP-A и SP-D) методом анализа кривой ROC у пациентов с ИЛФ (n=65), бактериальной пневмонией (n=31) и здоровых лиц (n=101) [15]](https://medblog.su/wp-content/uploads/2018/12/1544211905_107_idiopaticheskij-legochnyj-fibroz-sovremennyj-vzglyad-na-patogenez-i-rol-biomarkerov-leshhenko-i-v-zherebtsov-a-d.png)
Статистически значимые достоверные различия уровней биомаркеров MMP-7, CCL18, KL-6, SP-A и SP-D у пациентов с ИЛФ, бактериальной пневмонией и группой контроля (здоровые лица) показаны на рисунке 2 [15].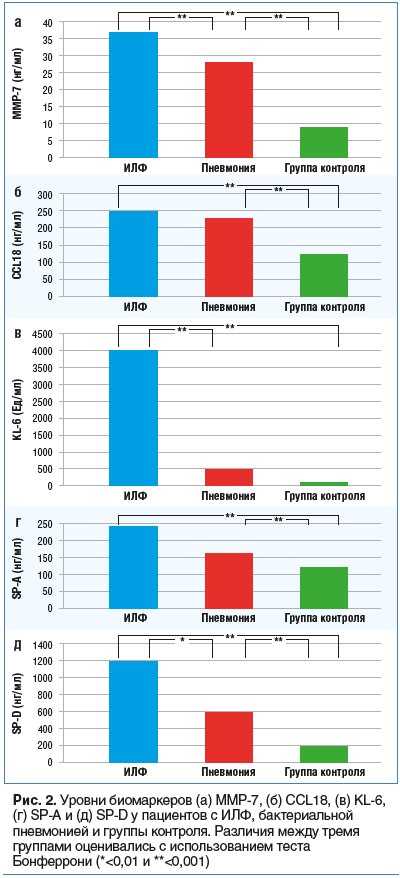
Также определено, какие биомаркеры являются независимыми предикторами прогноза у пациентов с ИЛФ. Многофакторный анализ Кокса чувствительности и специфичности, изученных в рассматриваемом исследовании биомаркеров в группах пациентов с ИЛФ, пневмонией и группе контроля, показал, что уровни биомаркеров MMP-7 и KL-6 являются независимыми предикторами прогноза у пациентов с ИЛФ. Кроме того, у пациентов с ИЛФ с повышенным уровнем MMP-7 и KL-6 были более низкие показатели выживаемости, а комбинация двух маркеров соответствовала наиболее высокому показателю смертности. Полученные результаты свидетельствуют, что и MMP-7, и KL-6 являются перспективными прогностическими маркерами ИЛФ, а комбинация двух маркеров способна улучшить оценку прогноза выживаемости у пациентов с ИЛФ. Кроме того, авторы данного исследования показали, что MMP-7 и KL-6 могут четко дифференцировать пациентов с ИЛФ от пациентов с бактериальной пневмонией и здоровых лиц, что еще раз указывает на их потенциал как диагностических биомаркеров.
Корреляции выживаемости пациентов с ИЛФ, разделенных на 3 группы по соотношению различных биомаркеров и выживаемости, представлены на рисунке 3.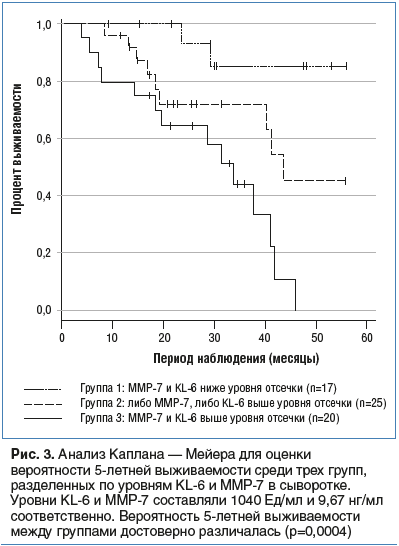
Настоящие результаты подтверждают, что у пациентов с ИЛФ с повышенным уровнем как MMP-7, так и KL-6 были более низкие показатели выживаемости, что свидетельствует о том, что оценка обоих факторов более эффективна при определении подгруппы высокого риска, чем индивидуальные оценки обоих биомаркеров. Предполагается, что MMP-7, семейство цинксодержащих ферментов с протеолитической активностью, и KL-6, высокомолекулярный гликопротеин, классифицированный как муцин MUC1, участвуют в прогрессировании ИЛФ с различными механизмами и требуют дальнейших перспективных исследований [16].
Биомаркеры для оценки эффективности таргетной антифибротической терапии
Увеличение производства ММР-8 и ММР-9 не сопровождается компенсаторным увеличением их основного эндогенного ингибитора, тканевого ингибитора металлопротеиназы-1 (TIMP-1) [17]. Поскольку объединенная активность этих двух ферментов может разрушить фибриллярные волокна и базальные мембраны коллагенов легочного интерстиция, их усиленная активность будет способствовать разрушению матрицы и ремоделированию в развитии фиброза. Анализ ММР-8 и ММР-9 из бронхоальвеолярной лаважной жидкости может обеспечить полезные биохимические маркеры для мониторинга эффективности и нежелательных явлений при лечении больных ИЛФ и саркоидозом легких в будущем.
Интересно проанализировать, может ли мономерный периостин прогнозировать эффективность двух одобренных Международным комитетом по ИЛФ ATS/ERS/JRS/ALAT антифибротических препаратов — пирфенидона и нинтаданиба [18]. Хотя и доказано, что эти препараты эффективны при лечении пациентов с ИЛФ, но до сих пор не найдены соответствующие биомаркеры прогноза эффективности этих лекарственных средств, что позволило бы разработать необходимую тактику ведения больных ИЛФ.
Заключение
Таким образом, с современных научных позиций патогенез ИЛФ рассматривается как 3-стадийный процесс, в результате которого вследствие дисфункции легочного эпителия (бронхоальвеолярного и альвеолярного) развивается фиброз легких.
Относительно биомаркеров ИЛФ установлено следующее. С диагностической и дифференциально-диагностической точки зрения при подозрении на ИЛФ необходимо определить уровень сывороточного SP-A. Диагностическая роль других биомаркеров не установлена. При определении прогноза ИЛФ может иметь значение IL-8, уровень которого коррелирует с тяжестью заболевания. Установлена обратно пропорциональная зависимость между концентрацией биомаркеров ММР-7 и KL-6 и прогнозом 5-летней выживаемости у больных с ИЛФ, однако достоверно установить их диагностическую и прогностическую роль еще предстоит. Представляет интерес изучение изменений и соотношения биомаркеров ИЛФ не по отдельности, а в совокупности. Мало серьезных работ в области оценки эффективности лечения по изменению концентрации биомаркеров, и имеющихся данных недостаточно даже для выделения потенциально пригодного биомаркера для таких целей. Еще одним недостатком опубликованных к настоящему времени исследований является их продолжительность. Для оценки прогностической возможности биомаркеров необходимы проспективные исследования. Диагностическая и прогностическая значимость биомаркеров у больных ИЛФ может быть установлена только с учетом клинико-анамнестических, рентгенологических и, в ряде случаев, морфологических методов исследования.
Литература
1. Homolka J. Idiopathic pulmonary fibrosis: a historical review // CMAJ. 1987. Vol. 137. P. 1003–1005.
2. Interstitial Lung Diseases / Edit. by Du Bois R. M., Richeldi L. Eur. Respir. Monograph, М: ERS. 2009. 395 p.
3. Диагностика и лечение идиопатического легочного фиброза. Федеральные клинические рекомендации [Электронный ресурс]. URL: www.pulmonology.ru. 2016 (дата обращения: 17.08.2018) [Diagnostika i lechenie idiopaticheskogo legochnogo fibroza. Federal’nye klini-cheskie rekomendacii [Jelektronnyj resurs]. URL: www.pulmonology.ru. 2016 (data obrashhenija 17.08.2018) (in Russian)].
4. Qiang D., Tracy L., Louise H. et al. New Insights into the Pathogenesis and Treatment of IPF: An Update // Drugs. 2011. Vol. 71 (8). P. 981–1001.
5. Paul J. W., Timothy S. B. Time for a change: is idiopathic pulmonary fibrosis still idiopathic and only fibrotic? // Lancet Respir. Med. 2018. Vol. 6. P. 154–160.
6. Giacomo S., Bruno I., Mariarosaria C. et al. Idiopathic pulmonary fibrosis: pathogenesis and management // Respir. Res. 2018. Vol. 19 (1). P. 32. DOI: 10.1186/s12931-018-0730-2.
7. Luca R., Harold R. C., Mark G. J. Idiopathic pulmonary fibrosis // Lancet. 2017. Vol. 389 (10082). P. 1941–1952.
8. Kai W., Qing J., Jing C. et al. Impact of serum SP-A and SP-D levels on comparison and prognosis of idiopathic pulmonary fibrosis // Medicine. 2017. Vol. 96. P. 23. DOI:10.1097/MD.0000000000007083.
9. Bhattacharyya P., Acharya D., Roychowdhury S. Role of matrix metalloproteinases in the pathophysiology of idiopathic pulmonary fibrosis // Lung India. 2007. Vol. 24. P. 61–65.
10. Henry M. T., McMahon K., Mackarel A. J. et al. Matrix metalloproteinases and tissue inhibitor of metalloproteinase-1 in sarcoidosis and IPF // Eur. Resp. J. 2002. Vol. 20. P. 1220–1227.
11. Shoichiro O., Masaki O., Kiminori F. et al. The usefulness of monomeric periostin as a biomarker for idiopathic pulmonary fibrosis // PLOS ONE. 2017. Vol. 12 (3). P. 1–17.
12. Guiot J., Henket M., Corhay J.– L. et. al. Sputum biomarkers in IPF: Evidence for raised gene expression and protein level of IGFBP-2, IL-8 and MMP-7 // PLOS ONE. 2017. Vol. 12 (2). P. 1–2.
13. Bentley J. B., Naik P. K., Bozyk P. D., Moore B. B. Periostin promotes fibrosis and predicts progression in patients with Idiopathic Pulmonary Fibrosis // AJP Lung Cell/ Mol. Physiol. 2012. Vol. 303. P. 12. DOI: 10.1152/ajplung.00139.2012. Epub 2012 Oct 5.
14. Ley B. A multidimensional index and staging system for idiopathic pulmonary fibrosis // Ann. Intern. Med. 2012. Vol. 15, 156 (10). P. 684–691.
15. Hamai K., Iwamoto H., Ishikawa N. et al. Comparative Study of Circulating MMP-7, CCL18, KL-6, SP-A, and SP-D as Disease Markers of Idiopathic Pulmonary Fibrosis // Disease Markers. 2016. Vol. 3. P. 1–8. http://dx.doi.org/10.1155/2016/4759040.
16. Rui N., Xiaohui L., Yuan Z. et al. Potential biomarkers of idiopathic pulmonary fibrosis discovered in serum by proteomic array analysis // Int. J. Clin. Exp. Pathol. 2016. Vol. 9 (9). P. 8922–8932.
17. Lagente V., Manoury B., Nénan S. et al. Role of matrix metalloproteinases in the development of airway inflammation and remodeling // Brazilian J. Med. Biol. Res. 2005. Vol. 38. P. 1521–1530.
18. Raghu G., Collard H. R., Egan J. J. et al. ATS/ERS/JRS/ALAT Committee on Idiopathic Pulmonary Fibrosis. An official ATS/ERS/JRS/ALAT statement: idiopathic pulmonary fibrosis; evidence-based guidelines for diagnosis and management // Am. J. Respir. Crit. Care Med. 2011. Vol. 183. P. 788–824.
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
Информация с rmj.ru