Эволюция представлений о функциональных заболеваниях желудочно-кишечного тракта в свете Римских критериев IV пересмотра (2016 г.)
Д.Н. Андреев1, А.В. Заборовский1, А.С. Трухманов2, И.В. Маев1, В.Т. Ивашкин2
1 ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава РФ, г. Москва, Российская Федерация
2 ФГБОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава РФ, г. Москва, Российская Федерация
- Андреев Дмитрий Николаевич — ассистент кафедры пропедевтики внутренних болезней и гастроэнтерологии ФГБОУ ВО «МГМСУ им. А.И. Евдокимова». Контактная информация: dna-mit8(а)mail.ru; 127473, Москва, ул. Делегатская, д. 20, стр. 1
- Маев Игорь Вениаминович — доктор медицинских наук, профессор, член-корреспондент РАН, заведующий кафедрой пропедевтики внутренних болезней и гастроэнтерологии ФГБОУ ВО «МГМСУ им. А.И. Евдокимова»
Цель обзора. Отразить современные представления о функциональных заболеваниях желудочно-кишечного тракта (ФЗ ЖКТ), а также проанализировать основные клинически релевантные изменения, внесенные в Римские критерии IV пересмотра (2016 г.) по сравнению с предшествующей редакцией.
Основные положения. Согласно новой дефиниции, предложенной экспертным советом Римского консенсуса IV пересмотра, ФЗ ЖКТ — это нарушение взаимодействия головного мозга и ЖКТ. Предложено исключить термин «функциональный». В обновленную классификацию ФЗ ЖКТ добавлены новые нозологические единицы с известным каузативным фактором (опиоидиндуцированная гастроинтестинальная гипералгезия, опиоидиндуцированный запор, каннабиноидиндуцированный рвотный синдром), гиперсенситивный рефлюксный синдром, синдром тошноты и рвоты (объединяет ранее выделявшиеся нозологии — хроническую идиопатическую тошноту и функциональную рвоту). В новой редакции Римских критериев конкретизирована тактика ведения пациентов с дисфункцией сфинктера Одди, а также уточнены критерии диагностики функциональной диспепсии и синдрома раздраженного кишечника.
Заключение. В обновленных Римских критериях произведена ревизия классификации ФЗ ЖКТ и уточнены диагностические критерии ряда нозологий.
Ключевые слова: Римские критерии IV пересмотра, функциональные заболевания, функциональная диспепсия, синдром раздраженного кишечника, алгоритм.
Для цитирования: Андреев Д.Н., Заборовский А.В., Трухманов А.С., Маев И.В., Ивашкин В.Т. Эволюция представлений о функциональных заболеваниях желудочно-кишечного тракта в свете Римских критериев IV пересмотра (2016 г.). Рос журн гастроэнтерол гепатол колопроктол 2017; 27(1):4-11 DOI: 10.22416/1382-4376-2017-27-1-4-11
Введение
Функциональные заболевания желудочно-кишечного тракта (ФЗ ЖКТ) — наиболее актуальная сфера современной гастроэнтерологии и область пересечения интересов практической и фундаментальной медицины. Данная тенденция обусловлена высокой распространенностью ФЗ ЖКТ в общемировой популяции, достигающей 15–25% взрослого населения развитых стран, а также недостаточностью данных о всех патогенетических звеньях, лежащих в основе развития этой патологии [1–3].
ФЗ ЖКТ не представляют непосредственной угрозы для жизни пациента, однако в значительной мере снижают качество его жизни [1, 4, 5]. Этот аспект приобретает особую актуальность в связи с тем, что ФЗ ЖКТ чаще развиваются у людей работоспособного возраста. «Яркость» восприятия болевого синдрома, частое рецидивирование симптомов и нередко меняющийся паттерн симптоматики приводят к значительному снижению работоспособности, обусловливая экономические потери, связанные с оформлением листков нетрудоспособности и снижением эффективности труда [6]. В системе здравоохранения увеличиваются прямые и косвенные экономические издержки в связи с необходимостью проведения диагностических мероприятий для исключения органической патологии [7, 8]. Такая характеристика ФЗ ЖКТ дает основание отнести их в класс социально значимых заболеваний.
С целью систематизации накопленных данных и разработки алгоритмов диагностики ФЗ ЖКТ и лечения больных с этой патологией более 20 лет тому назад была создана экспертная группа по ее изучению, результатом деятельности которой явилось создание первых консенсусных рекомендаций, получивших название «Римские критерии». За это время дефиниция ФЗ ЖКТ, принципы их классификации и лечебно-диагностическая тактика эволюционировали с учетом новых данных как фундаментальной, так и клинической медицины. Актуализацию поступающей информации проводят с позиций доказательной медицины с учетом результатов рандомизированных контролируемых клинических исследований, систематических обзоров и мета-анализов. Последний пересмотр Римских критериев был произведен в 2016 г. [9]. В настоящей статье рассмотрены современные представления об этиологии и патогенезе ФЗ ЖКТ, а также проведен анализ основных клинически релевантных изменений, внесенных в Римские критерии IV пересмотра (РК IV) по сравнению с предшествующей редакцией.
Современные представления о генезе ФЗ ЖКТ
К моменту пересмотра предшествующей редакции Римских критериев накопилось большое количество новых данных о патофизиологических механизмах ФЗ ЖКТ. В последние десятилетия изучение этих заболеваний в значительной мере проводили с позиций нейрогастроэнтерологии — науки, позволяющей проанализировать особенности нейральной регуляции деятельности органов ЖКТ [10]. Благодаря исследованиям в этой области стали более глубокими наши знания о роли центральной нервной системы (ЦНС) и периферической нервной системы в функционировании, регуляции моторики органов ЖКТ и инициации ноцицептивных сигналов [11, 12]. Впервые в РК IV Комитет экспертов акцентировал внимание на том, что ФЗ ЖКТ — это группа расстройств, характеризующихся нарушением взаимодействия ЦНС (головной мозг) и периферического звена нервной системы, обеспечивающего деятельность органов ЖКТ (ось «головной мозг–ЖКТ») [9]. По сути в этой характеристике отражена новая дефиниция ФЗ ЖКТ, предложенная экспертным советом обновленного Римского консенсуса.
Как и прежде, в качестве базовой концепции развития ФЗ ЖКТ рассматривается биопсихосоциальная модель, основанная на предположении о мультифакториальности генеза ФЗ ЖКТ (рис. 1) [12, 13]. В детском возрасте генетические, социокультурные и средовые факторы могут оказывать большое влияние на психосоциальное развитие человека, его личностные качества, восприимчивость к стрессам и навыки преодоления трудностей. Эти факторы также во многом определяют предрасположенность к развитию ФЗ ЖКТ, включая нарушения моторики и сенситивности, альтерацию локальных иммунных свойств слизистой оболочки и состава микробиоты [8, 12, 14, 15]. Именно в рамках этой модели формирования ФЗ ЖКТ центральное место занимает дисфункция оси «головной мозг — ЖКТ» на сенсорном, моторном и нейроэндокринном уровнях.
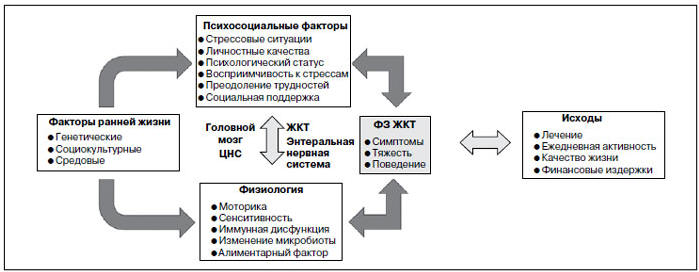
Рис. 1. Биопсихосоциальная модель генеза ФЗ ЖКТ [12]
Fig. 1. Biopsychosocial model of FGID [12]
При ФЗ ЖКТ нередко прослеживается связь между манифестацией симптоматики и психологической дезадаптацией [16, 17]. У пациентов этой группы в анамнезе чаще отмечаются элементы физического и сексуального насилия в детском и подростковом возрасте [17]. Предполагают, что под влиянием стрессовых ситуаций и психических травм могут возникать эмоциональные реакции, проявляющиеся вегетативно-соматической симптоматикой [16, 18]. У больных с ФЗ ЖКТ часто определяется высокий уровень невротизации, тревожности, депрессивных состояний, ипохондрических реакций, «соматовегетативных расстройств» [19]. Тревога наблюдается примерно у 50% пациентов с ФЗ ЖКТ [20]. Известно, что тревога индуцируется стрессовым ответом, опосредованным в первую очередь через высвобождение кортикотропин-рилизинг-гормона из гипоталамуса. Такой стрессовый ответ приводит к физиологическим изменениям, включая нарушения моторики ЖКТ. Помимо этого, кортикотропин-рилизинг-гормон может влиять на центральную обработку ноцицептивных сигналов, участвуя в формировании феномена висцеральной гиперчувствительности [21, 22].
Нарушения гастроинтестинальной моторики при ФЗ ЖКТ способствуют развитию таких симптомов, как тошнота, рвота, диарея, недержание кала, абдоминальная боль и многих других. У здоровых лиц, как и у пациентов с ФЗ ЖКТ, сильная эмоциональная реакция и экзогенный стресс могут приводить к нарушениям моторики через ось «головной мозг — ЖКТ» [12]. Однако у пациентов с ФЗ ЖКТ стрессорные факторы оказывают значительно более выраженное влияние на моторику ЖКТ, чем у здоровых [23]. В то же время моторные нарушения лишь частично коррелируют с клинической симптоматикой и их возникновением нельзя в полной мере объяснить развитие хронической и рецидивирующей абдоминальной боли.
Согласно современным представлениям, развитие болевого синдрома у пациентов с ФЗ ЖКТ детерминируется феноменом висцеральной гиперчувствительности [24–26]. У пациентов отмечаются снижение порога болевой чувствительности и повышение чувствительности полых органов к различным стимулам [12, 24]. Этот феномен базируется на нарушениях механизма передачи болевого импульса от органов ЖКТ в ЦНС (увеличение частоты передаваемых сигналов, амплификация нормального сигнала при прохождении через спинной мозг, амплификация сигнала в головном мозге) [27, 28]. Причины формирования висцеральной гиперчувствительности у пациентов с ФЗ ЖКТ продолжают изучать. Согласно наиболее распространенной гипотезе, данный патофизиологический механизм индуцируется цепочкой событий, связанных с повышением проницаемости слизистой оболочки и активацией ряда иммунокомпетентных клеток [29, 30]. Проникновение интралюминальных агентов в подслизистый слой ассоциируется с активацией тучных клеток и повышенным высвобождением провоспалительных цитокинов, оказывающих влияние на чувствительность нервных окончаний слизистой оболочки, тем самым индуцируя возникновение феномена висцеральной гиперчувствительности [31, 32]. Помимо этого, определенную роль в развитии висцеральной гиперчувствительности могут играть генетические факторы (полиморфизмы генов GNB3, TRPV1, SCN10A), однако, по-видимому, это характерно лишь для части популяции пациентов с ФЗ ЖКТ [28, 33–35].
В последнее время большое внимание в генезе ФЗ ЖКТ уделяют кишечной микробиоте. Предложена концепция существования оси «микробиота ЖКТ–головной мозг», согласно которой количественные и качественные сдвиги микробиоты ЖКТ рассматривают в качестве возможного инициирующего фактора в развитии симптоматики заболевания [36]. В недавно проведенных молекулярно-генетических исследованиях кишечной микробиоты установлено, что у пациентов с синдромом раздраженного кишечника (СРК) ее состав отличается от такового у лиц контрольной группы и зависит от превалирующего симптома [37, 38]. Такие изменения кишечной микрофлоры могут привести к повышенной пролиферации отдельных видов микроорганизмов, обладающих газопродуцирующими свойствами, что в свою очередь может способствовать развитию симптоматики заболевания [25, 39]. Эти данные косвенно подтверждаются умеренно выраженным терапевтическим эффектом пробиотиков, а также успешностью схем терапии СРК, в которые включены антибиотики (рифаксимин), однако к настоящему времени их доказательная база недостаточна [40].
Основные изменения, внесенные в Римские критерии IV пересмотра
Обновленная классификация ФЗ ЖКТ, предложенная в РК IV, содержит 33 нозологические единицы, описанные для взрослых пациентов, и 20 расстройств, наблюдающихся в педиатрической практике (см. таблицу) [12]. В основу выделения нозологической единицы положена анатомическая локализация конкретных симптомов заболевания.
Классификация ФЗ ЖКТ, предложенная Римским консенсусом IV пересмотра (2016 г.)
| Расстройства функции пищевода |
| А1. Функциональная загрудинная боль пищеводного происхождения А2. Функциональная изжога А3. Гиперсенситивный рефлюксный синдром А4. Ком в пищеводе (Globus) А5. Функциональная дисфагия |
| Гастродуоденальные расстройства |
| В1. Функциональная диспепсия В1а.Постпрандиальный дистресс-синдром В1b. Синдром эпигастральной боли В2. Расстройства, сопровождающиеся отрыжкой В2а. Аэрофагия В2b. Чрезмерная неспецифическая отрыжка В3. Расстройства, сопровождающиеся тошнотой и рвотой В3а. Хронический синдром тошноты и рвоты В3b. Синдром циклической рвоты В3с. Каннабиноидиндуцированный рвотный синдром В4. Синдром руминации у взрослых |
| Расстройства функции кишечника |
| С1. Синдром раздраженного кишечника С2. Функциональный запор С3. Функциональная диарея С4. Функциональное вздутие живота С5. Неспецифическое функциональное кишечное расстройство С6. Опиоидиндуцированный запор |
| Расстройства центрального генеза, проявляющиеся абдоминальной болью |
| D1. Болевой абдоминальный синдром центрального генеза D2. Опиоидиндуцированная гастроинтестинальная гипералгезия |
| Расстройства функции желчного пузыря и сфинктера Одди |
| E1. Билиарная боль E1а. Функциональные расстройства желчного пузыря E1b. Функциональное билиарное расстройство сфинктера Одди E2. Функциональное панкреатическое расстройство сфинктера Одди |
| Аноректальные расстройства |
| F1. Недержание кала F2. Функциональная аноректальная боль F2а. Синдром мышцы, поднимающей задний проход F2b. Неспецифическая функциональная аноректальная боль F2с. Прокталгия fugax F3. Функциональные расстройства дефекации F3а. Неадекватная пропульсия при дефекации F3 b. Диссинергическая дефекация |
| Детские функциональные желудочно-кишечные расстройства: новорожденные |
| G1. Срыгивание G2. Синдром руминации G3. Синдром циклической рвоты G4. Колики G5. Функциональная диарея G6. Дисхезия G7. Функциональный запор |
| Детские функциональные желудочно-кишечные расстройства: дети и подростки |
| H1. Функциональные расстройства, проявляющиеся тошнотой и рвотой H1а. Синдром циклической рвоты H1b. Функциональная тошнота и функциональная рвота H1b1. Функциональная тошнота H1b2. Функциональная рвота H1с. Синдром руминации H1d. Аэрофагия H2. Функциональные расстройства, проявляющиеся абдоминальной болью H2а. Функциональная диспепсия H2а1. Постпрандиальный дистресс-синдром H2а2. Синдром эпигастральной боли H2b. Синдром раздраженного кишечника Н2с. Абдоминальная мигрень Н2d. Функциональная абдоминальная боль Н3. Функциональные расстройства дефекации Н3а. Функциональный запор Н3b. Несдерживаемое недержание кала |
В новом пересмотре Римских критериев предложено избегать неоправданного использования термина «функциональный» и убрать его, где это возможно, из нозологической рубрификации. Безусловно, за десятилетия использования этого термина он прочно интегрировался в нозологическую систему и не может быть упразднен за короткий период. Экспертный совет Римского консенсуса предложил новую дефиницию этой группы заболеваний — «расстройства взаимодействия головного мозга и ЖКТ» [9, 12]. Термин «синдром функциональной абдоминальной боли» старой классификации ФЗ ЖКТ предложено заменить термином «болевой абдоминальный синдром центрального генеза» как более корректно отражающий патогенез рассматриваемого состояния. В то же время экспертным советом сохранены термины «функциональная диарея» и «функциональная изжога», позволяющие легко отличать указанные явления от состояний со схожей симптоматикой, но известной этиологией.
В обновленную классификацию ФЗ ЖКТ включены новые нозологические единицы с известным каузативным фактором (употребление наркотических веществ): опиоидиндуцированная гастроинтестинальная гипералгезия, опиоидиндуцированный запор, каннабиноидиндуцированный рвотный синдром [12]. Безусловно, это не истинная функциональная патология, так как известен этиологический фактор указанных состояний (наркотическое вещество). Однако включение этих нозологий в обновленную классификацию было обусловлено тем, что они соответствуют новой дефиниции ФЗ ЖКТ как расстройств, характеризующихся альтерацией взаимодействия головного мозга и ЖКТ.
В раздел «расстройства функции пищевода» включена новая нозологическая единица — «гиперсенситивный рефлюксный синдром». В РК III диагноз «функциональная изжога» предполагал наличие у пациента симптома изжоги в отсутствие доказательств органической патологии — гастроэзофагеальной рефлюксной болезни. Однако проведенные к настоящему времени исследования с применением импеданс-рН-мониторинга в различных популяциях пациентов с изжогой наглядно продемонстрировали, что существует группа лиц, у которых отмечается значимая ассоциация этого симптома с кислыми и некислыми рефлюксами в условиях нормальной экспозиции кислоты. В этом случае речь идет о «гиперсенситивном рефлюксном синдроме» (рис. 2) [41–44].
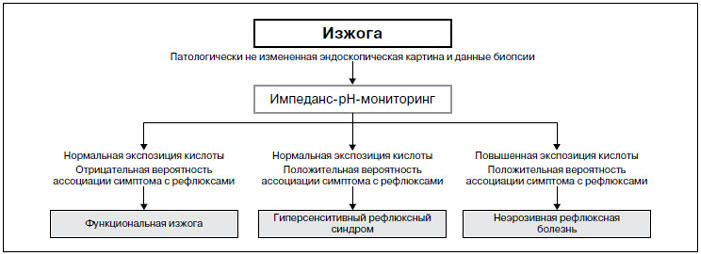
Рис. 2. Классификация пациентов с изжогой без эндоскопических признаков эзофагита
Fig. 2. Classification of patients with heartburn without endoscopic signs of esophagitis
Экспертным советом Римского консенсуса IV пересмотра в обновленную классификацию ФЗ ЖКТ внесена новая нозологическая единица — «синдром тошноты и рвоты». Этот диагноз объединяет ранее выделявшиеся заболевания — хроническую идиопатическую тошноту и функциональную рвоту. Данные изменения продиктованы частым сочетанием упомянутых выше заболеваний в рутинной практике, а также единством терапевтических подходов к купированию обоих состояний [45].
Небольшие изменения коснулись диагностических критериев функциональной диспепсии. Перед каждым из основных симптомов, характерных для данного заболевания (чувство переполнения в подложечной области, раннее насыщение, эпигастральная боль и жжение), был добавлен термин «беспокоящий», отражающий существенное влияние данной симптоматики на качество жизни пациента. Помимо этого, сделано уточнение, что симптомы, характерные для постпрандиального дистресс-синдрома, всегда возникают после приема пищи, тогда как при синдроме эпигастральной боли болевой абдоминальный синдром и чувство жжения в эпигастрии могут появляться и исчезать после приема пищи, а также возникать натощак [45, 46].
В РК IV был произведен пересмотр тактики ведения пациентов с дисфункцией сфинктера Одди. У лиц без признаков билиарной обструкции признано необязательным проведение манометрии, эндоскопической ретроградной панкреатохолангиографии (ЭРПХГ) и эндоскопической папиллосфинктеротомии. Таким пациентам рекомендовано проводить симптоматическое лечение. В случае умеренной функциональной билиарной обструкции необходимо проведение манометрии и ЭРПХГ для решения вопроса о целесообразности выполнения папиллосфинктеротомии [47]. Это отчасти обусловлено повышением риска развития рецидивирующего холангита вследствие частого «выключения» у таких больных запирающей функции сфинктера Одди и рефлюкса дуоденального содержимого в общий желчный проток.
Экспертным советом Римского консенсуса IV пересмотра внесены изменения в диагностические критерии СРК. Согласно РК III у пациентов, у которых отмечались длительные периоды, когда форма кала оставалась неизменной, диагностировали неклассифицируемую форму СРК. В РК IV предложено при определении подтипа СРК учитывать только эпизоды изменения формы кала (неоформленный/водянистый или твердый/ фрагментированный) [48]. Таким образом, группа лиц с неклассифицируемой формой СРК должна существенно уменьшиться, что позволит более индивидуализированно подходить к выбору фармакотерапии заболевания [12].
Помимо этого, из диагностических критериев СРК был исключен термин «дискомфорт». В РК III под термином «дискомфорт» подразумевали менее «яркую» симптоматику по сравнению с обозначаемой термином «абдоминальная боль». Однако его практическая интерпретация широко варьировала в зависимости от уровня медицинской грамотности и межкультуральных особенностей населения [49]. В связи с этим в РК IV в качестве ключевого диагностического критерия СРК в совокупности с изменением консистенции кала и кратности дефекации было оставлено только определение «абдоминальная боль». В новой дефиниции СРК в редакции РК IV пересмотрена также частота появления абдоминальной боли (ранее она составляла 3 дня в месяц, теперь — 1 раз в неделю в течение последних 3 мес) [48].
Отдельно следует отметить, что в соответствии с современными представлениями основные виды ФЗ кишечника (СРК, функциональный запор, функциональная диарея) представляют собой единый континуум с возможной трансформацией одного ФЗ кишечника в другое в зависимости от особенностей симптоматики у конкретного больного (рис. 3) [48]. В связи с этим практикующий врач должен проводить динамическую оценку жалоб пациента с последующей корректировкой схемы лечения в зависимости от преобладающих симптомов.
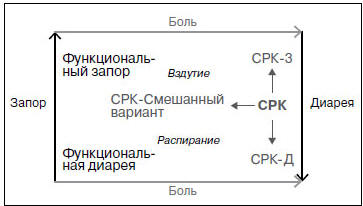
Рис. 3. ФЗ кишечника: единый континуум с возможной трансформацией одного заболевания в другое [48]
Fig. 3. Functional bowel disorders: uniform continuum with possible mutual transformation of diseases
Заключение
Римский консенсус IV пересмотра предлагает новую дефиницию ФЗ ЖКТ с исключением термина «функциональный». В настоящий момент ФЗ ЖКТ рассматривают как нарушения взаимодействия головного мозга и ЖКТ. Основанием для таких изменений послужили результаты многочисленных исследований в области нейрогастроэнтерологии. В новой редакции Римских критериев, помимо конкретизации классификации ФЗ ЖКТ, уточнена тактика ведения пациентов с дисфункцией сфинктера Одди, а также модернизированы критерии диагностики функциональной диспепсии и СРК.
Список литературы/References
- Sleisenger and Fordtran’s Gastrointestinaland Liver Disease: Pathophysiology, Diagnosis, Management / Edited by Mark Feldman, Lawrence S. Friedman, Laurence J. Brandt. 10th ed. 2015.
- Oshima Т., Miwa H. Epidemiology of Functional Gastrointestinal Disorders in Japan and in the World. J Neurogastroenterol Motil 2015;21(3):320-9.
- Lewis M.L., Palsson O.S., Whitehead W.E., van Tilburg M.A. Prevalence of Functional Gastrointestinal Disorders in Children and Adolescents. J Pediatr 2016 May 4. pii: S0022-3476(16)30056-7. [Epub ahead of print].
- Varni J.W., Bendo СВ., Nurko S., Shulman R.J., Self M.M., Franciosi J.P., Saps M., Pohl J.F. Pediatric Quality of Life Inventory (PedsQL) Gastrointestinal Symptoms Module Testing Study Consortium. Health-related quality of life in pediatric patients with functional and organic gastrointestinal diseases. J Pediatr 2015;166(1):85-90.
- Devanarayana N.M., Rajindrajith S., Benninga M.A. Quality of life and health care consultation in 13 to 18 year olds with abdominal pain predominant functional gastrointestinal diseases. BMC Gastroenterol 2014;14:150.
- Talley N.J. Functional gastrointestinal disorders as a public health problem. Neurogastroenterol Motil 2008 May;20 (Suppl 1):121-9.
- Canavan C, West J., Card T. Review article: the economic impact of the irritable bowel syndrome. Aliment Pharmacol Ther 2014;40(9):1023-34.
- Kovacic K. Current concepts in functional gastrointestinal disorders. Curr Opin Pediatr 2015;27(5):619-24.
- Drossman D.A., Hasler W.L. Rome IV-Functional GI Disorders: Disorders of Gut-Brain Interaction. Gastroenterology 2016;150(6):1257-61.
- Gaman A., Kuo B. Neuromodulatory processes of the brain-gut axis. Neuromodulation 2008;11:249-59.
- Pasricha P.J. Neurogastroenterology: a great career choice for aspiring gastroenterologists thinking about thefuture. Gastroenterology 2011;140:1126-8.
- Drossman D.A. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features and Rome IV. Gastroenterology 2016;150:1262-79.
- Engel G.L. The clinical application of the Biopsychosocialmodel. Am J Psychiatr 1980;137:535-44.
- Levy R.L., Olden K.W., Naliboff B.D., Bradley L.A., Francisconi C., Drossman D.A., Creed F. Psychosocial aspects of the functional gastrointestinal disorders. Gastroenterology 2006;130:1447-58.
- Saito Y.A., Mitra N., Mayer E.A. Genetic approaches to functional gastrointestinal disorders. Gastroenterology 2010;138:1276-85.
- Chen T.S., Lee Y.C., Chang F.Y., Wu H.C., Lee S.D. Psychosocial distress is associated with abnormal gastric myoelectrical activity in patients with functional dyspepsia. Scand J Gastroenterol 2006 Jul;41(7):791-6.
- Дмитриева В.А., Одинцова В.В. Энтеральная нервная система и психосоматические аспекты заболеваний желудочно-кишечного тракта. Мед альманах 2011; 1:166-9. [Dmitriyeva V.A., Odintsova V.V. Enteral nervous system and psychosomatic aspects of gastrointestinal diseases. Med almanakh 2011; 1:166-9].
- Drossman D.A. Presidental address: Gastrointestinal illness and the biopsychosocial model. Psychosomatic Med 1998; 60(3):258-67.
- Drossman D.A., Creed F.H., Fava G.A. Psychosocial aspects of the functional gastrointestinal disiders. Gastroenterol Int 1995; 8:47-90.
- Schurman J. V., Danda C.E., Friesen C.A., Hyman P.E., Simon S.D., Cocjin J.T. Variations in psychological profile among children with recurrent abdominal pain. J Clin Psychol Med Settings 2008;15:241-51.
- Rosen J.M., Cocjin J.T., Schurman J.V., Colombo J.M., Friesen C.A. Visceral hypersensitivity and electromechanical dysfunction as therapeutic targets in pediatric functional dyspepsia. World J Gastrointest Pharmacol Ther 2014;5(3):122-38.
- Fukudo S. Role of corticotropin-releasing hormone in irritable bowel syndrome and intestinal inflammation. J Gastroenterol 2007;42(Suppl. 17):48-51.
- Camilleri M. Peripheral mechanisms in irritable bowel-syndrome. N Engl J Med 2012;367:1626-35.
- Mayer E.A., Gebhart G.F. Basic and clinical aspects of visceral hyperalgesia. Gastroenterology 1994;107:271-93.
- Lee Y.J., Park K.S. Irritable bowel syndrome: emerging paradigm in pathophysiology. World J Gastroenterol 2014;20(10):2456-69.
- Maeв И.В., Кучерявый Ю.А., Андреев Д.Н. Функциональная диспепсия: эпидемиология, классификация, этиопатогенез, диагностика и лечение. М.; 2015 [Mayev I.V., Kucheryavy Yu.A., Andreyev D.N. Functional dyspepsia: epidemiology, classification, etiopathogenesis, diagnosis and treatment. M.; 2015].
- Vanheel H., Farre R. Changes in gastrointestinal tract function and structure in functional dyspepsia. Nat Rev Gastroenterol Hepatol 2013;10(3):142-9.
- Маев И.В., Андреев Д.Н., Кучерявый Ю.А. Современные представления о патофизиологических основах синдрома функциональной диспепсии. Рос журн гастроэнтерол гепатол колопроктол 2015; 4:15-22. [Mayev I.V., Andreyev D.N., Kucheryavy Yu.A. The modern concept on pathophysiological bases of functional dyspepsia syndrome. Ross z gastroenterol gepatol koloproktol 2015; 4:15-22].
- Piche T. Tight junctions and IBS-the link between epithelial permeability, low-grade inflammation, and symptom generation? Neurogastroenterol Motil 2014;26:296-302.
- Matricon J., Meleine M., Gelot A., Piche Т., Dapoigny M., Muller E., Ardid D. Review article: associations between immune activation, intestinal permeability and the irritable bowel syndrome. Aliment Pharmacol Ther 2012;36:1009-31.
- Ohman L, Simren M. Pathogenesis of IBS: role of inflammation, immunity and neuroimmune interactions. Nat Rev Gastroenterol Hepatol 2010;7:163-73.
- Самсонов А.А., Андреев Д.Н., Дичева Д.Т. Синдром раздраженного кишечника с позиций современной гастроэнтерологии. Фарматека 2014; 18:7-13. [Samsonov A.A., Andreyev D. N., Dicheva D.T. Irritable bowel syndrome from standpoints of modern gastroenterology. Farmateka 2014; 18:7-13].
- Sarnelli G., D’Alessandro A., Pesce M., Palumbo I., Cuomo R. Genetic contribution to motility disorders of the upper gastrointestinal tract. World J Gastrointest Pathophysiol 2013; 4(4):65-73.
- Tahara Т., Shibata Т., Nakamura M. et al. Homozygous TRPV1 315C influences the susceptibility to functional dyspepsia. J Clin Gastroenterol 2010; 44(1):e1-7.
- Arisawa Т., Tahara Т., Shiroeda H., Minato Т., Matsue Y., Saito Т., Fukuyama Т., Otsuka Т., Fukumura A., Nakamura M. et al. Genetic polymorphisms of SCN10A are associated with functional dyspepsia in Japanese subjects. J Gastroenterol 2013;48:73-80.
- De Palma G., Collins S.M., Bercik P. The microbiota-gut-brain axis in functional gastrointestinal disorders. Gut Microbes 2014;5(3):419-29.
- Krogius-Kurikka L., Lyra A., Malinen E., Aarnikunnas J., Tuimala J., Paulin L., Mäkivuokko H., Kajander K., Palva A. Microbial community analysis reveals high level phylogenetic alterations in the overall gastrointestinal microbiota of diarrhoea-predominant irritable bowel syndrome sufferers. BMC Gastroenterol 2009;9:95.
- Carroll I.M., Ringel-Kulka Т., Keku Т.О., Chang Y.H., Packey CD., Sartor R.B., Ringel Y. Molecular analysis of the luminal- and mucosal-associated intestinal microbiota in diarrhea-predominant irritable bowel syndrome. Am J Physiol Gastrointest Liver Physiol 2011;301: G799-G807.
- Dear K. L., Elia M., Hunter J. O. Do interventions which reduce colonic bacterial fermentation improve symptoms of irritable bowel syndrome? Dig Dis Sci 2005;50:758-66.
- Simren M., Barbara G., Flint H., Spiegel B.M., Spiller R.C., Vanner S., Verdu E.F., Whorwell P.J., Zoetendal E. G. Intestinal microbiota in functional bowel disorders: a Rome Foundation working team report. Gut 2013;62:159-76.
- Patel A., Sayuk G.S., Gyawali C.P. Prevalence, characteristics, and treatment outcomes of reflux hypersensitivity detected on pH-impedance monitoring. Neurogastroenterol Motil 2016;28(9):1382-90.
- Patel A., Sayuk G.S., Kushnir V.M., Chan W.W., Gyawali C.P. GERD phenotypes from pH-impedance monitoring predict symptomatic outcomes on prospective evaluation. Neurogastroenterol Motil 2016;28(4):513-21.
- Aziz Q., Fass R., Gyawali C.P., Miwa H., Pandolfino J.E., Zerbib F. Functional Esophageal Disorders. Gastroenterology 2016; 150:1368-79.
- Евсютина Ю.В., Трухманов А.С. Ведение пациентов с рефрактерной ГЭРБ. Русс мед журн 2015; 28:1684-8. [Yevsyutina Yu.V., Trukhmanov A.S. Management of refractory GERD. Russ med zhurn 2015; 28:1684-8].
- Stanghellini V., Chan F.K., Hasler W.L., Malagelada J.R., Suzuki H., Tack J., Talley N.J. Gastroduodenal Disorders. Gastroenterology 2016; 150(6):1380-92.
- Шептулин А.А., Курбатова А.А. Новые Римские критерии функциональной диспепсии IV пересмотра. Рос журн гастроэнтерол гепатол колопроктол 2016; 26(4):124-8. [Sheptulin A.A., Kurbatova A.A. New Rome IV criteria of functional dyspepsia (review). Ross z gastroenterol gepatol koloproktol 2016; 26(4):124-8].
- Cotton P.В., Elta G.H., Carter C.R., Pasricha P.J., Corazziari E.S. Gallbladder and Sphincter of Oddi Disorders. Gastroenterology 2016;150(6):1420-9.
- Lacy B.E., Mearin F., Chang L., Chey W.D., Lembo A.J., Simren M., Spiller R. Bowel Disorders. Gastroenterology 2016;150(6):1393-407.
- Spiegel B.M., Bolus R., Agarwal N., Sayuk G., Harris L.A., Lucak S., Esrailian E., Chey W.D., Lembo A., Karsan H., Tillisch K., Talley J., Chang L. Measuring symptoms in the irritable bowel syndrome: development of a framework for clinical trials. Aliment Pharmacol Ther 2010;32(10):1275-91.
Статья опубликована на сайте http://www.gastroscan.ru
материал MedLinks.ru







