Длительный прием никорандила уменьшает размеры поражения миокарда у пациентов с инфарктом миокарда с подъемом сегмента ST, перенесших первичное чрескожное коронарное вмешательство (реферат)
Содержание статьи
Введение
Своевременная реперфузионная терапия, особенно первичное чрескожное коронарное вмешательство (пЧКВ), играет ключевую роль в лечении инфаркта миокарда с подъемом сегмента ST (STEMI) и способствует значительному снижению смертности пациентов со STEMI в острой стадии [1]. Однако ишемическое/реперфузионное повреждение после пЧКВ остается нерешенной проблемой, приводящей к ухудшению восстановления миокарда и более частому развитию сердечной недостаточности [2, 3]. У пациентов с острым инфарктом миокарда (ОИМ) после проведения ЧКВ широко распространены микрососудистая обструкция коронарных сосудов (МОКС) и повреждение миокарда, которые влияют на окончательный размер инфаркта (РИ) [3–6]. РИ является основной детерминантой ремоделирования сердца, ассоциированной с неблагоприятным прогнозом. К сожалению, по результатам большого числа клинических исследований на сегодня не определена стратегия по уменьшению РИ [4, 6–8]. Таким образом, необходим поиск новых методов лечения.
Никорандил, комбинированный препарат, активатор аденозинтрифосфат-чувствительных калиевых (КАТФ) каналов с нитратоподобными свойствами, может улучшать клинические исходы при ишемической болезни сердца (ИБС) за счет улучшения микроциркуляторной дисфункции и уменьшения повреждения миокарда [9–11]. Кроме того, несколько экспериментальных исследований показали, что никорандил может уменьшить РИ примерно на 50% [12–14]. Однако по-прежнему остается спорным вопрос, уменьшает ли никорандил РИ у пациентов с ОИМ [15], поскольку в предшествующих исследованиях никорандил в основном назначался в течение короткого времени до ЧКВ или в периоперационном периоде [15, 16]. Известно, что после пЧКВ наблюдается прогрессирование МОКС, а для восстановления «оглушенного» миокарда (миокардиальный «станнинг») может потребоваться несколько дней или недель [10, 17]. Таким образом, было принято решение оценить эффективность длительного перорального приема никорандила в отношении снижения РИ и улучшения исходов у пациентов со STEMI и пЧКВ.
Материал и методы
Пациенты
В данное пилотное проспективное рандомизированное открытое контролируемое исследование было последовательно включено 134 пациента с первым STEMI, поступивших в кардиологическое отделение больницы Xijing с сентября 2016 г. по февраль 2017 г.
Критерии включения: возраст от 18 до 79 лет; первый диагноз STEMI и подготовка к пЧКВ и не более 12 ч с момента появления симптомов до госпитализации. Постановка диагноза STEMI осуществлялась на основании наличия боли в грудной клетке продолжительностью более 30 мин, подъема сегмента ST не менее чем на 1 мм в двух сопряженных отведениях и повышения уровня кардиоспецифических биомаркеров.
Критерии исключения: перенесенный инфаркт миокарда (ИМ) или кардиомиопатия; поражение ствола левой коронарной артерии с гемодинамической нестабильностью; класс III или IV по шкале Killip; невозможность открыть окклюзию с помощью пЧКВ или переход на коронарное шунтирование; применение препаратов сульфонилмочевины (ингибиторы КАТФ-каналов); тяжелые заболевания печени, почек или легких; лекарственная аллергия в анамнезе; тяжелая глаукома.
При соответствии критериям включения и исключения пациенты со STEMI были распределены в группу никорандила или контрольную группу на основании случайных чисел, сгенерированных компьютером. Все пациенты принимали перорально 5 мг никорандила после поступления в стационар. Затем пациенты в группе никорандила (n=60) принимали 5 мг никорандила 3 р./сут в течение 6 мес. после ЧКВ. Группу контроля составили 57 пациентов. Остальное лечение проводилось в соответствии со стандартными рекомендациями в обеих группах.
Протоколы
Все включенные пациенты получали лечение в соответствии с текущими рекомендациями по ведению пациентов со STEMI. Никорандил назначался в качестве адъювантной терапии.
После того как пациентам был поставлен диагноз STEMI, назначалась двойная антиагрегантная терапия с нагрузочной дозой ацетилсалициловой кислоты,
тиклопидина или клопидогрела. До катетеризации всем пациентам внутривенно вводился гепарин (70 МЕ/кг). Процедура пЧКВ проводилась стандартно. Пациентам без реперфузии (степень реперфузии 0–2 по шкале TIMI) назначали тирофибан, интракоронарное введение нитропруссида натрия или аденозин в катетеризационной лаборатории. Статины, бета-блокаторы, ингибиторы ангиотензинпревращающего фермента (ИАПФ) и блокаторы ангиотензиновых рецепторов (БРА) назначались в соответствии с клинической ситуацией.
Электрокардиография (ЭКГ) выполнялась перед поступлением в катетеризационную лабораторию. Образцы крови забирались для определения уровня кардиоспецифических ферментов или биомаркеров, таких как креатинкиназа-МВ (CK-MB) и тропонин I (TnI), после поступления и через 24 ч после ЧКВ. Однофотонную эмиссионную компьютерную томографию (ОФЭКТ) с ЭКГ-синхронизацией выполняли через 3 мес. после ЧКВ. Как описано ранее [18], получение изображений ОФЭКТ начиналось через 50–60 мин после введения технеция-99 м-сестамиби (740–900 МБк, с поправкой на вес). После обработки и реконструкции анализ изображения выполнялся с использованием процессора Entegra (GE Medical Systems). Площадь дефицита определялась количественно с порогом 50% от пикового поглощения. РИ выражался в процентах от площади левого желудочка. Эхокардиография (ЭхоКГ) (Рhilips Ultrasound, США) проводилась для оценки фракции выброса левого желудочка (ФВЛЖ) при поступлении и через 1, 3 и 6 мес. после ЧКВ. Как и в предыдущих исследованиях [18], ЭхоКГ проводилась двумя опытными специалистами, которые не знали, к какой группе принадлежит пациент. Если расхождение между показателями составляло >5%, то привлекался третий специалист для достижения консенсуса. Анализ вариабельности показателей между специалистами показал хорошую воспроизводимость (ФВЛЖ 1,2±4,1%) с помощью теста Бланда — Альтмана. Сиэтлский опросник для стенокардии (Seattle Angina Questionnaire — SAQ) заполнялся на 6-м мес. SAQ использовался для оценки определенных состояний здоровья и качества жизни при ИБС, в т. ч. ограничения физической нагрузки, стабильности стенокардии, ее частоты, удовлетворенности лечением и отношения к болезни [18]. Также собирались данные о серьезных нежелательных кардиологических явлениях (Major Adverse Cardiac Event — MACE), включая смерть от всех причин, повторный инфаркт миокарда, тяжелую сердечную недостаточность и внеплановую повторную госпитализацию по сердечной причине. Данные показатели оценивались опытными специалистами, которые не знали, к какой группе принадлежит пациент.
Первичной конечной точкой был РИ, количественно выраженный в процентах от площади стенки левого желудочка, что оценивалось с помощью ОФЭКТ на 3-м мес. Вторичными конечными точками были ФВЛЖ и SAQ, оцененные на 6-м мес. Настоящее исследование одобрено этическим комитетом больницы Xijing, Четвертый Военно-медицинский университет, Сиань, Шэньси, Китай. Протокол был зарегистрирован на www.chictr.org.cn (номер клинического испытания ChiCTR-IPC-16009477). Все пациенты подписали информированное согласие.
Статистический анализ
Настоящее исследование направлено на проверку гипотезы о том, что пероральный прием никорандила уменьшает РИ. Мощность статистического теста (1 — β) была определена как 0,8, уровень значимости α — как 0,05. Как и в современной литературе, стандартное отклонение (SD) РИ, оцененного с помощью ОФЭКТ, колебалось в пределах 4–18% [18–20]. Мы предположили, что среднее значение ± стандартное отклонение (SD) РИ в группе никорандила составляло 15±10%, в контрольной группе — 20±10%. Требуемый размер выборки составил 50 пациентов в каждой группе. С учетом потенциальных потерь в периоде наблюдения около 10% необходим набор не менее 110 пациентов. Некоторые пациенты отказались от ОФЭКТ или им не могла быть выполнена ОФЭКТ, поэтому было последовательно набрано еще 10 пациентов.
Статистический анализ был основан на принципе intent-to-treat (ITT, «по намеченному лечению»). Непрерывные данные с нормальным распределением описаны как средние и SD, сравнение проводилось с помощью t-критерия Стьюдента. При ненормальном распределении данные описаны как медиана и межквартильный размах (IQR) и оценивались по U-критерию Манна — Уитни. Категориальные параметры представлены в виде пропорции или числа, сравнивались с помощью критерия хи-квадрат Пирсона или точного критерия Фишера. Для анализа подгрупп первичная конечная точка РИ была преобразована в двоичные данные (большая или равная медиане РИ (14%) определялась как большая площадь). Отношение рисков (ОР) и 95% доверительные интервалы (ДИ) оценены и проанализированы с помощью логистического регрессионного анализа. Статистический анализ проводился с помощью программного пакета SPSS (SPSS, версия 14.0, США) и STATA (Stata-Corp LP, версия 10, США). Все тесты были двусторонними, и значение р<0,05 считалось статистически значимым.
Результаты исследования
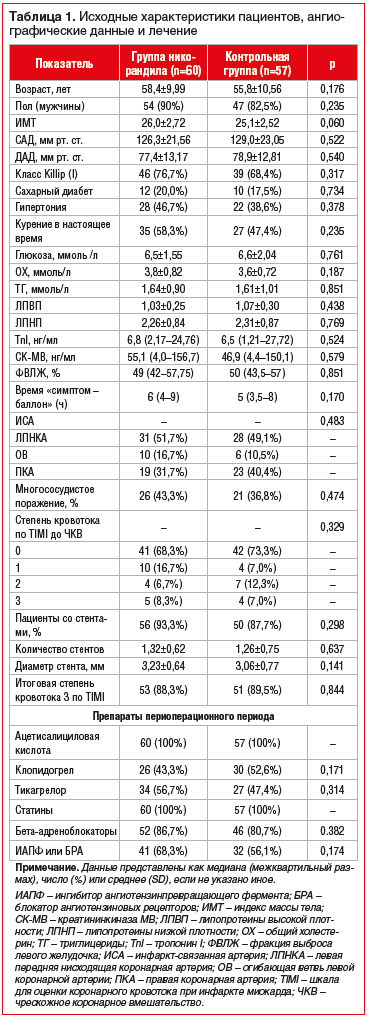
Из 134 пациентов, которым был поставлен диагноз STEMI, 17 были исключены по нескольким причинам (класс III–IV по Killip, перенесенный инфаркт миокарда, почечная недостаточность и пероральный прием препаратов сульфонилмочевины), 117 пациентов подходили для участия в исследовании. Исходные характеристики пациентов представлены в таблице 1. 99 пациентов в обеих группах с диагнозом STEMI завершили наблюдение через 6 мес. Не наблюдалось статистически значимой разницы по таким показателям, как ФВЛЖ, CK-MB и TnI до пЧКВ и выявление особенностей проведения коронарной ангиографии, что подтверждает одинаковую степень поражения миокарда в обеих группах до реперфузии (табл. 1).
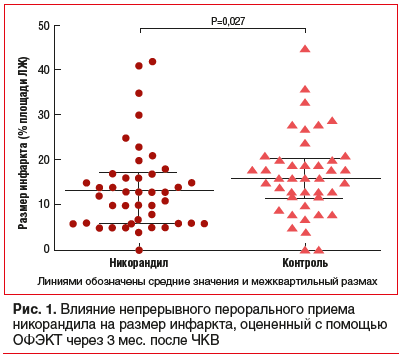
Влияние никорандила на РИ оценивалось с помощью ОФЭКТ через 3 мес. после пЧКВ и выражалось в процентах от площади стенки левого желудочка (рис. 1 и табл. 2). Лишь у 85 пациентов выполнена ОФЭКТ и было возможно оценить РИ. Не выявлено статистически достоверной разницы в популяционных характеристиках пациентов, которым была выполнена ОФЭКТ. В группе никорандила выявлен достоверно меньший РИ в сравнении с контрольной группой (13% (IQR 8–17) против 16% (IQR 12–20,3), p=0,027).
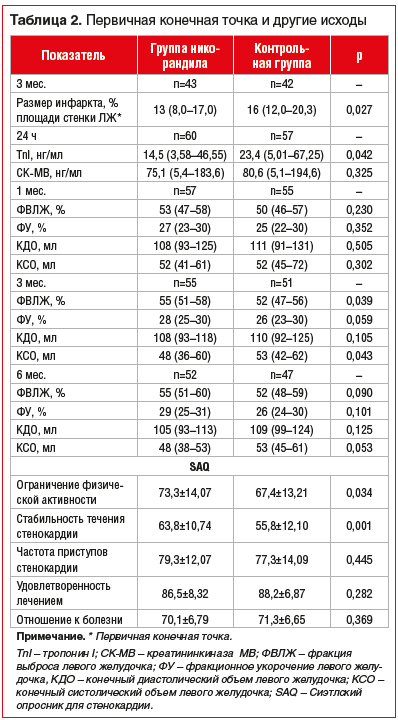
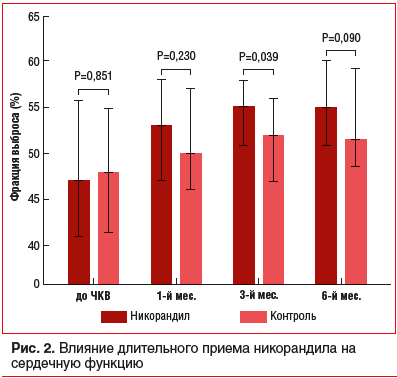
Уровень TnI и CK-MB через 24 ч после ЧКВ был выше, чем до лечения. Тем не менее уровень TnI в группе никорандила был относительно низкий в сравнении с контрольной группой (14,5 (3,58–46,55) против 23,4 (5,01–67,25), р=0,042), что указывает на уменьшение повреждения миокарда при непрерывном приеме никорандила. ЭХО-КГ проводилась для оценки сердечной функции через 1, 3 и 6 мес. после пЧКВ. На основании анализа данных выявлено, что длительный пероральный прием никорандила привел к статистически достоверному улучшению ФВЛЖ (55 (51–58) против 52 (47–56), p=0,039) и конечного систолического объема левого желудочка (КСО) (48 (36–60) против 53 (42–62), р=0,043) через 3 мес. Кроме того, наблюдалась тенденция к увеличению ФВЛЖ через 6 мес., хотя различия между группами не достигли уровня статистической значимости (55 (51–60) против 52 (48–59), р=0,090; (табл. 2 и рис. 2).
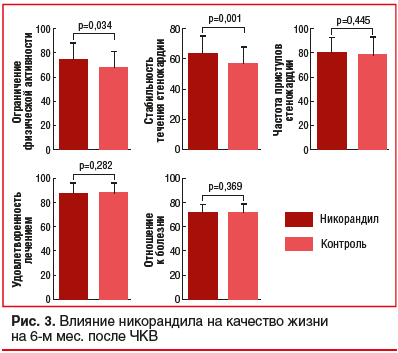
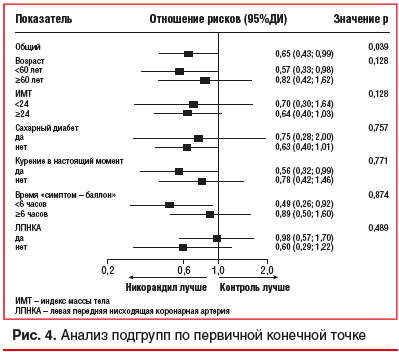
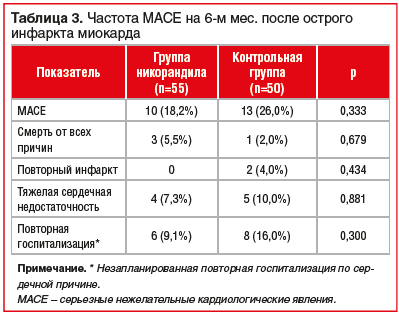
Непрерывный прием никорандила также улучшил качество жизни пациентов со STEMI (табл. 2 и рис. 3). Опросник SAQ оценивает пять аспектов: ограничение физической активности, стабильность течения стенокардии, частота приступов стенокардии, удовлетворенность лечением и отношение к болезни. Непрерывное лечение никорандилом улучшило такие показатели, как ограничение физической активности и стабильность течения стенокардии через 6 мес. после пЧКВ. Данные SAQ через 6 мес. после пЧКВ показали, что непрерывный прием никорандила привел к улучшению показателей ограничения физической нагрузки (73,3±14,07 против 67,4±13,21, р=0,034) и стабильности стенокардии (63,8±10,74 против 55,8±12,10, р=0,001). Анализ подгрупп не выявил какой-либо статистической неоднородности по возрасту, индексу массы тела, сахарному диабету, курению в настоящий момент, времени «симптом — баллон» и ЛПНКА (рис. 4). Не выявлено статистически достоверных различий по частоте неблагоприятных сердечных событий (табл. 3).
Обсуждение
Настоящее исследование показывает, что в сравнении с однократным пероральным приемом длительное применение никорандила приводило к уменьшению площади инфаркта миокарда (13% (8–17) против 16% (12–20,3), p=0,027) и повышению ФВЛЖ (55% против 52%, p=0,039) и КСО (48 мл против 53 мл, р=0,043) через 3 мес., качества жизни (ограничение физической активности (73,3±14,07 против 67,4±13,21, р=0,034) и стабильности течения стенокардии (63,8±10,74 против 55,8±12,10, р=0,001) через 6 мес. у пациентов со STEMI, перенесших пЧКВ. РИ тесно связан с клиническими исходами [21]. Основная цель настоящего исследования — оценить кардиопротективные эффекты непрерывного лечения никорандилом по уменьшению РИ у пациентов со STEMI и Killip I–II.
Благодаря уникальной структуре у никорандила есть различные кардиопротективные свойства, реализуемые через активацию (открытие) КАТФ-каналов и нитратный путь. Никорандил эффективно улучшает симптомы и исходы ИБС [11, 22]. В дополнение к расслаблению больших коронарных сосудов через NO никорандил расширяет микроциркуляторное русло, улучшая перфузию сердца путем специфической активации КАТФ-каналов. Никорандил также защищает миоциты путем открытия КАТФ-каналов, расположенных в сарколемме и митохондриях в условиях ишемии-реперфузии [9]. Более того, у никорандила есть другие кардиопротективные механизмы, такие как ингибирование апоптоза, регуляция симпатической активности и опосредование аутофагии [23–25].
Согласно вышеописанным механизмам у никорандила может быть многообещающий эффект — уменьшение РИ у пациентов с ОИМ. Как и ожидалось, эксперименты на животных показали, что никорандил уменьшает площадь инфаркта на 52–54,9% путем активации КАТФ-каналов [12, 13]. Тем не менее данные о способности никорандила ограничивать РИ у пациентов со STEMI оставались спорными. Целью исследования J-WIND стала оценка влияния никорандила на РИ у пациентов со STEMI. Неожиданно никорандил не уменьшал РИ, который оценивался по уровню креатинкиназы в сравнении с плацебо.
Еще в одно небольшое исследование Yamada et al. [16] было включено 55 пациентов с ОИМ, проходящих пЧКВ, которым на 4 дня назначалось внутрикоронарное введение никорандила или нитратов. По результатам никорандил снизил РИ на 18,9% по сравнению с нитратами. В настоящем исследовании было показано, что непрерывный пероральный прием никорандила привел к уменьшению РИ у пациентов со STEMI, перенесших пЧКВ.
Предположительно такое несоответствие результатов возникло по нескольким причинам. В исследовании J-WIND использовался непрерывный мониторинг CK для косвенной оценки РИ. Хотя некоторые исследования указывают на связь уровня CK и CK-MB с РИ (коэффициент корреляции 0,55–0,73), данные биомаркеры могут рассматриваться только как предикторы РИ, но не выступать вместо самого показателя РИ [21, 26, 27]. Поскольку при реперфузии возникает быстрый выброс CK в ишемическом диапазоне, это может влиять на оценку РИ [27].
Во-вторых, на эффект повлияла дозировка. Предыдущие исследования также показали дозозависимое улучшение переносимости физической нагрузки, сердечной функции и уменьшение повреждения миокарда у пациентов с ИБС при приеме никорандила. Исследователи J-WIND также сделали заключение о недостаточной дозировке никорандила. Точно так же результаты по первичной конечной точке в настоящем исследовании не оправдали ожиданий, что может быть связано с дозировкой.
Кроме того, продолжительность приема никорандила также может быть значима. Так, в исследовании J-WIND пациентам никорандил вводился внутривенно 1 день — различий выявлено не было, в исследовании Yamada et al. [16] никорандил назначали непрерывно в течение 4 дней — доказан положительный эффект.
В настоящей работе РИ оценивался через 3 мес. на фоне постоянного перорального приема никорандила, и достигнутые результаты свидетельствуют о важности длительности приема. В действительности даже через 6–10 дней после ИМ сохранялась постоянная
МОКС [28, 29]. Между тем для восстановления сократительной функции «оглушенного» миокарда может потребоваться несколько недель [17, 30]. Поэтому настоящее и предыдущие исследования показали, что непрерывное уменьшение МОКС и защита кардиомиоцитов оказали благоприятное влияние на сохранение миокарда.
В настоящем исследовании выявлено, что уровень TnI, а не уровень CK-MB, был достоверно ниже в группе постоянного приема никорандила по сравнению
с контрольной группой. Поскольку уровень биомаркера не измерялся последовательно, по имеющимся данным можно предположить, что уровень TnI через 24 ч после ЧКВ — более чувствительный прогностический маркер РИ, чем CK-MB. Кроме того, в других
работах показано, что уровень CK-MB через 4–12 ч после ЧКВ был хорошим предиктором РИ [26, 31]. В соответствии с ранее опубликованными результатами настоящее исследование показало, что непрерывный прием никорандила приводит к повышению ФВЛЖ и качества жизни [15, 32]. Однако не выявлено значительного изменения ФВЛЖ через 6 мес. в обеих группах. Отчасти поскольку с течением времени происходило восстановление функции сердца в обеих группах, у большего числа пациентов требовался анализ данного эффекта. Кроме того, многочисленные исследования показали снижение частоты развития МОКС при приеме никорандила [11, 33]. В данном исследовании непрерывный прием никорандила не оказывал влияния на частоту МОКС (частично из-за недостаточного размера выборки).
Ограничения исследования
В этом исследовании существовало несколько ограничений. Во-первых, для оценки РИ была выбрана ОФЭКТ. Действительно, у МРТ с отсроченным контрастированием лучше пространственное разрешение для обнаружения ИМ малого размера, чем у ОФЭКТ [34]. Во-вторых, оценка РИ проводилась через 3 мес. в сравнении с исходным повреждением миокарда, однако данные о зонах риска в острой фазе ИМ не собирались. Таким образом, индекс «спасенного» миокарда (Salvage index, SI) не рассчитывался. В-третьих, наблюдение в течение 6 мес. и небольшой размер выборки были недостаточны для оценки отдаленных клинических результатов и дальнейшего анализа подгрупп. В-четвертых, в данном экспериментальном исследовании назначалась стандартная дозировка. Разница по РИ была умеренной при отсутствии первичной конечной точки в 30% случаев, что могло привести к систематической ошибке в выборке. Поэтому результаты исследования не могут выступать в качестве клинического руководства. Никорандил играет различные биологические роли в зависимости от дозы [35–37], которая также может влиять на степень уменьшения РИ и требует дальнейшего изучения. Учитывая особую патофизиологию в острой фазе ИМ, необходимо дополнительно исследовать кардиопротективные свойства никорандила при ступенчатой терапии (большая доза в 1-ю нед. и непрерывный прием стандартной дозы в последующий период).
Заключение
Однократный прием никорандила перед ЧКВ может быть недостаточным для реализации его протективных свойств. Результаты настоящего исследования показывают, что длительное применение никорандила оказывает более благоприятное воздействие на такие параметры, как РИ и клинические исходы у пациентов со STEMI, перенесших пЧКВ. Кроме того, непрерывная медикаментозная поддержка является многообещающей стратегией для уменьшения размеров зоны некроза по сравнению с краткосрочным вмешательством, которая нуждается в дальнейших исследованиях.
Реферат подготовлен редакцией «РМЖ. Медицинское обозрение» по материалам статьи: Wang S., Duan Y., Feng X. et al. Sustained nicorandil administration reduces the infarct size in ST-segment elevation myocardial infarction patients with primary percutaneous coronary intervention. Anatol J Cardiol. 2019;21:163–171. DOI:10.14744/AnatolJCardiol.2018.57383.
Информация с rmj.ru