Содержание статьи
Введение
Последние десятилетия ознаменовались расширением спектра этиологических факторов хронического гастрита, глобальными изменениями подходов к диагностике и лечению этого заболевания [1, 2]. В качестве ведущих причин хронического гастрита рассматриваются инфекция Helicobacter pylori (Н. pylori), аутоиммунное воспаление слизистой оболочки желудка и химический гастрит (гастропатия, формирование которой обусловлено либо билиарным рефлюксом, либо приемом лекарственных препаратов). По данным эпидемиологических исследований, на долю билиарного гастрита приходится до 22% всех случаев хронического гастрита, при этом дискутабельными остаются вопросы дифференцированного подхода к установлению диагноза, выбору индивидуализированной терапии и определению прогноза [3].
Настоящий обзор подготовлен для систематизации данных о причинах, механизмах развития, подходах к диагностике и терапии хронического билиарного гастрита.
Билиарный гастрит
Под билиарным или дуоденогастральным рефлюксом (от лат. refluo — «течь назад») понимается ретроградный заброс содержимого двенадцатиперстной кишки, включая желчь и панкреатические ферменты, в желудок. Билиарный рефлюкс может наблюдаться и в физиологических условиях — в ранние утренние часы, в постпрандиальный период и на фоне длительного голодания [4]. Однако при увеличении частоты рефлюксов и/или длительности контакта агрессивных компонентов рефлюктата со слизистой оболочкой желудка возможно повреждение последней и развитие билиарного гастрита (синонимы: «рефлюкс-гастрит», «реактивная гастропатия», «химический гастрит», «гастропатия, связанная с рефлюксом желчи»).
К факторам риска, ассоциированным с формированием билиарного рефлюкс-гастрита, относятся анатомические изменения в зоне дуоденогастрального перехода (резекция желудка, гастроэнтеростомия, рукавная гастрэктомия, энтеростомия, пилоропластика), а также различные стадии желчнокаменной болезни, включая период постхолецистэктомии [5–7]. У лиц с сохраненным дуоденогастральным переходом доминирующим фактором являются моторные нарушения верхних отделов пищеварительного тракта (первичный билиарный гастрит), а у лиц после оперативных вмешательств — структурные изменения (вторичный билиарный гастрит) [8–10].
Механизм развития билиарного гастрита
При билиарном гастрите повреждающее действие на слизистую оболочку желудка оказывают желчные кислоты и их соли. Желчные кислоты являются основными компонентами желчи и по своей химической структуре относятся к производным холановой кислоты. Первичные желчные кислоты — холевая и хенодезоксихолевая — синтезируются из холестерина в гепатоцитах. В составе желчи первичные желчные кислоты находятся в виде конъюгатов — соединений с аминокислотами глицином или таурином [11]. Постпрандиальное сокращение желчного пузыря способствует выделению желчи в двенадцатиперстную кишку, где при активном участии желчных кислот происходит эмульгация жиров, активация липазы поджелудочной железы и всасывание целого ряда гидрофобных веществ (холестерин, жирорастворимые витамины, растительные стероиды и др.). Дойдя до терминального отдела подвздошной кишки, часть конъюгированных первичных желчных кислот освобождается от глицина и таурина и с портальным кровотоком поступает в печень, часть достигает толстой кишки и под действием 7α-гидроксилазы бактерий дегидроксилируется с образованием вторичных желчных кислот — литохолевой и дезоксихолевой [12, 13]. Дезоксихолевая кислота всасывается путем пассивной диффузии и продолжает участвовать в энтерогепатической циркуляции наравне с первичными желчными кислотами, а литохолевая, в силу своей плохой растворимости, не реабсорбируется и выводится с калом [14]. Общий пул желчных кислот у человека за один цикл энтерогепатической циркуляции составляет 2–4 г, сам цикл повторяется 7–10 раз в день, в результате чего всасывается до 30 г желчных кислот в сутки, при этом около 10% теряется с калом [15].
Когда возникает желчный рефлюкс, происходит регургитация желчных кислот в желудок, где они оказывают свое повреждающее действие за счет целого ряда механизмов:
лецитин из желчных кислот под действием фосфолипазы А превращается в лизолецитин, который разрушает фосфолипидный слой клеточных мембран эпителия слизистой оболочки желудка;
желчные кислоты ингибируют активность фермента синтазы оксида азота, приводя к повреждению ДНК, апоптозу и мутациям клеток;
желчные кислоты способствуют обратной диффузии H+ и стимулируют тучные клетки к высвобождению гистамина, усиливающего секрецию соляной кислоты — еще одного фактора агрессии по отношению к слизистой оболочке желудка, потенцирующего негативное действие самих желчных кислот [16, 17].
В условиях низкого рН желчные кислоты превращаются в еще более цитотоксичные неионогенные формы, способные проникать через клеточные мембраны, повреждая плотные межклеточные контакты [18]. Все вышеперечисленные механизмы способствуют также формированию синдрома повышенной эпителиальной проницаемости (СПЭП), который является наиболее активно изучаемым феноменом в патогенезе различных заболеваний пищеварительного тракта как органической, так и функциональной природы. СПЭП облегчает проникновение агрессивных молекул рефлюктата в подслизистый слой, что приводит к раздражению афферентных нейронов, развитию висцеральной гиперчувствительности, моторной дисфункции, и как следствие, появлению диспептических жалоб у пациентов.
Дуоденогастральный рефлюкс может увеличивать секрецию гастрина G-клетками, который, помимо повышения продукции соляной кислоты париетальными клетками, ингибирует сокращение пилорического сфинктера, что усугубляет билиарный рефлюкс и формирует порочный круг.
В последнее время появляются данные о том, что рефлюкс желчи в желудок посредством изменения рН может также модулировать микробиоту желудка с увеличением представительства бактерий с провоспалительным потенциалом [19]. Схематическое изображение энтерогепатической циркуляции желчных кислот и механизмы развития хронического билиарного гастрита представлены на рисунке 1 [20].
![Рис. 1. Энтерогепатическая циркуляция желчных кислот и механизмы развития хронического билиарного гастрита [22] Fig. 1. Enterohepatic circulation of bile acids and pathogenetic mechanisms of chronic biliary gastritis [22] Рис. 1. Энтерогепатическая циркуляция желчных кислот и механизмы развития хронического билиарного гастрита [22] Fig. 1. Enterohepatic circulation of bile acids and pathogenetic mechanisms of chronic biliary gastritis [22]](https://medblog.su/wp-content/uploads/2022/07/biliarnyj-gastrit-sovremennye-podhody-k-diagnostike-i-terapii-livzan-m-a-gaus-o-v-mozgovoj-s-i-telyatnikova-l-i.png)
Все больше данных свидетельствует о том, что желчный рефлюкс ассоциирован с развитием атрофического гастрита, кишечной метаплазией, дисплазией и, следовательно, канцерогенезом [21, 22]. T. Matsuhisa et al. [23] обнаружили, что высокие концентрации конъюгированных желчных кислот, по-видимому, связаны с повышенным риском развития кишечной метаплазии, независимо от наличия инфекции Н. pylori. Кроме того, даже после успешной эрадикации Н. pylori желчные кислоты и их соли могут вызывать дисфункцию мукозального барьера слизистой оболочки желудка с изменением профиля микроРНК, характерную для канцерогенеза [24]. При этом хорошо известно, что формирование кишечной метаплазии по пути прогрессирования хронического активного гастрита до рака желудка является своеобразной «точкой невозврата», которая ограничивает эффективность последующих мер канцеропревенции [25, 26]. Обсервационное исследование D. Li et al. [27] с использованием данных 30 465 пациентов также подтвердило, что рефлюкс желчи является независимым фактором риска возникновения предраковых поражений желудка, а затем и рака желудка.
Подходы к диагностике билиарного гастрита
Клинические проявления у пациентов с билиарным гастритом могут отсутствовать или ограничиваться наличием синдрома диспепсии, при этом каких-то специфических маркеров, которые указывали бы на этио-логический фактор, не существует. Более того, на сегодняшний день установлено, что наличие и выраженность синдрома диспепсии не коррелируют с наличием и выраженностью структурных изменений со стороны слизистой оболочки желудка. При воздействии агрессивных компонентов желчи на слизистую оболочку желудка возможно появление «голодных» болей в эпигастрии или пилородуоденальной зоне, нередко сопровождающихся чувством горечи во рту или отрыжкой горьким содержимым. При выраженных моторно-эвакуаторных нарушениях антродуоденальной зоны развивается постпрандиальный дистресс-синдром, проявлениями которого могут быть чувство тяжести в эпигастрии после еды и быстрого насыщения, тошнота, отрыжка воздухом, снижение аппетита.
Основной целью опроса и осмотра является выявление симптомов тревоги, сопутствующих заболеваний печени и желчевыводящих путей, сбор анамнеза, в первую очередь в отношении перенесенных оперативных вмешательств на органах брюшной полости.
Патогномоничные макро- и микроскопические стигмы билиарного гастрита отсутствуют. Эндоскопическая картина и гистологические изменения совпадают с таковыми при другом варианте реактивной гастропатии — гастропатии, ассоциированной с приемом нестероидных противовоспалительных препаратов. Важно помнить, что визуализация заброса желчи в желудок при эндоскопическом исследовании, равно как и констатация наличия неспецифических морфологических признаков, указывающих на повреждение эпителиального барьера, не являются достаточными для постановки диагноза гастрита, вызванного билиарным рефлюксом.
Как правило, эндоскопические проявления при билиарном гастрите представлены гиперемией и отеком слизистой оболочки, которые распространяются циркулярно от пилорического отдела в проксимальном направлении. При этом на поверхности слизистой оболочки часто обнаруживаются пятна желчи, отмечается видимый заброс желчи из двенадцатиперстной кишки в желудок или высокое содержание желчи в просвете желудка [28]. Типичная эндоскопическая картина хронического билиарного гастрита представлена на рисунке 2.
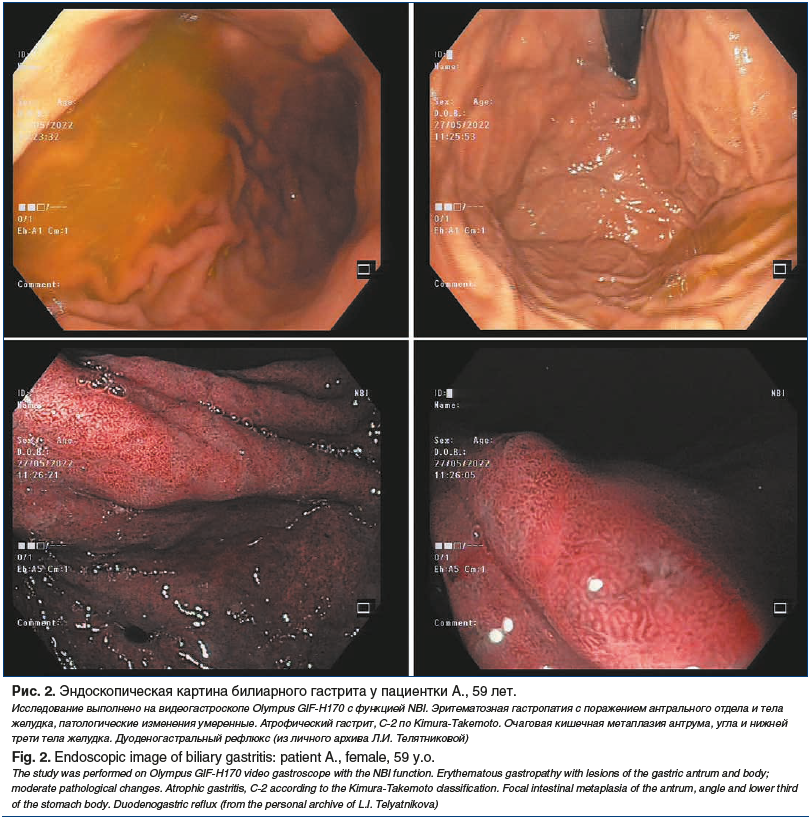
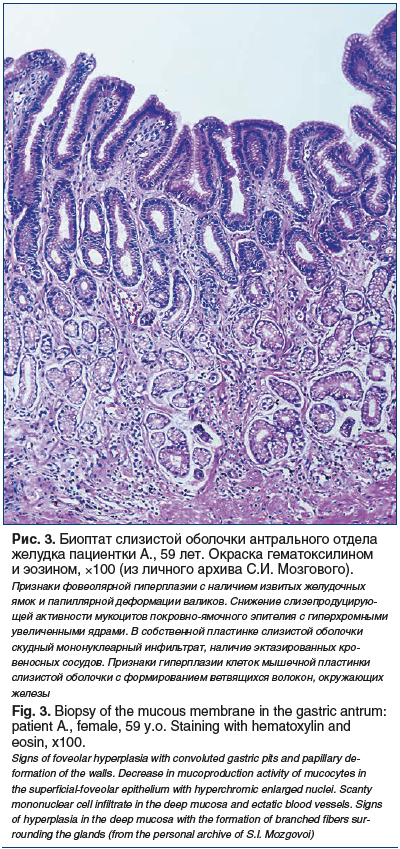
К микроскопическим признакам билиарного гастрита относят слабую диффузную, преимущественно мононуклеарную, воспалительную инфильтрацию собственной пластинки, выраженные регенераторные изменения эпителия (фовеолярная гиперплазия с гиперхромными ядрами клеток, снижение слизеобразования), отек с полнокровием сосудов в собственной пластинке слизистой оболочки, наличие субнуклеарной вакуолизации цитоплазмы (морфологический феномен, ассоциированный с синдромом оперированного желудка), наличие пучков гладкомышечных клеток в собственной пластинке слизистой оболочки, разделяющих железы на группы, и изменение продукции мукоцитами муцинов, играющих важную протективную роль (рис. 3).
Подходы к лечению билиарного гастрита
Важная роль в комплексной программе терапии пациентов с билиарным гастритом отводится модификации образа жизни и характера питания. В качестве основных принципов диетотерапии рассматриваются частый, дробный режим питания, исключение поздних и обильных приемов пищи, ограничение продуктов, которые могут вызывать моторную дисфункцию верхних отделов пищеварительного тракта (жиры животного происхождения, крепкий чай, кофе, газированные напитки), отказ от курения и употребления алкоголя.
Поскольку в повреждении слизистой оболочки желудка при билиарном рефлюкс-гастрите ключевую роль играет не гиперпродукция соляной кислоты, а действие других повреждающих факторов и повышение проницаемости слизистой оболочки, в схему лечения пациентов целесообразно включать цитопротективную терапию, которую следует рассматривать как комплекс мер, направленных на снижение активности ведущего повреждающего фактора и восстановление барьерных свойств слизистой оболочки ЖКТ.
Высокоэффективным лекарственным средством, устраняющим повышенную эпителиальную проницаемость, является ребамипид (Ребагит®), который имеет хорошую доказательную базу [29].
Ребамипид регулирует содержание простагландина Е2 в слизистой оболочке ЖКТ, способствует активации ферментов, ускоряющих биосинтез высокомолекулярных гликопротеинов, и увеличивает содержание слизи на поверхности эпителия. Кроме того, препарат стимулирует продукцию бикарбонатов, подавляет продукцию полиморфноядерными лейкоцитами и нейтрофилами свободных радикалов, усиливает пролиферацию эпителиальных клеток, улучшает микроциркуляцию, чем способствует поддержанию барьерной функции слизистой оболочки желудка [30, 31].
За счет своего противовоспалительного действия и способности восстанавливать клеточную структуру эпителия желудка ребамипид является высокоэффективным и безопасным средством первичной и вторичной профилактики рака желудка [32, 33]. Имеются данные рандомизированных клинических исследований о том, что ребамипид не только снижает воспаление, но и способствует нормализации пролиферативного потенциала и муцинпродуцирующей функции слизистой оболочки желудка [34, 35]. Кроме того, препарат обладает хорошим клиническим эффектом, в частности, в отношении купирования симптомов у пациентов с функциональной диспепсией [36] и обеспечения длительной ремиссии заболевания. Назначается курсом 4–8 нед. 100 мг 3 р/сут.
Группой средств патогенетической терапии для пациентов с билиарным рефлюкс-гастритом являются препараты урсодезоксихолевой кислоты (УДХК) (Урсосан®). УДХК, модулируя состав желчи путем замещения токсичных желчных кислот на нетоксичные, снижает агрессивность желчного рефлюктата и оказывает цитопротективное действие на эпителиоциты желудка и пищевода. В исследовании A.B. Stefaniwsky et al. [37] оценивали влияние измененного состава желчных кислот в рефлюктате на симптомы и гистологические параметры слизистой оболочки желудка. В ходе исследования 12 пациентов после операции на желудке с симптоматическим щелочным рефлюкс-гастритом в течение 4 нед. получали УДХК в дозе 1000 мг/сут или плацебо. Лечение УДХК привело к значительному снижению частоты и интенсивности болей, тошноты и рвоты, в то время как во время приема плацебо не было отмечено существенного изменения симптомов. Во время терапии доля УДХК, полученной из желудочного содержимого, возросла до 50% в общем пуле желчных кислот. Эти результаты свидетельствуют о том, что увеличение доли УДХК в рефлюксной желчи желудка уменьшает боль и частоту симптомов, связанных с рефлюксом желчи.
О.Н. Минушкин и соавт. [38] оценивали эффективность нетоксичной желчной кислоты в лечении больных хроническим (билиарным) рефлюкс-гастритом. Показано, что УДХК в суточной дозе 12,5 мг/кг 1–2 р/сут после еды в течение 28 дней оказалась эффективной у 100% больных, у 67% воспалительные изменения слизистой оболочки были купированы полностью, а у 33% воспаление перешло в очаговую форму.
При билиарном рефлюкс-гастрите УДХК назначается в дозе 250 мг/сут и принимается однократно перед сном. Длительность курса составляет от 10–14 дней до 6 мес., при необходимости — более продолжительный срок.
Поскольку нарушения моторики ЖКТ играют ключевую роль в возникновении симптомов билиарного гастрита, в качестве симптоматической терапии рассматривается назначение препаратов итоприда (Итомед®) 150 мг/сут курсом на 4 нед., обеспечивающее быстрое купирование диспепсических симптомов билиарного гастрита.
При наличии инфекции Н. pylori следует провести эрадикационную терапию для ликвидации дополнительного фактора, повреждающего слизистую оболочку желудка и увеличивающего риск развития синдрома диспепсии [39].
Патогенетически обоснованная схема терапии пациента с билиарным гастритом может быть представлена следующим образом: ребамипид 100 мг 3 р/сут 4–8 нед., УДХК 250 мг на ночь 4 нед., итоприд 50 мг 3 р/сут 4 нед.
Заключение
Хронический билиарный рефлюкс-гастрит может развиваться вследствие изменений желчевыводящих путей и пилородуоденальной зоны после оперативных вмешательств, а также у лиц с функциональными нарушениями моторики верхних отделов пищеварительного тракта без предшествующих операций в анамнезе. В свою очередь, несостоятельность сфинктерного аппарата, антродуоденальная дискоординация, ухудшение свойств самой желчи являются причинами формирования рецидивирующего заброса содержимого двенадцатиперстной кишки в желудок с повреждением его слизистой оболочки. Известно, что желчные кислоты, обладающие детергентными свойствами, непосредственно повреждают слизистую оболочку желудка, а также потенцируют негативное воздействие на нее других агрессивных компонентов (H. pylori, желудочный сок).
Специфичные клинические, эндоскопические и гистологические признаки у билиарного гастрита отсутствуют. Диагноз устанавливается на основе комплексной оценки объективного статуса и данных анамнеза, прежде всего, в отношении сопутствующих заболеваний билиарного тракта, а также предшествующих оперативных вмешательств на органах брюшной полости, способствующих формированию дуоденогастрального рефлюкса. В пользу билиарного гастрита свидетельствует наличие реактивных изменений слизистой оболочки при отсутствии выраженных признаков хронического воспаления и колонизации Н. pylori на фоне характерной эндоскопической картины (гиперемия и отек слизистой оболочки пилородуоденальной зоны, пятна желчи на поверхности).
Лечение билиарного гастрита должно быть комплексным и направленным не только на купирование диспепсических симптомов и улучшение качества жизни пациентов, но и на профилактику атрофических изменений слизистой оболочки желудка, а при их наличии — на замедление их прогрессирования. Поэтому в качестве средств патогенетической терапии пациентам с хроническим билиарным гастритом целесообразно назначение цитопротекторов, УДХК и препаратов, регулирующих моторику верхних отделов ЖКТ.
Сведения об авторах:
Ливзан Мария Анатольевна — д.м.н., профессор, член-корреспондент РАН, заведующая кафедрой факультетской терапии и гастроэнтерологии, ректор ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-6581-7017.
Гаус Ольга Владимировна — к.м.н., доцент кафедры факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0001-9370-4768.
Мозговой Сергей Игоревич — д.м.н., доцент, профессор кафедры патологической анатомии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-6733-5572.
Телятникова Лариса Ивановна — заведующая эндоскопическим отделением КДЦ «Ультрамед»; 644024, Россия, г. Омск, ул. Чкалова, д.12; ORCID iD 0000-0003-0876-7217.
Контактная информация: Гаус Ольга Владимировна, e-mail: gaus_olga@bk.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 04.04.2022.
Поступила после рецензирования 27.04.2022.
Принята в печать 26.05.2022.
About the authors:
Maria A. Livzan — Dr. Sc. (Med.), Professor, Corresponding Member of the RAS, Head of the Department of Faculty Therapy and Gastroenterology, Chancellor Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-6581-7017.
Olga V. Gaus — C. Sc. (Med.), Assistant Professor of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0001-9370-4768.
Sergei I. Mozgovoy — Dr. Sc. (Med.), Associate Professor, Professor of the Department of Pathological Anatomy, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-6733-5572.
Larisa I. Telyatnikova — Head of the Department of Endoscopy, Clinical Diagnostic Center «Ultramed»; 12, Chkalov str., Omsk, 644024, Russian Federation; ORCID iD 0000-0003-0876-7217.
Contact information: Olga V. Gaus, e-mail: gaus_olga@bk.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 04.04.2022.
Revised 27.04.2022.
Accepted 26.05.2022.
.
Информация с rmj.ru






