Введение
Актуальность применения антисептических средств в косметологии не вызывает сомнений ввиду большого количества инвазивных манипуляций в рутинной практике врача-косметолога. Инъекционное введение лекарственных и косметологических препаратов, татуаж, мануальное очищение и фракционная лазерная обработка кожи — все это ведет к механическому повреждению кожи, что является потенциальными входными воротами для инфекции. В пятерку лидирующих малоинвазивных процедур, имеющих потенциальный риск инфицирования, входят: коррекция ботулинотоксином, аугментация мягких тканей, химический пилинг, лазерная терапия и др.
Содержание статьи
Кожа и ее защитная функция
Кожа — орган, выполняющий множество функций, важнейшей из которых является защитная. Реализует защитную функцию кожи многослойный эпителий, клетки которого связаны между собой тесными межклеточными десмосомальными контактами, а клетки наружного (рогового) слоя кожи накладываются друг на друга как черепица, обеспечивая тем самым очень плотный защитный механический каркас. Вторым немаловажным защитным фактором служит полноценно функционирующий липидный барьер кожи, основной компонент которого — липидный матрикс — состоит из керамидов — важнейших липидов рогового слоя эпидермиса, содержание которых обратно пропорционально зрелости эпидермального барьера. К функциям керамидов относятся транс-кутанная регуляция потери воды, контроль темпа десквамации, а также воздействие на дифференцировку кератиноцитов путем синтеза филаггрина — структурного белка кожи [1].
Важную роль в реализации защитной функции выполняет микробиота кожи. H.J. Lee et al. [2] показали, что микробиота необходима для обеспечения целостности и полноценного функционирования эпидермального барьера. Эти функции опосредуются ариловодородным рецептором (AHR) кератиноцитов. Установлено, что у мышей, лишенных AHR, легче повреждается кожа и они более уязвимы к воздействию инфекции. Микроорганизмы в случае повреждения эпидермиса вырабатывают метаболиты, которые активируют AHR, способствуя дифференцировке клеток эпидермиса и тем самым поддерживая его целостность [2]. Очевидно, что при любом нарушении целостности кожи (фракционная лазерная обработка, татуаж, мануальная или аппаратная комедоноэкстракция и т. д.) повышается ее проницаемость и для микроорганизмов.
Инфекции кожи
Основными возбудителями поверхностных инфекций кожи являются постоянно персистирующие на ней Staphylococcus aureus и Streptococcus pyogenes [3]. Кроме того, инфекционно-воспалительные процессы во всех слоях кожи могут вызывать Enterococcus spp., Escherichia coli, Klebsiella spp. и другие энтеробактерии [4]. Далеко не всегда возможно выделить единственного возбудителя, выступающего причиной воспалительно-инфекционного осложнения. В некоторых случаях возбудителями инфекций кожи становятся колонии микроорганизмов, способные образовывать биопленки, что в настоящее время является серьезной проблемой мирового здравоохранения [5]. Биопленка — это сообщество бактерий, которое плотно зафиксировано на субстрате и погружено во внеклеточный полисахаридный матрикс. Бактериальное сообщество тесно связано между собой системой quorum sensing — особым видом коммуникации бактерий, который координирует экспрессию генов. Сила и активность этой связи зависят от популяционной плотности сообщества бактерий [5]. Коммуникация микроорганизмов осуществляется благодаря сигнальным молекулам. Микроорганизмы в биопленке способны противостоять действию антибактериальных препаратов за счет «дремлющих» бактерий, а также ферментов, которые способны инактивировать антибактериальные препараты (наиболее часто встречается выработка β-лактамаз, разрушающих β-лактамное кольцо пенициллинов, цефалоспоринов, монобактамов и карбапенемов путем катализа гидролиза амидной связи в β-лактамном кольце), способствуя развитию резистентности макроорганизма [6].
Осложнения, связанные с присоединением вторичной инфекции, опасны и тем, что при высокой активности воспалительного процесса, а также при несвоевременной постановке диагноза и нерациональном ведении такого пациента они могут привести к более серьезным структурным изменениям кожи в более глубоких слоях, некрозу тканей и, впоследствии, образованию грубых рубцов [7].
В зависимости от локализации инфекционного процесса можно выделить 4 вида инфекционного поражения кожи [8]:
-
поражение собственно эпидермиса. На этом уровне не повреждается базальная мембрана, благодаря чему заживление раны происходит без образования рубца;
-
поражение подкожно-жировой клетчатки (ПЖК);
-
поражение поверхностной фасции;
-
поражение глубоких фасциальных структур и мышц.
При поражениях второго и третьего вида повреждается базальная мембрана, что увеличивает впоследствии риск образования рубца [8].
В зависимости от причины повреждения кожи выделяют раны: операционные (в том числе наносимые во время электро-, лазеро-, криопроцедур, шлифовок, пилингов и т. д.), которые при соблюдении принципов асептики и антисептики являются стерильными; случайные, которые получают в бытовых, производственных, боевых условиях, а также возникающие на фоне существующих дерматозов. Большинство случайных ран являются первично бактериально инфицированными.
Под бактериальным (микробным) инфицированием, или «обсеменением», раны понимают инфицирование раны в момент ее возникновения (первичное бактериальное загрязнение) или в процессе терапии при нарушении правил асептики и антисептики (вторичное бактериальное загрязнение).
По степени бактериального инфицирования выделяют асептические, загрязненные и инфицированные раны [9].
В зависимости от времени возникновения инфекции кожи могут быть: острые, которые дебютируют в течение первых трех дней после проведения процедуры в виде эритематозно-пустулезных, акнеформных высыпаний, вплоть до формирования абсцессов; хронические, которые развиваются через 2 нед. и более после процедуры за счет окклюзии лимфатических сосудов и формирования биопленок в основном в местах с тонкой и подвижной кожей [9].
В косметологии преимущественно встречаются поражения собственно кожи и ПЖК, в тяжелых случаях в воспалительный процесс могут вовлекаться и глубокие фасциальные и мышечные структуры. Также нередки сосудистые осложнения, возникающие на фоне проведения инвазивных процедур. По данным [10], общая частота сосудистых нежелательных явлений при введении гиалуроновой кислоты составляет 1%, с учетом того, что в 2018 г. в США было проведено 2,7 млн инъекций. Среди осложнений, возникающих на фоне этой процедуры, наиболее тяжелыми являются локальная ишемия и некроз кожи, вызванные сосудистыми осложнениями, а также слепота и нарушения мозгового кровообращения [10].
В структуре причин инфекционно-воспалительных осложнений в косметологии можно выделить 3 категории:
-
Нарушение целостности кожных покровов во время проведения косметологических манипуляций, что увеличивает риск присоединения бактериальной инфекции.
-
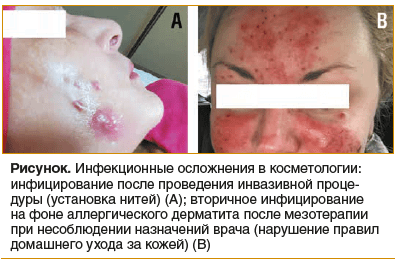
Нарушение технологии проведения процедуры и несоблюдение асептики и антисептики (см. рисунок, А).
-
Некорректное донесение пациенту информации по уходу за кожей после процедуры доктором или несоблюдение пациентом рекомендаций врача (см. рисунок, В).
Выполнение ряда процедур (например, мезотерапии и пилингов) неквалифицированными работниками ассоциируется со значительным увеличением риска осложнений — от пиодермий до некроза, изъязвления тканей с последующим формированием рубца [11].
Перечень нежелательных явлений, регистрируемых в косметологии, безусловно, не ограничивается осложнениями только инфекционной природы. Это могут быть различные по объему кровоизлияния, отеки, реакции гиперчувствительности, аллергические реакции разной степени выраженности. Однако вопрос профилактики воспалительно-инфекционных заболеваний кожи после косметологических процедур стоит довольно остро. Решение проблемы осложняется появлением резистентных к антибиотикам форм микроорганизмов, что обусловливает активный поиск альтернативных методов терапии [3].
Лечение и профилактика инфекций кожи
Методами профилактики развития инфекционных осложнений после любых инвазивных процедур в косметологии являются:
-
тщательный сбор анамнеза. В группе риска по формированию инфекционных осложнений кожи находятся больные с хроническими соматическими заболеваниями (кардиоваскулярные, заболевания дыхательной системы, сахарный диабет), а также с отягощенным аллергологическим анамнезом;
-
соблюдение правил асептики и антисептики во время проведения процедуры;
-
подробное инструктирование и обучение пациента всем аспектам ухода за кожей после выполнения различных манипуляций;
-
применение топических антибактериальных препаратов при появлении воспалительно-инфекционных элементов на коже.
При распространенном и тяжелом процессе возможно также назначение системных антибактериальных препаратов. Системная антибиотикотерапия имеет определенные ограничения к назначению, поскольку неоправданное широкое применение антибактериальных препаратов из различных фармакологических групп может привести к формированию антибиотикоустойчивой флоры, что в дальнейшем существенно осложняет выбор эффективного лечения. Показаниями к системному применению антибактериальных препаратов в косметологии являются: тяжелое течение гнойного процесса, общие симптомы интоксикации (повышение температуры тела, слабость), глубокие формы пиодермии с локализацией на лице и шее, регионарные осложнения (лимфаденит, лимфангит и т. п.), а также хроническое течение пиодермий с частыми рецидивами [7].
Сравнительно новой методикой лечения кожных инфекций являются антимикробные пептиды. Интерес к антимикробным пептидам в лечении дерматозов особенно вырос, когда было обнаружено высвобождение антимикробных пептидов: кателицидинов во время репарации ран, а также наличие β-дефензинов в чешуйках кожи при псориазе [12]. Антимикробные пептиды и белки (АМПБ) — это эндогенные соединения, напрямую воздействующие на бактерии, грибы и вирусы. АМПБ являются основным компонентом врожденного иммунитета, вырабатываются как эпителиальными клетками кожи, дыхательных путей, кишечника, мочевыводящих и половых путей, так и клетками иммунной системы, а также содержатся в секреторных жидкостях человека. Механизм действия АМПБ заключается в подавлении метаболических процессов микробной клетки, в результате чего нарушается целостность клеточной мембраны и, как следствие, наступает гибель микробной клетки. Кроме того, АМПБ могут выполнять роль хемоаттрактантов иммунокомпетентных клеток (нейтрофилы, моноциты, Т-лимфоциты, дендритные клетки) в очаге воспаления. Они оказывают влияние также на антигенпрезентирующие клетки, модулируя адаптивный T-клеточный иммунный ответ [13]. На данный момент изучается применение АМПБ в урологии, пульмонологии, стоматологии, а также дерматовенерологии и косметологии [13].
И все же осложнения в косметологии в основном носят поверхностный, локальный характер, это так называемые «малые раны», не требующие хирургического вмешательства и системной антибактериальной терапии. В таких случаях совместно с местными антисептиками возможно назначить и препараты, позволяющие ускорить процессы регенерации тканей — репаранты. В основе фармакологической регуляции процесса регенерации кожи лежат различные механизмы: стимуляция белкового синтеза, активация защитных свойств, противовоспалительное и антисептическое действие фармацевтических препаратов [9].
Местные антисептические препараты
Местное применение антисептиков по сравнению с системным антибактериальным лечением имеет ряд преимуществ: отсутствие системных побочных эффектов, минимальный риск формирования бактериальной резистентности и более высокая концентрация антибактериального агента в очаге инфекции [14, 15]. А.Н. Герке [16] отмечает возможность антисептиков дезактивировать резистентные штаммы патогенов в очаге воспаления.
Антисептики также входят в число препаратов, которые используются для предотвращения инфекционно-воспалительного процесса после проведения инвазивных процедур.
К наиболее часто используемым антисептикам в косметологии относят:
Хлоргексидин — двухвалентный катионный бигуанидный биоцид с широким спектром антибактериальной активности. За счет своего положительного заряда он связывается с отрицательно заряженными микробными мембранами и разрушает их.
Триклозан — бисфенол, который обладает широким спектром действия. Триклозан устойчив к биоразложению и может оставаться в окружающей среде более 10 лет [16]. Это делает его токсичным для микробиоты, растений и рыб, а также может формировать перекрестную устойчивость к антибиотикам.
Бензалкония хлорид — относится к группе четвертичных соединений аммония, обладает широким антимикробным действием. Длинная алкиловая цепь хлорида бензалкония пронизывает мембрану микроорганизмов, а заряженный азот остается на внешней поверхности. Это меняет заряд мембраны и приводит к денатурации мембранного белка, разрушая структуру микробной клетки.
Декаметоксин — относится к группе бис-кватернарных соединений аммония. Его действие заключается в его накоплении в цитоплазматической мембране и дальнейшем связывании с фосфатными группами мембранных липидов. За счет этого нарушается проницаемость мембран микробных клеток.
Диоксидин — проявляет свою активность в анаэробных условиях из-за увеличения высвобождения из его молекулы активного кислорода.
Бензилдиметил-миристоиламино-пропиламмоний (БМП) — относится к группе катионных антисептиков, поверхностно-активных веществ (четвертичные аммониевые соединения), оказывает противомикробное, противовоспалительное и местное действие. Обладает свойствами катионного детергента, гидрофобно взаимодействует с липидным бислоем мембран бактерий и других микроорганизмов, увеличивает проницаемость их клеточных стенок и цитоплазматических мембран и индуцирует цитолиз [16, 17].
Все вышеперечисленные антисептические препараты имеют жидкую форму (растворы). При этом именно в косметологии преимущественно применяются бесконтактные методы нанесения антисептических препаратов.
На российском фармацевтическом рынке появился новый препарат Митрасептин®-ПРО с активным действующим веществом в составе — БМП. Преимуществом данного препарата по сравнению с другими местными антисептиками является аэрозольная форма выпуска1, обеспечивающая мелкодисперсное распыление и воздействие на обширную зону в отличие от спреев и растворов, наносится 2–3 раза в сутки в течение 3–5 дней2.
Антисептический топический препарат Митрасептин®-ПРО в форме аэрозоля относится к классу химических препаратов (противомикробных агентов), который оказывает бактерицидное действие, а также воздействует на вирусы, грибы [17]. Действующее вещество препарата Митрасептин®-ПРО — БМП — проявляет бактерицидный эффект в отношении аэробных и анаэробных бактерий, включая штаммы с полирезистентностью к антибактериальным препаратам. По данным A. Osmanov et al. [17], после 18-часового воздействия на штаммы бактерий 0,01% раствора БМП только 9,3% изолятов (в основном стафилококки) остались жизнеспособными. Грамотрицательные кокки погибали через 6 ч, а стрептококки — через 1 ч после местного воздействия БМП. Местное лечение ран в среднем в течение 14 дней препятствовало увеличению размеров очагов воспаления [17].
Бактерицидное действие реализуется за счет взаимодействия с фосфатными группами мембранных липидов, что нарушает осмотическое равновесие в клетке, тем самым приводя к гибели микроорганизма. Препарат оказывает выраженное бактерицидное действие в отношении грамположительных (Staphylococcus spp., Streptococcus spp., Streptococcus pneumoniae), грамотрицательных (Pseudomonas aeruginosa, E. coli, Klebsiella spp.), аэробных и анаэробных бактерий, определяемых как в виде монокультур, так и в виде микробных ассоциаций, включая полирезистентные госпитальные штаммы [17, 18].
Противовирусное и противогрибковое действие заключается во взаимодействии положительного заряда БМП с отрицательно заряженным суперкапсидом вируса и клеточной стенкой грибов. БМП эффективен в отношении аскомицет рода Aspergillus и рода Penicillium, дрожжевых (Rhodotorula rubra, Torulopsis glabrata) и дрожжеподобных (Candida albicans, Candida tropicalis, Candida krusei, Pityrosporum orbiculare (Malassezia furfur)) грибов, дерматофитов (Trichophyton rubrum, Trichophyton mentagrophytes, Trichophyton verrucosum, Trichophyton schoenleini, Trichophyton violacent, Epidermophyton Kaufman-Wolf, Epidermophyton floccosum, Microsporum gypseum, Microsporum canis) в виде монокультур и микробных ассоциаций, включая грибковую микрофлору с резистентностью к химиотерапевтическим лекарственным средствам. Также он потенцирует действие антибактериальных средств. Как было отмечено выше, в основе действия БМП — прямое влияние на мембраны клеток микроорганизмов. Гидрофобное взаимодействие его молекулы с липидными мембранами приводит к фрагментации и разрушению микробной оболочки. При этом часть молекулы препарата погружается в гидрофобный участок мембраны микробной клетки, разрушает надмембранный слой, разрыхляет мембрану и повышает ее проницаемость для крупномолекулярных веществ1. БМП, помимо всего вышеперечисленного:
-
участвует в регенерации тканей и заживлении раны;
-
обладает выраженной гиперосмолярной активностью, вследствие чего способствует купированию раневого и перифокального воспаления;
-
абсорбирует гнойный экссудат, способствуя формированию сухого струпа;
-
не повреждает грануляции и жизнеспособные клетки кожи;
-
не угнетает краевую эпителизацию;
-
не обладает местнораздражающим действием и аллергизирующими свойствами [19].
Еще одна функция БМП — иммуностимулирующая — обусловлена активацией поглотительной функции фагоцитов и моноцитарно-макрофагальной системы в целом [17].
Микробиологические исследования демонстрируют воздействие препарата Митрасептин®-ПРО не только на планктонные формы бактерий, но и на микробные биопленки.
Способность бактерий образовывать биопленки является одним из факторов развития антибиотикорезистентности [5]. Проведенные исследования показывают, что Митрасептин®-ПРО способен ингибировать образование биопленок и подавляет рост уже сформированных биопленок бактерий. Митрасептин®-ПРО особенно эффективен для сформированных биопленок микроорганизмов: Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Klebsiella pneumoniае, Acinetobacter baumanii [17].
Таким образом, БМП (Митрасептин®-ПРО) оказывает противомикробное действие на многие бактерии, грибы и вирусы, а также обладает иммуностимулирующим действием, активируя моноцитарно-макрофагальную систему, способствует регенерации тканей.
Учитывая широкий спектр антимикробной и противогрибковой активности, Митрасептин®-ПРО можно использовать в терапии различных пиодермий, как поверхностных, например при стрепто-стафилодермиях, возникающих как осложнение после пилингов, мезотерапии, татуажа, эпиляции, пирсинга, так и в составе комплексной терапии глубоких пиодермий.
Заключение
Современная косметология, как и все здравоохранение, ищет оптимальные методы профилактики и лечения инфекционных осложнений. Рациональная терапия инфицированных осложнений в косметологии складывается из назначения местной и системной антибиотикотерапии. Как оптимальное местное антисептическое средство в арсенале специалиста, работающего в инвазивной косметологии, может рассматриваться БМП в форме аэрозоля, обеспечивающего мелкодисперсное распыление препарата, обладающего бактерицидным, иммуностимулирующим и репаративным действием. Врачам-косметологам необходимо учитывать постоянно меняющуюся роль патогенов в развитии инфекций кожи и мягких тканей, теперь это не только условно-патогенная микробная флора кожи и слизистых, но и атипичные микобактерии, грибы, вирусная инфекция, приводящие к быстрому, возможно, атипичному развитию пиодермий и формированию осложнений. Новые технологии и подходы в борьбе с резистентными микроорганизмами, а также индивидуальный подход, технологичное соблюдение процедур в косметологии, грамотное информирование пациентов должны быть в приоритете при решении эстетических проблем в медицине.
1Инструкция по медицинскому применению препарата Митрасептин®-ПРО. (Электронный ресурс.) URL: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=d7acfcf8-a507-4de3-a49a-614bf061efe8 (дата обращения: 10.07.2024).
2Фармакопея.рф. ОФС.1.4.1.0002.15 Аэрозоли и спреи. (Электронный ресурс.) URL: https://pharmacopoeia.ru/ofs-1-4-1-0002-15-aerozoli-i-sprei/?ysclid=lzbqzb00j7102250917 (дата обращения: 10.07.2024).
Информация с rmj.ru


