Содержание статьи
Введение
Анкилозирующий спондилит (АС) и псориатический артрит (ПсА) — самые распространенные заболевания из группы спондилоартритов [1], которые могут существенно снижать качество жизни больного и ее продолжительность. В настоящее время продолжают появляться новые препараты или регистрируются новые показания у ранее разработанных лекарств для лечения этой группы заболеваний.
Иксекизумаб, представитель группы ингибиторов интерлейкина (ИЛ) 17, зарегистрирован в РФ по показаниям псориаз, ПсА и АС в 2019 г., позднее в показания добавлен нерентгенологический спондилоартрит. Имеются особенности терминологии, в соответствии с которыми в Европе хроническое воспалительное заболевание с поражением осевого скелета относят к аксиальному спондилоартриту (аксСпА), который, в свою очередь, включает рентгенологический аксСпА (р-аксСпА), также называемый АС, и нерентгенологический аксСпА (нр-аксСпА) [2–4]. Разница между ними заключается в наличии или отсутствии достоверного сакроилиита на обычной рентгенограмме. В соответствии с российской версией модифицированных Нью-Йоркских критериев к АС может быть отнесен как рентгенологический аксСпА (классический АС с рентгенологическими проявлениями), так и нр-аксСпА, который верифицирован при выявлении достоверных МР-признаков аксиального поражения и также называется АС. Тем не менее расхождения в терминологии не меняют сути происходящего процесса.
У пациентов с аксСпА (АС) отмечается хроническая воспалительная боль в спине. Кроме этого, возможны внеаксиальные проявления в виде периферического артрита, энтезита, дактилита, увеита, псориаза или воспалительных заболеваний кишечника [4, 5–7]. Пациенты с р-аксСпА (АС) и персистирующей активностью заболевания (например, индекс BASDAI более 4), а также недостаточным ответом на нестероидные противовоспалительные препараты (НПВП) или их непереносимостью, нуждаются в лечении генно-инженерными биологическими препаратами (ГИБП) или таргетными препаратами [4]. В настоящее время для лечения акс-СпА используются ингибиторы фактора некроза опухоли α (иФНО-α), ИЛ-17 и ингибиторы янус-киназ.
Иксекизумаб представляет собой высокоаффинное моноклональное антитело, избирательно воздействующее на ИЛ-17A [8] и продемонстрировавшее эффективность и безопасность в трех рандомизированных плацебо-контролируемых исследованиях III фазы, два из которых включали пациентов с активным р-аксСпА, не получавших ранее ГИБП (COAST-V) [9, 10] или ранее получавших один или два ингибитора ФНО (COAST-W) [9, 11].
При ПсА главным образом наблюдается воспаление периферических суставов (артрит), пальцев кистей и стоп (дактилит), энтезисов (энтезит), а также может отмечаться воспаление в аксиальных структурах — телах позвонков (спондилит) и илиосакральных сочленениях (сакроилиит).
Псориатический артрит выявляется у 19,7% больных псориазом и у 24,6% пациентов с умеренной и высокой тяжестью псориаза [2]. При ПсА воспалительный процесс затрагивает не только скелетно-мышечные структуры (суставы, позвоночник, энтезы), но и кожу, ногти (псориаз), желудочно-кишечный тракт (воспалительные заболевания кишечника) и органы зрения (увеит, иридоциклит).
Терапия ПсА включает применение лекарственных средств, уменьшающих симптомы артрита: НПВП, глюкокортикоидов, вводимых внутрисуставно, синтетических базисных противовоспалительных препаратов (сБПВП), таргетных синтетических БПВП (тсБПВП) и ГИБП с различными механизмами действия, в частности иФНО-α, ИЛ 12/23 и 17 [1, 2–4].
Эффективность иксекизумаба при ПсА изучена в программе SPIRIT. SPIRIT-H2H — рандомизированное клиническое исследование (РКИ) III фазы, в котором оценивали эффективность двух схем дозирования иксекизумаба по сравнению с адалимумабом у пациентов со среднетяжелым и рефрактерным ПсА, ранее не получавших ГИБП. Иксекизумаб стал первым препаратом, который продемонстрировал более высокую эффективность при прямом сравнении с адалимумабом в отношении одновременного достижения ACR50 и PASI100 [12].
Несмотря на наличие РКИ, убедительно доказывающих эффективность и безопасность препарата [9, 10, 12, 13], несомненный интерес представляют данные реальной клинической практики. Пациенты, получающие лечение вне рамок клинических исследований, могут представлять собой более разнородную группу (с учетом отсутствия необходимости соответствовать критериям включения), иметь большее количество коморбидных состояний; кроме того, в реальной практике может чаще нарушаться режим введения препарата, что может влиять на его конечную эффективность. При этом сложностью анализа данных из клинической практики является не всегда полный комплект данных, что связано с консультациями различными специалистами и в различных центрах. Также анализ усложняет различная продолжительность терапии больных, однако с учетом достаточно быстрого эффекта препаратов мы сочли возможным включение всех пациентов, получавших лечение 3 мес. и более.
Цель исследования: изучить эффективность и безопасность иксекизумаба при лечении АС и ПсА в реальной клинической практике.
Материал и методы
В ретроспективное наблюдательное исследование были включены пациенты, страдающие АС и ПсА, получавшие терапию иксекизумабом в РГНКЦ с февраля 2021 г. по апрель 2022 г. У 3 пациентов терапия была инициирована в других лечебных учреждениях, в связи с чем данные для анализа оказались неполными. Также критерием включения являлось наличие письменного добровольного информированного согласия на участие в исследовании. Диагноз АС был установлен в соответствии с российской версией модифицированных Нью-Йоркских критериев [14], ПсА — в соответствии с критериями CASPAR. Всем пациентам перед началом биологической терапии и во время лечения проводился скрининг на инфекции и контроль лабораторных показателей в соответствии с актуальными клиническими рекомендациями4,.
Оценка активности заболевания проводилась 1 раз в 3–6 мес. по индексам BASDAI и ASDAS для АС, по индексам DAPSA и PASI для ПсА. Сохранению активности заболевания соответствовали значения индексов BASDAI ≥4, ASDAS ≥1,3, PASI >4 [15, 16]. Уровень СРБ считался повышенным при значениях >5 мг/л. Для пациентов, у которых инициация терапии проводилась в других учреждениях, показатели получены из предоставленной медицинской документации (при наличии).
Также у всех пациентов проводился лабораторный контроль безопасности и эффективности терапии в соответствии с актуальными клиническими рекомендациями. При контроле безопасности как для АС, так и для ПсА оценивалось, в первую очередь, наличие цитопений, снижение СКФ и повышение активности трансаминаз. В качестве лабораторного маркера активности использовался СРБ, который входит в индекс ASDAS (для АС) и DAPSA (для ПсА). Все использованные исследования, критерии и тесты представлены в российских клинических рекомендациях по лечению АС и ПсА. Объективное обследование включало в себя подсчет количества болезненных и припухших суставов, подсчет индекса PASI при наличии псориаза.
Статистический анализ данных выполнен с использованием программы IBM® SPSS® Statistics version 23.0 (SPSS Inc., США). Проверка на нормальность распределения не проводилась, в связи с чем использовались непараметрические методы статистики. Результаты представлены как медиана и 25-й и 75-й процентили (Ме [25%; 75%]). Для оценки динамики показателей внутри одной группы на фоне лечения использовали критерии Уилкоксона и χ2 МакНемара. Динамику показателей на фоне терапии оценивали по показателю Δ%, который рассчитывали по формуле: (n1 — n0) / n1 × 100%. Статистически значимыми считали различия при значении р<0,05.
Результаты исследования
Характеристика участников. В анализ включено 27 пациентов, среди них с диагнозом «анкилозирующий спондилит» — 10 человек, с диагнозом «псориатический артрит» — 17 человек. У всех пациентов проведена оценка безопасности лечения, 9 (АС) и 16 (ПсА) пациентов включены в анализ эффективности терапии.
В группе АС (4 мужчины и 5 женщин в возрасте от 29 до 64 лет) медиана возраста на момент начала терапии составила 34 [32; 41,5] года, в группе ПсА (11 мужчин и 6 женщин в возрасте от 19 до 56 лет) — 40 [32,5; 48,5] лет.
У всех пациентов отмечалась неэффективность или непереносимость стандартной терапии. Большинство пациентов до лечения иксекизумабом не получало таргетных препаратов, из 27 больных 4 получали ГИБП/ТСП, которые не позволили добиться ремиссии / низкой активности заболевания: 1 пациент — этанерцепт (ПсА), 1 — апремиласт (ПсА), 1 — нетакимаб (ПсА), и у 1 пациента с АС за время лечения болезни оказались неэффективными 5 иФНО, нетакимаб и секукинумаб или отмечалось последовательное ускользание их эффекта.
Анкилозирующий спондилит
В анализ эффективности включено 9 из 10 пациентов с АС (1 пациент прекратил лечение после первой инъекции по личным обстоятельствам). В связи с тем, что пациенты были включены в исследование в условиях реальной клинической практики, продолжительность терапии у них была разной — от 3 до 9 мес. (медиана 4,3 [3; 6] мес.): 7 человек получали терапию от 2 до 4 мес., 2 человека — 8 и 9 мес. Принимая во внимание быструю динамику на фоне лечения иксекизумабом (по данным исследований, достоверное улучшение отмечалось уже на 12–16-й неделе [11, 13]), такой период мы сочли допустимым для анализа. Иксекизумаб вводился в соответствии с инструкцией к препарату 80 мг каждые 4 нед..
Данные о динамике показателей BASAI, ASDAS до лечения и на фоне терапии представлены в таблице. Отмечалась выраженная положительная динамика, причем медиана индекса BASDAI и значения СРБ достигли низкой активности и нормальных показателей соответственно. Отмечено снижение ASDAS на 58,1 [69,6; 30,8] %, BASDAI на 71,4 [94,0; 50,6] % и уровня СРБ на 89,3 [92,8; 45,3] %.
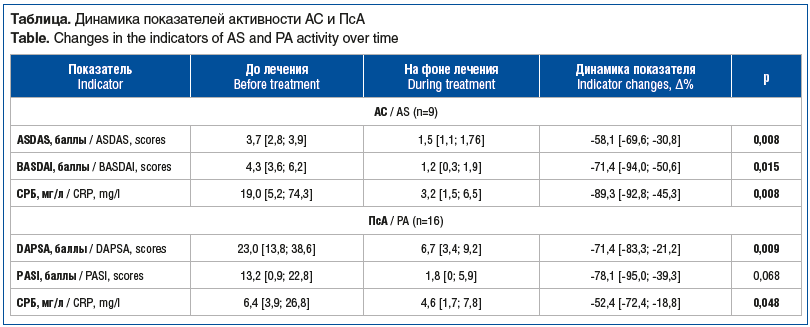
В группе АС повышение уровня СРБ отмечалось у 7 (77,8%) из 9 пациентов, индекс ASDAS соответствовал активному заболеванию у всех больных, активность болезни по индексу BASDAI отмечалась у 77,8% пациентов. На фоне лечения отмечена тенденция к уменьшению доли пациентов с высокой активностью заболевания по индексам ASDAS, BASDAI и доли пациентов с повышенным уровнем СРБ, причем для индекса BASDAI показатели были статистически значимы (рис. 1).
Таким образом, на фоне лечения отмечалось значимое снижение активности АС по показателям СРБ, ASDAS и BASDAI и уменьшение доли пациентов с активностью болезни по индексу BASDAI.
Псориатический артрит
В анализ эффективности включено 16 из 17 пациентов с ПсА (не проводился анализ данных 1 пациента в связи с недостаточным периодом наблюдения). Продолжительность терапии варьировала от 3 до 22 мес., медиана составила 3,5 [3; 11,8] мес. У 9 пациентов продолжительность терапии была менее 4 мес., у 6 — 9–14 мес., и 1 пациент получал терапию в течение 22 мес. С учетом достаточно быстрой динамики на фоне лечения иксекизумабом данный период был сочтен допустимым для анализа. Иксекизумаб вводили в соответствии с инструкцией к препарату 160 мг при инициации и далее 80 мг каждые 4 нед.
Данные о динамике показателей DAPSA, PASI и СРБ до лечения и на фоне терапии представлены в таблице. Отмечалась выраженная положительная динамика DAPSA и СРБ, причем медиана значений СРБ достигла нормы. Для индекса PASI не достигнута статистическая значимость в связи с малым числом наблюдений (n=4). В результате лечения отмечено снижение индекса DAPSA на 71,4 [83,3; 21,2] %, уровня СРБ на 52,4 [72,4; 18,8] %.
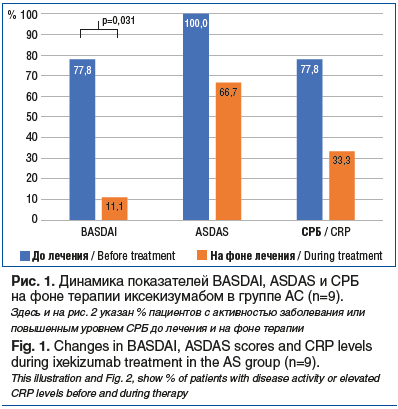
Повышение уровня СРБ отмечалось у 62,5% пациентов, значения индекса DAPSA соответствовали умеренной или высокой активности у 75,0% больных. DAPSA был повышен не у всех пациентов, так как у части больных (n=4) отмечалась минимальная активность аксиального или суставного процесса при тяжелом поражении кожи, что не учитывается при подсчете данного показателя. Данные о СРБ в динамике представлены у 14 пациентов. В результате лечения уменьшилась доля пациентов с повышенными показателями DAPSA и СРБ, однако динамика не достигла статистической значимости (рис. 2).
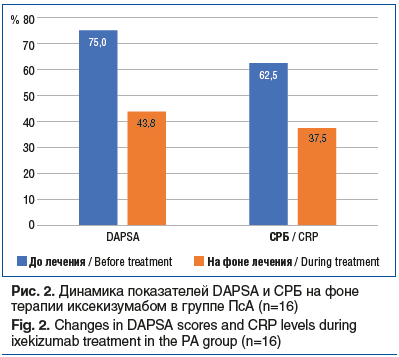
Информация об индексе PASI в динамике касалась 4 пациентов. Значения индекса до лечения варьировали от 0 до 48,6 балла. В результате проводимой терапии иксекизумабом значение индекса снизилось в среднем на 78,1 [95,0; 39,3] % (p=0,068), однако статистическая значимость достигнута не была. Изменения показателя PASI у 4 больных представлены на рисунке 3.
Таким образом, на фоне лечения отмечалось статистически значимо выраженное снижение активности ПсА по показателям СРБ, DAPSA и тенденция к снижению активности кожного поражения по индексу PASI.
Нежелательные явления
Нежелательные явления отмечены у двух пациентов. У пациентки 22 лет с ПсА развился глубокий фурункул в области правой орбиты, в связи с чем инъекция иксекизумаба была выполнена на 2 нед. позже, после заживления фурункула на фоне антибактериальной терапии; связь с проводимой терапией иксекизумабом не доказана. У мужчины 43 лет, также с ПсА, отмечались однократная гиперемия и отек в области инъекции препарата, причем через 6 мес. терапии. Вероятно, это было связано с недостаточным временем нагревания препарата, эпизод был купирован в/м введением антигистаминных препаратов, в дальнейшем такая реакция не наблюдалась. Смертельных исходов и тяжелых побочных эффектов не было.
Обсуждение
Уникальность исследования состоит в самой большой в России когорте пациентов, получающих иксекизумаб в реальной клинической практике. При анализе нашей когорты пациентов получены данные, подтверждающие эффективность и безопасность иксекизумаба в лечении спондилоартритов. При анализе русскоязычной литературы обнаружены отдельные наблюдения эффективности терапии иксекизумабом, публикаций с анализом групп пациентов, получавших данную терапию, не выявлено, что делает представленные данные уникальными.
Полученные результаты, в первую очередь, интересно сопоставить с данными, полученными в регистрационных клинических исследованиях. Сложность сопоставления результатов состоит в смешанной когорте больных (бионаивные и после предшествующей терапии), различной продолжительности терапии, различных критериях оценки активности в РКИ и клинической практике. Таким образом, данное сопоставление носит условный характер, однако, вероятно, позволяет охарактеризовать ряд отмечавшихся тенденций.
Анкилозирующий спондилит
С учетом преобладания бионаивных пациентов с АС в нашей группе сопоставление проводилось с данными исследования COAST V [10]. Наиболее приближенной к нашим исходным данным была подгруппа иксекизумаба с режимом введения 1 раз в 4 нед. с оценкой результатов к 16-й неделе.
Среди наших пациентов с АС повышение уровня СРБ отмечалось у 7 (77,8%) больных и у 52 (64%) в COAST-V. Медиана уровня СРБ до лечения в нашем наблюдении составила 19,0 [5,15; 74,30] мг/л, в COAST-V — 12,2±13,3 мг/л. Вероятно, более частое повышение уровня СРБ и более высокие значения показателя в нашей когорте связаны с направлением на терапию ГИБП изначально более тяжелых и прогностически неблагоприятных пациентов, чем в РКИ.
Исходный индекс BASDAI в нашем исследовании до лечения (медиана) составил 4,3 [3,6; 6,2] балла, в COAST-V — 6,8±1,3 балла. В результате проводимой терапии иксекизумабом BASDAI 50 достигли 8 (88,9%) и 34 (42%) пациента в нашем и рандомизированном исследованиях соответственно. Более низкие значения BASDAI, возможно, связаны с тем, что несколько пациентов были направлены на таргетную терапию, в первую очередь, в связи с повышением уровня СРБ, который не учитывается в данном индексе, при умеренном значении BASDAI.
Медиана ASDAS до лечения составила 3,7 [2,8; 3,9] балла, в COAST-V среднее значение составило 3,7±0,7 балла, что позволяет говорить о близких показателях в двух исследованиях. В результате проводимой терапии иксекизумабом индекс в среднем снизился на 58,1 [69,6; 30,8] % (p=0,008) в нашем исследовании и на 13,8 [5,2; 22,3] % (р=0,0074) в исследовании COAST-V. Ремиссии (ASDAS менее 1,3) в нашем наблюдении достигли 3 (33,33%) пациента, в COAST-V — 13 (16%) пациентов; низкой активности (ASDAS менее 2,1) — 8 (88,9%) и 35 (43%) больных соответственно. Таким образом, можно говорить о более выраженном снижении индекса ASDAS в нашем наблюдении при близких исходных значениях. Неясно, почему в нашей группе отмечалась более выраженная положительная динамика BASDAI и ASDAS. Из возможных вариантов объяснения можно рассматривать более частое включение фенотипа АС с повышенным уровнем СРБ, который может иметь наилучший ответ на иксекизумаб [17].
Псориатический артрит
С учетом преобладания бионаивных пациентов с ПсА в нашей группе сопоставление проводилось с данными исследования SPIRIT-P1 [18].
Среди наших пациентов с ПсА повышение уровня СРБ отмечалось у 9 (56,25%) из 16. Медиана уровня СРБ до лечения в нашем наблюдении составила 6,4 [3,9; 26,8] мг/л, среднее значение в SPIRIT-P1 — 9,8±13,5 мг/л.
В нашем наблюдении ключевым индексом активности был DAPSA, при этом в рандомизированных исследованиях использовались отдельные показатели активности (число болезненных суставов, энтезитов и т. п.), в связи с чем сопоставление данного показателя на исходном уровне и оценка динамики невозможны. Медиана PASI до лечения составила 13,2 [0,9; 22,8] балла, в SPIRIT-P1 среднее значение — 6,5±6,9 балла, что свидетельствует о более выраженном кожном поражении в нашем наблюдении. PASI 75 и PASI 90 достигли 4 (66,7%) из 6 пациентов, PASI 100 — 2 (33,3%) из 6 больных. В SPIRIT-P1 значения составили 71,0, 58,8 и 48,9% соответственно, однако сопоставление результатов в данном случае невозможно в связи с недостаточным количеством наших наблюдений. Тем не менее, учитывая достаточно выраженный кожный псориаз до старта терапии, у пациентов наблюдался хороший клинический ответ кожного поражения на терапию иксекизумабом.
Отдельно необходимо отметить, что в наше исследование была включена пациентка 64 лет с АС. Несмотря на поздний возраст дебюта АС (около 60 лет), наличие болезни сомнений не вызывало в связи с четким соответствием классификационным критериям. С учетом более высоких рисков, которые могут сопровождать использование таргетных препаратов в старших возрастных группах [19], у данной пациентки проводилось особенно тщательное мониторирование безопасности терапии. Тем не менее побочных эффектов терапии отмечено не было. В целом среди всех наблюдавшихся пациентов тяжелых побочных эффектов не отмечалось. При этом, безусловно, к ограничениям исследования необходимо отнести менее продолжительный (по сравнению с регистрационными исследованиями) период наблюдения и существенно меньшую выборку; также необходимо подчеркнуть, что исходная оценка переносимости препарата у части пациентов была невозможна в связи с инициацией терапии в других центрах.
Заключение
В условиях реальной клинической практики иксекизумаб продемонстрировал эффективность и безопасность при лечении АС и ПсА. Полученные данные не противоречат результатам крупных рандомизированных исследований. К преимуществам наблюдения можно отнести гетерогенность описываемой когорты (в отличие от клинических исследований с четкими критериями набора), в которой у пациентов с различной предшествующей терапией, активностью болезни и широким возрастным диапазоном наблюдается улучшение на фоне лечения иксекизумабом. Малое число пациентов и ограниченная продолжительность наблюдения не позволили в ряде случаев достигнуть статистической значимости динамики и провести сравнительный анализ подгрупп. Тем не менее описываемая когорта является одной из самых больших в России. Для дальнейшего анализа эффективности и безопасности иксекизумаба необходимо увеличение длительности наблюдения за пациентами и объединение с данными других центров.
Сведения об авторах:
Мешков Алексей Дмитриевич — к.м.н., врач-ревматолог, старший научный сотрудник лаборатории заболеваний костно-мышечной системы ОСП РГНКЦ РНИМУ им. Н.И. Пирогова Минздрава России; 129226, Россия, г. Москва, ул. 1-я Леонова, д. 16; ORCID iD 0000-0002-5187-0108.
Остапенко Валентина Сергеевна — к.м.н., врач-гериатр, заведующая отделением гериатрической терапии ОСП РГНКЦ РНИМУ им. Н.И. Пирогова Минздрава России; 129226, Россия, г. Москва, ул. 1-я Леонова, д. 16; доцент кафедры болезней старения РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0003-1222-3351.
Пыхтина Валентина Сергеевна — к.м.н., врач-ревматолог ОСП РГНКЦ РНИМУ им. Н.И. Пирогова Минздрава России; 129226, Россия, г. Москва, ул. 1-я Леонова, д. 16; ORCID iD 0000-0003-0622-1886.
Контактная информация: Мешков Алексей Дмитриевич, e-mail: alexeymeshkov@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 25.01.2023.
Поступила после рецензирования 17.02.2023.
Принята в печать 14.03.2023.
About the authors:
Aleksey D. Meshkov — C. Sc. (Med.), rheumatologist, senior researcher of the Laboratory of Musculoskeletal System Diseases, Autonomous Structural Unit — Russian Gerontology Research and Clinical Center, Pirogov Russian National Research Medical University; 16, 1st Leonov str., Moscow, 129226, Russian Federation; ORCID iD 0000-0002-5187-0108.
Valentina S. Ostapenko — C. Sc. (Med.), geriatrician, Head of the Department of Geriatric Therapy, Autonomous Structural Unit — Russian Gerontology Research and Clinical Center, Pirogov Russian National Research Medical University; 16, 1st Leonov str., Moscow, 129226, Russian Federation; associate professor of the Department of Aging-Associated Diseases, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0003-1222-3351.
Valentina S. Pykhtina — C. Sc. (Med.), rheumatologist, Autonomous Structural Unit — Russian Gerontology Research and Clinical Center, Pirogov Russian National Research Medical University; 16, 1st Leonov str., Moscow, 129226, Russian Federation; ORCID iD 0000-0003-0622-1886.
Contact information: Aleksey D. Meshkov, e-mail: alexeymeshkov@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 25.01.2023.
Revised 17.02.2023.
Accepted 14.03.2023.
Информация с rmj.ru
