Введение
Рост заболеваемости сахарным диабетом (СД) является глобальной проблемой здравоохранения. Согласно отчетам Международной диабетической федерации (IDF) 2017 г. общее количество взрослого населения с СД составляет около 425 млн человек во всем мире, и это число увеличится примерно до 629 млн к 2049 г. [1]. Основной причиной смерти пациентов с СД 2 типа (СД2) служит развитие сердечно-сосудистых заболеваний. Развитие воспаления и фиброза — неотъемлемый компонент неблагоприятного структурного ремоделирования сердечной мышцы у пациентов с СД2. В связи с этим возникает вопрос об оценке фиброзных изменений при СД2 и контроле за их динамикой на фоне терапии. Существуют как инвазивные, так и неинвазивные методики, которые позволяют оценивать накопление фиброзной ткани в миокарде. Кроме того, большое внимание уделяется поиску биомаркеров в крови, которые бы позволяли отслеживать раннюю динамику фиброзных изменений. Среди таких потенциальных маркеров активно изучается роль галектина-3, матриксных металлопротеиназ (MMP), ингибиторов MMP и различных молекул проколлагенов. Галектин-3 относится к семейству бета-галактозидсвязывающих лектинов, он участвует в регуляции процессов пролиферации и дифференцировки клеток, а также клеточной адгезии [2].
В исследованиях было показано, что галектин-3 участвует в патогенезе осложнений диабета и может быть прогностическим маркером при хронической сердечной недостаточности (ХСН) [3]. Мониторинг концентрации коллагена и его пептидов в сыворотке крови и других биологических жидкостях также рассматривается у пациентов с СД2 для оценки процессов фиброза [4]. Так, например, уровень карбокситерминального фрагмента проколлагена I типа (PIСP) ассоциирован с фиброзом миокарда у больных гипертонической болезнью [5] и пациентов с СД2 [6]. Циркулирующие маркеры деградации внеклеточного матрикса, такие как ММР и их тканевые ингибиторы (TIMP), принимают участие в атероматозных изменениях стенки сосудов. Показано, что TIMP-1 и MMP-9 могут быть вовлечены в процессы фиброза [7], а их концентрации значимо повышены у пациентов с СД2 [8]. Кроме того, TIMP-1
играет роль в развитии диастолической дисфункции и гипертрофии левого желудочка путем уменьшения деградации коллагена I типа и увеличения жесткости и массы миокарда [9]. В настоящее время существуют группы сахароснижающих препаратов, которые продемонстрировали положительное влияние на сердечно-сосудистые исходы. Так, представитель группы ингибиторов натрий-глюкозного котранспортера 2 типа (ИНГТ-2) —
эмпаглифлозин снижал сердечно-сосудистую смертность, общую смертность и комбинированную конечную точку MACE (нефатальный инсульт, нефатальный инфаркт, сердечно-сосудистая смертность), по данным исследования EMPAREG-OUTCOME [10]. Однако механизмы снижения сердечно-сосудистой смертности на фоне терапии ИНГТ-2
до сих пор не установлены. В связи с этим представляется актуальной оценка биомаркеров, отражающих патологические процессы в миокарде у пациентов с СД2.
Цель настоящего исследования — оценка динамики биомаркеров фиброза в ходе терапии эмпаглифлозином у пациентов с СД2 и очень высоким риском сердечно-сосудистых событий (ССС).
Материал и методы
В исследование включены 30 пациентов с СД2, которые в течение 24 нед. получали 10 мг/сут эмпаглифлозина. Перед исследованием пациенты подписывали информированное согласие.
Критерии включения
Женщины или мужчины в возрасте от 40 до 70 лет с СД2, гликированным гемоглобином (HbA1c) 7,0–11,0%, стабильной сахароснижающей терапией по крайней мере в течение 12 нед. до включения в исследование, наличием трех сердечно-сосудистых факторов риска (дислипидемия, артериальная гипертензия, ожирение).
Критерии исключения
Ишемическая болезнь сердца, хроническая сердечная недостаточность, уровень NT-proBNP >125 пг/мл, а также наличие другой клинически значимой сердечно-сосудистой патологии, расчетная скорость клубочковой фильтрации (СКФ) в соответствии с CKD-EPI (СКФ<60 мл/мин/1,73 м2), наличие противопоказаний для терапии эмпаглифлозином.
В ходе исследования проводилась оценка таких лабораторных параметров, как гликированный гемоглобин (HbA1c), креатинин с расчетом СКФ, галектин-3, TIMP-1, PICP, MMP-9, ST-2, NT-proBNP, общий холестерин, липопротеины низкой и высокой плотности, триглицериды. Всем пациентам проведена трансторакальная эхокардиография (Эхо-КГ). Лабораторные исследования и Эхо-КГ выполнялись до начала лечения и через 24 нед. терапии эмпаглифлозином. С целью оценки исходных значений биомаркеров фиброза в исследование дополнительно были включены 13 пациентов без СД2, но с наличием трех факторов риска ССС (артериальная гипертензия, ожирение, дислипидемия). Этим пациентам также были выполнены соответствующие лабораторные исследования.
Статистический анализ
Статистический анализ проводился с использованием пакета статистического программного обеспечения SPSS Statistics. Количественные признаки представлены в виде медианы и квартилей — Me (25% квартиль —
75% квартиль), качественные признаки — в виде числа наблюдений и процента (n (%)). Различия между количественными признаками анализировались с использованием критерия Уилкоксона. Для выявления различий между независимыми выборками использовался критерий Манна — Уитни. Корреляционный анализ проводился с использованием рангового коэффициента корреляции Спирмена. Нулевая гипотеза отвергалась при р<0,05.
Результаты
Исходная характеристика пациентов представлена в таблице 1.
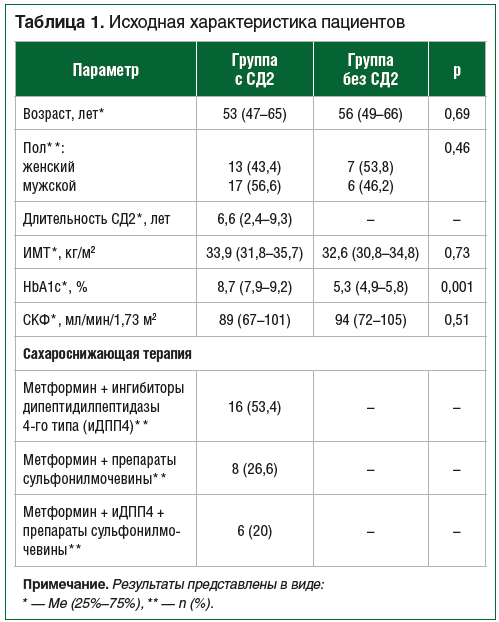
Через 24 нед. от начала лечения наблюдалось значимое снижение уровня HbA1c до 7,7% (7,3–8,0), р=0,0001, и ИМТ до 31,5 кг/м2 (29,8–33,2), р=0,002. По данным
Эхо-КГ: фракция выброса (ФВ) по Симпсону на начало исследования составила 61% (59–65%) и значимо не отличалась через 24 нед. лечения (60% (59–64%), p=0,7.
Пациенты в группах с СД2 и без СД2 значимо не различались по полу, возрасту и ИМТ. При сравнении исходных значений биомаркеров фиброза в этих группах показано, что средняя концентрация MMP-9 была значимо выше в группе СД2 — 580 нг/мл (390–1100) против 350,0 нг/мл (270,0–720,0) в группе без СД2, p=0,01. Кроме того, уровень галектина-3 — 8,9 нг/мл (7,5–10,3) и 5,2 нг/мл (3,5–6,9), р=0,03 и концентрации P1CP — 130,1 нг/мл (99,3–190,2) и 90,3 нг/мл (70,1–99,8), р=0,009, в среднем были значимо выше в группе СД2. Концентрации TIMP-1, NT-proBNP и ST-2 значимо не различались между группами.
Не было получено значимых различий между концентрациями галектина-3 до начала лечения и через 24 нед. терапии эмпаглифлозином: 8,9 нг/мл (7,5–10,3) и 10,1 нг/мл
(6,9–14,1) соответственно (р=0,6), как и между уровнями ST-2: 22,1 нг/мл (16,2–28,6) и 19,4 нг/мл (15,9–23,8) соответственно (p=0,4) и MMP-9: 580 нг/мл (390–1100) и 639,0 нг/мл (330,0–1060,0) соответственно (p=0,5). Наблюдалось значимое снижение концентрации P1CP через 24 нед. лечения по сравнению с исходными значениями — 102,6 нг/мл (87,1–160,2) и 130,1 нг/мл (99,3–190,2) соответственно (р=0,02). Уровень TIMP-1 через 24 нед. лечения значимо не различался по сравнению с исходным: 200 нг/мл (180–220) и 210 нг/мл (175–234) соответственно (р=0,6). Значимых корреляций между биомаркерами фиброза и уровнем HbA1c, длительностью СД2 и возрастом пациентов не получено. Отмечалась значимая положительная корреляция между концентрацией TIMP-1 и ФВ в конце исследования (r=0,699, р=0,008).
Обсуждение
Обширные клинические данные подтверждают наличие фиброза миокарда у пациентов с СД2, развивающегося независимо от артериальной гипертензии и атеросклероза коронарных артерий [11]. Ассоциированный с СД интерстициальный фиброз характеризуется накоплением коллагена I и III типа, затрагивает как левый, так и правый желудочек и описан при обоих типах СД [12]. В нашем исследовании выявлена более высокая концентрация P1CP у пациентов с СД2 по сравнению с контрольной группой. Повышение экспрессии P1CP при гипергликемии было описано в животных моделях [13], а в исследовании у пациентов с СД2 и макроальбуминурией уровень P1CP был значимо выше по сравнению со здоровым контролем [14]. Однако не удалось обнаружить исследований, в которых оценивались бы различия в содержании P1CP у пациентов с СД2 и пациентов без СД2, но с факторами риска сердечно-сосудистых заболеваний. По данным нашего исследования, у пациентов с СД2 также наблюдается значимо более высокий уровень галектина-3. Этот результат соответствует ранее полученным данным в других исследованиях [15]. Например, в проспективном исследовании было показано, что галектин-3 связан с ССС и смертностью от всех причин у пациентов с СД2, и эта взаимосвязь наблюдается у пациентов и без сердечно-сосудистых заболеваний [16]. Повышение MMP-9 у пациентов с СД2 также было описано в предыдущих исследованиях [17], что соотносится с полученными нами результатами. Кроме того, более высокое содержание MMP-9 описано у пациентов с СД2 и диабетической ретинопатией по сравнению с пациентами с СД2, но без ретинопатии в анамнезе, что свидетельствует о вовлечении MMP-9 не только в процессы миокардиального фиброза, но и в патогенез хронических микрососудистых осложнений СД [18]. В настоящем исследовании не было получено значимых различий между группами по уровню NT-proBNP и ST-2, что может отражать отсутствие ХСН в обеих группах, поскольку данные маркеры используются преимущественно в диагностике ХСН. В целом по результатам нашего исследования пациенты с СД2 и факторами риска сердечно-сосудистых заболеваний имеют более высокие концентрации маркеров фиброза. Данная ситуация, в свою очередь, может приводить к снижению желудочковой эластичности и развитию ХСН с сохранной фракцией выброса. Кроме того, связанный с диабетом фиброз предсердий может вызывать фибрилляцию предсердий, ухудшать течение ХСН и увеличивать частоту инсультов. Также фиброзные изменения в желудочках могут быть причиной повышенного риска желудочковых аритмий и внезапной смерти, наблюдаемой у пациентов с СД2 [19–23]. Таким образом, снижение выраженности миокардиального фиброза позволит уменьшить кардиоваскулярную заболеваемость и смертность у пациентов с СД2.
В настоящем исследовании на фоне 24-недельной терапии эмпаглифлозином не было получено значимой динамики биомаркеров фиброза, за исключением снижения уровня P1CP. Хотя в клеточных и животных моделях было продемонстрировано положительное влияние эмпаглифлозина на процессы ремоделирования и фиброзные изменения в миокарде, значимость этих влияний у людей остается малоизученной [24, 25]. Нами не обнаружено исследований, в которых оценивалась бы динамика биомаркеров фиброза у пациентов с СД2 без кардиоваскулярной патологии. Отсутствие значимой динамики биомаркеров фиброза в данной популяции пациентов по результатам нашего исследования может объясняться разными причинами. Во-первых, развитие миокардиального фиброза требует времени, соответственно, и регресс этих изменений представляет собой длительный процесс, а динамика биомаркеров фиброза может отсутствовать за время 24-недельного наблюдения. Во-вторых, небольшое количество пациентов, составивших выборку нашего исследования, может быть недостаточным для выявления значимых изменений в концентрации маркеров. Однако снижение уровня P1CP позволяет предположить, что в дальнейшем стоит ожидать значимых изменений в динамике маркеров фиброза на фоне терапии эмпаглифлозином.
Заключение
Пациенты с СД2 и очень высоким риском ССС имеют значимо более высокие концентрации биомаркеров фиброза по сравнению с пациентами без СД2, но с наличием трех факторов риска ССС (артериальная гипертензия, ожирение, дислипидемия). Терапия эмпаглифлозином в течение 24 нед. не приводит к значимому изменению биомаркеров фиброза, за исключением снижения концентрации PIСP. Требуются дальнейшие исследования с большей длительностью наблюдения для уточнения влияния эмпаглифлозина на процессы фиброза у пациентов с СД2.
Информация с rmj.ru






