Содержание статьи
Оптимизация комбинированной терапии при трудноконтролируемой артериальной гипертензии
Л. И. Маркова*, доктор медицинских наук, профессор
А. Э. Радзевич*, доктор медицинских наук, профессор
А. В. Лазарев*
С. В. Хамандяк*
С. Б. Соломатина**
Е. В. Маркова*
*ГБОУ ВПО МГМСУ Минздравсоцразвития России,
**НУЗ Отделенческая поликлиника на ст. Москва-Курская, Москва
Первостепенной задачей современной антигипертензивной терапии является сокращение числа больных с недостигнутым целевым артериальным давлением (АД), что позволит предотвратить или приостановить развитие сердечно-сосудистых осложнений и значительно улучшить прогноз больных артериальной гипертензией (АГ) [1]. Рациональный подбор комбинации антигипертензивных препаратов (АП) позволяет отчасти решить данную задачу. Однако целевых уровней АД в нашей стране достигают не более 20% больных, что во многом связано с нерациональным выбором лекарственных средств, ошибками в выборе дозирования, недостаточным использованием их приоритетных комбинаций [2]. По данным литературы 15–20% больным АГ требуется назначение трех и более АП, так как прием двух АП не позволяет достичь целевых значений АД [3]. Данный вариант АГ характеризуют как трудноконтролируемую или неконтролируемую [4]. Рациональные комбинации из трех АП были включены в «Рекомендации Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов (ВНОК)», 2010 [1]. Наиболее предпочтительным является сочетание ингибитора ангиотензин-превращающего фермента (ИАПФ) или блокатора рецепторов ангиотензина II (БРА) с тиазидным диуретиком (ТД) и с дигидропиридиновым антагонистом кальция (АК) [5]. Среди представителей БРА заслуживает внимания кандесартан. Рядом исследований доказано, что препарат в достаточной степени обладает органопротективными свойствами (CATCH, 2002; ALPINE, 2003; SCOPE, 2004) [6]. Сравнительно новым представителем АК дигидропиридинового ряда 3-го поколения является лерканидипин. Он отличается хорошими вазоселективными свойствами, не оказывает отрицательного инотропного действия, не вызывает рефлекторной тахикардии [7]. Препарат обладает достаточной безопасностью и низким числом побочных явлений и доказал эффективность как при лечении умеренной, так и выраженной АГ [8]. В большинстве рекомендаций тиазидные диуретики рассматриваются в качестве обязательного компонента лечения АГ. БРА и АК в сочетании с диуретиком потенциируют антигипертензивное действие друг друга и снижают риск таких побочных эффектов, как метаболические нарушения у больных АГ высокого риска [6, 9].
Таким образом, сегодня очевидно, что для значительного улучшения ситуации с трудноконтролируемой АГ необходима оптимизация лекарственной терапии, применение комбинации препаратов с доказанными протективными свойствами.
Цель исследования: оценить влияние трехкомпонентной антигипертензивной терапии кандесартаном в сочетании с гидрохлортиазидом и лерканидипином на суточный профиль АД, структурно-функциональные состояние миокарда и метаболические показатели у больных с трудноконтролируемой АГ.
Материал и методы
В исследование исходно были включены 30 амбулаторных больных с АГ 2–3 степени (по классификации ВНОК, 2010). Средний возраст больных 51,85 ± 5,09 года (66,7% женщин), продолжительность АГ 8,34 ± 3,21 года. У больных были отмечены метаболические нарушения: ожирение — у 20 (66,7%), дислипидемия — у 18 (60%), гиперурикемия — у 8 (26,7%), нарушенная толерантность к глюкозе — у 6 (20%), компенсированный СД — у 4 (13,3%). Кроме того, 12 женщин (60%) находились в состоянии постменопаузы, у 8 (26,7%) больных — длительный стаж курения, у 2 (0,07%) — стенокардия напряжения II функционального класса.
До включения в исследование больные получали комбинированную терапию ИАПФ (эналаприл, фозиноприл) или БРА (лозартан) в сочетании с тиазидным диуретиком, целевых значений АД не достигали.
Исходные клинические показатели артериального давления (АД) у обследуемых больных составили для систолического АД (САД) 174,21 ± 9,56 мм рт. ст. и диастолического АД (ДАД) 106,53 ± 6,31 мм рт. ст., ЧСС 78 ± 8,2 уд./мин.
Критериями включения больных в исследование были метаболические нарушения, гипертрофия левого желудочка (ГЛЖ), уровень САД более 160,0 мм рт. ст. и ДАД — более 90 мм рт. ст. на фоне длительного приема двух АП в максимальных дозах.
В исследование не включали пациентов с симптоматической или злокачественной АГ, с сопутствующими заболеваниями печени, почек, тяжелой эндокринной патологией, а также с сердечно-сосудистыми заболеваниями, требующими дополнительной медикаментозной терапии.
Исследование было открытым, рандомизированным. За 5 дней до исследования отменялись все принимаемые препараты. В случае существенного подъема АД назначались короткодействующие АП.
На старте лечения всем больным был назначен кандесартан 8 мг в сочетании с гидрохлортиазидом 12,5 мг однократно утром. При отсутствии снижения САД на 10% и ДАД на 5% от исходного уровня через 2 недели лечения дозу кандесартана увеличивали до 16 мг в сутки. Через 1 месяц при отсутствии целевых величин АД добавляли лерканидипин в начальной дозе 10 мг однократно утром, максимальная доза — 20 мг в сутки. Наблюдение продолжалось еще 2 месяца. В ходе исследования оценивали общее самочувствие, наличие побочных явлений. Критериями эффективности проводимой трехкомпонентной антигипертензивной терапии считали достижение целевого уровня АД (< 140/90 мм рт. ст.).
Исходно, через 1 и 3 месяца проводили обследование, включающее суточное мониторирование АД (СМАД), ЭхоКГ, лабораторные исследования.
Измерение клинического АД осуществлялось ручным сфигмоманометром по методу Н. С. Короткова в положении сидя трехкратно после 10-минутного отдыха с определением среднего значения.
Суточное мониторирование АД (СМАД) проводили с помощью прибора ABPM-04 (Meditech, Венгрия). При исследовании анализировали: среднесуточные САД и ДАД в мм рт. ст. (САДср.сут, ДАДср.сут), среднедневные и средненочные САД и ДАД в мм рт. ст. (САДср.д, ДАДср.д и САДср.н, ДАДср.н), временной гипертонический индекс (ВГИ) для САД и ДАД среднедневной и средненочной (ВГИ САДд%, ВГИ САДн%, ВГИ ДАДд%, ВГИ ДАДн%), вариабельность дневного и ночного САД, ДАД (Вар.САДд, Вар.САДн, Вар. ДАДд, Вар. ДАДн) [10].
Структурно-функциональное состояние миокарда оценивали методом трансторакальной ЭхоКГ с помощью многофункционального ультразвукового дуплексного сканера Logiq P6 (General Electric Healthcare) по стандартной методике. Рассчитывали следующие показатели: конечный систолический и диастолический размеры и объемы левого желудочка (ЛЖ: КСР, КДР, КСО, КДО), размер левого предсердия (ЛП), фракцию выброса (ФВ) ЛЖ, толщину межжелудочковой перегородки и задней стенки ЛЖ в конце диастолы (ТМЖП, ТЗСЛЖ), индекс массы миокарда ЛЖ (ИММЛЖ), масса миокарда ЛЖ (ММЛЖ) — по формуле R. Devereux. За верхнюю границу нормы ИММЛЖ принимали значения 110 г/м2 для женщин и 125 г/м2 — для мужчин. При исследовании диастолической функции (ДФЛЖ) определяли: Ve, м/с — максимальная скорость раннего диастолического наполнения, Va, м/с — максимальная скорость трансмитрального кровотока во время систолы левого предсердия, Ve/Va — отношение максимальных скоростей потоков ЛЖ, IVRT, мс — время изоволюметрического расслабления ЛЖ, DT, мс — время замедления раннего диастолического наполнения.
Лабораторные исследования включали определение в крови общего холестерина (ХС), триглицериды (ТГ), липопротеиды высокой плотности (ЛПВП), липопротеиды низкой плотности (ЛПНП), индекса атерогенности, уровня глюкозы и мочевой кислоты.
Результаты обрабатывали с помощью стандартного пакета программ STATISTICA 6.0, рассчитывали средние величины, стандартные отклонения, применяли критерий значимости. Различия считали достоверными при р < 0,05, высокодостоверными при p < 0,001.
Результаты и обсуждение
Исследование завершили 24 пациента (17 женщин, 7 мужчин). Отмечена хорошая переносимость препаратов у подавляющего числа пациентов. Через 2 недели от начала терапии увеличение дозы кандесартана до 16 мг в сутки потребовалось всем больным. Двое из них выбыли из исследования, так как к концу месяца был достигнут целевой уровень АД. Остальным 28 пациентам к терапии был добавлен лерканидипин в суточной дозе 10 мг однократно. Увеличение дозы лерканидипина до 20 мг в сутки потребовалось 15 больным.
Через 2 месяца из исследования были исключены еще 4 человека: у 2 пациентов сохранялся отек голеней, диспепсические явления; 2 — не соблюдали протокол исследования. Данные этих пациентов не учитывались в статистическом анализе.
На фоне терапии кандесартаном и гидрохлортиазидом через месяц отмечено снижение клинических САД и ДАД на 10% и 5% соответственно от исходного уровня, целевых значений АД больные не достигли. Исходно при анализе результатов СМАД выявлено повышение всех показателей, отражающих прессорную нагрузку на АД за сутки, день и ночь (табл. 1). Отмечался высокий уровень вариабельности АД, показателей «нагрузки давлением», что является фактором риска развития ассоциированных клинических состояний. Отмечена тенденция к снижению среднесуточных, среднедневных, средненочных показателей САД и ДАД, а также статистически значимое уменьшение времени нагрузки давлением в течение дневного периода для САД и на протяжении суток для ДАД (табл. 1). Вариабельность САД и ДАД достигла достоверных значений преимущественно в ночной период (р < 0,05).
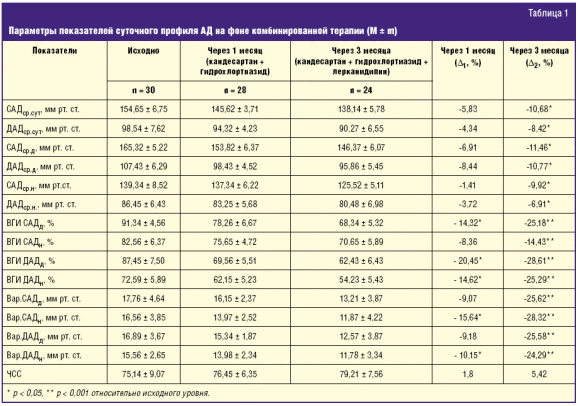
Аналогичные результаты демонстрирует исследование, в котором на фоне терапии кандесартаном в сочетании гидрохлортиазидом у больных АГ отмечена положительная динамика показателей суточного профиля АД преимущественно в ночное время [11]. ЧСС за этот период существенно не изменилась.
К концу третьего месяца на фоне трехкомпонентной терапии целевых значений клинического АД достигли 86% больных. Среднесуточные показатели САД и ДАД (табл. 1) достигли нормативных значений (р < 0,05), что подтверждает необходимость применения у данной категории больных трехкомпонентной схемы лечения [9, 11]. Снижение САД в дневное и ночное время суток было более выраженным (р < 0,05), по сравнению с ДАД в этот же период (р < 0,05), что связано с включением в терапию кандесартана, гидрохлортиазида и лерканидипина. Высокодостоверная динамика отмечена в показателях вариабельности САД и ДАД. На протяжении суток, в дневные и ночные часы данный показатель практически достиг нормативных значений, что согласуется с рекомендациями ряда экспертов [10]. ЧСС на фоне терапии несущественно увеличилась.
Таким образом, терапия кандесартаном в сочетании с гидрохлортиазидом и лерканидипином корригирует исходно нарушенные показатели суточного профиля АД у больных с трудноконтролируемой АГ.
У включенных в исследование больных исходно отмечалось увеличение объемных показателей и размеров ЛЖ. Размер левого предсердия составил 4,23 ± 0,52 см, что обусловило включение в исследование пациентов с ассоциированными клиническими проявлениями (ишемическая болезнь сердца). У всех больных была выявлена ГЛЖ, которая характеризовалась увеличением стенок ЛЖ и, соответственно, ММЛЖ с его диастолической дисфункцией (табл. 2).
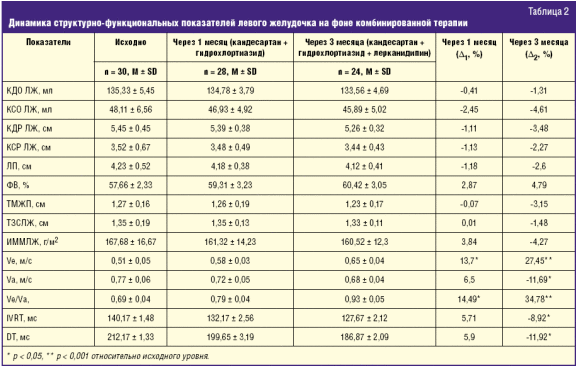
Через 1 месяц лечения наметилась тенденция к улучшению структурно-функциональных показателей левого желудочка (табл. 2). Выявленное достоверное увеличение показателя диастолической функции ЛЖ — Ve/Va на 14,49% (р < 0,05) обусловлено перестройкой структуры диастолического наполнения ЛЖ — увеличением скорости раннего диастолического наполнения на 13,7% (р < 0,05).
Через 3 месяца на фоне трехкомпонентной терапии констатирована более выраженная тенденция к снижению показателей, отражающих размеры и объемы ЛЖ, что связано с уменьшением прессорной нагрузки АД на ЛЖ. ИММЛЖ снизился на 4,27% (р > 0,05) за счет уменьшения ТМЖП, ТЗСЛЖ и КДР. Полученные результаты согласуются с данными крупного метаанализа, где показано, что сартаны и антагонисты кальция обладают достаточным кардиопротективным эффектом, обусловленным их способностью вызывать регресс ГЛЖ и улучшать диастолическую функцию ЛЖ [12, 13].
К концу исследования выявлено еще более выраженное улучшение диастолической функции ЛЖ, что проявилось достоверным увеличением таких показателей, как Ve, на 27,45% (р < 0,001), снижением IVRT на 8,92% (р < 0,05) и DT на 11,92% (р < 0,05).
Таким образом, результаты исследования продемонстрировали, что сочетанное применение кандесартана с гидрохлортиазидом и лерканидипином усиливает кардиопротективный эффект каждого из препаратов, что проявляется улучшением диастолической функции и тенденцией к снижению ИММЛЖ в более короткие сроки. Оптимизация комбинированной терапии позволяет перевести больных из группы трудноконтролируемой АГ в разряд контролируемой АГ.

В исходном состоянии у включенных в исследование больных отмечались метаболические нарушения (табл. 3). Через 1 месяц терапии кандесартаном в сочетании с гидрохлортиазидом отмечена тенденция к улучшению показателей липидного профиля, глюкозы крови и уровня мочевой кислоты. К концу исследования достоверно снизился уровень триглицеридов и мочевой кислоты. В работе Nishida Y. (2011) кандесартан продемонстрировал улучшение липидного спектра с более значимым снижением уровня триглицеридов у больных АГ [14]. В 2012 г. итальянские авторы констатировали положительные метаболические эффекты сочетанной терапии лерканидипином с БРА [15].
Таким образом, проводимая терапия кандесартаном в сочетании с гидрохлортиазидом и лерканидипином у больных с трудноконтролируемой АГ корригирует исходно нарушенные в крови показатели липидного спектра, глюкозы и мочевой кислоты.
Выводы
- Терапия кандесартаном в сочетании с гидрохлортиазидом и лерканидипином нормализует нарушенный суточный профиль артериального давления у больных с трудноконтролируемой артериальной гипертензией и позволяет достигнуть целевых значений артериального давления у 86% больных.
- Трехкомпонентная терапия кандесартаном, гидрохлортиазидом, лерканидипином у больных с трудноконтролируемой артериальной гипертензией оказывает кардиопротективное действие в течение трехмесячной терапии.
- При лечении больных с трудноконтролируемой артериальной гипертензией кандесартаном в сочетании с гидрохлортиазидом и лерканидипином отмечено положительное влияние на исходно нарушенные метаболические показатели крови.
Литература
- Чазова И. Е., Ратова Л. Г., Бойцов С. А. Диагностика и лечение артериальной гипертензии (Рекомендации Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов) // Системные гипертензии. 2010. № 3. С. 5–27.
- Шальнова С. А., Баланова Ю. А., Константинов В. В. и др. Артериальная гипертензия: распространенность, осведомленность, прием антигипертензивных препаратов и эффективность лечения среди населения Российской Федерации // Российский кардиологический журнал. 2006. № 4. С. 45–50.
- Pessina A., Rossi G. Uncontrolled hypertention: highlits and perspectives from the European Society of Hypertention Satellite Symposium // Exp. review of Cardiovasc. Therapy. 2011. Vol. 9, № 12. P. 1515–1518.
- Чазова И. Е., Фомин В. В., Разуваева М. А., Вигдорчик А. В. Эпидемиологическая характеристика резистентной и неконтролируемой артериальной гипертензии в Российской Федерации (Российский регистр неконтролируемой и резистентной артериальной гипертензии РЕГАТА-ПРИМА «РЕзистентная Гипертония АрТериАльная — ПРичины И Механизмы рАзвития») // Системные гипертензии. 2010. № 3. С. 34–42.
- Остроумова О. Д., Максимов М. Л. Комбинированная антигипертензивная терапия: первая тройная фиксированная комбинация // Consilium medicum. 2011. № 10. С. 6–10.
- Николаев Н. А. Инновационная антигипертензивная терапия в свете завершенных научных исследований // Рациональная фармакотерапия в кардиологии. 2009. № 2. С. 89–97.
- Borghi C. Lercanidipine in Hypertension // Vasc. Health Risk Manag. 2005. Vol. 1 (3). Р. 173–182.
- Barrios V., Navarro A., Esteras A. et. al Antihypertensive efficacy and tolerability of lercanidipine in daily clinical practice. The ELYPSE Study // Blood Press. 2002. Vol. 11 (2). P. 95–100.
- Calhoun D. A., Jones D., Textor S. et al. Resistant hypertension: diagnosis, evaluation, and treatment. A scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research // Hypertension. 2008. Vol. 51 (6). P. 1403–1419.
- Рогоза А. Н., Агальцов М. В., Сергеева М. В. Суточное мониторирование артериального давления: варианты врачебных заключений и комментарии. Нижний Новгород: ДЕКОМ, 2005. C. 64.
- Кобалава Ж. Д., Котовская Ю. В., Троицкая Е. А. Место трехкомпонентной терапии в лечении артериальной гипертонии: эффективность комбинации амлодипин/валсартан/гидрохлоротиазид // Русский медицинский журнал. 2011. T. 4: 271.
- Klingbeil A., Schneider M., Martus P. et al. A meta4 analysis of the effects of treatment on left ventricular mass in essential hypertension // Am J Med. 2003. Vol. 115, № 1. P. 41–46.
- Агеев Ф. Т., Сербул В. М., Овчинников А. Г. Влияние ингибитора АПФ эналаприла и антагониста рецепторов к А-II кандесартана, а также их комбинации на индекс массы миокарда ЛЖ у пациентов с гипертонической гипертрофией ЛЖ // Сердечная недостаточность. 2007. T. 8. C. 60–8.
- Nishida Y., Takahashi Y., Nakayama T. Comparative effect of olmesartan and candesartan on lipid metabolism and renal function in patients with hypertension: a retrospective observational study // Cardiovasc Diabetol. 2011, Aug 10. 10: 74.
- Чичеро А. Ф., Герокарни Б., Ростиччи М. и др. Антигипертензивные и метаболические эффекты комбинации лерканидипина с различными антигипертензивными препаратами в условиях повседневной клинической практики // Кардиоваскулярная терапия и профилактика. 2012. № 1. С. 36–40.
Статья опубликована в журнале Лечащий Врач
материал MedLinks.ru






