Роль эндоскопии с комбинированной хромоскопией в диагностике пищевода Барретта
Н.В. Корочанская1,2, В.М. Дурлештер1,2, С.А. Габриэль2, Р.М. Тлехурай2, В.В. Рябчун2, Н.Е. Шабанова2, Т.М. Семенихина3 , С.С. Хусаинова2
1 — Кафедра хирургии № 1 ФПК и ППС КГМУ, Россия, 350008, г. Краснодар, ул. Седина 4;
2 — МУЗ городская больница № 2 «КМЛДО», Россия, 350012, г. Краснодар, ул. Красных партизан, 6/2;
3 — больница скорой медицинской помощи, Россия, 350042, г. Краснодар, ул. 40-летия Победы, 14. E-mail: Nshabanova1980@mail.ru
В статье приведены собственные данные эндоскопического обследования больных с длительным анамнезом гастроэзофагеальной рефлюксной болезни и наличием пищевода Барретта (ПБ). Для уточнения диагностики ПБ использовали комбинированную хромоскопию по оригинальной методике. Продемонстрировано, что эндоскопия является основным методом диагностики ПБ (чувствительность — от 85 до 90%), позволяющим получить материал для гистологического исследования. Использование прижизненной окраски витальными красителями слизистой пищевода повышает качество диагностики данного заболевания.
Ключевые слова: гастроэзофагеальная рефлюксная болезнь, пищевод Барретта, аденокарцинома пищевода, эндоскопия с хромоскопией.
За последние 20 лет в РФ и во всем мире отмечен достоверный рост аденокарциномы пищевода (АКП). Около 95% случаев АКП регистрируется у больных с ПБ. Частота ее развития у таких пациентов возрастает до 800 случаев на 100 000 населения в год [3, 7]. ПБ является грозным осложнением гастроэзофагеальной рефлюксной болезни (ГЭРБ), характеризуется замещением плоскоклеточного эпителия цилиндрическим в виде специализированной кишечной метаплазии в пределах пищевода. ПБ рассматривается мировым сообществом гастроэнтерологов как предраковое состояние [1, 6].
Современные эндоскопические технологии облегчают диагностику пищевода Барретта. К ним относятся: флюоресцентная эндоскопия, технологии NBI — с высоким разрешением и увеличением; ультразвуковое эндоскопическое исследование [2]. Большим прогрессом в эндоскопии стало создание методики с использованием витальных красителей (метиленового синего, раствора Люголя, конго красного, индигокармина), которые применяются для более точной диагностики ранних форм рака и предраковых заболеваний, изучения топографии функциональных и органических поражений, осуществления контроля за эффективностью лечения [5].
Цель работы — оценить значение комбинированной хромоскопии в диагностике ПБ.
Материалы и методы
Обобщены результаты обследования 97 пациентов, находившихся на лечении в МУЗ «Городская больница № 2 «КМЛДО» с 2007 по 2009 г. и имеющих в анамнезе ГЭРБ длительностью более 5 лет. Из них 41 женщина и 56 мужчин в возрасте от 18 до 70 лет. Всем больным провели комплекс диагностических исследований, включавший: стандартную эндоскопию (видеоинформационная система с цифровым анализатором изображения фирмы «Olympus» Evis Exera GIF—150, Япония) с хромоскопией и последующей биопсией слизистой оболочки (СО) пищевода, полипозиционное рентгенологическое исследование, суточное рН-мониторирование с помощью прибора «Гастроскан 24» (фирмы «Исток-система», г. Фрязино) с использованием стандартных зондов с 3 сурьмяными электродами и накожным хлорсеребряным электродом сравнения. В своей работе мы впервые использовали комбинированную хромоскопию (приоритетная справка № 2009120040 от 26.05.2009 г.) растворами Люголя 1%-ного и метиленового синего 1%-ного во время эндоскопии с целью улучшения визуализации патологических изменений СО. Первым наносили раствор Люголя, неизмененный эпителий приобретал темный коричневый цвет, и четко визуализировались края пораженной СО пищевода. Вторым красителем наносили метиленовый синий. Очаги метаплазии окрашивались в темный сине-коричневый цвет, а неизмененная СО приобретала светлый сине-коричневый цвет. После комбинированной окраски визуализировались участки слизистой с неровными краями по типу языков пламени, как правило, не возвышающиеся над поверхностью, из маркированных при хромоскопии участков брали биопсию для морфологической верификации диагноза. Границы и протяженность очагов цилиндроклеточной метаплазии дистального отдела пищевода мы оценивали на основании Пражских критериев, разработанных Международной рабочей группой экспертов по классификации эзофагитов на 12-й Европейской гастроэнтерологической неделе в 2004 году [4]. Всем пациентам проводили консервативную терапию ингибиторами протонной помпы в средних терапевтических дозах (омепразол или его аналоги 40 мг в сутки — 4 недели при неэрозивной ГЭРБ, 8 недель при эрозивно-язвенной форме, далее поддерживающая терапия 20 мг в сутки), курсовой прием в течение 3 недель прокинетиков (домперидон по 30-40 мг в сутки), а также антациды по требованию. Через 2 месяца после проведения медикаментозного лечения пациентам с ПБ повторяли эндоскопическое исследование с комбинированной хромоскопией и биопсией.
Результаты и обсуждение
По данным морфологического исследования наличие метаплазии подтвердилось у 21 пациента, что составило 21,6% от общего количества обследованных больных ГЭРБ.
Из них 6 женщин и 15 мужчин в возрасте от 18 до 70 лет. Результаты патогистологического исследования СО представлены в таблице 1.
Таблица 1. Морфологические изменения слизистой оболочки пищевода у пациентов с пищеводом Барретта (n=21)
| Патогистологическое исследование (ПГИ) слизистой пищевода | Количество случаев, чел. (%) |
| Желудочная метаплазия | 7 (33,33) |
|
Кишечная метаплазия |
9 (42,86) |
|
Желудочно-кишечная метаплазия |
5 (23,81) |
На рисунке 1 показана нативная картина ПБ: визуализируется ярко-красный участок слизистой на уровне Z-линии.
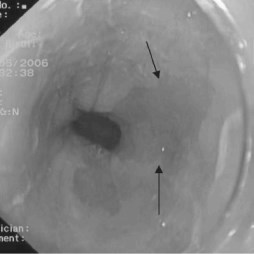
Рис. 1. ФГДС. Визуализируется ярко-красный участок слизистой на уровне Z-линии
Нами выявлены следующие типы протяженности ПБ: ультракороткий сегмент до 1 см — 8 случаев, из них одна желудочная, пять — желудочно-кишечных и две — кишечные метаплазии; коротких сегментов от 1 до 3 см — 11 соответственно, из них 4 — желудочные, 4 — желудочно-кишечные и 3 — кишечные метаплазии; длинных два сегмента с желудочной метаплазией.
В связи с отсутствием референтного метода невозможно просчитать чувствительность и специфичность предложенной нами методики диагностики ПБ.
На фоне консервативной терапии отмечено обратное развитие воспалительных изменений СО пищевода, в то время как очаги метаплазии остались без динамики, что повлияло на улучшение качества выявления ПБ. Проведение комбинированной хромоскопии после медикаментозного лечения позволило более качественно провести биопсию с последующей морфологической верификацией диагноза. Все пациенты с ПБ продолжили терапию ингибиторами протонной помпы в поддерживающих дозах.
Комбинированная хромоскопия представлена на рисунке 2, очаг метаплазии и его границы визуализируются более четко.
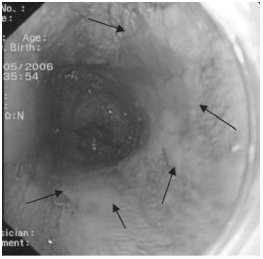
Рис. 2. Комбинированная хромоскопия раствором Люголя и метиленового синего. Очаг прокрашенной слизистой с усиленной рельефностью
Показатели суточной рН-метрии представлены в таблице 2. Среднее значение рН было незначительно ниже нормы за счет наличия патологических рефлюксов. У пациентов с ПБ % общего времени с рН<4 практически в 1,5 раза превосходил нормы. Число продолжительных рефлюксов больше 5 мин и индекс De Meester были выше нормы. Время наибольшей продолжительности рефлюкса почти в два раза выше нормальных значений.
Таблица 2. Показатели суточной рН-метрии у больных с ГЭРБ, осложненной пищеводом Барретта
| Показатели рН-метрии | Средние значения | Норма |
|
Среднее значение рН |
5,9 ± 0,3 | 6,00-8,00 |
|
% общего времени с рН<4 |
7,0 ± 6,5 | < 4,50 |
|
Число продолжительных рефлюксов > 5 мин (рефл./сут.) |
4,0 ± 4,5 | < 3,50 |
|
Наибольшая продолжительность рефлюкса (мин) |
15,51 ± 12,9 | < 9,20 |
|
Индекс De Meester |
15,27 ± 12,4 | < 14,72 |
Примечание: норма цитируется по А. А. Ильченко и Э. Я. Селезневой, 2001.
Использование во время эндоскопического исследования комбинированной хромоскопии позволяет выявить границы очагов метаплазии для проведения прицельной биопсии с последующей морфологической верификацией диагноза. Проведение консервативной терапии у пациентов с длительным анамнезом ГЭРБ способствует исчезновению воспалительных изменений эрозивного характера, но при этом очаги метаплазии СО при повторных эндоскопиях более четко визуализируются, что улучшает качество хромоскопии с последующей биопсией.
ЛИТЕРАТУРА
1. Годжелло Э. А. Пищевод Барретта: эндоскопическая диагностика, стратегия наблюдения и лечения // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2002. — Т. XII. № 3. — С. 67-71.
2. Давыдов М. И., Стилиди И. С. Рак пищевода.-3-е изд., испр. и доп. — М.: изд. группа РОНЦ, Практическая медицина, 2007. -С. 392.
3. Ивашкин В. Т., Трухманов А. С. Программное лечение гастроэзофагеальной рефлюксной болезни в повседневной практике врача // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2003.- № 6. — С. 18-26.
4. Кашин С. В., Иванников И. О. Пищевод Барретта: принципы эндоскопической диагностики и медикаментозной терапии // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2006. — Т. XVI. № 6. — С. 73-78.
5. Савельев В. С, Исаков Ю. Ф., Лопаткин Н. А. и др. Руководство по клинической эндоскопии / Под ред. В. С. Савельева, В. М. Буянова, Г. И. Лукомского — М.: Медицина. -1985. — С. 544.
6. Falk G. W. Gastroesophageal refux disease and Barrett’s esophagus // Endoscopy. — 2001. -Vol. 33. № 2. — P. 109-118.
7. Lagergren J. Adenocarcinoma of oesophagus: what exactly is the size of the problem and who is at risk? // Gut. — 2005. — V. 54. -P. 11-15.
Статья опубликована на сайте http://www.gastroscan.ru
материал с сайта MedLinks.ru







