Содержание статьи
Введение
Во всем мире ежегодно более 2 млн молодых людей страдают от ишемических инсультов (ИИ) [1, 2]. Инсульт у молодых (от 18 до 50 лет) людей составляет примерно 10–14% всех ИИ в странах с высоким уровнем дохода [3, 4]. Инсульты в молодом возрасте связаны с высокой ранней смертностью [5] и инвалидностью [6] и для взрослых трудоспособного возраста имеют особенно большое экономическое значение [7].
Согласно классификации TOAST (Trial of Org 10172 in Acute Stroke Treatment) [8] выделяют несколько патогенетических подтипов ИИ. Лакунарный инсульт (ЛИ), вследствие окклюзии мелких сосудов составляет четверть всех ИИ [9]. Развитие ЛИ связано с окклюзирующим поражением одной из перфорантных артерий. Эти окклюзии развиваются в результате деструкции микрососудов (липогиалиноз или артериолосклероз) или на фоне локального атеросклеротического процесса [10]. G. Lammie et al. [11] представили данные патоморфологического исследования 70 препаратов головного мозга с верифицированной микроангиопатией перфорантных артерий, в которых морфологические изменения были одинаковыми в виде концентрических гиалиновых утолщений стенок малых сосудов с одновременным сужением их просвета (липогиалиноз). В настоящее время, согласно классификации (критериям) TOAST, к ЛИ относят ИИ, имеющие следующие характеристики: один из классических лакунарных синдромов и отсутствие симптомов поражения коры головного мозга; сахарный диабет (СД) или артериальная гипертензия (АГ) в анамнезе свидетельствуют в пользу диагноза; очаги поражения в стволе или подкорковом веществе диаметром <1,5 см или отсутствие изменений при компьютерной томографии (КТ) / магнитно-резонансной томографии (МРТ); отсутствие критериев инсульта вследствие поражения крупных сосудов или кардиоэмболии [8].
В странах Европы, по данным различных исследований, частота ЛИ у лиц молодого возраста варьирует от 3–5 до 16–22% [12–17]. По нашим данным, среди 145 мужчин и женщин в возрасте 18–45 лет ЛИ встречался у 24% [18].
Цель исследования: оценить основные факторы риска, особенности течения инсульта и состояние эндотелиальной функции у мужчин молодого возраста (18–50 лет) с ЛИ.
Материал и методы
Проведено клинико-инструментальное исследование 46 мужчин молодого возраста с ЛИ. Для оценки выраженности клинических симптомов и тяжести ИИ использовались общепринятые шкалы: National Institute of Health Stroke Scale (NIHSS), модифицированная шкала Рэнкина и индекс мобильности Ривермид [19–21].
Критерии включения в исследование: мужчины в возрасте 18–50 лет, поступившие в региональный сосудистый центр с диагнозом «острое нарушение мозгового кровообращения по ишемическому типу, лакунарный подтип»; наличие добровольного информированного согласия на участие в исследовании.
Из факторов риска анализировались наличие АГ, ишемической болезни сердца, инфаркта миокарда в анамнезе, острого нарушения мозгового кровообращения в анамнезе, курение (длительность и количество выкуриваемых сигарет в день), СД, дислипидемия, регулярное употребление алкоголя, в том числе накануне развития инсульта.
Дислипидемия определялась, когда в сыворотке крови натощак выявлялись уровень триглицеридов более 1,7 ммоль/л и уровень липопротеинов низкой плотности (ЛПНП) более 3,4 ммоль/л [22].
Всем пациентам при поступлении проведены КТ головного мозга, при необходимости — МРТ, ультразвуковое исследование и дуплексное сканирование сосудов шеи и головы, ЭКГ, эхокардиоскопия, биохимическое исследование крови, исследование крови на липидный спектр, коагулограмма, анализ крови на ВИЧ, сифилис, ревмопробы.
Для оценки сосудодвигательной функции эндотелия использовалась ультразвуковая манжеточная проба (МП) по методике D.S. Celermajer et al. [23] с исследованием потокозависимой вазодилатации плечевой артерии (ПА) (эндотелий-опосредованная реакция). Потокозависимая дилатация ПА рассчитывалась как отношение изменения диаметра ПА в течение реактивной гиперемии (dmax) к диаметру ПА в исходном состоянии (dисх), выраженному в процентах [24]. Нормальной реакцией ПА в пробе с реактивной гиперемией считается ее дилатация более чем на 10% от исходного диаметра, а вазодилатация менее 10% или вазоконстрикция рассматриваются как патологические состояния [25, 26].
Исследование одобрено локальным этическим комитетом ФГБОУ ВО ЯГМУ Минздрава России (протокол № 26 от 11.10.2018) и проведено с соблюдением международных стандартов и биоэтических норм.
Статистический анализ полученных данных осуществляли с использованием программы Statistica 10.0 (StatSoft Inc., США), методов описательной статистики. Данные по группам представлены в виде среднего (М) ± стандартное отклонение (δ) в выборке для количественных переменных, а в выборке для качественных переменных указывались абсолютное значение и частота встречаемости (%).
Результаты исследования
В исследование было включено 46 мужчин в возрасте от 22 до 50 лет (средний возраст 41,4±6,4 года) с ЛИ, среди которых с первичным инсультом было 38 (82,6%) больных, с повторным — 8 (17,4%). Средний возраст при первичном инсульте составил 41,1±6,4 года, при повторном — 43,3±5,3 года. В группе в целом ИИ в 63% случаев развивался в бассейнах левой или правой средних мозговых артерий, в 26,1% — в бассейне задней мозговой артерии, в 6,5% — в бассейне передней мозговой артерии и в 4,4% — в вертебрально-базилярной системе. На момент поступления в среднем степень выраженности неврологических изменений по шкале NIHSS у пациентов составила 4,85±2,5 балла; средний балл по шкале Рэнкина, оценивающий степень инвалидизации после инсульта, составил 3,7±0,83; среднее значение индекса мобильности Ривермид — 3,88±3,74 балла.
Основными факторами риска у пациентов с ЛИ были АГ (n=45, 97,8%), при этом регулярно принимали антигипертензивные средства 7 (15,6%) пациентов. Другие факторы риска включали курение (67,4%), дислипидемию (41,3%), ожирение (8,7%) и СД 1 типа (2,2%, n=1) и 2 типа (4,3%, n=2). Атеросклеротическое поражение магистральных артерий головы (МАГ) встречалось у 56,5% больных. Сочетание АГ и курения отмечалось в 67,4% случаев, сочетание АГ, курения и регулярного употребления алкоголя — в 17,4% случаев. Оба пациента с СД 2 типа имели АГ (регулярно принимали антигипертензивные препараты) и были курильщиками. Пациент с СД 1 типа не курил, не употреблял алкоголь и не имел АГ.
Атеросклеротическое поражение сонных артерий локализовалось преимущественно в области бифуркации общей сонной артерии (ОСА) с переходом на устья внутренней сонной артерии (ВСА), дистальные отделы при этом оставались проходимыми. Атеросклеротические бляшки в области бифуркации ОСА справа выявлялись у 12 (46,2%) пациентов, слева — у 11 (42,3%), при этом у 8 больных они были двусторонними. Степень стеноза варьировала от 45 до 80%. В группе в целом стенозы ОСА и ВСА встречались в 39,1% случаев. Среди пациентов со стенозами изолированные стенозы ОСА отмечались в 22,2% случаев (от 20 до 35%), стенозы ВСА — в 50% (от 20 до 40%), а сочетанные стенозы в бассейнах ОСА и ВСА — в 33,3% (от 25 до 60%) случаев.
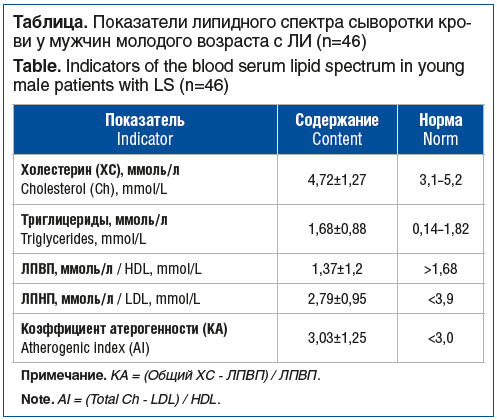
Средняя величина комплекса интима-медиа в ОСА составила 1,01+0,33 мм. По данным эхокардиоскопии уплотнение аорты регистрировалось у 25 (54,3%) больных. Показатели липидного спектра сыворотки крови представлены в таблице.
«Острые» очаги инфаркта головного мозга <1,5 см на момент поступления по данным КТ/МРТ выявлялись у всех (100%) пациентов: корково-подкорковая локализация была у 84,8%, корковая — у 8,7%, стволовая — у 4,3% и в области мозжечка — у 2,2%.
При рассмотрении отдельно подгруппы с повторным ИИ оказалось, что средний возраст этих пациентов составил 43,3±5,3 года и они были старше пациентов с первичным инсультом. Все эти пациенты имели АГ и регулярно принимали антигипертензивные препараты, курили от 10 до 40 сигарет в день, трое (37,5%) из них регулярно употребляли алкоголь. На момент поступления у пациентов с повторными ИИ средняя степень выраженности неврологических изменений по шкале NIHSS была выше — 6±3,7 балла, отражая большую тяжесть неврологических симптомов, чем при первичном инсульте (4,7 балла); также был выше средний балл по шкале Рэнкина — 4±0,87 (при первичном — 3,6±0,81) и средний индекс мобильности Ривермид составил 3,1±3,3 балла (при первичном — 4,03±3,4).
При проведении ультразвуковой МП исходная скорость (Vисх) по ПА у пациентов с ЛИ составила 64±0,4 см/с, исходный диаметр (dисх) ПА — 4,47±0,26 мм. После МП Vmax по ПА у пациентов с ЛИ составила 157±2,3 см/с, dmax ПА — 4,85±0,33 мм. Значения Vmax по ПА выросли в среднем на 146,2±27,6%. Степень максимального расширения ПА после МП у пациентов с ИИ составила 8,47±3,59%. Нормальной реакцией считалась дилатация ПА на фоне реактивной гиперемии более чем на 10% от исходного диаметра, недостаточная вазодилатация регистрировалась при приросте диаметра от 3 до 10%, вазоконстрикция — при приросте менее 2,9% [23, 27]. Среди пациентов с ЛИ нормальная реакция ПА в пробе с реактивной гиперемией с ее дилатацией более чем на 10% от исходного диаметра выявлялась в 41,1% (n=14) случаев, вазодилатация менее 10% — в 47,1% (n=16) и вазоконстрикция — в 11,8% (n=4) случаев. Ультразвуковая МП выявила нарушение в виде снижения вазомоторной реактивности у 20 (58,8%) из 34 обследованных.
Обсуждение
Инсульт является второй по частоте причиной смерти в возрасте старше 60 лет и пятой — среди лиц в возрасте от 15 до 59 лет, согласно данным Всемирной организации здравоохранения [28]. За последние 2–3 десятилетия заболеваемость ИИ возросла во всем мире. Наиболее часто используемый возрастной диапазон определения инсульта в молодом возрасте составляет 18–49 лет [29]. Возросла частота инсульта у молодых пациентов [30]. По данным Датского национального регистра пациентов, частота первичных госпитализаций по поводу ИИ и транзиторной ишемической атаки у молодых людей значительно возросла с середины 1990-х годов, в то время как частота госпитализаций по поводу внутримозгового кровоизлияния и субарахноидального кровоизлияния остается стабильной [31]. Наблюдается преобладание мужчин с данной патологией, хотя чаще встречается у женщин моложе 30 лет [3, 14].
Большая часть данных литературы указывает на то, что традиционные факторы риска — АГ, СД и дислипидемия по-прежнему являются наиболее распространенными, причем АГ занимает первое место. Другие факторы риска среди молодых людей с ИИ включают курение, чрезмерное употребление алкоголя, употребление наркотиков, использование оральных контрацептивов и мигрень [32].
По полученным результатам, в нашем исследовании средний возраст пациентов с ЛИ с первичным инсультом составил 41,1±6,4 года, с повторным — 43,3±5,3 года, что согласуется с данными других исследований [33, 34].
Среди обследованных пациентов основными факторами риска были АГ (97,8%), курение (67,4%), дислипидемия (41,3%) и ожирение (8,7%). При этом сочетание АГ и курения отмечалось в 67,4% случаев, сочетание АГ, курения и регулярного употребления алкоголя — в 17,4% случаев. Атеросклеротическое поражение МАГ встречалось в 56,5% случаев. В 22,2% случаев наблюдались изолированные стенозы ОСА, степень которых варьировала от 20 до 35%, в 50% — стенозы ВСА (от 20 до 40%) и в 33,3% — сочетанные стенозы в бассейнах ОСА и ВСА (от 25 до 60%). Эти результаты сопоставимы с данными других исследований [3, 30, 35, 36–38]. В недавно опубликованном исследовании A. Schwarzwald et al. [39] показано, что среди 689 пациентов 16–55 лет без учета подтипа ИИ у мужчин (они составили 60,8%) были более распространены следующие модифицируемые факторы риска: дислипидемия (57,9%), курение (45,0%), избыточная масса тела (40,3%). По данным R. Renna et al. [33], все пациенты молодого возраста с ЛИ страдали АГ и большинство из них имели дополнительные факторы риска. Также отмечено, что частота АГ, СД и дислипидемии увеличивалась с возрастом [34]. В некоторых сериях у молодых пациентов с ИИ употребление алкоголя было описано как один из основных факторов риска [13, 16, 40, 41], как и в нашем исследовании.
Недавняя работа в области ЛИ, связанного с окклюзией мелких сосудов, была сосредоточена на выяснении двух патогенетических механизмов: эндотелиальной дисфункции и нарушения гематоэнцефалического барьера [42], при этом эндотелиальная дисфункция может быть наиболее важной для развития ЛИ. Эндотелий регулирует тонус сосудов, фибринолиз/коагуляцию, участвует в воспалении и в ангиогенезе. Его дисфункция отражает сдвиг в сторону сосудосуживающего, прокоагуляционного, провоспалительного и пролиферативного эффектов [43]. Считается, что АГ является наиболее важным фактором, вызывающим эндотелиальную дисфункцию [44, 45]. Эндотелий подвергается структурным и функциональным повреждениям. Дальнейшее повреждение приводит к нарушению ауторегуляции, сосудистой вазодилaтации, способствуя ухудшению церебральной перфузии [44]. Стенка сосуда утолщается, поскольку соединительная ткань заменяет нормальные слои стенки с окончательным сужением просвета, тромбозом и окклюзией [42].
При проведении МП восстановление кровотока по ПА после ее окклюзии приводит к временному увеличению напряжения сдвига, что, в свою очередь, в норме сопровождается высвобождением из эндотелия ряда веществ, обладающих вазодилататорной активностью, что и обусловливает увеличение диаметра ПА [23, 24]. В исследованиях [46, 47] у молодых пациентов со спонтанным расслоением МАГ и у пациентов среднего возраста с ИИ были выявлены нарушения потокоопосредованной вазодилатации. В недавно опубликованной работе [48] отмечено наличие эндотелиальной дисфункции у пациентов с инсультом в возрасте от 18 до 49 лет.
В нашей выборке у мужчин в возрасте 18–50 лет нарушение потокоопосредованной вазодилатации наблюдалось в 58,8% случаев (у 20 из 34 обследованных). Степень максимального расширения ПА после МП у наших пациентов с ЛИ составила 8,47±3,59%. Полученные нами данные указывают на наличие ультразвуковых признаков эндотелиальной дисфункции. Это сопоставимо с данными предыдущих исследований, однако в этих работах пациенты были более старшего возраста [24, 49]. Выявленные нами ультразвуковые признаки эндотелиальной дисфункции у мужчин с ЛИ в более молодом возрасте, у большинства из которых была АГ (97,8%), соответствуют данным о взаимосвязи эндотелиальной дисфункции и АГ [24, 50, 51]. Показано, что АГ способствует развитию функциональных нарушений в эндотелии сосудов и в то же время сама является их следствием [52]. Несколько исследований, посвященных молодым людям без инсульта, показали, что мужской пол, отягощенная наследственность, увеличение возраста, массы тела, употребление алкоголя, курение, СД и нарушение липидного обмена были связаны с эндотелиальной дисфункцией [53–55]. Поэтому можно сказать, что основная стратегия врачебной работы — это массовый охват населения скринингом на наличие данных факторов риска и пристальное внимание к выявленным пациентам, а также работа по снижению факторов риска у данной группы лиц [56].
Заключение
Таким образом, у мужчин молодого возраста (18–50 лет) с ЛИ основными факторами риска являются АГ, курение, употребление алкоголя и дислипидемия, причем у большинства из них отмечалось наличие сразу нескольких модифицируемых факторов риска. Более чем у половины пациентов с ЛИ выявлено нарушение потокоопосредованной вазодилатации, что говорит о наличии эндотелиальной дисфункции. Высокая частота традиционных факторов риска у молодых пациентов подчеркивает необходимость оптимизации планов первичной и вторичной профилактики.
Сведения об авторах:
Пизов Николай Александрович — заведующий отделением медицинской реабилитации пациентов с нарушениями функции центральной нервной системы ГБУЗ ЯО «КБ № 2»; 150030, Россия, г. Ярославль, Суздальское ш., д. 39; ORCID iD 0000-0002-3009-3020.
Баранова Наталья Сергеевна — д.м.н., профессор кафедры нервных болезней с медицинской генетикой и нейрохирургией ФГБОУ ВО ЯГМУ Минздрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5; ORCID iD 0000-0003-1745-5354.
Пизова Наталия Вячеславовна — д.м.н., профессор кафедры нервных болезней с медицинской генетикой и нейрохирургией ФГБОУ ВО ЯГМУ Минздрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5; ORCID iD 0000-0002-7465-0677.
Бакучева Муза Владимировна — заведующая отделением функциональной диагностики ГБУЗ ЯО «КБ № 2»; 150030, Россия, г. Ярославль, Суздальское ш., д. 39.
Контактная информация: Пизова Наталия Вячеславовна, e-mail: pizova@yandex.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 18.08.2023.
Поступила после рецензирования 12.09.2023.
Принята в печать 28.09.2023.
About the authors:
Nikolay A. Pizov — Head of the Department of Rehabilitation of Patients with Central Nervous System Disorders, Clinical Hospital No. 2; 39, Suzdalskoye highway, Yaroslavl, 150030, Russian Federation; ORCID iD 0000-0002-3009-3020.
Natalia S. Baranova — Dr. Sc. (Med.), Professor of the Department of Nervous Diseases with Medical Genetics and Neurosurgery, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation; ORCID iD 0000-0003-1745-5354.
Natalia V. Pizova — Dr. Sc. (Med.), Professor of the Department of Nervous Diseases with Medical Genetics and Neurosurgery, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation; ORCID iD 0000-0002-7465-0677.
Musa V. Bakucheva — Head of the Department of Functional Diagnostics, Clinical Hospital No. 2; 39, Suzdalskoye highway, Yaroslavl, 150030, Russian Federation.
Contact information: Natalia V. Pizova, e-mail: pizova@yandex.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 18.08.2023.
Revised 12.09.2023.
Accepted 28.09.2023.
Информация с rmj.ru